Гелий (от греч . ἥλιος , романизированный : helios , букв. «солнце») — химический элемент ; имеет символ He и атомный номер 2. Это бесцветный, не имеющий запаха, нетоксичный, инертный , одноатомный газ и первый в группе благородных газов в периодической таблице . [a] Его температура кипения является самой низкой среди всех элементов , и он не имеет температуры плавления при стандартных давлениях. Это второй по легкости и второй по распространенности элемент в наблюдаемой Вселенной после водорода . Он присутствует примерно в 24% от общей элементарной массы, что более чем в 12 раз превышает массу всех более тяжелых элементов вместе взятых. Его распространенность аналогична этой как в Солнце, так и в Юпитере из - за очень высокой энергии ядерной связи (на нуклон ) гелия-4 по отношению к следующим трем элементам после гелия. Эта энергия связи гелия-4 также объясняет, почему он является продуктом как ядерного синтеза , так и радиоактивного распада . Наиболее распространенным изотопом гелия во Вселенной является гелий-4, подавляющее большинство которого образовалось во время Большого взрыва . Большие количества нового гелия создаются в результате ядерного синтеза водорода в звездах .
Гелий был впервые обнаружен как неизвестная желтая спектральная линия в солнечном свете во время солнечного затмения в 1868 году Жоржем Райе [14] , капитаном К. Т. Хейгом [15] , Норманом Р. Погсоном [16] и лейтенантом Джоном Гершелем [17] , а впоследствии это подтвердил французский астроном Жюль Янссеном [18] . Янссену часто приписывают открытие этого элемента совместно с Норманом Локьером . Янссен зарегистрировал спектральную линию гелия во время солнечного затмения 1868 года, в то время как Локьер наблюдал ее из Великобритании. Однако только Локьер предположил, что эта линия была связана с новым элементом, который он назвал в честь Солнца. Официальное открытие элемента было сделано в 1895 году химиками сэром Уильямом Рэмзи , Пером Теодором Клеве и Нильсом Абрахамом Ланглетом , которые обнаружили гелий, выделяющийся из урановой руды клевеита , который в настоящее время рассматривается не как отдельный минеральный вид, а как разновидность уранинита . [19] [20] В 1903 году большие запасы гелия были обнаружены в месторождениях природного газа в некоторых частях Соединенных Штатов, которые на сегодняшний день являются крупнейшим поставщиком газа.
Жидкий гелий используется в криогенике (его крупнейшее единичное применение, потребляющее около четверти производства), и для охлаждения сверхпроводящих магнитов , с его основным коммерческим применением в сканерах МРТ . Другие промышленные применения гелия — в качестве наддувочного и продувочного газа, в качестве защитной атмосферы для дуговой сварки и в таких процессах, как выращивание кристаллов для изготовления кремниевых пластин — составляют половину производимого газа. Небольшое, но хорошо известное применение — в качестве подъемного газа в воздушных шарах и дирижаблях . [21] Как и в случае с любым газом, плотность которого отличается от плотности воздуха, вдыхание небольшого объема гелия временно изменяет тембр и качество человеческого голоса . В научных исследованиях поведение двух жидких фаз гелия-4 (гелий I и гелий II) важно для исследователей, изучающих квантовую механику (в частности, свойство сверхтекучести ), и для тех, кто изучает такие явления, как сверхпроводимость , возникающие в веществе вблизи абсолютного нуля .
На Земле он встречается относительно редко — 5,2 ppm по объёму в атмосфере . Большая часть земного гелия, присутствующего сегодня, образуется в результате естественного радиоактивного распада тяжёлых радиоактивных элементов ( тория и урана , хотя есть и другие примеры), поскольку альфа-частицы , испускаемые такими распадами, состоят из ядер гелия-4 . Этот радиогенный гелий улавливается природным газом в концентрациях до 7% по объёму, из которого он извлекается в коммерческих целях с помощью низкотемпературного процесса разделения, называемого фракционной перегонкой . Земной гелий является невозобновляемым ресурсом, поскольку после попадания в атмосферу он быстро улетает в космос . Считается, что его запасы быстро сокращаются. [22] [23] Однако некоторые исследования показывают, что гелий, образующийся глубоко в Земле в результате радиоактивного распада, может накапливаться в запасах природного газа в больших, чем ожидалось, количествах, [24] в некоторых случаях высвобождаясь в результате вулканической активности. [25]
Первое свидетельство наличия гелия было обнаружено 18 августа 1868 года в виде ярко-желтой линии с длиной волны 587,49 нанометров в спектре хромосферы Солнца . Линия была обнаружена французским астрономом Жюлем Жанссеном во время полного солнечного затмения в Гунтуре , Индия. [26] [27] Первоначально предполагалось, что эта линия принадлежит натрию . 20 октября того же года английский астроном Норман Локьер наблюдал желтую линию в солнечном спектре, которую он назвал D 3 , поскольку она находилась вблизи известных линий Фраунгофера натрия D 1 и D 2. [28] [29] Он пришел к выводу, что она была вызвана элементом на Солнце, неизвестным на Земле. Локьер назвал элемент греческим словом, обозначающим Солнце, ἥλιος ( гелиос ). [30] [31] Иногда говорят, что английский химик Эдвард Франкленд также был вовлечен в название, но это маловероятно, так как он сомневался в существовании этого нового элемента. Окончание «-ium» необычно, так как оно обычно применяется только к металлическим элементам; вероятно, Локьер, будучи астрономом, не знал о химических соглашениях. [32]
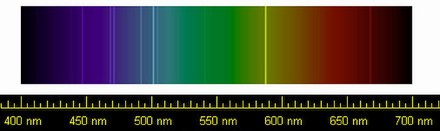
В 1881 году итальянский физик Луиджи Пальмиери впервые обнаружил гелий на Земле по его спектральной линии D3 , когда он анализировал материал, который был сублимирован во время недавнего извержения Везувия . [33]

.jpg/440px-Clevite_sample_(35321726345).jpg)
26 марта 1895 года шотландский химик сэр Уильям Рамзай выделил гелий на Земле, обработав минерал клевеит (разновидность уранинита с содержанием редкоземельных элементов не менее 10% ) минеральными кислотами . Рамзай искал аргон , но после отделения азота и кислорода от газа, выделившегося серной кислотой , он заметил яркую желтую линию, которая соответствовала линии D3, наблюдаемой в спектре Солнца. [29] [35] [36] [37] Эти образцы были идентифицированы как гелий Локьером и британским физиком Уильямом Круксом . [38] [39] Он был независимо выделен из клевеита в том же году химиками Пером Теодором Клеве и Авраамом Ланглетом в Уппсале , Швеция, которые собрали достаточно газа, чтобы точно определить его атомный вес . [40] [41] [27] [42] Гелий был также выделен американским геохимиком Уильямом Фрэнсисом Хиллебрандом до открытия Рамзая, когда он заметил необычные спектральные линии во время тестирования образца минерала уранинита. Хиллебранд, однако, приписал линии азоту . [43] Его поздравительное письмо Рамзаю представляет собой интересный случай открытия и почти открытия в науке. [44]
В 1907 году Эрнест Резерфорд и Томас Ройдс продемонстрировали, что альфа-частицы являются ядрами гелия, позволив частицам проникнуть через тонкую стеклянную стенку вакуумной трубки , а затем создав разряд в трубке, чтобы изучить спектр нового газа внутри. [45] В 1908 году гелий был впервые сжижен голландским физиком Хайке Камерлинг-Оннесом, охладив газ до температуры ниже 5 К (−268,15 °C; −450,67 °F). [46] [47] Он попытался затвердеть его, еще больше понизив температуру, но потерпел неудачу, потому что гелий не затвердевает при атмосферном давлении. Ученик Оннеса Виллем Хендрик Кеесом в конечном итоге смог затвердеть 1 см 3 гелия в 1926 году, приложив дополнительное внешнее давление. [48] [49]
В 1913 году Нильс Бор опубликовал свою «трилогию» [50] [51] об атомной структуре, которая включала пересмотр серии Пикеринга–Фаулера как центрального доказательства в поддержку его модели атома . [52] [53] Эта серия названа в честь Эдварда Чарльза Пикеринга , который в 1896 году опубликовал наблюдения ранее неизвестных линий в спектре звезды ζ Кормы [54] (теперь известно, что они встречаются у Вольфа–Райе и других горячих звезд). [55] Пикеринг приписал наблюдение (линии при 4551, 5411 и 10123 Å ) новой форме водорода с полуцелыми уровнями перехода. [56] [57] В 1912 году Альфред Фаулер [58] сумел получить похожие линии из смеси водорода и гелия и подтвердил вывод Пикеринга относительно их происхождения. [59] Модель Бора не допускает полуцелых переходов (как и квантовая механика), и Бор пришел к выводу, что Пикеринг и Фаулер ошибались, и вместо этого приписал эти спектральные линии ионизированному гелию, He + . [60] Фаулер изначально был настроен скептически [61] , но в конечном итоге убедился [62] , что Бор был прав, [50] и к 1915 году «спектроскописты окончательно перенесли [серию Пикеринга–Фаулера] [с водорода] на гелий». [53] [63] Теоретическая работа Бора по серии Пикеринга продемонстрировала необходимость «пересмотра проблем, которые, казалось, уже были решены в рамках классических теорий», и предоставила важное подтверждение его атомной теории. [53]
В 1938 году русский физик Пётр Леонидович Капица обнаружил, что гелий-4 почти не имеет вязкости при температурах, близких к абсолютному нулю , явление, которое теперь называется сверхтекучестью . [64] Это явление связано с конденсацией Бозе-Эйнштейна . В 1972 году то же самое явление наблюдалось в гелии-3 , но при температурах, гораздо более близких к абсолютному нулю, американскими физиками Дугласом Д. Ошероффом , Дэвидом М. Ли и Робертом К. Ричардсоном . Считается, что явление в гелии-3 связано с образованием пар фермионов гелия-3 для создания бозонов , по аналогии с куперовскими парами электронов, создающими сверхпроводимость . [65]
В 1961 году Вигнос и Фэрбэнк сообщили о существовании другой фазы твердого гелия-4, названной гамма-фазой. Она существует в узком диапазоне давлений от 1,45 до 1,78 К. [66]

После операции по бурению нефтяной скважины в 1903 году в Декстере, штат Канзас, в результате которой образовался газовый гейзер, который не горел, геолог из штата Канзас Эразмус Хаворт собрал образцы вытекающего газа и отвез их в Университет Канзаса в Лоуренсе, где с помощью химиков Гамильтона Кэди и Дэвида Макфарланда он обнаружил, что газ состоял из 72% по объему азота, 15% метана ( горючий процент только при достаточном количестве кислорода), 1% водорода и 12% неидентифицируемого газа. [27] [67] При дальнейшем анализе Кэди и Макфарланд обнаружили, что 1,84% образца газа составлял гелий. [68] [69] Это показало, что, несмотря на его общую редкость на Земле, гелий был сконцентрирован в больших количествах под Американскими Великими равнинами и был доступен для извлечения в качестве побочного продукта природного газа . [70]
По предложению сэра Ричарда Трелфолла ВМС США спонсировали три небольших экспериментальных гелиевых завода во время Первой мировой войны. Целью было снабжение аэростатов заграждения негорючим, более легким, чем воздух, газом. В рамках программы было произведено в общей сложности 5700 м 3 (200 000 куб. футов) 92% гелия, хотя ранее было получено менее кубического метра газа. [29] Часть этого газа использовалась в первом в мире заполненном гелием дирижабле, дирижабле ВМС США класса C C-7, который совершил свой первый полет из Хэмптон-Роудс, Вирджиния , в Боллинг-Филд в Вашингтоне, округ Колумбия, 1 декабря 1921 года, [71] почти за два года до того, как первый жесткий заполненный гелием дирижабль ВМС , построенный на военно-морском авиационном заводе USS Shenandoah , поднялся в воздух в сентябре 1923 года.
Хотя процесс извлечения с использованием низкотемпературного сжижения газа не был разработан вовремя, чтобы стать значительным во время Первой мировой войны, производство продолжалось. Гелий в основном использовался в качестве подъемного газа в аппаратах легче воздуха. Во время Второй мировой войны возрос спрос на гелий для подъемного газа и для сварки в защитной дуге . Гелиевый масс-спектрометр также имел жизненно важное значение в Манхэттенском проекте атомной бомбы . [72]
Правительство Соединенных Штатов создало Национальный резерв гелия в 1925 году в Амарилло, штат Техас , с целью снабжения военных дирижаблей во время войны и коммерческих дирижаблей в мирное время. [29] Из-за Закона о гелии 1925 года , который запретил экспорт дефицитного гелия, на производство которого США тогда имели монополию, а также из-за непомерно высокой стоимости газа, немецкие цеппелины были вынуждены использовать водород в качестве подъемного газа, что получило дурную славу в катастрофе Гинденбурга . Рынок гелия после Второй мировой войны был в упадке, но резерв был расширен в 1950-х годах, чтобы обеспечить поставку жидкого гелия в качестве охладителя для создания ракетного топлива кислород/водород (среди других применений) во время космической гонки и холодной войны . Использование гелия в Соединенных Штатах в 1965 году более чем в восемь раз превышало пиковое потребление во время войны. [73]
После поправок к Закону о гелии 1960 года (публичный закон 86–777) Бюро горнодобывающей промышленности США организовало пять частных заводов для извлечения гелия из природного газа. Для этой программы по сохранению гелия Бюро построило 425-мильный (684 км) трубопровод из Буштона, Канзас , чтобы соединить эти заводы с частично истощенным государственным газовым месторождением Клиффсайд около Амарилло, Техас. Эта смесь гелия и азота была закачана и хранилась в газовом месторождении Клиффсайд до тех пор, пока не понадобится, после чего она была дополнительно очищена. [74]
К 1995 году был собран миллиард кубометров газа, а долг по резерву составил 1,4 миллиарда долларов США, что побудило Конгресс США в 1996 году прекратить резерв. [27] [75] Принятый в 1996 году Закон о приватизации гелия [76] (публичный закон 104–273) предписал Министерству внутренних дел США опустошить резерв, начав продажи к 2005 году. [77]
Гелий, произведенный между 1930 и 1945 годами, имел чистоту около 98,3% (2% азота), что было достаточно для дирижаблей. В 1945 году небольшое количество 99,9% гелия было произведено для сварки. К 1949 году были доступны коммерческие количества гелия класса А чистотой 99,95%. [78]
В течение многих лет Соединенные Штаты производили более 90% коммерчески пригодного гелия в мире, в то время как экстракционные заводы в Канаде, Польше, России и других странах производили остаток. В середине 1990-х годов новый завод в Арзеве , Алжир, производящий 17 миллионов кубических метров (600 миллионов кубических футов), начал работу с достаточным производством, чтобы покрыть весь спрос Европы. Между тем, к 2000 году потребление гелия в США выросло до более чем 15 миллионов кг в год. [79] В 2004–2006 годах были построены дополнительные заводы в Рас-Лаффане , Катар , и Скикде , Алжир. Алжир быстро стал вторым по величине производителем гелия. [80] За это время увеличилось как потребление гелия, так и затраты на его производство. [81] С 2002 по 2007 год цены на гелий удвоились. [82]
По состоянию на 2012 год [обновлять]Национальный резерв гелия США составлял 30 процентов мирового гелия. [83] Ожидалось, что резерв закончится в 2018 году. [83] Несмотря на это, предложенный законопроект в Сенате США позволит резерву продолжать продавать газ. Другие крупные резервы находились в Хьюготоне в Канзасе , США, и близлежащих газовых месторождениях Канзаса и в Техасе и Оклахоме . Новые гелиевые заводы планировалось открыть в 2012 году в Катаре , России и американском штате Вайоминг , но они не должны были уменьшить дефицит. [83]
В 2013 году Катар запустил крупнейшую в мире гелиевую установку, [84] хотя дипломатический кризис 2017 года в Катаре серьезно повлиял на производство гелия там. [85] 2014 год был широко признан годом избыточного предложения в гелиевом бизнесе после многих лет известного дефицита. [86] Nasdaq сообщил (2015), что для Air Products , международной корпорации, которая продает газы для промышленного использования, объемы гелия остаются под экономическим давлением из-за ограничений поставок сырья. [87]

С точки зрения квантовой механики гелий является вторым по простоте моделирования атомом после атома водорода . Гелий состоит из двух электронов на атомных орбиталях , окружающих ядро, содержащее два протона и (обычно) два нейтрона. Как и в ньютоновской механике, ни одна система, состоящая более чем из двух частиц, не может быть решена с помощью точного аналитического математического подхода (см. задачу трех тел ), и гелий не является исключением. Таким образом, требуются численные математические методы, даже для решения системы из одного ядра и двух электронов. Такие методы вычислительной химии были использованы для создания квантово-механической картины связывания электронов гелия, которая точна в пределах < 2% от правильного значения, за несколько вычислительных шагов. [88] Такие модели показывают, что каждый электрон в гелии частично экранирует ядро от другого, так что эффективный ядерный заряд Z eff , который видит каждый электрон, составляет около 1,69 единиц, а не 2 заряда классического «голого» ядра гелия.
Ядро атома гелия-4 идентично альфа-частице . Эксперименты по рассеянию электронов высокой энергии показывают, что его заряд экспоненциально уменьшается от максимума в центральной точке, точно так же, как и плотность заряда собственного электронного облака гелия . Эта симметрия отражает схожую базовую физику: пара нейтронов и пара протонов в ядре гелия подчиняются тем же квантово-механическим правилам, что и пара электронов гелия (хотя ядерные частицы подвержены разному ядерному связывающему потенциалу), так что все эти фермионы полностью занимают 1s-орбитали парами, ни один из них не обладает орбитальным угловым моментом, и каждый из них отменяет собственный спин другого. Таким образом, такое расположение энергетически чрезвычайно стабильно для всех этих частиц и имеет астрофизические последствия. [89] А именно, добавление еще одной частицы — протона, нейтрона или альфа-частицы — потребляло бы, а не выделяло энергию; все системы с массовым числом 5, а также бериллий-8 (состоящий из двух альфа-частиц) являются несвязанными. [90]
Например, стабильность и низкая энергия состояния электронного облака в гелии объясняет химическую инертность элемента, а также отсутствие взаимодействия атомов гелия друг с другом, что приводит к самым низким температурам плавления и кипения среди всех элементов. Аналогичным образом, особая энергетическая стабильность ядра гелия-4, вызванная аналогичными эффектами, объясняет легкость получения гелия-4 в атомных реакциях, которые включают либо испускание тяжелых частиц, либо синтез. Некоторое количество стабильного гелия-3 (два протона и один нейтрон) производится в реакциях синтеза из водорода, хотя его предполагаемое содержание во Вселенной составляет около10−5 относительно гелия-4. [ 91 ]

Необычная стабильность ядра гелия-4 также важна с космологической точки зрения : она объясняет тот факт, что в первые несколько минут после Большого взрыва , когда «суп» свободных протонов и нейтронов, который изначально был создан в соотношении примерно 6:1, остыл до такой степени, что стало возможным ядерное связывание, почти все первые образовавшиеся составные атомные ядра были ядрами гелия-4. Из-за относительно тесной связи ядер гелия-4 его производство поглотило почти все свободные нейтроны за несколько минут, прежде чем они смогли подвергнуться бета-распаду, и, таким образом, лишь немногие нейтроны были доступны для образования более тяжелых атомов, таких как литий, бериллий или бор. Ядерная связь гелия-4 на нуклон сильнее, чем в любом из этих элементов (см. нуклеогенез и энергия связи ), и поэтому после образования гелия не было энергетического стимула для создания элементов 3, 4 и 5. [92] Для гелия едва ли энергетически выгодно слиться со следующим элементом с более низкой энергией на нуклон , углеродом. Однако из-за короткого времени жизни промежуточного бериллия-8 этот процесс требует, чтобы три ядра гелия ударялись друг о друга почти одновременно (см. тройной альфа-процесс ). [90] Таким образом, не было времени для образования значительного количества углерода в течение нескольких минут после Большого взрыва, прежде чем ранняя расширяющаяся Вселенная охладилась до температуры и давления, при которых синтез гелия в углерод стал невозможен. Это оставило раннюю Вселенную с очень похожим соотношением водорода/гелия, которое наблюдается сегодня (3 части водорода на 1 часть гелия-4 по массе), при этом почти все нейтроны во Вселенной были захвачены гелием-4.
Все более тяжелые элементы (включая те, которые необходимы для каменистых планет, таких как Земля, и для углеродной или другой жизни) были созданы после Большого взрыва в звездах, которые были достаточно горячими, чтобы синтезировать сам гелий. Все элементы, кроме водорода и гелия, сегодня составляют всего 2% массы атомной материи во Вселенной. Гелий-4, напротив, составляет около 24% массы обычной материи Вселенной — почти всю обычную материю, которая не является водородом. [91] [93]

Гелий является вторым наименее реакционноспособным благородным газом после неона , и, таким образом, вторым наименее реакционноспособным из всех элементов. [94] Он химически инертен и одноатомен во всех стандартных условиях. Из-за относительно низкой молярной (атомной) массы гелия его теплопроводность , удельная теплоемкость и скорость звука в газовой фазе больше, чем у любого другого газа, за исключением водорода . По этим причинам и из-за небольшого размера одноатомных молекул гелия гелий диффундирует через твердые тела со скоростью, в три раза превышающей скорость воздуха, и примерно на 65% превышающей скорость водорода. [29]
Гелий является наименее растворимым в воде одноатомным газом [95] и одним из наименее растворимых в воде газов ( CF 4 , SF 6 и C 4 F 8 имеют более низкую молярную растворимость: 0,3802, 0,4394 и 0,2372 x 2 /10 −5 соответственно, по сравнению с 0,70797 x 2 /10 −5 у гелия ), [96] а показатель преломления гелия ближе к единице, чем у любого другого газа. [97] Гелий имеет отрицательный коэффициент Джоуля-Томсона при нормальной температуре окружающей среды, что означает, что он нагревается, когда ему позволяют свободно расширяться. Только ниже его температуры инверсии Джоуля-Томсона (примерно от 32 до 50 К при 1 атмосфере) он охлаждается при свободном расширении. [29] После предварительного охлаждения ниже этой температуры гелий можно превратить в жидкость посредством охлаждения расширением.
Большая часть внеземного гелия — это плазма в звездах, свойства которой сильно отличаются от свойств атомарного гелия. В плазме электроны гелия не связаны с его ядром, что приводит к очень высокой электропроводности, даже когда газ лишь частично ионизирован. Заряженные частицы находятся под сильным влиянием магнитных и электрических полей. Например, в солнечном ветре вместе с ионизированным водородом частицы взаимодействуют с магнитосферой Земли , вызывая токи Биркеланда и полярные сияния . [98]
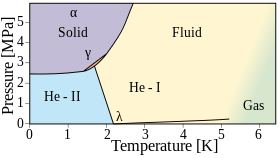

Гелий становится жидким при охлаждении ниже 4,2 К при атмосферном давлении. Однако, в отличие от любого другого элемента, гелий остается жидким вплоть до температуры абсолютного нуля . Это прямое следствие квантовой механики: в частности, энергия нулевой точки системы слишком высока, чтобы позволить замерзнуть. Для ее замерзания требуется давление выше примерно 25 атмосфер. Существует две жидкие фазы: гелий I — обычная жидкость, а гелий II, который существует при более низкой температуре, является сверхтекучей жидкостью .
Ниже точки кипения 4,22 К (−268,93 °C; −452,07 °F) и выше точки лямбда 2,1768 К (−270,9732 °C; −455,7518 °F) изотоп гелий-4 существует в обычном бесцветном жидком состоянии, называемом гелием I. [ 29] Как и другие криогенные жидкости, гелий I кипит при нагревании и сжимается при понижении температуры. Однако ниже точки лямбда гелий не кипит и расширяется при дальнейшем понижении температуры.
Гелий I имеет газообразный показатель преломления 1,026, что делает его поверхность настолько трудноразличимой, что поплавки из пенополистирола часто используются для того, чтобы показать, где находится поверхность. [29] Эта бесцветная жидкость имеет очень низкую вязкость и плотность 0,145–0,125 г/мл (примерно между 0 и 4 К), [99] что составляет всего одну четвертую от значения, ожидаемого из классической физики . [29] Для объяснения этого свойства необходима квантовая механика , и поэтому оба состояния жидкого гелия (гелий I и гелий II) называются квантовыми жидкостями , то есть они проявляют атомные свойства в макроскопическом масштабе. Это может быть следствием того, что его точка кипения так близка к абсолютному нулю, что не позволяет случайному молекулярному движению ( тепловой энергии ) маскировать атомные свойства. [29]
Жидкий гелий ниже своей лямбда-точки (называемый гелием II ) проявляет очень необычные характеристики. Из-за своей высокой теплопроводности , когда он кипит, он не пузырится, а испаряется прямо с поверхности. Гелий-3 также имеет сверхтекучую фазу, но только при гораздо более низких температурах; в результате о свойствах изотопа известно меньше. [29]

Гелий II — сверхтекучая жидкость, квантово-механическое состояние материи со странными свойствами. Например, когда он течет через капилляры толщиной от 10 до 100 нм , он не имеет измеримой вязкости . [27] Однако, когда измерения проводились между двумя движущимися дисками, наблюдалась вязкость, сравнимая с вязкостью газообразного гелия. Существующая теория объясняет это с помощью двухжидкостной модели для гелия II. В этой модели жидкий гелий ниже точки лямбда рассматривается как содержащий долю атомов гелия в основном состоянии , которые являются сверхтекучими и текут с точно нулевой вязкостью, и долю атомов гелия в возбужденном состоянии, которые ведут себя скорее как обычная жидкость. [100]
В эффекте фонтана конструируется камера, которая соединена с резервуаром гелия II спеченным диском , через который легко просачивается сверхтекучий гелий, но через который не может пройти несверхтекучий гелий. Если внутренняя часть контейнера нагревается, сверхтекучий гелий превращается в несверхтекучий гелий. Чтобы поддерживать равновесную долю сверхтекучего гелия, сверхтекучий гелий просачивается и увеличивает давление, заставляя жидкость фонтанировать из контейнера. [101]
Теплопроводность гелия II больше, чем у любого другого известного вещества, в миллион раз больше, чем у гелия I, и в несколько сотен раз больше, чем у меди . [29] Это происходит потому, что теплопроводность происходит по исключительному квантовому механизму. Большинство материалов, которые хорошо проводят тепло, имеют валентную зону свободных электронов, которые служат для передачи тепла. Гелий II не имеет такой валентной зоны, но тем не менее хорошо проводит тепло. Поток тепла регулируется уравнениями, которые похожи на волновое уравнение, используемое для характеристики распространения звука в воздухе. Когда вводится тепло, оно движется со скоростью 20 метров в секунду при 1,8 К через гелий II в виде волн в явлении, известном как второй звук . [29]
Гелий II также проявляет эффект ползучести. Когда поверхность простирается за пределы уровня гелия II, гелий II движется вдоль поверхности, против силы тяжести . Гелий II будет выходить из сосуда, который не запечатан, ползая вдоль стенок, пока не достигнет более теплой области, где он испаряется. Он движется в пленке толщиной 30 нм независимо от материала поверхности. Эта пленка называется пленкой Роллина и названа в честь человека, который первым охарактеризовал эту особенность, Бернарда В. Роллена. [29] [102] [103] В результате этого ползучего поведения и способности гелия II быстро просачиваться через крошечные отверстия, его очень трудно ограничить. Если контейнер не сконструирован тщательно, гелий II будет ползти вдоль поверхностей и через клапаны, пока не достигнет более теплого места, где он испарится. Волны, распространяющиеся по пленке Роллина, подчиняются тому же уравнению, что и гравитационные волны на мелководье, но вместо силы тяжести восстанавливающей силой является сила Ван-дер-Ваальса . [104] Эти волны известны как третий звук . [105]
Гелий остается жидким вплоть до абсолютного нуля при атмосферном давлении, но замерзает при высоком давлении. Твердый гелий требует температуры 1–1,5 К (около −272 °C или −457 °F) при давлении около 25 бар (2,5 МПа). [106] Часто бывает трудно отличить твердый гелий от жидкого, поскольку показатель преломления двух фаз почти одинаков. Твердый гелий имеет резкую точку плавления и кристаллическую структуру, но он сильно сжимаем ; приложение давления в лаборатории может уменьшить его объем более чем на 30%. [107] При объемном модуле около 27 МПа [108] он примерно в 100 раз более сжимаем, чем вода. Твердый гелий имеет плотность0,214 ± 0,006 г/см 3 при 1,15 К и 66 атм; проектируемая плотность при 0 К и 25 бар (2,5 МПа) составляет0,187 ± 0,009 г/см 3 . [109] При более высоких температурах гелий затвердеет при достаточном давлении. При комнатной температуре для этого требуется около 114 000 атм. [110]
Гелий-4 и гелий-3 оба образуют несколько кристаллических твердых фаз, все требуют не менее 25 бар. Они оба образуют α-фазу, которая имеет гексагональную плотноупакованную (hcp) кристаллическую структуру, β-фазу, которая является гранецентрированной кубической (fcc), и γ-фазу, которая является объемно-центрированной кубической (bcc). [111]
Известно девять изотопов гелия, два из которых, гелий-3 и гелий-4 , являются стабильными . В атмосфере Земли один атом3
Он за каждый миллион, который есть4
He . [27] В отличие от большинства элементов, изотопное содержание гелия сильно варьируется в зависимости от происхождения из-за различных процессов формирования. Самый распространенный изотоп, гелий-4, производится на Земле в результате альфа-распада более тяжелых радиоактивных элементов; альфа-частицы, которые появляются, являются полностью ионизированными ядрами гелия-4. Гелий-4 является необычайно стабильным ядром, поскольку его нуклоны организованы в полные оболочки . Он также был образован в огромных количествах во время нуклеосинтеза Большого взрыва . [112]
Гелий-3 присутствует на Земле только в следовых количествах. Большая его часть присутствует с момента образования Земли, хотя часть падает на Землю, захваченная космической пылью . [113] Следовые количества также производятся бета-распадом трития . [ 114] Породы из земной коры имеют изотопные соотношения, варьирующиеся в десять раз, и эти соотношения могут быть использованы для исследования происхождения пород и состава мантии Земли . [113] 3
Он гораздо более распространен в звездах как продукт ядерного синтеза. Таким образом, в межзвездной среде доля3
Он к4
Он примерно в 100 раз выше, чем на Земле. [115] Внепланетный материал, такой как лунный и астероидный реголит , имеет следовые количества гелия-3 из-за бомбардировки солнечными ветрами . Поверхность Луны содержит гелий-3 в концентрациях порядка 10 ppb , что намного выше, чем приблизительно 5 ppt , обнаруженных в атмосфере Земли. [116] [117] Ряд людей, начиная с Джеральда Кульчински в 1986 году, [118] предлагали исследовать Луну, добывать лунный реголит и использовать гелий-3 для термоядерного синтеза .
Жидкий гелий-4 можно охладить примерно до 1 К (−272,15 °C; −457,87 °F) с помощью испарительного охлаждения в 1-К горшке . Аналогичное охлаждение гелия-3, имеющего более низкую температуру кипения, может дать около0,2 кельвина в холодильнике на гелии-3 . Равные смеси жидкости3
Он и4
Он ниже0,8 К разделяются на две несмешивающиеся фазы из-за их несходства (они следуют разной квантовой статистике : атомы гелия-4 являются бозонами , а атомы гелия-3 являются фермионами ). [29] Рефрижераторы разбавления используют эту несмешиваемость для достижения температур в несколько милликельвинов. [119]
Можно производить экзотические изотопы гелия , которые быстро распадаются на другие вещества. Самый короткоживущий тяжелый изотоп гелия — это несвязанный гелий-10 с периодом полураспада2,6(4) × 10−22 с . [6] Гелий-6 распадается, испуская бета-частицу , и имеет период полураспада 0,8 секунды. Гелий-7 и гелий-8 создаются в определенных ядерных реакциях . [29] Известно , что гелий-6 и гелий-8 демонстрируют ядерное гало . [29]
Таблица тепловых и физических свойств газообразного гелия при атмосферном давлении: [120] [121]

Гелий имеет валентность , равную нулю, и химически неактивен при всех нормальных условиях. [107] Он является электрическим изолятором, если не ионизирован . Как и другие благородные газы, гелий имеет метастабильные энергетические уровни , которые позволяют ему оставаться ионизированным в электрическом разряде с напряжением ниже его потенциала ионизации . [29] Гелий может образовывать нестабильные соединения , известные как эксимеры , с вольфрамом, йодом, фтором, серой и фосфором, когда он подвергается тлеющему разряду , электронной бомбардировке или восстанавливается до плазмы другими способами. Молекулярные соединения HeNe, HgHe 10 и WHe 2 и молекулярные ионы He+
2, Он2+
2, Хе-хе+
, и ХеД+
были созданы таким образом. [122] HeH + также стабилен в своем основном состоянии, но чрезвычайно реактивен — это самая сильная известная кислота Бренстеда , и поэтому может существовать только в изоляции, поскольку она протонирует любую молекулу или противоанион, с которыми она контактирует. Эта техника также дала нейтральную молекулу He 2 , которая имеет большое количество систем полос , и HgHe, которая, по-видимому, удерживается вместе только силами поляризации. [29]
Ван-дер-ваальсовы соединения гелия также могут быть образованы с криогенным гелиевым газом и атомами некоторых других веществ, таких как LiHe и He 2 . [123]
Теоретически возможны и другие истинные соединения, такие как фторгидрид гелия (HHeF), который будет аналогичен HArF , открытому в 2000 году. [124] Расчеты показывают, что два новых соединения, содержащие связь гелий-кислород, могут быть стабильными. [125] Два новых молекулярных вида, предсказанных с использованием теории, CsFHeO и N(CH 3 ) 4 FHeO, являются производными метастабильного аниона FHeO −, впервые теоретически предложенного в 2005 году группой из Тайваня. [126]
Атомы гелия были вставлены в полые молекулы углеродной клетки ( фуллерены ) путем нагревания под высоким давлением. Образованные эндоэдральные молекулы фуллерена стабильны при высоких температурах. Когда образуются химические производные этих фуллеренов, гелий остается внутри. [127] Если используется гелий-3 , его можно легко наблюдать с помощью спектроскопии ядерного магнитного резонанса гелия . [128] Сообщалось о многих фуллеренах, содержащих гелий-3. Хотя атомы гелия не связаны ковалентными или ионными связями, эти вещества обладают различными свойствами и определенным составом, как и все стехиометрические химические соединения.
Под высоким давлением гелий может образовывать соединения с различными другими элементами. Кристаллы клатрата гелия-азота (He(N 2 ) 11 ) выращивались при комнатной температуре при давлении около 10 ГПа в ячейке с алмазными наковальнями . [129] Было показано, что изолирующий электрид Na 2 He термодинамически стабилен при давлении выше 113 ГПа. Он имеет структуру флюорита . [ 130]
Хотя он редок на Земле, гелий является вторым по распространенности элементом в известной Вселенной, составляя 23% ее барионной массы. Только водород более распространен. [27] Подавляющее большинство гелия образовалось в результате нуклеосинтеза Большого взрыва через одну-три минуты после Большого взрыва. Таким образом, измерения его распространенности вносят вклад в космологические модели. В звездах он образуется в результате ядерного синтеза водорода в цепных реакциях протон-протон и цикле CNO , части звездного нуклеосинтеза . [112]
В атмосфере Земли концентрация гелия по объему составляет всего 5,2 частей на миллион. [131] [132] Концентрация низкая и довольно постоянная, несмотря на постоянное производство нового гелия, поскольку большая часть гелия в атмосфере Земли улетучивается в космос в результате нескольких процессов. [133] [134] [135] В гетеросфере Земли , части верхней атмосферы, гелий и водород являются наиболее распространенными элементами.
Большая часть гелия на Земле является результатом радиоактивного распада . Гелий в больших количествах содержится в минералах урана и тория , включая уранинит и его разновидности клевеит и настурана , [19] [136] карнотит и монацит (групповое название; «монацит» обычно относится к монациту-(Ce) ), [137] [138] потому что они испускают альфа-частицы (ядра гелия, He 2+ ), с которыми электроны немедленно соединяются, как только частица останавливается породой. Таким образом, по оценкам, ежегодно в литосфере образуется 3000 метрических тонн гелия . [ 139] [140] [141] В земной коре концентрация гелия составляет 8 частей на миллиард. В морской воде концентрация составляет всего 4 части на триллион. Также есть небольшие количества в минеральных источниках , вулканическом газе и метеоритном железе . Поскольку гелий удерживается в недрах в условиях, которые также удерживают природный газ, самые большие естественные концентрации гелия на планете находятся в природном газе, из которого извлекается большая часть коммерческого гелия. Концентрация варьируется в широком диапазоне от нескольких ppm до более 7% в небольшом газовом месторождении в округе Сан-Хуан, штат Нью-Мексико . [142] [143]
По состоянию на 2021 год [обновлять]мировые запасы гелия оцениваются в 31 миллиард кубических метров, треть из которых находится в Катаре . [144] В 2015 и 2016 годах было объявлено о дополнительных вероятных запасах под Скалистыми горами в Северной Америке [145] и в Восточно-Африканском разломе [25] .
Для крупномасштабного использования гелий извлекается путем фракционной перегонки из природного газа, который может содержать до 7% гелия. [146] Поскольку гелий имеет более низкую температуру кипения , чем любой другой элемент, низкие температуры и высокое давление используются для сжижения почти всех других газов (в основном азота и метана ). Полученный сырой гелий очищается путем последовательного воздействия пониженных температур, при котором почти весь оставшийся азот и другие газы осаждаются из газовой смеси. Активированный уголь используется в качестве конечного этапа очистки, обычно приводящего к получению гелия класса А чистотой 99,995%. [29] Основной примесью в гелии класса А является неон . На конечном этапе производства большая часть производимого гелия сжижается с помощью криогенного процесса. Это необходимо для приложений, требующих жидкого гелия, а также позволяет поставщикам гелия сократить расходы на транспортировку на большие расстояния, поскольку самые большие контейнеры для жидкого гелия имеют вместимость более чем в пять раз больше, чем самые большие прицепы для перевозки газообразного гелия. [80] [147]
В 2008 году из природного газа или из запасов гелия было извлечено около 169 миллионов стандартных кубических метров (СКМ), из которых около 78% — из США, 10% — из Алжира, а большая часть остатка — из России, Польши и Катара. [148] К 2013 году рост производства гелия в Катаре (под управлением компании Qatargas, управляемой Air Liquide ) увеличил долю Катара в мировом производстве гелия до 25%, что сделало его вторым по величине экспортером после США. [149] По оценкам , в 2016 году в Танзании было обнаружено месторождение гелия объемом 54 миллиарда кубических футов (1,5 × 10 9 м 3 ) . [150] В 2020 году в Нинся , Китай, был открыт крупномасштабный гелиевый завод. [151]
В Соединенных Штатах большая часть гелия добывается из природного газа месторождений Хьюготон и близлежащих газовых месторождений в Канзасе, Оклахоме и Панхэндл-Филд в Техасе. [80] [152] Большая часть этого газа когда-то отправлялась по трубопроводу в Национальный резерв гелия , но с 2005 года этот резерв был истощен и распродан, и ожидается, что он будет в значительной степени истощен к 2021 году [149] в соответствии с Законом об ответственном управлении и управлении гелием от октября 2013 года (HR 527). [153] Гелиевые месторождения на западе Соединенных Штатов становятся альтернативным источником поставок гелия, особенно месторождения региона « Четыре угла » (штаты Аризона, Колорадо, Нью-Мексико и Юта). [154]
Диффузия сырого природного газа через специальные полупроницаемые мембраны и другие барьеры является еще одним методом извлечения и очистки гелия. [155] В 1996 году в США были подтверждены запасы гелия в таких газовых скважинных комплексах в объеме около 147 миллиардов стандартных кубических футов (4,2 миллиарда SCM). [156] При темпах использования в то время (72 миллиона SCM в год в США; см. круговую диаграмму ниже) этого было бы достаточно для использования в США примерно на 58 лет, и меньше (возможно, 80% времени) при мировых темпах использования, хотя факторы экономии и переработки влияют на эффективные цифры запасов.
Гелий обычно извлекается из природного газа, поскольку он присутствует в воздухе в количестве, составляющем лишь малую часть от количества неона, однако спрос на него гораздо выше. Подсчитано, что если бы все производство неона было переоборудовано для экономии гелия, то было бы удовлетворено 0,1% мировых потребностей в гелии. Аналогично, только 1% мировых потребностей в гелии можно было бы удовлетворить путем переоборудования всех заводов по перегонке воздуха. [157] Гелий можно синтезировать путем бомбардировки лития или бора высокоскоростными протонами или бомбардировки лития дейтронами , но эти процессы являются совершенно неэкономичным методом производства. [158]
Гелий коммерчески доступен в жидкой или газообразной форме. В жидком виде он может поставляться в небольших изолированных контейнерах, называемых дьюарами , которые вмещают до 1000 литров гелия, или в больших контейнерах ISO, которые имеют номинальную емкость до 42 м 3 (около 11 000 галлонов США ). В газообразной форме небольшие количества гелия поставляются в баллонах высокого давления, вмещающих до 8 м 3 (приблизительно . 282 стандартных кубических футов), в то время как большие количества газа высокого давления поставляются в трубчатых прицепах, которые имеют емкость до 4860 м 3 (приблизительно 172 000 стандартных кубических футов).
По словам защитников гелия, таких как лауреат Нобелевской премии по физике Роберт Коулман Ричардсон , писавших в 2010 году, свободная рыночная цена гелия способствовала «расточительному» использованию (например, для гелиевых шаров ). Цены в 2000-х годах были снижены решением Конгресса США распродать большой запас гелия в стране к 2015 году. [22] По словам Ричардсона, цену необходимо было умножить на 20, чтобы исключить чрезмерное расточительство гелия. В статье Наттолл и др. 2012 года под названием «Хватит растрачивать гелий» также предлагалось создать Международное агентство по гелию, которое бы построило устойчивый рынок для «этого драгоценного товара». [159]

Расчетное фракционное использование гелия в США по категориям в 2014 году. Общее использование составляет 34 миллиона кубических метров. [160]
Хотя воздушные шары, возможно, являются наиболее известным применением гелия, они составляют незначительную часть всего использования гелия. [75] Гелий используется для многих целей, которые требуют некоторых из его уникальных свойств, таких как его низкая температура кипения , низкая плотность , низкая растворимость , высокая теплопроводность или инертность . Из общего объема мирового производства гелия в 2014 году, составлявшего около 32 миллионов кг (180 миллионов стандартных кубических метров) гелия в год, наибольшее использование (около 32% от общего объема в 2014 году) приходится на криогенные приложения, большинство из которых включает охлаждение сверхпроводящих магнитов в медицинских сканерах МРТ и ЯМР- спектрометрах. [161] Другими основными применениями были системы нагнетания и продувки, сварка, поддержание контролируемых атмосфер и обнаружение утечек. Другие применения по категориям были относительно незначительными фракциями. [160]
Гелий используется в качестве защитного газа при выращивании кристаллов кремния и германия , в производстве титана и циркония , а также в газовой хроматографии , [107] поскольку он инертен. Благодаря своей инертности, термически и калорически совершенной природе, высокой скорости звука и высокому значению коэффициента теплоемкости он также полезен в сверхзвуковых аэродинамических трубах [162] и импульсных установках . [163]
Гелий используется в качестве защитного газа в процессах дуговой сварки материалов, которые при температурах сварки загрязняются и ослабляются воздухом или азотом. [27] Ряд инертных защитных газов используется в газовой дуговой сварке вольфрамовым электродом, но гелий используется вместо более дешевого аргона , особенно для сварки материалов с более высокой теплопроводностью , таких как алюминий или медь .

Одним из промышленных применений гелия является обнаружение утечек . Поскольку гелий диффундирует через твердые тела в три раза быстрее, чем воздух, он используется в качестве индикаторного газа для обнаружения утечек в высоковакуумном оборудовании (например, криогенных резервуарах) и контейнерах высокого давления. [164] Испытуемый объект помещается в камеру, которая затем откачивается и заполняется гелием. Гелий, который выходит через утечки, обнаруживается чувствительным устройством ( гелиевым масс-спектрометром ), даже при скоростях утечки всего 10−9 мбар ·л/с (10−10 Па ·м3 / с). Процедура измерения обычно является автоматической и называется интегральным испытанием гелия. Более простая процедура заключается в заполнении испытываемого объекта гелием и ручном поиске утечек с помощью ручного устройства. [165]
Утечки гелия через трещины не следует путать с проникновением газа через объемный материал. В то время как гелий имеет документированные константы проницаемости (следовательно, вычисляемую скорость проницаемости) через стекла, керамику и синтетические материалы, инертные газы, такие как гелий, не будут проникать через большинство объемных металлов. [166]

Поскольку он легче воздуха , дирижабли и воздушные шары надуваются гелием для подъема . В то время как водородный газ более плавучий и просачивается через мембрану с меньшей скоростью, гелий имеет то преимущество, что он не воспламеняется и действительно огнестойкий . Другое незначительное применение - в ракетостроении , где гелий используется в качестве среды для заполнения баков ракетного топлива в полете и для конденсации водорода и кислорода для производства ракетного топлива . Он также используется для продувки топлива и окислителя из наземного вспомогательного оборудования перед запуском и для предварительного охлаждения жидкого водорода в космических аппаратах . Например, ракете Saturn V , используемой в программе Apollo, требовалось около 370 000 кубических метров (13 миллионов кубических футов) гелия для запуска. [107]
Гелий как дыхательный газ не имеет наркотических свойств , поэтому гелиевые смеси, такие как тримикс , гелиокс и гелиэйр, используются для глубоких погружений , чтобы уменьшить эффекты наркоза, которые ухудшаются с увеличением глубины. [167] [168] По мере того, как давление увеличивается с глубиной, плотность дыхательного газа также увеличивается, и обнаружено, что низкий молекулярный вес гелия значительно снижает усилие дыхания за счет снижения плотности смеси. Это уменьшает число Рейнольдса потока, что приводит к уменьшению турбулентного потока и увеличению ламинарного потока , что требует меньшего дыхания. [169] [170] На глубине ниже 150 метров (490 футов) водолазы, дышащие гелий-кислородными смесями, начинают испытывать тремор и снижение психомоторной функции, симптомы нервного синдрома высокого давления . [171] Этот эффект можно в некоторой степени нейтрализовать, добавив в смесь гелия и кислорода определенное количество наркотического газа, например водорода или азота. [172]
Гелий-неоновые лазеры , тип маломощного газового лазера, создающего красный луч, имели различные практические применения, включая считыватели штрих-кодов и лазерные указки , прежде чем они были почти повсеместно заменены более дешевыми диодными лазерами . [27]
Благодаря своей инертности и высокой теплопроводности , прозрачности для нейтронов, а также тому, что он не образует радиоактивных изотопов в реакторных условиях, гелий используется в качестве теплоносителя в некоторых ядерных реакторах с газовым охлаждением . [164]
Гелий, смешанный с более тяжелым газом, таким как ксенон, полезен для термоакустического охлаждения из-за высокого коэффициента теплоемкости и низкого числа Прандтля . [173] Инертность гелия имеет экологические преимущества по сравнению с обычными холодильными системами, которые способствуют истощению озонового слоя или глобальному потеплению. [174]
Гелий также используется в некоторых жестких дисках . [175]
Использование гелия уменьшает искажающее воздействие температурных изменений в пространстве между линзами в некоторых телескопах из-за его чрезвычайно низкого показателя преломления . [29] Этот метод особенно используется в солнечных телескопах, где вакуумно-плотная телескопическая труба была бы слишком тяжелой. [176] [177]
Гелий является широко используемым газом-носителем в газовой хроматографии .
Возраст горных пород и минералов, содержащих уран и торий , можно оценить, измерив уровень гелия с помощью процесса, известного как гелиевое датирование . [27] [29]
Гелий при низких температурах используется в криогенике и в некоторых криогенных приложениях. В качестве примеров приложений, жидкий гелий используется для охлаждения некоторых металлов до чрезвычайно низких температур, необходимых для сверхпроводимости , например, в сверхпроводящих магнитах для магнитно-резонансной томографии . Большой адронный коллайдер в ЦЕРНе использует 96 метрических тонн жидкого гелия для поддержания температуры на уровне 1,9 К (−271,25 °C; −456,25 °F). [178]
Гелий был одобрен для медицинского применения в Соединенных Штатах в апреле 2020 года для людей и животных. [179] [180]
Хотя гелий химически инертен, он ухудшает работу микроэлектромеханических систем (МЭМС), из-за чего iPhone может выйти из строя. [181]
Нейтральный гелий при стандартных условиях нетоксичен, не играет биологической роли и обнаруживается в следовых количествах в крови человека.
Скорость звука в гелии почти в три раза превышает скорость звука в воздухе. Поскольку собственная резонансная частота газонаполненной полости пропорциональна скорости звука в газе, при вдыхании гелия происходит соответствующее увеличение резонансных частот голосового тракта , который является усилителем голосового звука. [27] [182] Это увеличение резонансной частоты усилителя (голосового тракта) дает повышенное усиление высокочастотных компонентов звуковой волны, создаваемой прямой вибрацией голосовых связок, по сравнению со случаем, когда голосовой аппарат заполнен воздухом. Когда человек говорит после вдыхания гелия, мышцы, управляющие голосовым аппаратом, по-прежнему двигаются так же, как и при заполнении голосового аппарата воздухом; поэтому основная частота ( иногда называемая высотой тона ), создаваемая прямой вибрацией голосовых складок, не изменяется. [183] Однако, предпочтительное усиление высоких частот вызывает изменение тембра усиленного звука, что приводит к пронзительному, утиному вокальному качеству. Противоположный эффект, снижение резонансных частот, может быть получен путем вдыхания плотного газа, такого как гексафторид серы или ксенон .
Вдыхание гелия может быть опасным, если его делать чрезмерно, так как гелий является простым удушающим веществом и поэтому вытесняет кислород, необходимый для нормального дыхания. [27] [184] Были зарегистрированы смертельные случаи, включая молодого человека, который задохнулся в Ванкувере в 2003 году, и двух взрослых, которые задохнулись в Южной Флориде в 2006 году. [185] [186] В 1998 году австралийская девочка из Виктории потеряла сознание и временно посинела после того, как вдохнула все содержимое воздушного шара для вечеринки. [187] [188] [189] Вдыхание гелия непосредственно из баллонов под давлением или даже из клапанов наполнения воздушных шаров чрезвычайно опасно, так как высокая скорость потока и давление могут привести к баротравме , смертельному разрыву легочной ткани. [184] [190]
Смерть от гелия случается редко. Первый зафиксированный в СМИ случай произошел с 15-летней девочкой из Техаса, которая умерла в 1998 году от вдыхания гелия на вечеринке у друга; точный тип смерти от гелия неизвестен. [187] [188] [189]
В Соединенных Штатах было зарегистрировано только два смертельных случая в период с 2000 по 2004 год, включая мужчину, который умер в Северной Каролине от баротравмы в 2002 году. [185] [190] Молодой человек задохнулся в Ванкувере в 2003 году, а у 27-летнего мужчины в Австралии случилась эмболия после дыхания из баллона в 2000 году. [185] С тех пор двое взрослых задохнулись в Южной Флориде в 2006 году, [185] [186] [191] и были случаи в 2009 и 2010 годах, одним из которых был молодой человек из Калифорнии, которого нашли с мешком на голове, прикрепленным к баллону с гелием, [192] а еще один подросток в Северной Ирландии умер от удушья. [193] В Игл-Пойнт, штат Орегон, в 2012 году от баротравмы на вечеринке умерла девочка-подросток. [194] [195] [196] Девочка из Мичигана умерла от гипоксии позже в том же году. [197]
4 февраля 2015 года выяснилось, что во время записи их главного телешоу 28 января 12-летняя участница (имя не разглашается) японской женской вокальной группы 3B Junior пострадала от воздушной эмболии , потеряв сознание и впав в кому из -за того, что пузырьки воздуха заблокировали приток крови к мозгу после вдыхания огромного количества гелия во время игры. Инцидент был обнародован лишь неделю спустя. [198] [199] Сотрудники TV Asahi провели экстренную пресс-конференцию, чтобы сообщить, что участница была доставлена в больницу и демонстрирует признаки реабилитации, такие как движение глаз и конечностей, но ее сознание еще недостаточно восстановилось. Полиция начала расследование в связи с пренебрежением мерами безопасности. [200] [201]
Вопросы безопасности для криогенного гелия аналогичны вопросам безопасности жидкого азота ; его чрезвычайно низкие температуры могут привести к холодным ожогам , а соотношение расширения жидкости и газа может вызвать взрывы, если не установлены устройства сброса давления. С контейнерами с гелием при температуре от 5 до 10 К следует обращаться так, как если бы они содержали жидкий гелий из-за быстрого и значительного теплового расширения , которое происходит, когда гелий при температуре менее 10 К нагревается до комнатной температуры . [107]
При высоких давлениях (более 20 атм или двух МПа ) смесь гелия и кислорода ( гелиокс ) может привести к нервному синдрому высокого давления , своего рода обратному анестезирующему эффекту; добавление небольшого количества азота в смесь может облегчить проблему. [202] [171]
и Локьер обнаружили, что желтые протуберанцы дают очень определенную яркую линию недалеко от D, но до сих пор не отождествляемую ни с каким земным пламенем. Кажется, это указывает на новое вещество, которое они предлагают назвать гелием
Raccolsi alcun tempo fa una sostanza amorfa di Constenza Butirracea e di colore giallo sbiadato sublimata sull'orlo di una fumarola prossima alla bocca di eruzione. Saggiata questa sublimazione allo spettroscopio, ho ravvisato le righe del sodio e del potassio ed una lineare ben distinta che corrisponde esattamente alla D
3
che è quella dell'Helium. Для того, чтобы сделать простое объявление о жире, пропонендоми риторнаре по поводу этого аргумента, докажите, что сублимация и химический анализ.
(Некоторое время назад я собрал аморфное вещество, имеющее маслянистую консистенцию и блеклую желтую окраску, которое сублимировалось на краю фумаролы вблизи устья извержения. Проанализировав это сублимированное вещество с помощью спектроскопа, я распознал линии натрия и калий и очень отчетливая линейная линия, которая точно соответствует D
3
, то есть гелию. В настоящее время я просто объявляю об этом факте, предлагая вернуться к этой теме после того, как подвергну сублимат химическому анализу .)
У истоков метода обнаружения утечек гелия стоял Манхэттенский проект и беспрецедентные требования к герметичности, предъявляемые к заводам по обогащению урана. Требуемая чувствительность, необходимая для проверки утечек, привела к выбору масс-спектрометра, разработанного доктором AOC Nier, настроенного на массу гелия.
{{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка )Общий
Подробнее
Разнообразный
Нехватка гелия