Титан — химический элемент ; его символ Ti , атомный номер 22. Встречающийся в природе только в виде оксида , он может быть восстановлен до блестящего переходного металла серебристого цвета , с низкой плотностью и высокой прочностью, устойчивого к коррозии в морской воде , царской водке и хлоре .
Титан был открыт в Корнуолле , Великобритания , Уильямом Грегором в 1791 году и был назван Мартином Генрихом Клапротом в честь титанов из греческой мифологии . Элемент встречается в ряде минералов , в основном в рутиле и ильмените , которые широко распространены в земной коре и литосфере ; он встречается почти во всех живых существах, а также в водоемах, горных породах и почвах. [10] Металл извлекается из его основных минеральных руд с помощью процессов Кролла и Хантера . [11] Наиболее распространенное соединение, диоксид титана , является популярным фотокатализатором и используется в производстве белых пигментов. [12] Другие соединения включают тетрахлорид титана (TiCl4 ) , компонент дымовых завес и катализаторов ; и трихлорид титана (TiCl3 ) , который используется в качестве катализатора при производстве полипропилена . [10]
Титан может быть сплавлен с железом , алюминием , ванадием и молибденом , среди других элементов. Полученные титановые сплавы прочные, легкие и универсальные, с приложениями, включая аэрокосмическую промышленность ( реактивные двигатели , ракеты и космические корабли ), военную промышленность, промышленные процессы (химия и нефтехимия, опреснительные установки , целлюлоза и бумага ), автомобилестроение, сельское хозяйство (фермерство), спортивные товары, ювелирные изделия и бытовая электроника . [10] Титан также считается одним из самых биосовместимых металлов, что приводит к ряду медицинских применений, включая протезы , ортопедические имплантаты , зубные имплантаты и хирургические инструменты . [13]
Два самых полезных свойства металла — коррозионная стойкость и отношение прочности к плотности , самое высокое среди всех металлических элементов. [14] В нелегированном состоянии титан такой же прочный, как некоторые стали , но менее плотный. [15] Существуют две аллотропные формы [16] и пять встречающихся в природе изотопов этого элемента, от 46 Ti до 50 Ti, причем 48 Ti является наиболее распространенным (73,8%). [17]
Как металл , титан известен своим высоким отношением прочности к весу . [16] Это прочный металл с низкой плотностью , который является довольно пластичным (особенно в бескислородной среде), [10] блестящим и имеет металлически-белый цвет . [18] Из-за своей относительно высокой температуры плавления (1668 °C или 3034 °F) его иногда описывают как тугоплавкий металл , но это не так. [19] Он парамагнитен и имеет довольно низкую электро- и теплопроводность по сравнению с другими металлами. [10] Титан становится сверхпроводящим при охлаждении ниже своей критической температуры 0,49 К. [20] [21]
Коммерчески чистые (99,2% чистоты) сорта титана имеют предел прочности на растяжение около 434 МПа (63 000 фунтов на квадратный дюйм ), что равно прочности обычных низкосортных стальных сплавов, но они менее плотные. Титан на 60% плотнее алюминия, но более чем в два раза прочнее [15], чем наиболее часто используемый алюминиевый сплав 6061-T6 . Некоторые титановые сплавы (например, Beta C ) достигают предела прочности на растяжение более 1400 МПа (200 000 фунтов на квадратный дюйм). [22] Однако титан теряет прочность при нагревании выше 430 °C (806 °F). [23]
Титан не такой твердый, как некоторые виды термообработанной стали; он немагнитен и плохо проводит тепло и электричество. Обработка требует мер предосторожности, поскольку материал может царапаться, если не использовать острые инструменты и не использовать надлежащие методы охлаждения. Как и стальные конструкции, конструкции из титана имеют предел усталости , который гарантирует долговечность в некоторых применениях. [18]
Металл представляет собой диморфный аллотроп гексагональной плотноупакованной α-формы, которая переходит в объемно-центрированную кубическую (решетчатую) β-форму при 882 °C (1620 °F). [23] [24] Удельная теплоемкость α-формы резко возрастает по мере нагревания до этой температуры перехода, но затем падает и остается довольно постоянной для β-формы независимо от температуры. [23]
Подобно алюминию и магнию , поверхность титана и его сплавов немедленно окисляются при контакте с воздухом, образуя тонкий непористый пассивирующий слой, который защищает основной металл от дальнейшего окисления или коррозии. [10] Когда этот защитный слой впервые образуется, его толщина составляет всего 1–2 нм , но он продолжает медленно расти, достигая толщины 25 нм за четыре года. [26] Этот слой придает титану отличную устойчивость к коррозии под воздействием окисляющих кислот, но он растворяется в разбавленной плавиковой кислоте , горячей соляной кислоте и горячей серной кислоте.
Титан способен выдерживать воздействие разбавленных серной и соляной кислот при комнатной температуре, растворов хлоридов и большинства органических кислот. [11] Однако титан разъедается концентрированными кислотами. [27] Титан — очень реактивный металл, который горит на обычном воздухе при температурах ниже точки плавления. Плавление возможно только в инертной атмосфере или вакууме. При температуре 550 °C (1022 °F) он соединяется с хлором. [11] Он также реагирует с другими галогенами и поглощает водород. [12]
Титан легко реагирует с кислородом при 1200 °C (2190 °F) на воздухе и при 610 °C (1130 °F) в чистом кислороде, образуя диоксид титана . [16] Титан является одним из немногих элементов, которые горят в чистом азоте, реагируя при 800 °C (1470 °F) с образованием нитрида титана , который вызывает хрупкость. [28] Из-за своей высокой реакционной способности с кислородом, азотом и многими другими газами титан, который испаряется из нитей , является основой для титановых сублимационных насосов , в которых титан служит поглотителем этих газов, химически связываясь с ними. Такие насосы недорого производят чрезвычайно низкие давления в сверхвысоковакуумных системах.
Титан является девятым по распространенности элементом в земной коре (0,63% по массе ) [29] и седьмым по распространенности металлом. Он присутствует в виде оксидов в большинстве магматических пород , в отложениях, полученных из них, в живых существах и естественных водоемах. [10] [11] Из 801 типа магматических пород, проанализированных Геологической службой США , 784 содержали титан. Его доля в почвах составляет приблизительно 0,5–1,5%. [29]
Распространенными титансодержащими минералами являются анатаз , брукит , ильменит , перовскит , рутил и титанит (сфен). [26] Акаогиит — чрезвычайно редкий минерал, состоящий из диоксида титана. Из этих минералов только рутил и ильменит имеют экономическое значение, но даже их трудно найти в высоких концентрациях. Около 6,0 и 0,7 млн тонн этих минералов было добыто в 2011 году соответственно. [30] Значительные месторождения титансодержащего ильменита существуют в Австралии , Канаде , Китае , Индии , Мозамбике , Новой Зеландии , Норвегии , Сьерра-Леоне , Южной Африке и Украине . [26] Около 210 000 тонн титановой металлической губки было произведено в 2020 году, в основном в Китае (110 000 тонн), Японии (50 000 тонн), России (33 000 тонн) и Казахстане (15 000 тонн). Общие запасы анатаза, ильменита и рутила оцениваются более чем в 2 миллиарда тонн. [30]
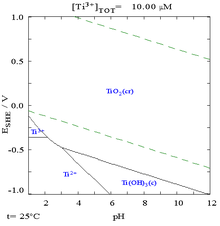
Концентрация титана в океане составляет около 4 пикомоляр . При 100 °C концентрация титана в воде оценивается менее чем в 10−7 M при pH 7. Идентичность видов титана в водном растворе остается неизвестной из-за его низкой растворимости и отсутствия чувствительных спектроскопических методов, хотя только степень окисления 4+ является стабильной на воздухе. Нет никаких доказательств биологической роли, хотя известно, что редкие организмы накапливают высокие концентрации титана. [31]
Титан содержится в метеоритах , и он был обнаружен на Солнце и в звездах М-типа [11] (самый холодный тип) с температурой поверхности 3200 °C (5790 °F). [32] Камни , привезенные с Луны во время миссии Аполлон-17, состоят из 12,1% TiO 2 . [11] Самородный титан (чистый металлический) встречается очень редко. [33]
Природный титан состоит из пяти стабильных изотопов : 46 Ti, 47 Ti, 48 Ti, 49 Ti и 50 Ti, причем 48 Ti является наиболее распространенным (73,8% естественного содержания ). Было охарактеризовано по крайней мере 21 радиоизотоп , наиболее стабильными из которых являются 44 Ti с периодом полураспада 63 года; 45 Ti, 184,8 минут; 51 Ti, 5,76 минут; и 52 Ti, 1,7 минут. Все остальные радиоактивные изотопы имеют период полураспада менее 33 секунд, причем большинство из них менее половины секунды. [17]
Изотопы титана имеют атомный вес от39.002 Да ( 39 Ти) до63,999 Да ( 64 Ti). [34] Основной режим распада для изотопов легче 46 Ti — это позитронная эмиссия (за исключением 44 Ti, который подвергается захвату электронов ), приводящая к образованию изотопов скандия , а основной режим для изотопов тяжелее 50 Ti — это бета-эмиссия , приводящая к образованию изотопов ванадия . [17]
Титан становится радиоактивным при бомбардировке дейтронами , испуская в основном позитроны и жесткие гамма-лучи . [11]

Степень окисления +4 доминирует в химии титана, [35] но соединения в степени окисления +3 также многочисленны. [36] Обычно титан принимает октаэдрическую координационную геометрию в своих комплексах, [37] [38] но тетраэдрический TiCl 4 является заметным исключением. Из-за своей высокой степени окисления соединения титана(IV) демонстрируют высокую степень ковалентной связи . [35]
Наиболее важным оксидом является TiO 2 , который существует в трех важных полиморфах : анатаз, брукит и рутил. Все три являются белыми диамагнитными твердыми веществами, хотя образцы минералов могут казаться темными (см. рутил ). Они принимают полимерные структуры, в которых Ti окружен шестью оксидными лигандами, которые связываются с другими центрами Ti. [39]
Термин титанаты обычно относится к соединениям титана(IV), представленным титанатом бария (BaTiO 3 ). Имея структуру перовскита, этот материал проявляет пьезоэлектрические свойства и используется в качестве преобразователя при взаимопревращении звука и электричества . [16] Многие минералы являются титанатами, например, ильменит (FeTiO 3 ). Звездчатые сапфиры и рубины получают свой астеризм (звездообразный блеск) из-за присутствия примесей диоксида титана. [26]
Известны различные восстановленные оксиды ( субоксиды ) титана, в основном восстановленные стехиометрии диоксида титана, полученные методом атмосферного плазменного распыления . Ti 3 O 5 , описанный как разновидность Ti(IV)-Ti(III), представляет собой фиолетовый полупроводник, полученный путем восстановления TiO 2 водородом при высоких температурах, [40] и используется в промышленности, когда поверхности необходимо покрыть парами диоксида титана: он испаряется как чистый TiO, тогда как TiO 2 испаряется как смесь оксидов и осаждает покрытия с переменным показателем преломления. [41] Также известны Ti 2 O 3 , со структурой корунда , и TiO , со структурой каменной соли , хотя часто нестехиометрические . [42]
Алкоксиды титана(IV), полученные путем обработки TiCl4 спиртами , представляют собой бесцветные соединения, которые при реакции с водой превращаются в диоксид. Они используются в промышленности для осаждения твердого TiO2 с помощью золь-гель процесса . Изопропоксид титана используется в синтезе хиральных органических соединений с помощью эпоксидирования Шарплесса . [43]
Титан образует множество сульфидов, но только TiS2 привлек значительный интерес. Он принимает слоистую структуру и использовался в качестве катода при разработке литиевых батарей . Поскольку Ti(IV) является «жестким катионом» , сульфиды титана нестабильны и имеют тенденцию гидролизоваться до оксида с выделением сероводорода . [ 44]
Нитрид титана (TiN) — тугоплавкое твердое вещество, обладающее чрезвычайной твердостью, тепло- и электропроводностью и высокой температурой плавления. [45] TiN имеет твердость, эквивалентную сапфиру и карборунду (9,0 по шкале Мооса ), [46] и часто используется для покрытия режущих инструментов, таких как сверла . [47] Он также используется в качестве декоративного покрытия золотистого цвета и в качестве барьерного слоя при производстве полупроводников . [48] Карбид титана (TiC), который также очень тверд, используется в режущих инструментах и покрытиях. [49]

Тетрахлорид титана (хлорид титана (IV), TiCl 4 [50] ) представляет собой бесцветную летучую жидкость (коммерческие образцы желтоватые), которая на воздухе гидролизуется с эффектным выделением белых облаков. С помощью процесса Кролла TiCl 4 используется для преобразования титановых руд в металлический титан. Тетрахлорид титана также используется для получения диоксида титана, например, для использования в белой краске. [51] Он широко используется в органической химии в качестве кислоты Льюиса , например, в альдольной конденсации Мукаямы . [52] В процессе Ван Аркеля-де Бура тетраиодид титана (TiI 4 ) образуется при производстве металлического титана высокой чистоты. [53]
Титан(III) и титан(II) также образуют стабильные хлориды. Ярким примером является хлорид титана(III) (TiCl3 ) , который используется в качестве катализатора для производства полиолефинов (см. катализатор Циглера-Натта ) и восстановителя в органической химии. [54]
В связи с важной ролью соединений титана как катализатора полимеризации , интенсивно изучаются соединения со связями Ti-C. Наиболее распространенным органотитано-комплексом является дихлорид титаноцена ((C 5 H 5 ) 2 TiCl 2 ). Родственные соединения включают реагент Теббе и реагент Петазиса . Титан образует карбонильные комплексы , например (C 5 H 5 ) 2 Ti(CO) 2 . [55]
После успеха химиотерапии на основе платины , комплексы титана(IV) были одними из первых неплатиновых соединений, которые были протестированы для лечения рака. Преимущество соединений титана заключается в их высокой эффективности и низкой токсичности in vivo . [56] В биологических средах гидролиз приводит к безопасному и инертному диоксиду титана. Несмотря на эти преимущества, первые соединения-кандидаты не прошли клинические испытания из-за недостаточного соотношения эффективности к токсичности и сложностей с формулировкой. [56] Дальнейшие разработки привели к созданию потенциально эффективных, селективных и стабильных препаратов на основе титана. [56]

Титан был открыт в 1791 году священнослужителем и геологом Уильямом Грегором как включение минерала в Корнуолле , Великобритания. [57] Грегор узнал о наличии нового элемента в ильмените [12] , когда он нашел черный песок у ручья и заметил, что песок притягивается магнитом . [ 57] Анализируя песок, он определил наличие двух оксидов металлов: оксида железа (объясняющего притяжение к магниту) и 45,25% белого металлического оксида, который он не мог идентифицировать. [29] Поняв, что неопознанный оксид содержит металл, который не соответствует ни одному известному элементу, в 1791 году Грегор сообщил о своих открытиях как в немецких, так и во французских научных журналах: Crell's Annalen и Observations et Mémoires sur la Physique . [57] [58] [59] Он назвал этот оксид манакканитом . [60]
Примерно в то же время Франц-Йозеф Мюллер фон Райхенштейн получил похожее вещество, но не смог его идентифицировать. [12] Оксид был независимо заново открыт в 1795 году прусским химиком Мартином Генрихом Клапротом в рутиле из Бойника (немецкое название Баймочка), деревни в Венгрии (ныне Бойнички в Словакии). [57] [b] Клапрот обнаружил, что он содержит новый элемент, и назвал его в честь титанов греческой мифологии . [32] Услышав о более раннем открытии Грегора, он получил образец манакканита и подтвердил, что он содержит титан. [62]
Известные в настоящее время процессы извлечения титана из различных руд трудоемки и дороги; невозможно восстановить руду путем нагревания с углеродом (как при выплавке железа), поскольку титан соединяется с углеродом, образуя карбид титана. [57] Чистый металлический титан (99,9%) был впервые получен в 1910 году Мэтью А. Хантером в Политехническом институте Ренсселера путем нагревания TiCl4 с натрием при 700–800 °C (1292–1472 °F) под большим давлением [63] в периодическом процессе, известном как процесс Хантера . [11] Металлический титан не использовался за пределами лаборатории до 1932 года, когда Уильям Джастин Кролл получил его путем восстановления тетрахлорида титана (TiCl4 ) кальцием . [ 64] Восемь лет спустя он усовершенствовал этот процесс с помощью магния и натрия в том, что стало известно как процесс Кролла. [64] Хотя исследования продолжают искать более дешевые и эффективные пути, такие как процесс FFC Cambridge , процесс Кролла по-прежнему в основном используется для коммерческого производства. [11] [12]

Титан очень высокой чистоты был получен в небольших количествах, когда Антон Эдуард ван Аркель и Ян Хендрик де Бур в 1925 году открыли йодидный процесс, реагируя с йодом и разлагая образовавшиеся пары над горячей нитью накаливания до чистого металла. [65]
В 1950-х и 1960-х годах Советский Союз был пионером в использовании титана в военных целях и на подводных лодках [63] ( классы «Альфа» и «Майк» ) [66] в рамках программ, связанных с холодной войной. [67] Начиная с начала 1950-х годов титан стал широко использоваться в военной авиации, особенно в высокопроизводительных реактивных самолетах, начиная с таких самолетов, как F-100 Super Sabre и Lockheed A-12 и SR-71 . [68]
На протяжении всего периода холодной войны правительство США считало титан стратегическим материалом , и большой запас титановой губки (пористая форма чистого металла) поддерживался Национальным центром запасов обороны , пока запасы не были рассредоточены в 2000-х годах. [69] По состоянию на 2021 год четырьмя ведущими производителями титановой губки были Китай (52%), Япония (24%), Россия (16%) и Казахстан (7%). [30]


Процесс Хантера был первым промышленным процессом для получения чистого металлического титана. Он был изобретен в 1910 году Мэтью А. Хантером , химиком, родившимся в Новой Зеландии и работавшим в Соединенных Штатах. [71] Процесс включает восстановление тетрахлорида титана (TiCl 4 ) натрием (Na) в реакторе периодического действия с инертной атмосферой при температуре 1000 °C. Затем разбавленная соляная кислота используется для выщелачивания соли из продукта. [72]
Обработка титанового металла происходит в четыре основных этапа: преобразование титановой руды в «губку», пористую форму; плавка губки или губки с лигатурой для формирования слитка; первичное изготовление, где слиток преобразуется в обычные прокатные изделия, такие как заготовки , прутки, пластины , листы , полосы и трубы ; и вторичное изготовление готовых форм из прокатных изделий. [73]
Поскольку его нельзя легко получить путем восстановления диоксида титана, [18] металлический титан получают путем восстановления тетрахлорида титана (TiCl4 ) металлическим магнием в процессе Кролла. Сложность этого серийного производства в процессе Кролла объясняет относительно высокую рыночную стоимость титана, [74] несмотря на то, что процесс Кролла менее затратен, чем процесс Хантера. [63] Для получения TiCl4 , необходимого для процесса Кролла, диоксид подвергают карботермическому восстановлению в присутствии хлора . В этом процессе газообразный хлор пропускают над раскаленной смесью рутила или ильменита в присутствии углерода. После тщательной очистки фракционной перегонкой TiCl4 восстанавливают расплавленным магнием при температуре 800 °C ( 1470 °F) в атмосфере аргона . [16]
Процесс Ван Аркеля–де Бура был первым полупромышленным процессом получения чистого титана. Он включает термическое разложение тетраиодида титана .
Титановый порошок производится с использованием поточного процесса производства, известного как процесс Армстронга [75] , который похож на процесс Хантера для пакетного производства . Поток газа тетрахлорида титана добавляется к потоку расплавленного натрия; продукты (соль хлорида натрия и частицы титана) фильтруются от излишков натрия. Затем титан отделяется от соли промывкой водой. И натрий, и хлор перерабатываются для производства и переработки большего количества тетрахлорида титана. [76]
Методы электролитического производства металлического Ti из TiO 2 с использованием расплавленных солевых электролитов были исследованы и испытаны в лабораторных и небольших пилотных масштабах. Ведущий автор беспристрастного обзора, опубликованного в 2017 году, считал свой собственный процесс «готовым к масштабированию». [77] Обзор 2023 года «обсуждает электрохимические принципы, используемые при восстановлении металлов из водных растворов и расплавленных солевых электролитов», причем особое внимание уделяется титану. В то время как некоторые металлы, такие как никель и медь, могут быть очищены электролизом при комнатной температуре, титан должен находиться в расплавленном состоянии, и «существует большая вероятность воздействия расплавленного титана на огнеупорную футеровку». [78] Чжан и др. в своей работе «Перспективы термохимических и электрохимических процессов для производства металлического титана» в 2017 году пришли к выводу, что «несмотря на то, что в отрасли существует сильная заинтересованность в поиске лучшего метода производства металлического титана, и большое количество новых концепций и усовершенствований было исследовано в лабораторных условиях или даже в масштабах пилотных установок, на сегодняшний день не существует нового процесса, который мог бы заменить процесс Кролла в коммерческих целях». [79]
В процессе магнезиотермического восстановления с участием водорода (HAMR) используется дигидрид титана .

Вся сварка титана должна выполняться в инертной атмосфере аргона или гелия , чтобы защитить его от загрязнения атмосферными газами (кислородом, азотом и водородом). [23] Загрязнение вызывает различные состояния, такие как охрупчивание , которые снижают целостность сварных швов и приводят к разрушению соединений. [80]
Титан очень трудно паять напрямую, поэтому паяемый металл или сплав, такой как сталь, покрывают титаном перед пайкой. [81] Титан можно обрабатывать на том же оборудовании и теми же процессами, что и нержавеющую сталь . [23]
Обычные титановые сплавы изготавливаются методом восстановления. Например, восстанавливаются купротитан (рутил с добавлением меди ), ферроуглеродистый титан (ильменит, восстановленный коксом в электропечи) и манганотитан (рутил с марганцем или оксидами марганца). [82]
Около пятидесяти марок титановых сплавов разработаны и в настоящее время используются, хотя только пара десятков легкодоступны в продаже. [83] ASTM International признает 31 марку титанового металла и сплавов, из которых марки с первой по четвертую являются коммерчески чистыми (нелегированными). Эти четыре марки различаются по пределу прочности на разрыв в зависимости от содержания кислорода, причем марка 1 является наиболее пластичной (самая низкая прочность на разрыв при содержании кислорода 0,18%), а марка 4 — наименее пластичной (самая высокая прочность на разрыв при содержании кислорода 0,40%). [26] Остальные марки представляют собой сплавы, каждая из которых разработана для определенных свойств пластичности, прочности, твердости, электрического сопротивления, сопротивления ползучести , удельной коррозионной стойкости и их комбинаций. [84]
В дополнение к спецификациям ASTM, титановые сплавы также производятся в соответствии со спецификациями аэрокосмической и военной промышленности (SAE-AMS, MIL-T), стандартами ISO и спецификациями, характерными для конкретных стран, а также фирменными спецификациями конечного пользователя для аэрокосмической, военной, медицинской и промышленной отраслей. [85]
Коммерчески чистый плоский продукт (лист, пластина) может быть легко сформирован, но обработка должна учитывать тенденцию металла к пружинению . Это особенно верно для некоторых высокопрочных сплавов. [86] [87] Воздействие кислорода воздуха при повышенных температурах, используемых при ковке, приводит к образованию хрупкого богатого кислородом металлического поверхностного слоя, называемого « альфа-корпус », который ухудшает усталостные свойства, поэтому его необходимо удалять фрезерованием, травлением или электрохимической обработкой. [88] Обработка титана очень сложна, [89] [90] [91] и может включать сварку трением , [92] криоковку, [93] и вакуумную дуговую переплавку .

Титан используется в стали в качестве легирующего элемента ( ферротитан ) для уменьшения размера зерна и как раскислитель , а в нержавеющей стали для уменьшения содержания углерода. [10] Титан часто легируют алюминием (для измельчения размера зерна), ванадием , медью (для закалки), железом , марганцем , молибденом и другими металлами. [94] Титановые прокатные изделия (листы, пластины, прутки, проволока, поковки, отливки) находят применение в промышленности, аэрокосмической отрасли, рекреации и на развивающихся рынках. Порошкообразный титан используется в пиротехнике как источник ярко горящих частиц. [95]
_oxide.jpg/440px-Titanium(IV)_oxide.jpg)
Около 95% всей титановой руды направляется на переработку в диоксид титана ( TiO
2), интенсивно белый постоянный пигмент, используемый в красках, бумаге, зубной пасте и пластмассах. [30] Он также используется в цементе, драгоценных камнях и в качестве оптического глушителя в бумаге. [96]
TiO
2Пигмент химически инертен, устойчив к выцветанию на солнце и очень непрозрачен: он придает чистый и блестящий белый цвет коричневым или серым химикатам, которые образуют большинство бытовых пластиков. [12] В природе это соединение встречается в минералах анатаз, брукит и рутил. [10] Краска, изготовленная с использованием диоксида титана, хорошо переносит суровые температуры и морскую среду. [12] Чистый диоксид титана имеет очень высокий показатель преломления и оптическую дисперсию выше, чем у алмаза . [11] Диоксид титана используется в солнцезащитных кремах, поскольку он отражает и поглощает ультрафиолетовый свет . [18]

Поскольку титановые сплавы имеют высокое отношение предела прочности к плотности, [16] высокую коррозионную стойкость , [11] усталостную стойкость, высокую трещиностойкость, [97] и способность выдерживать умеренно высокие температуры без ползучести, они используются в самолетах, броневых покрытиях, военных кораблях, космических аппаратах и ракетах. [11] [12] Для этих целей титан легируют алюминием, цирконием, никелем, [98] ванадием и другими элементами для производства различных компонентов, включая критически важные структурные детали, шасси , противопожарные экраны , выхлопные трубы (вертолеты) и гидравлические системы. Фактически, около двух третей всего произведенного титанового металла используется в авиационных двигателях и рамах. [99] Титановый сплав 6AL-4V составляет почти 50% всех сплавов, используемых в авиационных приложениях. [100]
Lockheed A-12 и SR-71 «Blackbird» были двумя из первых каркасов самолетов, где использовался титан, что проложило путь для гораздо более широкого использования в современных военных и коммерческих самолетах. Большое количество титановых прокатных изделий используется в производстве многих самолетов, таких как (следующие значения представляют собой количество использованных сырых прокатных изделий, только часть из них попадает в готовый самолет): 116 метрических тонн используются в Boeing 787 , 77 в Airbus A380 , 59 в Boeing 777 , 45 в Boeing 747 , 32 в Airbus A340 , 18 в Boeing 737 , 18 в Airbus A330 и 12 в Airbus A320 . [101] В авиационных двигателях титан используется для роторов, лопаток компрессора, компонентов гидравлической системы и гондол . [102] [103] Раннее использование в реактивных двигателях было на самолете Orenda Iroquois в 1950-х годах. [ необходим лучший источник ] [104]
Поскольку титан устойчив к коррозии в морской воде, его используют для изготовления гребных валов, такелажа, теплообменников в опреснительных установках , [11] нагревателей-охладителей для аквариумов с соленой водой, лески и поводка, а также ножей водолазов. Титан используется в корпусах и компонентах океанских разведывательных и контрольных устройств для науки и военных. В бывшем Советском Союзе были разработаны методы изготовления подводных лодок с корпусами из титановых сплавов, [105] ковки титана в огромных вакуумных трубках. [98]

Сварные титановые трубы и технологическое оборудование (теплообменники, резервуары, технологические сосуды, клапаны) используются в химической и нефтехимической промышленности в первую очередь для коррозионной стойкости. Определенные сплавы используются в нефтяных и газовых скважинах и в гидрометаллургии никеля из-за их высокой прочности (например, титановый бета-C сплав), коррозионной стойкости или того и другого. Целлюлозно -бумажная промышленность использует титан в технологическом оборудовании, подвергающемся воздействию агрессивных сред, таких как гипохлорит натрия или влажный хлорный газ (в отбеливании). [106] Другие области применения включают ультразвуковую сварку , пайку волной припоя , [107] и распыляемые мишени. [108]
Тетрахлорид титана (TiCl 4 ), бесцветная жидкость, играет важную роль в качестве промежуточного продукта в процессе получения TiO 2 , а также используется для производства катализатора Циглера-Натта. Тетрахлорид титана также используется для иридизации стекла и, поскольку он сильно дымит во влажном воздухе, его используют для изготовления дымовых завес. [18]

Титановый металл используется в автомобильной промышленности, особенно в гонках на автомобилях и мотоциклах, где решающее значение имеют малый вес, высокая прочность и жесткость. [109] (стр. 141) Этот металл, как правило, слишком дорог для массового потребительского рынка, хотя некоторые последние модели Corvette выпускались с титановыми выхлопными трубами, [110] а в двигателе Corvette Z06 с наддувом LT4 используются легкие, цельные титановые впускные клапаны для большей прочности и устойчивости к нагреву. [111]
Титан используется во многих спортивных товарах: теннисных ракетках, клюшках для гольфа, клюшках для лакросса; решетках для шлемов для крикета, хоккея, лакросса и футбола, а также рамах и компонентах велосипедов. Хотя титановые велосипеды не являются основным материалом для производства велосипедов, их использовали гоночные команды и любители велоспорта . [112]
Титановые сплавы используются в оправах для очков, которые довольно дороги, но очень прочны, долговечны, легки и не вызывают кожной аллергии. Титан является распространенным материалом для походной посуды и столовых приборов. Хотя они дороже традиционных стальных или алюминиевых альтернатив, титановые изделия могут быть значительно легче без ущерба для прочности. Кузнецы предпочитают титановые подковы стальным, потому что они легче и долговечнее. [113]
.jpg/440px-El_Guggenheim_vizcaíno._(1454058701).jpg)
Титан иногда использовался в архитектуре. 42,5-метровый (139 футов) памятник Юрию Гагарину , первому человеку, совершившему полет в космос ( 55°42′29.7″N 37°34′57.2″E / 55.708250°N 37.582556°E / 55.708250; 37.582556 ), а также 110-метровый (360 футов) памятник Покорителям космоса на крыше Музея космонавтов в Москве изготовлены из титана из-за привлекательного цвета металла и ассоциации с ракетной техникой. [114] [115] Музей Гуггенхайма в Бильбао и Библиотека Миллениум Серритоса были первыми зданиями в Европе и Северной Америке, соответственно, которые были обшиты титановыми панелями. [99] Титановая обшивка использовалась в здании Фредерика К. Гамильтона в Денвере, штат Колорадо. [116]
Из-за превосходной прочности и легкости титана по сравнению с другими металлами (сталь, нержавеющая сталь и алюминий), а также из-за недавних достижений в области металлообработки, его использование стало более распространенным в производстве огнестрельного оружия. Основные области применения включают рамки пистолетов и револьверные цилиндры. По тем же причинам он используется в корпусе некоторых ноутбуков (например, в PowerBook G4 от Apple ). [117] [118]
В 2023 году Apple выпустила iPhone 15 Pro , в котором используется титановый корпус. [119]
Некоторые высококачественные легкие и устойчивые к коррозии инструменты, такие как лопаты, рукоятки ножей и фонарики, изготавливаются из титана или титановых сплавов. [118]

Из-за своей прочности титан стал более популярным для дизайнерских украшений (в частности, титановых колец ). [113] Его инертность делает его хорошим выбором для людей с аллергией или тех, кто будет носить украшения в таких местах, как бассейны. Титан также сплавляют с золотом для получения сплава, который может продаваться как 24-каратное золото, потому что 1% легированного Ti недостаточно, чтобы требовать меньшей пробы. Полученный сплав имеет примерно такую же твердость, как 14-каратное золото, и более долговечен, чем чистое 24-каратное золото. [120]
Прочность титана, его малый вес, а также устойчивость к вмятинам и коррозии делают его пригодным для корпусов часов . [113] Некоторые художники работают с титаном для создания скульптур, декоративных предметов и мебели. [121]
Титан может быть анодирован для изменения толщины поверхностного оксидного слоя, вызывая оптические интерференционные полосы и множество ярких цветов. [122] Благодаря этой окраске и химической инертности титан является популярным металлом для пирсинга . [123]
Титан используется в небольших количествах в специальных нециркуляционных монетах и медалях. В 1999 году Гибралтар выпустил первую в мире титановую монету к празднованию тысячелетия. [124] Gold Coast Titans , австралийская команда регбийной лиги, награждает своего игрока года медалью из чистого титана. [125]
Поскольку титан биосовместим (нетоксичен и не отторгается организмом), он имеет множество медицинских применений, включая хирургические инструменты и имплантаты, такие как бедренные шары и гнезда ( замена суставов ) и зубные имплантаты , которые могут оставаться на месте до 20 лет. [57] Титан часто легируют примерно 4% алюминия или 6% Al и 4% ванадия. [126]

Титан обладает присущей ему способностью к остеоинтеграции , что позволяет использовать его в зубных имплантатах , которые могут прослужить более 30 лет. Это свойство также полезно для ортопедических имплантатов. [57] Они выигрывают от более низкого модуля упругости титана ( модуля Юнга ), чтобы более точно соответствовать модулю упругости кости, которую такие устройства предназначены для восстановления. В результате скелетные нагрузки более равномерно распределяются между костью и имплантатом, что приводит к снижению частоты деградации кости из-за экранирования напряжения и перипротезных переломов кости, которые происходят на границах ортопедических имплантатов. Однако жесткость титановых сплавов по-прежнему более чем в два раза превышает жесткость кости, поэтому прилегающая кость несет значительно меньшую нагрузку и может разрушаться. [127] [128]
Поскольку титан не является ферромагнитным , пациентов с титановыми имплантатами можно безопасно обследовать с помощью магнитно-резонансной томографии (удобно для долгосрочных имплантатов). Подготовка титана к имплантации в организм включает в себя воздействие на него высокотемпературной плазменной дуги, которая удаляет поверхностные атомы, обнажая свежий титан, который мгновенно окисляется. [57]
Современные достижения в области аддитивных технологий производства увеличили потенциал использования титана в ортопедических имплантатах. [129] Сложные конструкции каркасов имплантатов могут быть напечатаны на 3D-принтере с использованием титановых сплавов, что позволяет применять их более индивидуально для каждого пациента и повышает остеоинтеграцию имплантатов. [130]
Титан используется для хирургических инструментов, используемых в хирургии под контролем изображений , а также для инвалидных кресел, костылей и любых других изделий, где желательны высокая прочность и малый вес. [131]
Наночастицы диоксида титана широко используются в электронике, а также для доставки фармацевтических препаратов и косметики. [132]
Из-за своей коррозионной стойкости контейнеры из титана были изучены для долгосрочного хранения ядерных отходов. Контейнеры, которые прослужат более 100 000 лет, считаются возможными при производственных условиях, которые минимизируют дефекты материала. [133] Титановый «капельный щит» также может быть установлен над контейнерами других типов для повышения их долговечности. [134]
Титан нетоксичен даже в больших дозах и не играет никакой естественной роли в организме человека . [32] По оценкам, ежедневно человек потребляет около 0,8 миллиграмма титана, но большая его часть проходит через него, не всасываясь в ткани. [32] Однако иногда он биоаккумулируется в тканях, содержащих кремний . Одно исследование указывает на возможную связь между титаном и синдромом желтых ногтей . [135]
В виде порошка или металлической стружки титановый металл представляет значительную пожароопасность, а при нагревании на воздухе — опасность взрыва. [136] Вода и углекислый газ неэффективны для тушения титанового пожара; вместо них следует использовать сухие порошковые огнетушащие вещества класса D. [12]
При использовании в производстве или обращении с хлором титан не следует подвергать воздействию сухого хлорного газа, поскольку это может привести к возгоранию титана и хлора. [137]
Титан может загореться, когда свежая, неокисленная поверхность вступает в контакт с жидким кислородом . [138]

Неизвестный механизм в растениях может использовать титан для стимуляции производства углеводов и поощрения роста. Это может объяснить, почему большинство растений содержат около 1 части на миллион (ppm) титана, пищевые растения содержат около 2 ppm, а хвощ и крапива содержат до 80 ppm. [32]
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на май 2024 г. ( ссылка )