

Карбонилы металлов — координационные комплексы переходных металлов с лигандами монооксида углерода . Карбонилы металлов полезны в органическом синтезе и в качестве катализаторов или предшественников катализаторов в гомогенном катализе , таком как гидроформилирование и химия Реппе . В процессе Монда тетракарбонил никеля используется для получения чистого никеля . В металлоорганической химии карбонилы металлов служат предшественниками для получения других металлоорганических комплексов.
Карбонилы металлов токсичны при контакте с кожей, вдыхании или проглатывании, отчасти из-за их способности карбонилировать гемоглобин с образованием карбоксигемоглобина , который предотвращает связывание кислорода . [1]
Номенклатура карбонилов металлов зависит от заряда комплекса, числа и типа центральных атомов, а также количества и типа лигандов и способов их связывания. Они встречаются в виде нейтральных комплексов, положительно заряженных катионов карбонилов металлов или отрицательно заряженных карбонилатов металлов . Лиганд монооксида углерода может быть связан концевым образом с одним атомом металла или мостиком с двумя или более атомами металла. Эти комплексы могут быть гомолептическими , содержащими только лиганды CO, такие как тетракарбонил никеля (Ni(CO) 4 ), но чаще карбонилы металлов являются гетеролептическими и содержат смесь лигандов. [ нужна цитата ]
Мононуклеарные карбонилы металлов содержат только один атом металла в качестве центрального атома. За исключением гексакарбонила ванадия , только металлы с четным атомным номером, такие как хром , железо , никель и их гомологи, образуют нейтральные моноядерные комплексы. Полиядерные карбонилы металлов образуются из металлов с нечетными атомными номерами и содержат связь металл-металл . [2] Комплексы с разными металлами, но только с одним типом лиганда называются изолептическими. [2]
Оксид углерода имеет различные способы связывания с карбонилами металлов. Они различаются по тактильности , обозначаемой η , и по способу соединения. В комплексах η 2 -CO и углерод, и кислород связаны с металлом. Чаще всего связан только углерод, и в этом случае тактильность не упоминается. [3]
Карбонильный лиганд участвует в широком диапазоне способов связывания в димерах и кластерах карбонила металлов. В наиболее распространенном мостиковом режиме, обозначаемом μ 2 или просто μ , лиганд CO связывает пару металлов. Этот тип связи наблюдается в общедоступных карбонилах металлов: Co 2 (CO) 8 , Fe 2 (CO) 9 , Fe 3 (CO) 12 и Co 4 (CO) 12 . [1] [4] В некоторых кластерах с более высокой ядерностью CO образует мостики между тремя или даже четырьмя металлами. Эти лиганды обозначены μ 3 -CO и μ 4 -CO. Менее распространены способы соединения, при которых и C, и O связываются с металлом, например, μ 3 η 2 . [ нужна цитата ]

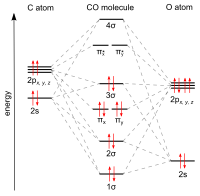
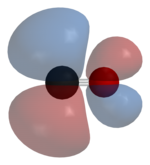
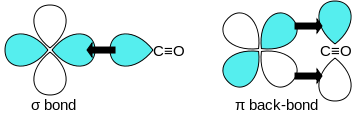
Окись углерода связывается с переходными металлами с помощью «синергетической обратной связи pi* ». Связь M–C состоит из трех компонентов, образующих частичную тройную связь. Сигма -связь возникает в результате перекрытия несвязывающей (или слабо разрыхляющей) sp-гибридизированной электронной пары углерода со смесью d- , s- и p-орбиталей металла. Пара пи(π)-связей возникает в результате перекрытия заполненных d-орбиталей на металле с парой π* -разрыхляющих орбиталей, выступающих из атома углерода CO. Последний вид связи требует, чтобы металл имел d-электроны. и что металл находится в относительно низкой степени окисления (0 или +1), что делает выгодным обратное донорство электронной плотности. Поскольку электроны металла заполняют π-разрыхляющую орбиталь CO, они ослабляют связь углерод-кислород по сравнению со свободным окисью углерода, а связь металл-углерод усиливается. Из-за характера кратной связи связи M-CO расстояние между металлом и атомом углерода относительно короткое, часто менее 1,8 Å, что примерно на 0,2 Å короче, чем связь металл- алкил . Расстояние M-CO и MC-O чувствительно к другим лигандам на металле. Показательными для этих эффектов являются следующие данные для расстояний Mo-C и CO в Mo(CO) 6 и Mo(CO) 3 (4-метилпиридин) 3 : 2,06 против 1,90 и 1,11 против 1,18 Å. [5]
Инфракрасная спектроскопия является чувствительным методом обнаружения мостиковых карбонильных лигандов. Для соединений с двумостиковыми лигандами CO, обозначаемыми μ 2 -CO или часто просто μ -CO, частота растяжения связи ν CO обычно смещается на 100–200 см -1 в сторону более низких энергий по сравнению с признаками концевого CO, которые находятся в область 1800 см -1 . Полосы закрывающих грани ( μ 3 ) лигандов CO появляются при еще более низких энергиях. В дополнение к симметричным мостиковым модам, CO может быть мостиком асимметрично или за счет донорства с d-орбитали металла на π*-орбиталь CO. [6] [7] [8] Увеличение π-связей из-за обратного донорства от наличие нескольких металлоцентров приводит к дальнейшему ослаблению связи C–O. [ нужна цитата ]
Большинство моноядерных карбонильных комплексов представляют собой бесцветные или бледно-желтые летучие жидкости или твердые вещества, легковоспламеняющиеся и токсичные. [9] Гексакарбонил ванадия , уникально стабильный карбонил металла с 17 электронами, представляет собой твердое вещество сине-черного цвета. [1] Диметаллические и полиметаллические карбонилы имеют тенденцию быть более насыщенными. Додекакарбонил трижелеза (Fe 3 (CO) 12 ) образует темно-зеленые кристаллы. Кристаллические карбонилы металлов часто сублимируются в вакууме, хотя этот процесс часто сопровождается деградацией. Карбонилы металлов растворимы в неполярных и полярных органических растворителях ( бензол , диэтиловый эфир , ацетон , ледяная уксусная кислота , четыреххлористый углерод) . Некоторые соли катионных и анионных карбонилов металлов растворимы в воде или низших спиртах. [10]

Помимо рентгеновской кристаллографии , важными аналитическими методами для характеристики карбонилов металлов являются инфракрасная спектроскопия и 13 C ЯМР-спектроскопия . Эти два метода предоставляют структурную информацию в двух очень разных временных масштабах. Инфракрасно-активные колебательные моды , такие как валентные колебания CO, часто происходят быстрее по сравнению с внутримолекулярными процессами, тогда как ЯМР-переходы происходят на более низких частотах и, следовательно, в структурах образца в масштабе времени, который, как оказалось, сравним со скоростью внутримолекулярного лиганда. обменные процессы. Данные ЯМР предоставляют информацию об «усредненных по времени структурах», тогда как ИК представляет собой мгновенный «снимок». [11] Для иллюстрации различных временных масштабов исследование октакарбонила дикобальта (Co 2 (CO) 8 ) с помощью инфракрасной спектроскопии дает 13 полос ν CO , что намного больше, чем ожидалось для одного соединения. Эта сложность отражает наличие изомеров с мостиковыми лигандами CO и без них. В спектре ЯМР 13 С того же вещества наблюдается только один сигнал при химическом сдвиге 204 м.д. Эта простота указывает на то, что изомеры быстро (в шкале времени ЯМР) взаимопревращаются. [ нужна цитата ]
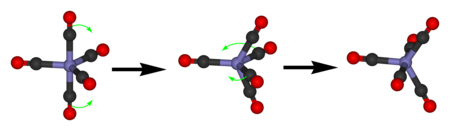
Пентакарбонил железа демонстрирует только один сигнал ЯМР 13 С из-за быстрого обмена аксиальных и экваториальных лигандов CO за счет псевдовращения Берри . [ нужна цитата ]

Важным методом характеристики карбонилов металлов является инфракрасная спектроскопия . [13] Колебания C–O, обычно обозначаемые ν CO , возникают при частоте 2143 см –1 для газообразного угарного газа. Энергии полосы ν CO для карбонилов металлов коррелируют с прочностью связи углерод-кислород и обратно коррелируют с прочностью π-основной связи между металлом и углеродом. π-основность металлоцентра зависит от множества факторов; в изоэлектронном ряду ( от титана до железа ) в нижней части этого раздела гексакарбонилы демонстрируют уменьшение π-связей по мере увеличения (делания более положительным) заряда металла. π-Основные лиганды увеличивают π-электронную плотность в металле, а улучшение обратной связи снижает ν CO . Электронный параметр Толмана использует фрагмент Ni(CO) 3 для упорядочения лигандов по их π-донорным способностям. [14] [15]
Число колебательных мод карбонильного комплекса металла можно определить с помощью теории групп . Только колебательные моды, которые преобразуются как электрический дипольный оператор, будут иметь ненулевые прямые продукты и наблюдаться. Таким образом, можно предсказать количество наблюдаемых ИК-переходов (но не их энергии). [16] [17] [18] Например, лиганды CO октаэдрических комплексов, таких как Cr (CO) 6 , преобразуются как в 1g , например , и t 1u , но только в моду t 1u (антисимметричное растяжение апикальные карбонильные лиганды) разрешены для ИК-излучения. Таким образом, в ИК-спектрах октаэдрических гексакарбонилов металлов наблюдается только одна полоса ν CO . Спектры комплексов более низкой симметрии более сложны. Например, в ИК-спектре Fe 2 (CO) 9 присутствуют полосы CO при 2082, 2019 и 1829 см -1 . Число наблюдаемых в ИК-диапазоне колебательных мод для карбонилов некоторых металлов показано в таблице. Имеются исчерпывающие таблицы. [13] Эти правила применяются к карбонилам металлов в растворе или газовой фазе. Низкополярные растворители идеально подходят для высокого разрешения. При измерениях на твердых образцах карбонилов металлов число полос может увеличиваться, отчасти из-за симметрии узлов. [19]
Карбонилы металлов часто характеризуют с помощью 13 C ЯМР-спектроскопии . Чтобы повысить чувствительность этого метода, комплексы часто обогащают 13 CO. Типичный диапазон химического сдвига для терминально связанных лигандов составляет от 150 до 220 частей на миллион . Мостиковые лиганды резонируют между 230 и 280 м.д. [1] Сигналы 13 C смещаются в сторону более высоких полей с увеличением атомного номера центрального металла.
ЯМР-спектроскопия может быть использована для экспериментального определения текучести . [26]
Энергию активации процессов лигандного обмена можно определить по температурной зависимости уширения линий. [27]
Масс-спектрометрия дает информацию о структуре и составе комплексов. Спектры поликарбонилов металлов часто легко интерпретируются, поскольку доминирующим процессом фрагментации является потеря карбонильных лигандов ( m / z = 28).
Электронная ионизация является наиболее распространенным методом определения характеристик нейтральных карбонилов металлов. Нейтральные карбонилы металлов могут быть преобразованы в заряженные соединения путем дериватизации , что позволяет использовать ионизацию электрораспылением (ESI), приборы для которой часто широко доступны. Например, обработка карбонила металла алкоксидом приводит к образованию анионного металлоформиата , который поддается анализу с помощью ESI-MS:
Карбонилы некоторых металлов реагируют с азидом с образованием изоцианатных комплексов с выделением азота . [28] Регулируя напряжение или температуру конуса, можно контролировать степень фрагментации. Можно определить молярную массу исходного комплекса, а также информацию о структурных перегруппировках, связанных с потерей карбонильных лигандов в условиях ESI-MS. [29]
Масс-спектрометрия в сочетании с инфракрасной фотодиссоциационной спектроскопией может предоставить информацию о колебании ионных карбонильных комплексов в газовой фазе. [30]

При исследовании инфракрасного спектра Галактического центра Млечного Пути были обнаружены монооксидные колебания карбонилов железа в межзвездных пылевых облаках. [32] Карбонильные кластеры железа также наблюдались в хондритах Jiange H5, идентифицированных с помощью инфракрасной спектроскопии. Для концевых и мостиковых лигандов монооксида углерода были обнаружены четыре частоты инфракрасного растяжения. [33]
В богатой кислородом атмосфере Земли карбонилы металлов подвергаются окислению до оксидов металлов. Обсуждается, формировались ли в восстановительных гидротермальных условиях добиотической предыстории такие комплексы и могли ли они быть доступны в качестве катализаторов синтеза важнейших биохимических соединений , таких как пировиноградная кислота . [34] Следы карбонилов железа, никеля и вольфрама были обнаружены в газообразных выделениях осадка сточных вод городских очистных сооружений . [35]
Ферменты гидрогеназы содержат CO, связанный с железом. Считается, что CO стабилизирует низкие степени окисления, что облегчает связывание водорода . Ферменты дегидрогеназа монооксида углерода и ацетил-КоА-синтаза также участвуют в биопереработке CO. [36] Комплексы, содержащие монооксид углерода, используются из-за токсичности CO и передачи сигналов. [37]
Синтез карбонилов металлов — широко изучаемая тема металлоорганических исследований. Со времени работ Монда, а затем Хибера было разработано множество методик получения моноядерных карбонилов металлов, а также гомо- и гетерометаллических карбонильных кластеров. [38]
Тетракарбонил никеля и пентакарбонил железа можно получить по следующим уравнениям реакцией мелкодисперсного металла с окисью углерода : [39]
Тетракарбонил никеля образуется с окисью углерода уже при 80°С и атмосферном давлении, мелкодисперсное железо реагирует при температуре от 150 до 200°С и давлении окиси углерода 50–200 бар. [40] Карбонилы других металлов получают менее прямыми методами. [41]
Некоторые карбонилы металлов получают восстановлением галогенидов металлов в присутствии монооксида углерода под высоким давлением. Используются различные восстановители, включая медь , алюминий , водород , а также алкилы металлов, такие как триэтилалюминий . Показательным является образование гексакарбонила хрома из безводного хлорида хрома(III) в бензоле с алюминием в качестве восстановителя и хлоридом алюминия в качестве катализатора: [39]
Использование алкилов металлов, таких как триэтилалюминий и диэтилцинк , в качестве восстановителя приводит к окислительному связыванию алкильного радикала с образованием димерного алкана :
Соли вольфрама , молибдена , марганца и родия можно восстановить алюмогидридом лития . Гексакарбонил ванадия получают с использованием натрия в качестве восстановителя в хелатирующих растворителях, таких как диглим . [9]
В водной фазе соли никеля или кобальта можно восстановить, например, дитионитом натрия . В присутствии оксида углерода соли кобальта количественно превращаются в анион тетракарбонилкобальта(-1): [9]
Некоторые карбонилы металлов получают с использованием CO непосредственно в качестве восстановителя . Таким способом Хибер и Фукс впервые получили из оксида декакарбонил дирения : [42]
При использовании оксидов металлов в качестве продукта реакции образуется углекислый газ . При восстановлении хлоридов металлов монооксидом углерода образуется фосген , как и при получении карбонилхлорида осмия из хлоридных солей. [38] Оксид углерода также подходит для восстановления сульфидов , где карбонилсульфид является побочным продуктом.
Фотолиз или термолиз моноядерных карбонилов приводит к образованию ди- и полиметаллических карбонилов, таких как нонакарбонил дижелеза (Fe 2 (CO) 9 ). [43] [44] При дальнейшем нагревании продукты разлагаются на металл и окись углерода. [ нужна цитата ]
Термическое разложение додекакарбонила триосмия (Os 3 (CO) 12 ) приводит к образованию карбонильных кластеров осмия с более высоким содержанием ядер, таких как Os 4 (CO) 13 , Os 6 (CO) 18 до Os 8 (CO) 23 . [9]
Карбонилы со смешанными лигандами рутения , осмия , родия и иридия часто образуются путем отделения CO от растворителей, таких как диметилформамид (ДМФ) и 2-метоксиэтанол . Типичным является синтез IrCl(CO)(PPh 3 ) 2 по реакции хлорида иридия(III) и трифенилфосфина в кипящем растворе ДМФА. [45]
Реакция метатезиса солей , таких как KCo(CO) 4 , с [Ru(CO) 3 Cl 2 ] 2 избирательно приводит к карбонилам смешанных металлов, таким как RuCo 2 (CO) 11 . [46]
Синтез ионных карбонильных комплексов возможен путем окисления или восстановления нейтральных комплексов. Анионные карбонилаты металлов можно получить, например, восстановлением биядерных комплексов с натрием. Известным примером является натриевая соль тетракарбонилата железа (Na 2 Fe(CO) 4 , реактив Коллмана ), которая используется в органическом синтезе. [47]
Катионные гексакарбонильные соли марганца , технеция и рения могут быть получены из карбонилгалогенидов под давлением монооксида углерода реакцией с кислотой Льюиса .
С помощью сильных кислот удалось получить карбонильные катионы золота, такие как [Au(CO) 2 ] + , который используется в качестве катализатора карбонилирования алкенов . [48] Катионный карбонильный комплекс платины [Pt(CO) 4 ] 2+ можно получить, работая с так называемыми суперкислотами , такими как пентафторид сурьмы . [49] Хотя CO обычно рассматривается как лиганд для ионов низковалентных металлов, комплекс четырехвалентного железа [Cp* 2 Fe] 2+ (комплекс с 16-валентными электронами) количественно связывает CO с образованием диамагнитного Fe(IV)-карбонила. [Cp* 2 FeCO] 2+ (18-валентный электронный комплекс). [50]
Карбонилы металлов являются важными предшественниками для синтеза других металлоорганических комплексов. Обычными реакциями являются замещение оксида углерода другими лигандами, реакции окисления или восстановления металлоцентра и реакции на лиганде оксида углерода. [1]
Замещение лигандов CO может быть индуцировано термически или фотохимически донорными лигандами. Диапазон лигандов широк и включает фосфины , цианиды (CN- ) , доноры азота и даже простые эфиры, особенно хелатирующие. Алкены , особенно диены , являются эффективными лигандами, дающими синтетически полезные производные. Замещение 18-электронных комплексов обычно происходит по диссоциативному механизму с участием 16-электронных промежуточных продуктов. [51]
Замещение протекает по диссоциативному механизму :
Энергия диссоциации составляет 105 кДж/моль (25 ккал/моль) для тетракарбонила никеля и 155 кДж/моль (37 ккал/моль) для гексакарбонила хрома . [1]
Замещение в 17-электронных комплексах, которые встречаются редко, протекает по ассоциативным механизмам с 19-электронными интермедиатами.
Скорость замещения в 18-электронных комплексах иногда катализируется каталитическими количествами окислителей посредством переноса электронов . [52]
Карбонилы металлов реагируют с восстановителями , такими как металлический натрий или амальгама натрия, с образованием карбонилметаллатных (или карбонилатных) анионов:
Для пентакарбонила железа получается тетракарбонилферрат с потерей CO:
Ртуть может внедряться в связи металл-металл некоторых полиядерных карбонилов металлов:
Лиганд CO часто подвержен атаке нуклеофилов . Например, оксид триметиламина и бис(триметилсилил)амид калия превращают лиганды CO в CO 2 и CN - соответственно. В « реакции основания Хибера » ион гидроксида атакует лиганд CO с образованием металлокарбоновой кислоты с последующим выделением углекислого газа и образованием гидридов или карбонилметаллатов металлов. Хорошо изученным примером этого нуклеофильного присоединения является превращение пентакарбонила железа в гидридожелезо тетракарбонильный анион :
Гидридные реагенты также атакуют лиганды CO, особенно в катионных комплексах металлов, с образованием формильного производного :
Литийорганические реагенты присоединяют карбонилы металлов к ацилметаллкарбонильным анионам. O - Алкилирование этих анионов, например, солями Меервейна , дает карбены Фишера .
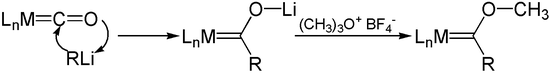
Несмотря на то, что карбонилы металлов находятся в низких формальных степенях окисления , они относительно нереактивны по отношению ко многим электрофилам . Например, они устойчивы к воздействию алкилирующих агентов, слабых кислот и мягких окислителей . Большинство карбонилов металлов подвергаются галогенированию . Пентакарбонил железа , например, образует галогениды карбонила железа:
Связи металл-металл расщепляются галогенами. В зависимости от используемой схемы счета электронов это можно рассматривать как окисление атомов металла:
Большинство карбонильных комплексов металлов содержат смесь лигандов. Примеры включают исторически важный IrCl(CO)(P(C 6 H 5 ) 3 ) 2 и антидетонатор (CH 3 C 5 H 4 )Mn(CO) 3 . Исходными соединениями для многих из этих комплексов со смешанными лигандами являются бинарные карбонилы, разновидности формулы [M x (CO) n ] z , многие из которых коммерчески доступны. Формулы многих карбонилов металлов можно вывести из правила 18 электронов .
Хорошо известны также крупные анионные кластеры никеля , палладия и платины . Многие карбонильные анионы металлов могут быть протонированы с образованием карбонилгидридов металлов .
Неклассический описывает те карбонильные комплексы, в которых ν CO выше, чем у свободного монооксида углерода. В неклассических комплексах CO расстояние CO короче, чем у свободного CO (113,7 пм). Структура [Fe(CO) 6 ] 2+ с d CO = 112,9 пм иллюстрирует этот эффект. Эти комплексы обычно катионные, иногда дикатионные. [58]

Карбонилы металлов используются в ряде промышленных процессов. Возможно, самым ранним применением была экстракция и очистка никеля посредством тетракарбонила никеля по процессу Монда (см. Также карбонильную металлургию ). [ нужна цитата ]
По аналогичному процессу термическим разложением пентакарбонила железа получают карбонильное железо , металлический порошок высокой чистоты. Карбонильное железо используется, в частности, для приготовления индукторов , пигментов , в качестве пищевых добавок , [59] при производстве радиопоглощающих материалов, в стелс-технологиях , [60] и при термическом напылении . [ нужна цитата ]
Карбонилы металлов используются в ряде промышленно важных реакций карбонилирования . В оксо-процессе алкен , газообразный водород и окись углерода реагируют вместе с катализатором (таким как октакарбонил дикобальта ) с образованием альдегидов . Показательным является производство бутиральдегида из пропилена :
Бутиральдегид преобразуется в промышленном масштабе в 2-этилгексанол , предшественник пластификаторов ПВХ , путем альдольной конденсации с последующим гидрированием полученного гидроксиальдегида. «Оксоальдегиды», образующиеся в результате гидроформилирования, используются для крупномасштабного синтеза жирных спиртов, которые являются предшественниками моющих средств . Гидроформилирование представляет собой реакцию с высокой атомной экономией , особенно если реакция протекает с высокой региоселективностью . [ нужна цитата ]
Другой важной реакцией, катализируемой карбонилами металлов, является гидрокарбоксилирование . Ниже приведен пример синтеза акриловой кислоты и эфиров акриловой кислоты:
Также при циклизации ацетилена в циклооктатетраен используются металлкарбонильные катализаторы: [61]
В процессах Monsanto и Cativa уксусная кислота производится из метанола, оксида углерода и воды с использованием йодистого водорода , а также карбонильных катализаторов родия и иридия соответственно. Связанные реакции карбонилирования дают уксусный ангидрид . [62]
Молекулы, высвобождающие угарный газ, представляют собой карбонильные комплексы металлов, которые разрабатываются в качестве потенциальных лекарств для высвобождения CO. В низких концентрациях CO действует как сосудорасширяющее и противовоспалительное средство. CO-RM были задуманы как фармакологический стратегический подход к переносу и доставке контролируемых количеств CO к тканям и органам. [63]
Известно, что многие лиганды образуют гомолептические и смешанно-лигандные комплексы , аналогичные карбонилам металлов. [ нужна цитата ]
Нитрозилы металлов, соединения, содержащие NO-лиганды , многочисленны. Однако, в отличие от карбонилов металлов, гомолептические нитрозилы металлов встречаются редко. NO является более сильным π-акцептором, чем CO. К хорошо известным нитрозильным карбонилам относятся CoNO(CO) 3 и Fe(NO) 2 (CO) 2 , которые являются аналогами Ni(CO) 4 . [64]
Комплексы, содержащие CS, известны, но встречаются редко. [65] [66] Редкость таких комплексов частично объясняется тем фактом, что очевидный исходный материал, моносульфид углерода , нестабилен. Таким образом, синтез тиокарбонильных комплексов требует непрямых путей, таких как реакция тетракарбонилферрата динатрия с тиофосгеном :
Охарактеризованы комплексы CSe и CTe. [67]
Изоцианиды также образуют обширные семейства комплексов, родственных карбонилам металлов. Типичными изоцианидными лигандами являются метилизоцианид и т -бутилизоцианид (Me 3 CNC). Особым случаем является CF 3 NC , нестабильная молекула, образующая стабильные комплексы, поведение которых близко к поведению карбонилов металлов. [68]
Токсичность карбонилов металлов обусловлена токсичностью монооксида углерода , металла, а из-за летучести и нестабильности комплексов любая присущая металлу токсичность обычно становится гораздо более серьезной из-за легкости воздействия. Воздействие происходит при вдыхании, жидких карбонилов металлов при проглатывании или из-за хорошей растворимости в жирах при резорбции через кожу. Наибольший клинический опыт получен при токсикологическом отравлении тетракарбонилом никеля и пентакарбонилом железа в связи с их применением в промышленности. Тетракарбонил никеля считается одним из самых сильных ингаляционных ядов. [69]
Вдыхание тетракарбонила никеля вызывает острые неспецифические симптомы , сходные с отравлением угарным газом , такие как тошнота , кашель , головная боль , лихорадка и головокружение . Через некоторое время возникают тяжелые легочные симптомы, такие как кашель, тахикардия и цианоз , или проблемы в желудочно-кишечном тракте . Помимо патологических изменений легких, например при металлировании альвеол, наблюдаются поражения головного мозга, печени, почек, надпочечников и селезенки. Отравление карбонилами металлов часто требует длительного выздоровления. [70]
Хроническое воздействие при вдыхании низких концентраций тетракарбонила никеля может вызвать неврологические симптомы, такие как бессонница, головные боли, головокружение и потеря памяти. [70] Тетракарбонил никеля считается канцерогенным, но от начала воздействия до клинических проявлений рака может пройти от 20 до 30 лет. [71]

Первые опыты по реакции угарного газа с металлами были проведены Юстусом фон Либихом в 1834 году. Пропуская угарный газ над расплавленным калием, он получил вещество, имеющее эмпирическую формулу KCO, которое он назвал кохленоксидкалием . [72] Как было показано позже, соединение было не карбонилом, а калиевой солью бензолгексола (K 6 C 6 O 6 ) и калиевой солью ацетилендиола (K 2 C 2 O 2 ). [38]

Синтез первого настоящего гетеролептического карбонильного комплекса металла был осуществлен Паулем Шютценбергером в 1868 году путем пропускания хлора и оксида углерода над платиновой чернью , в результате чего образовалась дикарбонилдихлорплатина (Pt(CO) 2 Cl 2 ). [73]
Людвиг Монд , один из основателей Imperial Chemical Industries , исследовал в 1890-х годах вместе с Карлом Лангером и Фридрихом Квинке различные процессы восстановления хлора, который был потерян в процессе Сольве металлическим никелем , оксидами и солями. [38] В рамках своих экспериментов группа обрабатывала никель окисью углерода. Они обнаружили, что образующийся газ окрашивает газовое пламя горелки в зеленовато-желтоватый цвет; при нагревании в стеклянной трубке образовывалось никелевое зеркало. Газ можно было конденсировать в бесцветную, прозрачную жидкость с температурой кипения 43 °C. Таким образом, Монд и его коллега открыли первый чистый гомолептический карбонил металла — тетракарбонил никеля (Ni(CO) 4 ). [74] Необычно высокая летучесть соединения металла тетракарбонила никеля привела Кельвина к утверждению, что Монд «дал крылья тяжелым металлам». [75]
В следующем году Монд и Марселлин Бертло независимо открыли пентакарбонил железа , который получают по той же методике, что и тетракарбонил никеля. Монд осознал экономический потенциал этого класса соединений, который он коммерчески использовал в процессе Монда , и профинансировал дополнительные исследования родственных соединений. Генрих Хирц и его коллега М. Далтон Ковап синтезировали карбонилы металлов кобальта , молибдена , рутения и нонакарбонила дижелеза . [76] [77] В 1906 году Джеймс Дьюар и Х.О. Джонс смогли определить структуру нонакарбонила дижелеза, который образуется из пентакарбонила железа под действием солнечного света. [78] После смерти Монда в 1909 году химия карбонилов металлов на несколько лет оказалась в забвении. В 1924 году компания BASF начала промышленное производство пентакарбонила железа с помощью процесса, разработанного Алвином Митташем . Пентакарбонил железа использовался для производства железа высокой чистоты, так называемого карбонильного железа , и пигмента оксида железа . [40] Только в 1927 году А. Джобу и А. Кассалу удалось получить гексакарбонил хрома и гексакарбонил вольфрама , что стало первым синтезом других гомолептических карбонилов металлов. [ нужна цитата ]
Вальтер Хибер сыграл в годы после 1928 года решающую роль в развитии химии карбонилов металлов. Он систематически исследовал и открыл, среди прочего, основную реакцию Хибера , первый известный путь получения карбонилгидридов металлов, а также синтетические пути, ведущие к карбонилам металлов, таким как декакарбонил дирения . [79] Хибер, который с 1934 года был директором Института неорганической химии Мюнхенского технического университета, опубликовал за четыре десятилетия 249 статей по химии карбонилов металлов. [38]
Также в 1930-х годах Уолтер Реппе , промышленный химик, а затем член правления BASF, открыл ряд гомогенных каталитических процессов, таких как гидрокарбоксилирование , в которых олефины или алкины реагируют с окисью углерода и водой с образованием таких продуктов, как ненасыщенные кислоты и их соединения. производные. [38] В этих реакциях, например, в качестве катализаторов выступают тетракарбонил никеля или карбонилы кобальта. [80] Реппе также обнаружил циклотримеризацию и тетрамеризацию ацетилена и его производных до бензола и производных бензола с карбонилами металлов в качестве катализаторов. В 1960-х годах компания BASF построила завод по производству акриловой кислоты по процессу Реппе, который только в 1996 году был заменен более современными методами, основанными на каталитическом окислении пропилена . [ нужна цитата ]

Для рационального проектирования новых комплексов оказалась полезной концепция изолобальной аналогии. За разработку концепции Роальд Хоффманн был удостоен Нобелевской премии по химии. Это описывает металлические карбонильные фрагменты M(CO) n как части октаэдрических строительных блоков по аналогии с тетраэдрическими фрагментами CH 3 –, CH 2 – или CH– в органической химии. В примере декакарбонил димарганца образуется по изолобальной аналогии двух фрагментов d 7 Mn(CO) 5 , изолобальных метиловому радикалу CH.•
3. По аналогии с тем, как метильные радикалы объединяются с образованием этана , они могут образовывать декакарбонил димарганца . Наличие изолобальных аналоговых фрагментов не означает возможности синтеза желаемых структур. В своей лекции, присужденной Нобелевской премии, Хоффман подчеркнул, что изолобальная аналогия является полезной, но простой моделью и в некоторых случаях не приводит к успеху. [81]
Экономические выгоды от карбонилирования , катализируемого металлами , такого как химия Реппе и гидроформилирование , привели к росту этой области. Карбонильные соединения металлов были обнаружены в активных центрах трех природных ферментов. [82]
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ){{cite journal}}: Отсутствует или пусто |title=( помощь )