- Гекс-3-ен имеет внутреннюю двойную углерод-углеродную связь
- Гекс-1-ен имеет концевую двойную связь
- Гекс-3-ин имеет внутреннюю тройную углерод-углеродную связь
- Гекс-1-ин имеет концевую тройную связь
| Refresh | This website ru.stringtranslate.com/%D0%BA%D0%BB%D0%B8%D0%BD%D0%BE%D0%B2%D1%8B%D0%B5%20%D1%81%D0%B2%D1%8F%D0%B7%D0%B8/Skeletal_formula is currently offline. Cloudflare's Always Online™ shows a snapshot of this web page from the Internet Archive's Wayback Machine. To check for the live version, click Refresh. |
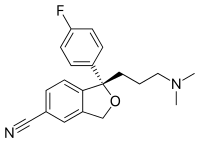
Формула скелета , формула линии-угла , формула линии связи или сокращенная формула органического соединения — это тип молекулярной структурной формулы , которая служит в качестве сокращенного представления связей молекулы и некоторых деталей ее молекулярной геометрии . Формула скелета показывает структуру скелета или скелет молекулы, которая состоит из атомов скелета , составляющих молекулу. [1] Она представлена в двух измерениях, как на листе бумаги. Она использует определенные соглашения для представления атомов углерода и водорода , которые являются наиболее распространенными в органической химии.
Ранняя форма этого представления была впервые разработана химиком-органиком Августом Кекуле , в то время как современная форма тесно связана и находится под влиянием структуры Льюиса молекул и их валентных электронов. Поэтому их иногда называют структурами Кекуле [a] или структурами Льюиса–Кекуле . Скелетные формулы стали повсеместными в органической химии , отчасти потому, что их относительно быстро и просто рисовать, а также потому, что обозначение изогнутой стрелки, используемое для обсуждения механизмов реакции и делокализации электронов, можно легко наложить.
Несколько других способов изображения химических структур также широко используются в органической химии (хотя и реже, чем скелетные формулы). Например, конформационные структуры выглядят похоже на скелетные формулы и используются для изображения приблизительных положений атомов в трехмерном пространстве в виде перспективного рисунка. Другие типы представления, такие как проекция Ньюмена , проекция Хауорта или проекция Фишера , также выглядят несколько похожими на скелетные формулы. Однако существуют небольшие различия в используемых соглашениях, и читателю необходимо знать о них, чтобы понять структурные детали, закодированные в изображении. Хотя скелетные и конформационные структуры также используются в металлоорганической и неорганической химии , используемые соглашения также несколько отличаются.
Скелетная структура органического соединения представляет собой ряд атомов, связанных вместе, которые формируют основную структуру соединения. Скелет может состоять из цепей, ветвей и/или колец связанных атомов. Скелетные атомы, отличные от углерода или водорода, называются гетероатомами . [2]
Скелет имеет водород и/или различные заместители, связанные с его атомами. Водород является наиболее распространенным неуглеродным атомом, который связан с углеродом и, для простоты, явно не изображен. Кроме того, атомы углерода обычно не маркируются как таковые напрямую (т. е. как "C"), тогда как гетероатомы всегда явно отмечаются как таковые ("N" для азота , "O" для кислорода и т. д.)
Гетероатомы и другие группы атомов, которые приводят к относительно высоким показателям химической реактивности или вносят специфические и интересные характеристики в спектры соединений, называются функциональными группами , поскольку они придают молекуле функцию. Гетероатомы и функциональные группы совместно называются «заместителями», поскольку они считаются заменой атома водорода, который присутствовал бы в исходном углеводороде органического соединения.
Как и в структурах Льюиса, ковалентные связи обозначены отрезками линий, причем двойной или тройной отрезок указывает на двойную или тройную связь соответственно. Аналогично, скелетные формулы обозначают формальные заряды , связанные с каждым атомом (хотя неподеленные пары обычно необязательны, см. ниже ). Фактически, скелетные формулы можно рассматривать как сокращенные структуры Льюиса, которые соблюдают следующие упрощения:
В стандартном изображении молекулы изображается каноническая форма (резонансная структура) с наибольшим вкладом. Однако считается, что скелетная формула представляет «реальную молекулу» – то есть средневзвешенное значение всех канонических форм, вносящих вклад. Таким образом, в случаях, когда две или более канонических форм вносят вклад с равным весом (например, в бензоле или карбоксилатном анионе) и одна из канонических форм выбирается произвольно, считается, что скелетная формула отображает истинную структуру, содержащую эквивалентные связи дробного порядка, даже если делокализованные связи изображены как неэквивалентные одинарные и двойные связи.
С тех пор как скелетные структуры были введены во второй половине XIX века, их внешний вид претерпел значительную эволюцию. Графические соглашения, используемые сегодня, датируются 1980-ми годами. Благодаря принятию программного пакета ChemDraw в качестве фактического отраслевого стандарта ( например, Американским химическим обществом , Королевским обществом химии и публикациями Gesellschaft Deutscher Chemiker ), эти соглашения стали практически универсальными в химической литературе с конца 1990-х годов. Несколько незначительных условных вариаций, особенно в отношении использования стереосвязей, продолжают существовать в результате различий в практике США, Великобритании и Европы или в силу личных предпочтений. [3] В качестве еще одного незначительного различия между авторами формальные заряды могут быть показаны со знаком плюс или минус в круге (⊕, ⊖) или без круга. Ниже приведен набор соглашений, которых придерживается большинство авторов, вместе с наглядными примерами.





Например, ниже показана скелетная формула гексана (вверху). Атом углерода, обозначенный как C 1 , по-видимому, имеет только одну связь, поэтому с ним также должно быть связано три атома водорода, чтобы общее число связей стало четыре. Атом углерода, обозначенный как C 3, имеет две связи с другими атомами углерода и, следовательно, также связан с двумя атомами водорода. Для сравнения показаны структура Льюиса (в середине) и шаростержневая модель (внизу) фактической молекулярной структуры гексана, определенной с помощью рентгеновской кристаллографии .



Неважно, с какого конца цепи начинать нумерацию, главное, чтобы сохранялась последовательность при рисовании диаграмм. Сокращенная формула или название ИЮПАК подтвердят ориентацию. Некоторые молекулы станут знакомыми независимо от ориентации.
Все атомы, которые не являются углеродом или водородом, обозначаются их химическим символом , например, Cl для хлора , O для кислорода , Na для натрия и т. д. В контексте органической химии эти атомы обычно известны как гетероатомы ( префикс гетеро- происходит от греческого ἕτερος héteros, что означает «другой»).
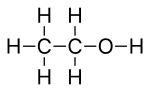
Любые атомы водорода, связанные с гетероатомами, изображены явно. Например, в этаноле, C2H5OH , атом водорода , связанный с кислородом, обозначен символом H, тогда как атомы водорода, связанные с атомами углерода, не показаны напрямую .
Линии, представляющие связи гетероатом-водород, обычно опускаются для ясности и компактности, поэтому функциональная группа, такая как гидроксильная группа, чаще всего записывается как −OH вместо −O−H. Эти связи иногда рисуются полностью, чтобы подчеркнуть их присутствие, когда они участвуют в механизмах реакции .
Ниже для сравнения показаны скелетная формула (вверху), ее структура Льюиса (в середине) и ее шаростержневая модель (внизу) реальной трехмерной структуры молекулы этанола в газовой фазе, определенной с помощью микроволновой спектроскопии .


Существуют также символы, которые кажутся символами химических элементов , но представляют некоторые очень распространенные заместители или указывают на неопределенного члена группы элементов. Они называются символами псевдоэлементов или органическими элементами и рассматриваются как одновалентные «элементы» в скелетных формулах. [4] Список распространенных символов псевдоэлементов:
Эфиры сульфоната часто являются уходящими группами в реакциях нуклеофильного замещения. Для получения дополнительной информации см. статьи о сульфонильных и сульфонатных группах.
Защитная группа или защитная группа вводится в молекулу путем химической модификации функциональной группы для получения хемоселективности в последующей химической реакции, что облегчает многостадийный органический синтез.
Два атома могут быть связаны, разделяя более одной пары электронов. Обычные связи с углеродом — одинарные, двойные и тройные связи. Одинарные связи наиболее распространены и представлены одной сплошной линией между двумя атомами в скелетной формуле. Двойные связи обозначаются двумя параллельными линиями, а тройные связи — тремя параллельными линиями.
В более продвинутых теориях связывания существуют нецелые значения порядка связи . В этих случаях комбинация сплошных и пунктирных линий указывает на целые и нецелые части порядка связи соответственно.
В последние годы бензол обычно изображают в виде шестиугольника с чередующимися одинарными и двойными связями, что очень похоже на структуру, первоначально предложенную Кекуле в 1872 году. Как упоминалось выше, чередующиеся одинарные и двойные связи «1,3,5-циклогексатриена» понимаются как рисунок одной из двух эквивалентных канонических форм бензола (той, которая явно показана, и той, которая имеет противоположный рисунок формальных одинарных и двойных связей), в которой все связи углерод-углерод имеют эквивалентную длину и порядок связи ровно 1,5. Для арильных колец в целом две аналогичные канонические формы почти всегда вносят основной вклад в структуру, но они неэквивалентны, поэтому одна структура может вносить немного больший вклад, чем другая, и порядки связей могут несколько отличаться от 1,5.
Альтернативное представление, подчеркивающее эту делокализацию, использует круг, нарисованный внутри шестиугольника одинарных связей, для представления делокализованной π-орбитали . Этот стиль, основанный на предложенном Иоганнесом Тиле , был очень распространен в учебниках по вводной органической химии и до сих пор часто используется в неформальной обстановке. Однако, поскольку это изображение не отслеживает электронные пары и не может показать точное движение электронов, оно в значительной степени было заменено изображением Кекуле в педагогических и формальных академических контекстах. [f]

Стереохимию удобно обозначать в скелетных формулах: [5]
Соответствующие химические связи можно изобразить несколькими способами:

Раннее использование этой нотации можно проследить до Ричарда Куна , который в 1932 году использовал сплошные толстые линии и пунктирные линии в публикации. Современные сплошные и заштрихованные клинья были введены в 1940-х годах Джулио Наттой для представления структуры высокополимеров и широко популяризированы в учебнике 1959 года «Органическая химия» Дональда Дж. Крэма и Джорджа С. Хэммонда . [6]
Скелетные формулы могут отображать цис- и транс- изомеры алкенов. Волнистые одинарные связи являются стандартным способом представления неизвестной или неопределенной стереохимии или смеси изомеров (как в случае с тетраэдрическими стереоцентрами). Иногда использовалась скрещенная двойная связь; она больше не считается приемлемым стилем для общего использования, но все еще может потребоваться для компьютерного программного обеспечения. [5]
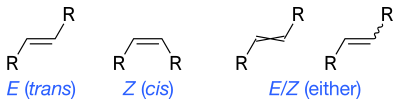

Водородные связи обычно обозначаются пунктирными или штриховыми линиями. В других контекстах штриховые линии могут также представлять частично сформированные или разорванные связи в переходном состоянии .