Лактоны — это циклические карбоновые эфиры . Они получены из соответствующих гидроксикарбоновых кислот путем этерификации . Они могут быть насыщенными или ненасыщенными. Некоторые содержат гетероатомы, заменяющие один или несколько атомов углерода кольца. [1]
Лактоны образуются путем лактонизации , внутримолекулярной этерификации соответствующих гидроксикарбоновых кислот, которая происходит спонтанно, когда образующееся кольцо состоит из пяти или шести звеньев. Лактоны с трех- или четырехзвенными кольцами (α-лактоны и β-лактоны) очень реакционноспособны, что затрудняет их выделение. Для лабораторного синтеза лактонов с малыми кольцами, а также тех, которые содержат кольца больше шестичленных, обычно требуются специальные методы. [2]
Греческие префиксы в алфавитном порядке указывают размер кольца.
Лактоны обычно называются в соответствии с молекулой кислоты-предшественника ( ацето = 2 атома углерода, пропио = 3, бутиро = 4, валеро = 5, капро = 6 и т. д.), с суффиксом -лактон и префиксом греческой буквы, который указывает число атомов углерода в гетероцикле — то есть расстояние между соответствующими группами -ОН и -СООН вдоль указанного остова. Первый атом углерода после углерода в группе -СООН в исходном соединении обозначается как α, второй будет обозначаться как β и т. д. Поэтому префиксы также указывают на размер лактонного кольца: α-лактон = 3-членное кольцо, β-лактон = 4-членное, γ-лактон = 5-членное, δ-лактон = 6-членное и т. д.Макроциклические лактоны известны как макролактоны . [3]
Другой суффикс, используемый для обозначения лактона, -олид , используется в названиях классов веществ, таких как бутенолид , макролид , карденолид или буфадиенолид .
Для получения предпочтительных названий ИЮПАК лактоны называют гетероциклическими псевдокетонами, добавляя суффикс «один», «дион», «тион» и т. д. и соответствующие мультипликативные префиксы к названию гетероциклического исходного гидрида. [4]
Название лактон происходит от кольцевого соединения, называемого лактидом , которое образуется при дегидратации 2-гидроксипропановой кислоты ( молочной кислоты ) CH 3 -CH(OH)-COOH. Молочная кислота, в свою очередь, получила свое название от своего первоначального выделения из кислого молока (лат. lac, lactis). Название было придумано в 1844 году французским химиком Теофилем-Жюлем Пелузом , который впервые получил его как производное молочной кислоты. [5] Внутренняя реакция дегидратации в той же молекуле молочной кислоты привела бы к образованию альфа-пропиолактона , лактона с 3-членным кольцом.
В 1880 году немецкий химик Вильгельм Рудольф Фиттиг распространил название «лактон» на все внутримолекулярные карбоновые эфиры. [6]
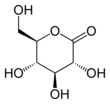
Распространены 5-членные γ-лактоны и 6-членные δ-лактоны. β-лактоны встречаются в ряде природных продуктов. [7] α-лактоны могут быть обнаружены как транзиентные виды в экспериментах по масс-спектрометрии . [8]
Макроциклические лактоны также являются важными натуральными продуктами. Циклопентадеканолид отвечает за мускусный запах масла корня дягиля . Из встречающихся в природе бициклических лактонов фталиды отвечают за запахи масел сельдерея и любистока , а кумарин — за запахи ясменника . [9] Лактоны присутствуют в древесине дуба и вносят вклад в вкусовой профиль пива, выдержанного в бочках . [10]
Лактонные кольца широко встречаются в природе в качестве строительных блоков, например, в аскорбиновой кислоте , каваине , непеталактоне , глюконолактоне , гормонах ( спиронолактоне , мевалонолактоне), ферментах ( лактоназе ), нейротрансмиттерах ( бутиролактоне , авермектинах ), антибиотиках ( макролидах , таких как эритромицин ; амфотерицине В ), противораковых препаратах ( вернолепине , эпотилонах ), фитоэстрогенах ( лактонах резорциловой кислоты , сердечных гликозидах ).

Многие методы синтеза эфиров могут быть применены и к лактонам. Лактонизация конкурирует с полимеризацией за более длинные гидроксикислоты или напряженные β-лактоны. γ-лактоны, с другой стороны, настолько стабильны, что 4-гидроксикислоты (R-CH(OH)-(CH 2 ) 2 -CO 2 H) спонтанно циклизуются.
В одном из промышленных синтезов оксандролона ключевым этапом образования лактона является органическая реакция – этерификация. [11] [12]

При галогенлактонизации алкен подвергается атаке галогена посредством электрофильного присоединения , при этом катионный промежуточный продукт захватывается внутримолекулярно соседней карбоновой кислотой . [13]
Конкретные методы включают этерификацию Ямагучи , макролактонизацию Шиины , макролактонизацию Кори-Николау , окисление Байера-Виллигера и нуклеофильную абстракцию .

γ-Лактоны γ-окталактон , γ-ноналактон , γ-декалактон , γ-ундекалактон могут быть получены с хорошим выходом в одностадийном процессе путем радикального присоединения первичных жирных спиртов к акриловой кислоте с использованием ди-трет-бутилпероксида в качестве катализатора. [9]
Альтернативной радикальной реакцией, приводящей к образованию γ-лактонов, является реакция сочетания, опосредованная марганцем .
Лактоны проявляют реакции, характерные для сложных эфиров.
Нагревание лактона с основанием ( гидроксидом натрия ) гидролизует лактон до его исходного соединения, бифункционального соединения с прямой цепью. Как и в случае с эфирами с прямой цепью, реакция гидролиза-конденсации лактонов является обратимой реакцией с равновесием . Однако константа равновесия реакции гидролиза лактона ниже, чем у эфира с прямой цепью, т. е. продукты (гидроксикислоты) менее предпочтительны в случае лактонов. Это происходит потому, что, хотя энтальпии гидролиза эфиров и лактонов примерно одинаковы, энтропия гидролиза лактонов меньше энтропии эфиров с прямой цепью. Эфиры с прямой цепью дают два продукта при гидролизе, что делает изменение энтропии более благоприятным, чем в случае лактонов, которые дают только один продукт.
Лактоны также реагируют с аминами, образуя спирт с раскрытым кольцом и амид.
Лактоны могут быть восстановлены до диолов с использованием алюмогидрида лития . Например, гамма-лактоны восстанавливаются до бутан-1,4-диола, (CH 2 (OH)-(CH 2 ) 2 -CH 2 (OH).
Некоторые лактоны преобразуются в полиэфиры: [14] [15] Например, двойной лактон, называемый лактидом, полимеризуется в полимолочную кислоту (полилактид). Полученная полимолочная кислота была тщательно исследована для коммерческого применения. [16] [17]
Лактоны вносят значительный вклад во вкус фруктов, а также неферментированных и ферментированных молочных продуктов [18] и поэтому используются в качестве ароматизаторов и отдушек. [9] Некоторые примеры: γ-декалактон (4-деканолид), который имеет характерный персиковый вкус; [18] δ-декалактон (5-деканолид), который имеет сливочный кокосовый/персиковый вкус; γ-додекалактон (4-додеканолид), который также имеет кокосовый/фруктовый вкус [18] описание, которое также подходит для γ-окталактона (4-октанолида), [19] хотя он также имеет травянистый характер; [18] γ-ноналактон , который имеет интенсивный кокосовый вкус этой серии, несмотря на то, что не встречается в кокосе, [20] и γ-ундекалактон .
Макроциклические лактоны ( циклопентадеканолид , 15-пентадеканолид-11/12-енолид) имеют запахи, похожие на запахи макроциклических кетонов животного происхождения ( мускон , циветон ), но их можно получить проще, например, деполимеризацией соответствующих линейных полиэфиров . Замена метиленовой группы кислородом почти не влияет на запах этих соединений, и в дополнение к циклопентадеканолиду образуются оксалактоны с 15–17-членными кольцами (например, 12-окса-16-гексадеканолид). [9]
Поликапролактон — важный пластик. Его образование даже рассматривалось в контексте происхождения жизни . [21]