Марганец — химический элемент ; он имеет символ Mn и атомный номер 25. Это твердый, хрупкий, серебристый металл, часто встречающийся в минералах в сочетании с железом . Марганец был впервые выделен в 1770-х годах. Марганец — это переходный металл , который широко используется в промышленных сплавах , особенно в нержавеющих сталях . Повышает прочность, работоспособность и устойчивость к износу. В качестве окислителя используется оксид марганца; в качестве резиновой добавки; а также в производстве стекла, удобрений и керамики. Сульфат марганца можно использовать в качестве фунгицида.
Марганец также является важным элементом питания человека, играющим важную роль в метаболизме макронутриентов, формировании костей и системах защиты от свободных радикалов . Это важнейший компонент десятков белков и ферментов. [6] Он содержится в основном в костях, а также в печени, почках и мозге. [7] В человеческом мозге марганец связан с металлопротеинами марганца , особенно с глутаминсинтетазой в астроцитах .
В лаборатории он известен в виде темно-фиолетовой соли перманганата калия . Это происходит в активных центрах некоторых ферментов . [8] Особый интерес представляет использование кластера Mn-O , комплекса , выделяющего кислород , в производстве кислорода растениями.
Марганец — серебристо-серый металл , напоминающий железо. Он тверд и очень хрупок, его трудно плавить, но легко окислить. [9] Металлический марганец и его общие ионы парамагнитны . [10] Марганец медленно тускнеет на воздухе и окисляется («ржавеет»), как железо в воде, содержащей растворенный кислород. [ нужна цитата ]
Встречающийся в природе марганец состоит из одного стабильного изотопа 55 Mn . Было выделено и описано несколько радиоизотопов с атомным весом от 46 u ( 46 Mn) до 72 u ( 72 Mn). Наиболее стабильными являются 53 Mn с периодом полураспада 3,7 млн лет, 54 Mn с периодом полураспада 312,2 дня и 52 Mn с периодом полураспада 5,591 день. Все остальные радиоактивные изотопы имеют период полураспада менее трёх часов, а большинство — менее одной минуты. Первичным режимом распада изотопов, более легких, чем наиболее распространенный стабильный изотоп 55 Mn, является захват электрона , а основным режимом распада более тяжелых изотопов является бета-распад . [11] Марганец также имеет три метасостояния . [11]
Марганец входит в группу элементов железа , которые, как полагают, синтезируются в крупных звездах незадолго до взрыва сверхновой . [12] 53 Mn распадается до 53 Cr с периодом полураспада 3,7 миллиона лет. Из-за относительно короткого периода полураспада 53 Mn относительно редок и образуется в результате воздействия космических лучей на железо . [13] Содержание изотопов марганца обычно сочетается с содержанием изотопов хрома и нашло применение в изотопной геологии и радиометрическом датировании . Изотопные отношения Mn–Cr подтверждают данные о 26 Al и 107 Pd в ранней истории Солнечной системы . Вариации в отношениях 53 Cr/ 52 Cr и Mn/Cr в нескольких метеоритах предполагают первоначальное соотношение 53 Mn/ 55 Mn, что указывает на то, что изотопный состав Mn–Cr должен быть результатом распада 53 Mn in situ в дифференцированных планетарных телах. Таким образом, 53 Mn является дополнительным свидетельством нуклеосинтетических процессов непосредственно перед слиянием Солнечной системы. [14] [15] [16] [17]
Известны четыре аллотропа (структурные формы) твердого марганца, обозначенные α, β, γ и δ и встречающиеся при последовательно более высоких температурах. Все они металлические, стабильны при стандартном давлении и имеют кубическую кристаллическую решетку, но их атомная структура сильно различается. [18] [19] [20]
Альфа-марганец (α-Mn) является равновесной фазой при комнатной температуре. Он имеет объемноцентрированную кубическую решетку и необычен среди элементарных металлов тем, что имеет очень сложную элементарную ячейку с 58 атомами на ячейку (29 атомов на примитивную элементарную ячейку) в четырех различных типах узлов. [21] [18] Он парамагнитен при комнатной температуре и антиферромагнитен при температуре ниже 95 К (-178 ° C). [22]
Бета-марганец (β-Mn) образуется при нагревании выше температуры перехода 973 К (700 ° C; 1290 ° F). Он имеет примитивную кубическую структуру с 20 атомами на элементарную ячейку в двух типах узлов, которая столь же сложна, как и структура любого другого элементарного металла. [23] Его легко получить в виде метастабильной фазы при комнатной температуре путем быстрой закалки. Он не демонстрирует магнитного упорядочения и остается парамагнитным вплоть до самой низкой измеренной температуры (1,1 К). [23] [24] [25]
Гамма-марганец (γ-Mn) образуется при нагревании выше 1370 К (1100 ° C; 2010 ° F). Он имеет простую гранецентрированную кубическую структуру (четыре атома на элементарную ячейку). При закалке до комнатной температуры он превращается в β-Mn, но его можно стабилизировать при комнатной температуре, легировав его не менее чем с 5 процентами других элементов (таких как C, Fe, Ni, Cu, Pd или Au), и эти растворенные вещества -стабилизированные сплавы искажаются, образуя гранецентрированную тетрагональную структуру. [26] [25]
Дельта-марганец (δ-Mn) образуется при нагревании выше 1406 К (1130 °C; 2070 °F) и стабилен до температуры плавления марганца 1519 К (1250 °C; 2270 °F). Он имеет объемноцентрированную кубическую структуру (два атома на кубическую элементарную ячейку). [19] [25]

Обычные степени окисления марганца +2, +3, +4, +6 и +7, хотя наблюдались все степени окисления от -3 до +7, кроме -2. Марганец в степени окисления +7 представлен солями интенсивно-фиолетового перманганат-аниона MnO 4 - . Перманганат калия является широко используемым лабораторным реагентом из-за его окислительных свойств; применяется как местное лекарственное средство (например, при лечении болезней рыб). Растворы перманганата калия были одними из первых красителей и фиксаторов, которые стали использовать при подготовке биологических клеток и тканей к электронной микроскопии. [28]
Помимо различных перманганатных солей, Mn(VII) представлен нестабильным летучим производным Mn 2 O 7 . Оксигалогениды (MnO 3 F и MnO 3 Cl) являются сильными окислителями . [9] Наиболее ярким примером Mn в степени окисления +6 является манганат зеленого аниона , [MnO 4 ] 2- . Манганатные соли являются полупродуктами при извлечении марганца из руд. Соединения со степенью окисления +5 несколько неуловимы, одним из примеров является синий анион гипоманганат [MnO 4 ] 3- .
Соединения со степенью окисления +5 встречаются редко и часто встречаются в сочетании с оксидным (О 2- ) или нитридным (N 3- ) лигандом. [29] [30]
Mn(IV) несколько загадочный, поскольку он широко распространен в природе, но гораздо реже встречается в синтетической химии. Самая распространенная марганцевая руда — пиролюзит — MnO2 . Это темно-коричневый пигмент многих наскальных рисунков , но он также является распространенным ингредиентом сухих батарей. Комплексы Mn(IV) хорошо известны, но они требуют сложных лигандов. Комплексы Mn(IV)-OH являются промежуточными соединениями в некоторых ферментах , включая центр выделения кислорода (OEC) в растениях. [31]
Простые производные Mn +3 встречаются редко, но могут быть стабилизированы подходящими основными лигандами. Ацетат марганца(III) — окислитель, используемый в органическом синтезе . Твердые соединения марганца (III) характеризуются сильным пурпурно-красным цветом и предпочтением искаженной октаэдрической координации в результате эффекта Яна-Теллера . [ нужна цитата ]

Наиболее распространенная степень окисления марганца в водном растворе составляет +2, который имеет бледно-розовый цвет. Известны многие соединения марганца(II), такие как аквакомплексы , полученные из сульфата марганца(II) (MnSO 4 ) и хлорида марганца(II) (MnCl 2 ). Эта степень окисления также наблюдается в минерале родохрозите ( карбонат марганца (II) ). Марганец (II) обычно существует с высоким спином, основным состоянием S = 5/2 из-за высокой энергии спаривания марганца (II). В марганце (II) нет разрешенных по спину d – d-переходов, что объясняет его слабый цвет. [32]
Марганец образует большое разнообразие металлоорганических производных, т. е. соединений со связями Mn-C. Металлоорганические производные включают многочисленные примеры Mn в его низших степенях окисления, т.е. от Mn(-III) до Mn(I). Эта область металлоорганической химии привлекательна тем, что марганец недорог и относительно малотоксичен. [ нужна цитата ]
Наибольший коммерческий интерес представляет «ММТ», метилциклопентадиенилтрикарбонил марганца , который в некоторых странах используется в качестве антидетонационного соединения, добавляемого в бензин (бензин). Он содержит Mn(I). В соответствии с другими аспектами химии Mn(II), манганоцен ( Mn(C 5 H 5 ) 2 ) является высокоспиновым. Напротив, соседнее с ним металлическое железо образует устойчивое на воздухе низкоспиновое производное в форме ферроцена ( Fe(C 5 H 5 ) 2 ). Восстановление солей Mn(II) в атмосфере монооксида углерода дает декакарбонил димарганца Mn 2 (CO) 10 , летучее твердое вещество оранжевого цвета. Устойчивость этого соединения Mn(0) (и его многих производных) на воздухе отражает мощные электроноакцепторные свойства монооксида углерода. Многие алкеновые и алкиновые комплексы происходят из Mn 2 (CO) 10 . [ нужна цитата ]
В Mn(CH 3 ) 2 (dmpe) 2 Mn(II) имеет низкий спин, что контрастирует с высокоспиновым характером его предшественника MnBr 2 (dmpe) 2 ( dmpe = (CH 3 ) 2 PCH 2 CH 2 P (СН 3 ) 2 ). [34] Полиалкильные и полиарильные производные марганца часто существуют в более высоких степенях окисления, что отражает свойства высвобождения электронов алкильных и арильных лигандов. Одним из примеров является [Mn(CH 3 ) 6 ] 2- . [ нужна цитата ]
Происхождение названия марганец сложное. В древние времена в регионах Магнетес были идентифицированы два черных минерала ( либо Магнезия , расположенная на территории современной Греции, либо Магнезия-ад-Сипилум , расположенная на территории современной Турции). [35] Их обоих называли магнами по месту их происхождения, но считалось, что они различаются по полу. Мужские магнесы притягивали железо и представляли собой железную руду, теперь известную как магнит или магнетит , которая, вероятно, и дала нам термин «магнит» . Женская магнетическая руда не притягивала железо, но использовалась для обесцвечивания стекла. Этот женский магнез позже был назван магнезией , а в наше время известен как пиролюзит или диоксид марганца . [36] Ни этот минерал, ни элементарный марганец не являются магнитными. В 16 веке стеклодувы называли диоксид марганца марганцем (обратите внимание на две буквы N вместо одной), возможно, как искажение и объединение двух слов, поскольку алхимикам и стекольщикам в конечном итоге пришлось отличать магнезию черную (черную руду) от магнезии . alba (белая руда, также из магнезии, также используемая в производстве стекла). Микеле Меркати назвал магнезию нигра марганцем , а наконец выделенный из нее металл стал называться марганцем ( нем . Mangan ). Название «магнезия» в конечном итоге стало использоваться только для обозначения белой магнезии белой (оксид магния), что дало название « магний» для свободного элемента, когда он был выделен гораздо позже. [37]

Диоксид марганца, которого много в природе, издавна использовался в качестве пигмента. Наскальные рисунки в Гаргасе возрастом от 30 000 до 24 000 лет выполнены из минеральной формы пигментов MnO 2 . [39]
Соединения марганца использовались египетскими и римскими стеклодувами для придания или удаления цвета стекла. [40] Использование в качестве «мыла стеклодувов» продолжалось в средние века до наших дней и очевидно в стекле 14-го века из Венеции . [41]

Поскольку диоксид марганца использовался в производстве стекла, он был доступен для экспериментов алхимикам, первым химикам. Игнатий Готфрид Каим (1770 г.) и Иоганн Глаубер (17 век) обнаружили, что диоксид марганца можно превратить в перманганат — полезный лабораторный реагент. [42] Каим также мог восстановить диоксид марганца, чтобы изолировать металл, но это сомнительно. [43] К середине 18 века шведский химик Карл Вильгельм Шееле использовал диоксид марганца для производства хлора . Сначала соляная кислота или смесь разбавленной серной кислоты и хлорида натрия подвергалась реакции с диоксидом марганца, а позже использовалась соляная кислота из процесса Леблана , а диоксид марганца был переработан по процессу Уэлдона . Крупным потребителем марганцевых руд было производство хлорных и гипохлоритных отбеливателей . [ нужна цитата ]
Шееле и другие знали, что пиролюзит (минеральная форма диоксида марганца) содержит новый элемент. Йохан Готлиб Ган в 1774 году выделил нечистый образец металлического марганца, восстановив его диоксид углеродом . [ нужна цитата ]
Содержание марганца в некоторых железных рудах, используемых в Греции, привело к предположениям, что сталь, произведенная из этой руды, содержит дополнительный марганец, что делает спартанскую сталь исключительно твердой. [44] Примерно в начале 19 века марганец использовался в производстве стали, и было получено несколько патентов. В 1816 году было документально подтверждено, что железо, легированное марганцем, тверже, но не более хрупко. В 1837 году британский академик Джеймс Купер отметил связь между тяжелым воздействием марганца на шахтеров и формой болезни Паркинсона . [45] В 1912 году в США были выданы патенты на защиту огнестрельного оружия от ржавчины и коррозии с помощью электрохимических конверсионных покрытий из фосфата марганца, и с тех пор этот процесс получил широкое распространение. [46]
Изобретение элемента Лекланше в 1866 году и последующее усовершенствование батарей, содержащих диоксид марганца в качестве катодного деполяризатора , увеличили спрос на диоксид марганца. До разработки никель-кадмиевых и литиевых батарей большинство батарей содержало марганец. В цинк-углеродных батареях и щелочных батареях обычно используется диоксид марганца промышленного производства, поскольку природный диоксид марганца содержит примеси. В XX веке диоксид марганца широко использовался в качестве катода для коммерческих одноразовых сухих батарей как стандартного (цинко-угольного), так и щелочного типа. [47]
Марганец составляет около 1000 ppm (0,1%) земной коры , занимая 12-е место по распространенности среди элементов земной коры. [7] Почва содержит 7–9000 частей на миллион марганца, в среднем 440 частей на миллион. [7] В атмосфере содержится 0,01 мкг/м 3 . [7] Марганец встречается главным образом в виде пиролюзита ( MnO 2 ), браунита (Mn 2+ Mn 3+ 6 )SiO 12 ), [48] псиломелана (Ba,H 2 O) 2 Mn 5 O 10 и в меньшей степени в виде родохрозит ( MnCO 3 ).

Наиболее важной марганцевой рудой является пиролюзит ( MnO 2 ). Другие экономически важные марганцевые руды обычно имеют близкое пространственное отношение к железным рудам, например сфалерит . [9] [50] Земельные ресурсы велики, но распределены неравномерно. Около 80% известных мировых ресурсов марганца находятся в Южной Африке; другие важные месторождения марганца находятся в Украине, Австралии, Индии, Китае, Габоне и Бразилии. [49] По оценкам 1978 года, на дне океана имеется 500 миллиардов тонн марганцевых конкреций . [51] Попытки найти экономически выгодные методы добычи марганцевых конкреций были оставлены в 1970-х годах. [52]
В Южной Африке большинство выявленных месторождений расположены недалеко от Хотазеля в Северо-Капской провинции (марганцевые месторождения Калахари), их запасы на 2011 год оцениваются в 15 миллиардов тонн. В 2011 году Южная Африка произвела 3,4 миллиона тонн, превзойдя все другие страны. [53]
Марганец в основном добывают в Южной Африке, Австралии, Китае, Габоне, Бразилии, Индии, Казахстане, Гане, Украине и Малайзии. [54]
Для производства ферромарганца марганцевую руду смешивают с железной рудой и углеродом, а затем восстанавливают либо в доменной печи, либо в электродуговой печи. [55] Полученный ферромарганец имеет содержание марганца 30–80%. [9] Чистый марганец, используемый для производства безжелезных сплавов, получают путем выщелачивания марганцевой руды серной кислотой и последующего процесса электролиза . [56]

Более прогрессивный процесс добычи включает прямое восстановление (низкосортной) марганцевой руды путем кучного выщелачивания . Это делается путем просачивания природного газа через дно кучи; природный газ обеспечивает тепло (должно быть не менее 850 °C) и восстановитель (окись углерода). Это превращает всю марганцевую руду в оксид марганца (MnO), который является выщелачиваемой формой. Затем руда проходит через контур измельчения , чтобы уменьшить размер частиц руды до 150–250 мкм, увеличивая площадь поверхности и способствуя выщелачиванию. Затем руду добавляют в резервуар для выщелачивания серной кислоты и двухвалентного железа (Fe 2+ ) в соотношении 1,6:1. Железо реагирует с диоксидом марганца (MnO 2 ) с образованием гидроксида железа (FeO(OH)) и элементарного марганца (Mn). [ нужна цитата ]
Этот процесс дает около 92% извлечения марганца. Затем для дальнейшей очистки марганец можно отправить на установку электролиза . [57]
В 1972 году проект ЦРУ «Азориан» через миллиардера Говарда Хьюза заказал судно «Хьюз Гломар Эксплорер» под предлогом добычи марганцевых конкреций со дна моря. [58] Это вызвало всплеск активности по сбору марганцевых конкреций, что на самом деле было непрактично. Настоящая миссия Hughes Glomar Explorer заключалась в подъеме затонувшей советской подводной лодки К-129 с целью восстановления советских кодовых книг. [59]
Богатый ресурс марганца в виде марганцевых конкреций, обнаруженных на дне океана. [60] [61] Эти конкреции, которые на 29% состоят из марганца, [62] расположены вдоль дна океана , и потенциальное воздействие добычи этих конкреций исследуется. Из-за добычи конкреций могут возникнуть физические, химические и биологические воздействия на окружающую среду, которые нарушают морское дно и вызывают образование шлейфов отложений. В состав этой взвеси входят металлы и неорганические питательные вещества, что может привести к загрязнению придонных вод растворенными токсичными соединениями. Марганцевые конкреции также служат пастбищами, жилым пространством и защитой эндо- и эпифауны. Когда эти узелки удаляются, эти системы напрямую затрагиваются. В целом это может привести к тому, что виды покинут этот район или полностью вымрут. [63] До начала самой добычи аффилированные с Организацией Объединенных Наций органы и компании, спонсируемые государством , проводят исследования в попытке полностью понять воздействие на окружающую среду в надежде смягчить это воздействие. [64]
Многие микроэлементы в океане поступают из богатых металлами гидротермальных частиц из гидротермальных источников. [65] Растворенный марганец (dMn) встречается во всем Мировом океане, 90% которого поступает из гидротермальных источников. [66] Частицы Mn образуются в плавучих шлейфах над активным источником выбросов, в то время как dMn ведет себя консервативно. [65] Концентрация Mn варьируется в зависимости от толщи воды океана. На поверхности уровень dMn повышается из-за поступления внешних источников, таких как реки, пыль и шельфовые отложения. Прибрежные отложения обычно имеют более низкие концентрации Mn, но могут увеличиваться из-за антропогенных выбросов таких отраслей, как горнодобывающая и сталелитейная промышленность, которые попадают в океан с речными стоками. Концентрации dMn на поверхности также могут повышаться биологически за счет фотосинтеза и физически за счет прибрежного апвеллинга и ветровых поверхностных течений. Внутренний цикл, такой как фотовосстановление под воздействием УФ-излучения, также может повышать уровни за счет ускорения растворения оксидов Mn и окислительного удаления, предотвращая попадание Mn в более глубокие воды. [67] Повышенные уровни на средних глубинах могут возникать вблизи срединно-океанических хребтов и гидротермальных жерл. Гидротермальные источники выбрасывают в воду жидкость, обогащенную dMn. Затем dMn может путешествовать на расстояние до 4000 км благодаря присутствующим микробным капсулам, предотвращающим обмен частицами и снижающим скорость погружения. Концентрации растворенного Mn еще выше при низком уровне кислорода. В целом, концентрации dMn обычно выше в прибрежных регионах и снижаются при перемещении к морю. [67]
Марганец встречается в почвах в трех степенях окисления: в виде двухвалентного катиона Mn 2+ и в виде буровато-черных оксидов и гидроксидов, содержащих Mn (III,IV), таких как MnOOH и MnO 2 . рН почвы и окислительно-восстановительные условия влияют на то, какая из этих трех форм Mn является доминирующей в данной почве. При значениях рН менее 6 или в анаэробных условиях преобладает Mn(II), а в более щелочных и аэробных условиях преобладают оксиды и гидроксиды Mn(III,IV). Это влияние кислотности почвы и состояния аэрации на форму Mn можно модифицировать или контролировать с помощью микробной активности. Микробное дыхание может вызывать как окисление Mn 2+ до оксидов, так и восстановление оксидов до двухвалентного катиона. [68]
Оксиды Mn(III,IV) присутствуют в виде коричневато-черных пятен и мелких узелков на частицах песка, ила и глины. Эти поверхностные покрытия на других частицах почвы имеют большую площадь поверхности и несут отрицательный заряд. Заряженные центры способны адсорбировать и удерживать различные катионы, особенно тяжелые металлы (например, Cr 3+ , Cu 2+ , Zn 2+ и Pb 2+ ). Кроме того, оксиды способны адсорбировать органические кислоты и другие соединения. Адсорбция металлов и органических соединений может затем привести к их окислению, в то время как оксиды Mn(III,IV) восстанавливаются до Mn2 + (например, Cr3 + до Cr(VI), а бесцветный гидрохинон до хиноновых полимеров чайного цвета). ). [69]
Марганец не имеет удовлетворительной замены в своих основных применениях в металлургии. [49] В небольших применениях (например, фосфатирование марганца) цинк и иногда ванадий являются жизнеспособными заменителями.

Марганец необходим для производства железа и стали благодаря своим серофиксирующим , раскисляющим и легирующим свойствам, как впервые признал британский металлург Роберт Форестер Мушет (1811–1891), который в 1856 году представил этот элемент в форме Spiegeleisen , в сталь с конкретной целью удаления избытка растворенного кислорода, серы и фосфора, чтобы улучшить ее ковкость. Производство стали , [70] включая его компонент по производству железа, отвечает за большую часть спроса на марганец, в настоящее время колеблющегося от 85% до 90% от общего спроса. [56] Марганец является ключевым компонентом недорогой нержавеющей стали . [71] [72] Часто ферромарганец (обычно около 80% марганца) является промежуточным продуктом в современных процессах.
Небольшие количества марганца улучшают обрабатываемость стали при высоких температурах за счет образования тугоплавкого сульфида и предотвращения образования жидкого сульфида железа на границах зерен. Если содержание марганца достигает 4%, охрупчивание стали становится доминирующим признаком. Охрупчивание снижается при более высоких концентрациях марганца и достигает приемлемого уровня при 8%. Сталь, содержащая от 8 до 15% марганца, имеет высокую прочность на разрыв — до 863 МПа. [73] [74] Сталь с 12% марганца была открыта в 1882 году Робертом Хэдфилдом и до сих пор известна как сталь Гадфилда (мангаллой) . Он использовался для стальных шлемов британской армии , а затем и в армии США. [75]
Марганец используется при производстве сплавов с алюминием. Алюминий с содержанием марганца примерно 1,5% обладает повышенной устойчивостью к коррозии благодаря зернам, которые поглощают примеси, которые могут привести к гальванической коррозии . [76] Коррозионностойкие алюминиевые сплавы 3004 и 3104 (от 0,8 до 1,5% марганца) используются для изготовления большинства банок для напитков . [77] До 2000 года было использовано более 1,6 миллиона тонн этих сплавов; при 1% марганца на это было потрачено 16 000 тонн марганца. [ не удалось пройти проверку ] [77]
Оксид марганца (IV) использовался в оригинальном типе сухих батарей в качестве акцептора электронов от цинка и является черноватым материалом в элементах фонарика углеродно-цинкового типа. Диоксид марганца при разрядке восстанавливается до оксида-гидроксида марганца MnO(OH), предотвращая образование водорода на аноде аккумулятора. [78]
Тот же материал действует и в новых щелочных батареях (обычно в аккумуляторных элементах), в которых используется та же основная реакция, но другая смесь электролитов. В 2002 году для этой цели было использовано более 230 тысяч тонн диоксида марганца. [47] [78]

Медные сплавы марганца, такие как манганин , обычно встречаются в шунтирующих резисторах с металлическими элементами , используемых для измерения относительно больших величин тока. Эти сплавы имеют очень низкий температурный коэффициент сопротивления и устойчивы к сере. Это делает сплавы особенно полезными в суровых автомобильных и промышленных условиях. [79]
Оксид и сульфат марганца входят в состав удобрений. В 2000 году только в США в удобрениях было использовано около 20 000 тонн этих соединений. Сопоставимое количество соединений Mn также использовалось в кормах для животных. [80]
Метилциклопентадиенилтрикарбонил марганца является добавкой в некоторые неэтилированные бензины для повышения октанового числа и уменьшения детонации двигателя . [81]
Оксид марганца(IV) (диоксид марганца, MnO 2 ) применяется в качестве реагента в органической химии для окисления бензиловых спиртов (где гидроксильная группа соседствует с ароматическим кольцом ). Диоксид марганца использовался с древности для окисления и нейтрализации зеленоватого оттенка стекла из-за следовых количеств загрязнения железом. [41] MnO 2 также используется при производстве кислорода и хлора и при сушке черных красок. В некоторых препаратах это коричневый пигмент для красок , входящий в состав натуральной умбры . [82]
Четырехвалентный марганец используется в качестве активатора в люминофорах красного свечения . Хотя известно множество соединений, которые проявляют люминесценцию , [83] большинство из них не используются в коммерческом применении из-за низкой эффективности или темно-красного излучения. [84] [85] Однако сообщалось, что несколько активированных фторидов Mn 4+ являются потенциальными красными люминофорами для тепло-белых светодиодов. [86] [87] Но на сегодняшний день только K 2 SiF 6 :Mn 4+ коммерчески доступен для использования в светодиодах теплого белого цвета . [88]
Металл иногда используется в монетах; до 2000 года единственной монетой Соединенных Штатов, в которой использовался марганец, был никель «военного времени» с 1942 по 1945 год. [89] Для производства никелевых монет традиционно использовался сплав, состоящий из 75% меди и 25% никеля. Однако из-за нехватки металлического никеля во время войны он был заменен более доступными серебром и марганцем, в результате чего получился сплав, состоящий из 56% меди, 35% серебра и 9% марганца. С 2000 года долларовые монеты , например доллар Сакагавеа и президентские монеты достоинством 1 доллар , изготавливаются из латуни, содержащей 7% марганца, с сердечником из чистой меди. [90] В обоих случаях с никелем и долларом использование марганца в монете должно было дублировать электромагнитные свойства предыдущей монеты идентичного размера и стоимости в механизмах торговых автоматов. В случае более поздних долларовых монет США марганцевый сплав должен был дублировать свойства медно-никелевого сплава, использованного в предыдущем долларе Сьюзен Б. Энтони .
Соединения марганца использовались в качестве пигментов и для окраски керамики и стекла. Коричневый цвет керамики иногда является результатом соединений марганца. [91] В стекольной промышленности соединения марганца используются для достижения двух эффектов. Марганец(III) реагирует с железом(II), уменьшая ярко-зеленый цвет стекла, образуя менее окрашенное железо(III) и слегка розовый марганец(II), компенсируя остаточный цвет железа(III). [41] Большие количества марганца используются для производства розового стекла. В 2009 году профессор Мас Субраманиан и его коллеги из Университета штата Орегон обнаружили, что марганец можно объединить с иттрием и индием с образованием интенсивно синего , нетоксичного, инертного, устойчивого к выцветанию пигмента — синего цвета YInMn — первого нового синего пигмента, открытого в 200 году. годы. [ нужна цитата ]
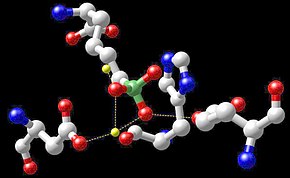
Многие классы ферментов содержат кофакторы марганца, включая оксидоредуктазы , трансферазы , гидролазы , лиазы , изомеразы и лигазы . Другими ферментами, содержащими марганец, являются аргиназа и Mn-содержащая супероксиддисмутаза ( Mn-SOD ). Некоторые обратные транскриптазы многих ретровирусов (но не лентивирусов , таких как ВИЧ ) содержат марганец. Марганецсодержащие полипептиды — это дифтерийный токсин , лектины и интегрины . [92]
Кислородвыделяющий комплекс (ОКЭ), содержащий четыре атома марганца, входит в состав фотосистемы II, содержащейся в тилакоидных мембранах хлоропластов. OEC отвечает за терминальное фотоокисление воды во время световых реакций фотосинтеза , т. е. является катализатором, производящим O2, вырабатываемым растениями. [93] [94]
Марганец является важным элементом питания человека. Он присутствует в качестве кофермента в нескольких биологических процессах, включая метаболизм макронутриентов, формирование костей и системы защиты от свободных радикалов . Это важнейший компонент десятков белков и ферментов. [6] В организме человека содержится около 12 мг марганца, в основном в костях. Остальная часть мягких тканей сосредоточена в печени и почках. [7] В человеческом мозге марганец связан с металлопротеинами марганца , особенно с глутаминсинтетазой в астроцитах . [95]
Институт медицины США (МОМ) обновил расчетные средние потребности (EAR) и рекомендуемые диетические нормы (RDA) для минералов в 2001 году. По марганцу не было достаточной информации для установления EAR и RDA, поэтому потребности описываются как оценки адекватного потребления ( ИИ). Что касается безопасности, МОМ устанавливает допустимые верхние уровни потребления (UL) для витаминов и минералов, когда есть достаточные доказательства. В случае марганца допустимая норма для взрослых установлена на уровне 11 мг/день. В совокупности EAR, RDA, AI и UL называются эталонными диетическими нормами потребления (DRI). [96] Дефицит марганца встречается редко. [97]
Европейское управление по безопасности пищевых продуктов (EFSA) называет совокупный набор информации эталонными диетическими значениями, с эталонным потреблением для населения (PRI) вместо RDA и средней потребностью вместо EAR. AI и UL определены так же, как и в США. Для людей в возрасте 15 лет и старше ИИ устанавливается на уровне 3,0 мг/день. ИИ при беременности и лактации составляет 3,0 мг/день. Для детей в возрасте 1–14 лет доза ИА увеличивается с возрастом от 0,5 до 2,0 мг/день. ИИ для взрослых выше, чем RDA в США. [98] EFSA рассмотрело тот же вопрос безопасности и решило, что информации недостаточно для установления UL. [99]
Для целей маркировки пищевых продуктов и пищевых добавок в США количество в порции выражается в процентах от дневной нормы (% ДВ). Для целей маркировки марганца 100% дневной нормы составляло 2,0 мг, но по состоянию на 27 мая 2016 года она была пересмотрена до 2,3 мг, чтобы привести ее в соответствие с RDA. [100] [101] Таблица старых и новых дневных норм для взрослых представлена в разделе «Справочная суточная норма» .
Чрезмерное воздействие или потребление может привести к состоянию, известному как марганизм , нейродегенеративному заболеванию, которое вызывает гибель дофаминергических нейронов и симптомы, похожие на болезнь Паркинсона . [7] [102]
Дефицит марганца у человека, который встречается редко, приводит к ряду медицинских проблем. Дефицит марганца вызывает деформацию скелета у животных и подавляет выработку коллагена при заживлении ран. [103]
Переносимый водой марганец имеет большую биодоступность , чем пищевой марганец. Согласно результатам исследования 2010 года, [104] более высокие уровни воздействия марганца в питьевой воде связаны с увеличением интеллектуальных нарушений и снижением коэффициентов интеллекта у детей школьного возраста. Предполагается, что долгосрочное воздействие из-за вдыхания марганца, встречающегося в природе в воде для душа, подвергает риску до 8,7 миллионов американцев. [105] Однако данные показывают, что организм человека может оправиться от некоторых неблагоприятных последствий чрезмерного воздействия марганца, если прекратить воздействие и организм сможет вывести излишки. [106]
Уровни марганца могут повышаться в морской воде в периоды гипоксии. [107] С 1990 года поступали сообщения о накоплении Mn в морских организмах, включая рыб, ракообразных, моллюсков и иглокожих. У разных видов мишенью являются определенные ткани, включая жабры, мозг, кровь, почки и печень/ гепатопанкреас . Сообщалось о физиологических эффектах у этих видов. Марганец может влиять на обновление иммуноцитов и их функциональность, например, на фагоцитоз и активацию профенолоксидазы , подавляя иммунную систему организма. Это делает микроорганизмы более восприимчивыми к инфекциям. По мере изменения климата распространение патогенов увеличивается, и для того, чтобы организмы могли выжить и защитить себя от этих патогенов, им необходима здоровая и сильная иммунная система. Если их системы будут нарушены из-за высокого уровня Mn, они не смогут бороться с этими патогенами и умрут. [66]

Метилциклопентадиенилтрикарбонил марганца (ММТ) — присадка, разработанная для замены соединений свинца в бензинах с целью повышения октанового числа . ММТ используется лишь в нескольких странах. Топливо, содержащее марганец, имеет тенденцию образовывать карбиды марганца, которые повреждают выпускные клапаны .
По сравнению с 1953 годом уровень марганца в воздухе снизился. [108] Как правило, воздействие окружающего воздуха с концентрацией Mn, превышающей 5 мкг Mn/м 3 , может привести к симптомам, вызванным Mn. Повышенная экспрессия белка ферропортина в клетках эмбриональной почки человека (HEK293) связана со снижением внутриклеточной концентрации Mn и ослаблением цитотоксичности , характеризующейся обратным снижением поглощения глутамата с помощью Mn и уменьшением утечки лактатдегидрогеназы . [109]
Воздействие марганца в США регулируется Управлением по охране труда (OSHA). [110] Люди могут подвергнуться воздействию марганца на рабочем месте, вдыхая его или проглатывая. OSHA установило законный предел ( предел допустимого воздействия ) воздействия марганца на рабочем месте на уровне 5 мг/м 3 в течение 8-часового рабочего дня. Национальный институт охраны труда (NIOSH) установил рекомендуемый предел воздействия (REL) 1 мг/м 3 в течение 8-часового рабочего дня и краткосрочный предел 3 мг/м 3 . При уровне 500 мг/м 3 марганец сразу опасен для жизни и здоровья . [111]
Марганец необходим для здоровья человека, хотя и в миллиграммовых количествах.
Текущая максимальная безопасная концентрация согласно правилам Агентства по охране окружающей среды США составляет 50 мкг Mn/л. [112]
Чрезмерное воздействие марганца чаще всего связано с марганцем — редким неврологическим расстройством, связанным с чрезмерным употреблением или вдыханием марганца. Исторически сложилось так, что люди, занятые в производстве или переработке марганцевых сплавов [113] [114], подвергались риску развития марганца; однако правила охраны труда и техники безопасности защищают работников в развитых странах. [110] Расстройство было впервые описано в 1837 году британским академиком Джоном Купером, который изучал двух пациентов, которые измельчали марганец. [45]
Манганизм – это двухфазное заболевание. На ранних стадиях опьяненный человек может испытывать депрессию, перепады настроения, компульсивное поведение и психоз. Ранние неврологические симптомы сменяются поздней стадией манганизма, напоминающей болезнь Паркинсона . Симптомы включают слабость, монотонность и замедленность речи, невыразительное лицо, тремор, походку с наклоном вперед, неспособность идти назад, не падая, ригидность и общие проблемы с ловкостью, походкой и равновесием. [45] [115] В отличие от болезни Паркинсона , манганизм не связан с потерей обоняния, и пациенты обычно не реагируют на лечение L-ДОФА . [116] Симптомы поздней стадии марганца со временем становятся более серьезными, даже если источник воздействия удален и уровень марганца в мозге возвращается к норме. [115]
Было показано, что хроническое воздействие марганца приводит к заболеванию, подобному паркинсонизму, характеризующемуся нарушениями движений. [117] Это состояние не реагирует на типичные методы лечения, используемые при лечении БП , что позволяет предположить альтернативный путь, отличный от типичной потери дофаминергических веществ в черной субстанции . [117] Марганец может накапливаться в базальных ганглиях , что приводит к аномальным движениям. [118] Мутация гена SLC30A10, переносчика оттока марганца, необходимого для снижения внутриклеточного Mn, была связана с развитием этого заболевания, подобного паркинсонизму. [119] Тельца Леви , типичные для БП, не наблюдаются при Mn-индуцированном паркинсонизме. [118]
Эксперименты на животных дали возможность изучить последствия чрезмерного воздействия марганца в контролируемых условиях. У (неагрессивных) крыс марганец вызывает поведение, убивающее мышей. [120]
Соединения марганца менее токсичны, чем соединения других распространенных металлов, таких как никель и медь . [122] Однако воздействие марганцевой пыли и паров не должно превышать предельное значение в 5 мг/м 3 даже в течение коротких периодов времени из-за уровня его токсичности. [123] Отравление марганцем связано с нарушением моторики и когнитивными расстройствами . [124]
Белок под названием DMT1 является основным транспортером при всасывании марганца из кишечника и может быть основным переносчиком марганца через гематоэнцефалический барьер . DMT1 также переносит вдыхаемый марганец через носовой эпителий . Предполагаемый механизм токсичности марганца заключается в том, что нарушение регуляции приводит к окислительному стрессу , митохондриальной дисфункции , глутамат-опосредованной эксайтотоксичности и агрегации белков. [125]
{{cite book}}: |journal=игнорируется ( помощь ){{cite book}}: |journal=игнорируется ( помощь )Красно-коричневая земля, содержащая оксиды железа и марганца, более темная, чем охра и сиена, используемая для изготовления различных пигментов.