Метилмалоновая ацидемия , также называемая метилмалоновой ацидурией , [примечание 1] представляет собой группу наследственных нарушений обмена веществ, которые мешают организму правильно расщеплять белки и жиры . [1] Это приводит к накоплению токсичного уровня метилмалоновой кислоты в жидкостях и тканях организма. Из-за нарушения метаболизма аминокислот с разветвленной цепью (BCAA) они относятся к классическим органическим ацидемиям . [2]
Метилмалоновая ацидемия имеет различные диагнозы, требования к лечению и прогнозы, которые определяются конкретной генетической мутацией, вызывающей наследственную форму заболевания. [3]
Первые симптомы могут начаться уже в первый день жизни или уже в зрелом возрасте. [4] Симптомы могут варьироваться от легких до опасных для жизни. [1] Некоторые формы могут привести к смерти, если их не диагностировать или не лечить.
Метилмалоновая ацидемия встречается с одинаковой частотой в разных этнических границах. [5]
В зависимости от пораженного гена(ов) и мутации текущие симптомы могут варьироваться от легких до опасных для жизни.
Как правило, метилмалоновая ацидемия не проявляется при рождении, поскольку симптомы не проявляются до тех пор, пока в рацион ребенка не будут добавлены белки. [10] По этой причине симптомы обычно проявляются в любое время в течение первого года жизни. [12] Однако существуют формы, симптомы которых развиваются только во взрослом возрасте. [4]
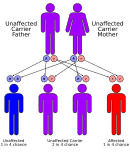
Метилмалоновая ацидемия имеет аутосомно-рецессивный тип наследования, что означает, что дефектный ген расположен на аутосоме , и чтобы заболевание затронуло заболевание, должны быть унаследованы две копии гена — по одной от каждого родителя. Родители ребенка с аутосомно-рецессивным заболеванием являются носителями одной копии дефектного гена, но обычно не страдают этим заболеванием. [ нужна цитация ] Исключением являются метилмалоновая ацидемия и гомоцистинурия типа cblX из-за вариантов гена HCFC1 , который наследуется по Х-сцепленному рецессивному типу. [13]
Ниже приведены известные генотипы, ответственные за изолированные метилмалоновые ацидемии : [13]
Тип mut далее можно разделить на подтипы mut0 и mut-, причем mut0 характеризуется полным отсутствием метилмалонил-КоА-мутазы и более тяжелыми симптомами, а mut- характеризуется пониженной активностью мутазы. [5]
Кроме того, за метилмалоновую ацидемию также ответственны следующие гены: [13] [19]
Хотя тяжелый дефицит витамина B12 в питании не всегда объединяется с наследственными вариантами, он также может привести к синдрому с такими же симптомами и лечением, как и при генетической метилмалоновой ацидемии. [37] Метилмалонил-КоА требует витамина B 12 для образования сукцинил-КоА. Когда количества B 12 недостаточно для превращения кофактора метилмалонил-КоА в сукцинил-КоА, накопление неиспользованного метилмалонил-КоА в конечном итоге приводит к метилмалоновой ацидемии. Этот диагноз часто используется как индикатор дефицита витамина B12 в сыворотке крови . [38]

При метилмалоновой ацидемии организм не может должным образом расщеплять:
В результате метилмалоновая кислота накапливается в жидкостях и тканях. У людей, страдающих этим расстройством, либо отсутствуют функциональные копии, либо адекватные уровни одного или нескольких из следующих ферментов: [6] [11] [9]
Они кратко представлены ниже:
Подсчитано, что до 60% изолированных случаев метилмалоновой ацидемии являются результатом мутированного гена MMUT , который кодирует белок метилмалонил-КоА-мутазу. Этот фермент отвечает за переваривание потенциально токсичных производных распада вышеупомянутых аминокислот и жиров, в первую очередь холестерина , [11] в частности, этот фермент превращает метилмалонил-КоА в сукцинил-КоА. [40] Без этого фермента организм не сможет нейтрализовать или удалить метилмалоновую кислоту и родственные соединения. Действие этого фермента также может быть нарушено мутациями в генах MMAA , MMAB и MMADHC , каждый из которых кодирует белок, необходимый для нормального функционирования метилмалонил-КоА-мутазы. [11]
CMAMMA, вероятно, является наиболее распространенной формой метилмалоновой ацидемии, но ее редко диагностируют из-за пропуска обычного обследования новорожденных , большого разнообразия симптомов и, в некоторых случаях, симптомов, появляющихся только во взрослом возрасте. [9] [41] Мутации гена ACSF3 приводят к дефициту митохондриального фермента, члена семейства 3 ацил-КоА-синтетазы, что приводит к повышению уровня метилмалоновой кислоты и малоновой кислоты . [9] Поскольку задачей фермента является как превращение метилмалоновой кислоты в метилмалонил-КоА, чтобы ее можно было подавать в цикл трикарбоновых кислот , так и превращение малоновой кислоты в малонил-КоА , что является первым этапом митохондриального жирового синтез кислоты (mtFASII). [42] [43] Таким образом, CMAMMA можно определить не только как органическую ацидемию , но и как дефект синтеза митохондриальных жирных кислот. [43]
Мутации в гене MCEE , который кодирует белок эпимеразы метилмалонил-КоА, также называемый метилмалонил-рацемазой, вызывают гораздо более легкую форму заболевания, чем родственный вариант мутазы метилмалонил-КоА. Как и мутаза, эпимераза расщепляет те же вещества, но в значительно меньшей степени, чем мутаза. [11] Фенотипические различия , вызванные дефицитом эпимеразы в отличие от мутазы, настолько незначительны, что в медицинском сообществе ведутся споры о том, можно ли считать этот генетический дефицит расстройством или клиническим синдромом. [44]
Эта форма кобаламина , также известная как витамин B12 , является необходимым кофактором мутазы метилмалонил-КоА. Даже при функциональной версии фермента на физиологически нормальном уровне, если B 12 не может быть преобразован в эту активную форму, мутаза не сможет функционировать. [11]
Из-за тяжести и скорости, с которой это заболевание может вызвать осложнения, если его не диагностировать, скрининг на метилмалоновую ацидемию часто включается в скрининговый осмотр новорожденных . [10] [45] С этой целью в возрасте 24–48 часов проводят пробу сухой капли крови на показатель пропионилкарнитин (С3) с целью выявления изолированных метилмалоновых ацидемий. [13] [46]
Из-за нормального уровня пропионилкарнитина и бессимптомных симптомов на момент тестирования, вероятно, наиболее распространенная форма метилмалоновой ацидемии, CMAMMA, не проходит скрининг новорожденных. [9] [13] Аутосомно-рецессивное нарушение интеллектуального развития 69 также имеет нормальный уровень пропионилкарнитина. [13] Метилмалоновая ацидемия и гомоцистинурия типа cblC, если они легкие и с поздним началом, также могут протекать. [47]
Обычно параметр метилмалоновой кислоты проверяется только в том случае, если ранее был повышен уровень пропионилкарнитина. [48]
Из-за невозможности полного расщепления аминокислот побочный продукт переваривания белков, соединение метилмалоновая кислота, обнаруживается в непропорциональной концентрации в крови и моче больных. Эти аномальные уровни используются в качестве основных диагностических критериев для диагностики расстройства. Это заболевание обычно определяется с помощью анализа мочи или анализа крови . [12] Повышенные уровни аммиака , глицина и кетоновых тел также могут присутствовать в крови и моче. [6]
С включением параметра малоновая кислота CMAMMA можно быстро отличить от классической метилмалоновой ацидемии путем расчета соотношения малоновой кислоты к метилмалоновой кислоте, но только со значениями из плазмы крови, а не из мочи. [49] Это соотношение затем также можно использовать для определения того, является ли это ЦМАММА (МА<ММА) или малоновой ацидурией (МА>ММА). [49] [7] [50]
Тест используется для дальнейшей дифференциальной диагностики и проверки эффективности лечения витамином В 12 , последний позволяет предотвратить ненужные инъекции (витамина В 12 ) детям. [51] Для лучшей сопоставимости и интерпретации отчетов пациентов Фаулер и др. разработали протокол стандартизированного теста на чувствительность к витамину B12 ( in vivo ): [51]
Кроме того, чувствительность к витамину B12 также можно проверить in vitro . [13] [51] Это может дать некоторую информацию, но не всегда может правильно предсказать реакцию организма на витамин B 12 in vivo . [13]
Окончательный диагноз подтверждается молекулярно-генетическим исследованием, если в пораженном гене(ах) обнаруживаются двуаллельные варианты патогена. Благодаря своей высокой чувствительности, более легкой доступности и неинвазивности молекулярно-генетические тесты в большинстве случаев заменяют ферментные анализы. [13] Существуют специальные мультигенные панели для метилмалоновой ацидемии, но конкретные тестируемые гены могут варьироваться от лаборатории к лаборатории и могут быть адаптированы клиницистом к индивидуальному фенотипу. [13] [19] Молекулярно-генетические методы, используемые в этих группах, варьируются от анализа последовательностей , анализа делеций/дублирования и других тестов, не основанных на секвенировании, но в подавляющем большинстве случаев диагноз ставится с помощью анализа последовательностей. [13]
Кроме того, молекулярно-генетические тесты необходимы для проверки предполагаемых диагнозов и исправления ошибочных диагнозов, которые могли быть вызваны вводящими в заблуждение симптомами и результатами теста на чувствительность к витамину B12 . [52]
Наличие метилмалоновой ацидемии также можно заподозрить с помощью КТ или МРТ , однако эти тесты ни в коем случае не являются специфичными и требуют клинических и метаболических/корреляционных исследований. [10]
Лечение всех форм этого состояния в первую очередь основано на низкобелковой диете и, в зависимости от того, каким вариантом заболевания страдает человек, на различных пищевых добавках. Все варианты реагируют на лево-изомер карнитина , поскольку неправильное расщепление затронутых веществ приводит к тому, что у больных развивается дефицит карнитина. Карнитин также способствует удалению ацил-КоА, накопление которого является обычным явлением при диетах с низким содержанием белка, путем превращения его в ацил-карнитин, который может выводиться с мочой. Некоторые формы метилмалониловой ацидемии чувствительны к кобаламину, хотя добавки цианокобаламина могут оказаться вредными для некоторых форм. [53] Если человек реагирует как на добавки кобаламина, так и на карнитин, тогда он может принимать вещества, которые включают небольшое количество проблемных аминокислот изолейцин, треонин, метионин и валин, не вызывая приступа. [10] Было обнаружено, что версии метилмалоновой ацидемии CblA и cblB чувствительны к кобаламину.
Более радикальное лечение включает трансплантацию почки или печени от донора без этого заболевания. Инородные органы будут производить функциональную версию дефектных ферментов и переваривать метилмалоновую кислоту, однако все недостатки трансплантации органов, конечно, применимы и в этой ситуации. [10] Имеются данные, позволяющие предположить, что центральная нервная система может метаболизировать метилмалонил-КоА в системе, изолированной от остального организма. Если это так, трансплантация не может обратить вспять неврологические эффекты метилмалоновой кислоты, предшествовавшие трансплантации, или предотвратить дальнейшее повреждение головного мозга за счет продолжающегося накопления. [54] [40]
Доклинические исследования на животных моделях показали, что терапия мРНК также подходит для лечения редких метаболических заболеваний, включая изолированную метилмалоновую ацидемию. [55] [56] В этом контексте стоит упомянуть мРНК-3705- кандидата для терапии мут-метилмалоновой ацидемии от биотехнологической компании Moderna , которая в настоящее время находится в фазе 1/2. [57]
Здесь следует упомянуть исследуемый низкомолекулярный терапевтический препарат HST5040 от HemoShear Therapeutics для лечения метилмалоновой ацидурии и пропионовой ацидурии, который в настоящее время находится на стадии 2. [58] [59] При ежедневном приеме внутрь или через желудочный зонд он предназначен для предотвращения токсического накопления пропионил-КоА и метилмалонил-КоА или их производных путем отвода КоА от пути пропионил-КоА, что приводит к нормальному или близкому к нормальному состоянию. уровни этих метаболитов и потенциально улучшают метаболическое состояние и пути производства энергии. [60] [59]
Еще одним разрабатываемым низкомолекулярным терапевтическим средством является BBP-671 от BridgeBio Pharma для лечения нейродегенерации, связанной с пантотенаткиназой (PKAN), пропионовой и метилмалоновой ацидемии, которая в настоящее время находится в фазе 1. [61] Ожидается, что BBP-671 , активируя пантотенаткиназы , будет увеличить выработку КоА из витамина В 5 и тем самым нормализовать обменные процессы. [62]
Хотя четких стадий заболевания нет, метилмалоновая ацидемия является прогрессирующим состоянием; симптомы этого расстройства усугубляются по мере увеличения концентрации метилмалоновой кислоты. Если провоцирующие белки и жиры не исключить из рациона, их накопление может привести к непоправимому повреждению почек или печени и, в конечном итоге, к смерти. [10]
Прогноз будет варьироваться в зависимости от тяжести состояния и реакции человека на лечение. Прогноз обычно лучше для пациентов с вариантами, реагирующими на кобаламин, и необнадеживающим для тех, кто страдает вариантами, не реагирующими на кобаламин. [40] Более легкие варианты встречаются среди населения чаще, чем более тяжелые. [12] Даже при изменении диеты и непрерывном медицинском уходе предотвратить неврологические повреждения у людей с невосприимчивой ацидемией может оказаться невозможным. [40] Без надлежащего лечения или диагностики первый приступ ацидемии нередко заканчивается смертельным исходом. [10]
Несмотря на эти проблемы, с тех пор, как оно было впервые выявлено в 1967 году, лечение и понимание этого состояния улучшились до такой степени, что уже не является чем-то необычным, что даже люди с неподдающимися лечению формами метилмалоновой ацидемии могут достичь взрослого возраста и даже вынашивать и рожать детей. безопасно. [54]
Первая метилмалоновая ацидемия была охарактеризована Oberholzer et al. в 1967 году. [63] [54]
Уже давно сообщалось о том, что метилмалоновая кислота может оказывать катастрофическое воздействие на нервную систему; однако механизм, посредством которого это происходит, так и не был определен. В 2015 году было опубликовано исследование влияния метилмалоновой кислоты на нейроны, выделенные из эмбрионов крыс в условиях in vitro с использованием контрольной группы нейронов, обработанных альтернативной кислотой с аналогичным pH . [64] Эти тесты показали, что метилмалоновая кислота вызывает уменьшение размера клеток и увеличение скорости клеточного апоптоза в зависимости от концентрации, при этом более экстремальные эффекты наблюдаются при более высоких концентрациях. [64] Кроме того, микроматричный анализ этих обработанных нейронов также показал, что на эпигенетическом уровне метилмалоновая кислота изменяет скорость транскрипции 564 генов, в частности, включая те, которые участвуют в апоптозе, p53 и сигнальных путях MAPK . [64]
Поскольку превращение метилмалонил-КоА в сукцинил-КоА происходит внутри митохондрий , митохондриальная дисфункция в результате снижения функции цепи переноса электронов уже давно подозревается как особенность метилмалоновой ацидемии. Недавние [ когда? ] исследование показало, что на крысиных моделях митохондрии крыс, страдающих этим заболеванием, вырастают до необычных размеров, получивших название мегамитохондрии . Эти мегамитохондрии также, по-видимому, имеют деформированную внутреннюю структуру и потерю электронного богатства в своем матриксе . Эти мегамитохондрии также показали признаки снижения функции дыхательной цепи, особенно в дыхательном комплексе IV , который функционировал только с эффективностью около 50%. Аналогичные изменения были выявлены в митохондриях образца печени, взятого при трансплантации у 5-летнего мальчика, страдающего метилмалоновой ацидемией мутного типа. [65]
Тематические исследования у нескольких пациентов с невосприимчивой к мутной метилмалоновой ацидемией со специфической мутацией, обозначенной p.P86L, позволили предположить, что может существовать возможность дальнейшего подразделения на метилмалоновую ацидемию mut-типа. [66] Хотя в настоящее время неясно, связано ли это с конкретной мутацией или ранним выявлением и лечением, несмотря на полное отсутствие ответа на добавки кобаламина, у этих людей, по-видимому, развивалась в основном доброкачественная и почти полностью бессимптомная версия метилмалоновой ацидемии. [66] Несмотря на постоянный повышенный уровень метилмалоновой кислоты в крови и моче, эти люди по большей части выглядели нормально развитыми. [66]