Озон ( / ˈ oʊ z oʊ n / ) (или трикислород ) — неорганическая молекула с химической формулой O
3. Это бледно-голубой газ с характерным резким запахом. Это аллотроп кислорода , который гораздо менее стабилен, чем двухатомный аллотроп O.
2, распадающийся в нижних слоях атмосферы до O
2( дикислород ). Озон образуется из дикислорода под действием ультрафиолетового (УФ) света и электрических разрядов в атмосфере Земли . Он присутствует в очень низких концентрациях по всей атмосфере, при этом его самая высокая концентрация находится в озоновом слое стратосферы , который поглощает большую часть ультрафиолетового (УФ) излучения Солнца .
Запах озона напоминает запах хлора , и многие люди ощущают его при концентрациях всего лишь0,1 ppm в воздухе. Структура О 3 озона была определена в 1865 году. Позже было доказано, что молекула имеет изогнутую структуру и слабо диамагнитна . В стандартных условиях озон представляет собой бледно-голубой газ, который конденсируется при криогенных температурах в темно-синюю жидкость и, наконец, в фиолетово-черное твердое вещество . Нестабильность озона по отношению к более распространенному дикислороду такова, что как концентрированный газ, так и жидкий озон могут взрыворазлагаться при повышенных температурах, физическом ударе или быстром нагревании до точки кипения. [5] [6] Поэтому он используется в коммерческих целях только в низких концентрациях.
Озон является мощным окислителем (в гораздо большей степени, чем дикислород ) и имеет множество промышленных и потребительских применений, связанных с окислением. Однако тот же самый высокий окислительный потенциал приводит к тому, что озон повреждает слизистые и дыхательные ткани животных, а также ткани растений при концентрациях выше примерно0,1 ч/млн . Хотя это делает озон серьезной опасностью для органов дыхания и загрязнителем вблизи уровня земли , более высокая концентрация в озоновом слое (от двух до восьми частей на миллион) полезна, предотвращая попадание вредного ультрафиолетового света на поверхность Земли.
Тривиальное название «озон» является наиболее часто используемым и предпочтительным названием IUPAC . Систематические названия 2λ 4 -триоксидиен [ сомнительно ] и катена-триоксиген , действительные названия ИЮПАК , построены по замещающей и аддитивной номенклатуре соответственно. Название озон происходит от слова «озеин» (ὄζειν), греческого причастия среднего рода настоящего времени, обозначающего запах, [7] обозначающего характерный запах озона.
В соответствующих контекстах озон можно рассматривать как триоксидан с удаленными двумя атомами водорода, и поэтому триоксиданилиден можно использовать в качестве систематического названия в соответствии с замещающей номенклатурой. По умолчанию эти имена не учитывают радикальность молекулы озона. В еще более конкретном контексте это также может называться нерадикальным синглетным основным состоянием, тогда как дирадикальное состояние называется триоксидандиилом .
Триоксидандиил (или озонид ) используется бессистемно для обозначения группы заместителя (-OOO-). Следует проявлять осторожность, чтобы не перепутать название группы с контекстно-зависимым названием озона, приведенным выше.

.jpg/440px-Smyths_revised_ozonometer,_1865._(9660571191).jpg)
В 1785 году голландский химик Мартинус ван Марум проводил эксперименты с электрическим искрением над водой, когда заметил необычный запах, который он объяснил электрическими реакциями, не понимая, что на самом деле он создал озон. [8] [9]
Полвека спустя Кристиан Фридрих Шенбейн заметил тот же резкий запах и узнал в нем запах, часто следующий за ударом молнии . В 1839 году ему удалось выделить газообразный химикат и назвать его «озоном», от греческого слова « озеин » ( ὄζειν ), означающего «пахнуть». [10] [11] По этой причине Шенбейну обычно приписывают открытие озона. [12] [13] [14] [8] Он также отметил сходство запаха озона с запахом фосфора, а в 1844 году доказал, что продукт реакции белого фосфора с воздухом идентичен. [10] Последующую попытку назвать озон «электрифицированным кислородом» он высмеял, предложив называть озон из белого фосфора «фосфорированным кислородом». [10] Формула озона O 3 не была определена до 1865 года Жаком-Луи Соре [15] и подтверждена Шёнбейном в 1867 году. [10] [16]
На протяжении большей части второй половины 19-го века и вплоть до 20-го века натуралисты и любители здоровья считали озон полезным компонентом окружающей среды. Официальным слоганом Бомонта, штат Калифорния , было «Бомонт: зона озона», о чем свидетельствуют открытки и фирменные бланки Торговой палаты. [17] Натуралисты, работающие на открытом воздухе, часто считали, что возвышенности полезны из-за содержания там озона. «Существует совершенно другая атмосфера [на большей высоте] с достаточным количеством озона для поддержания необходимой энергии [для работы]», - писал натуралист Генри Хеншоу , работающий на Гавайях. [18] Приморский воздух считался полезным для здоровья из-за содержания в нем озона. Запах, породивший это убеждение, на самом деле является запахом галогенированных метаболитов морских водорослей [19] и диметилсульфида . [20]
Большая часть привлекательности озона, по-видимому, обусловлена его «свежим» запахом, который вызывал ассоциации с очищающими свойствами. Ученые отметили его вредное воздействие. В 1873 году Джеймс Дьюар и Джон Грей Маккендрик задокументировали, что лягушки становились вялыми, птицы задыхались, а в крови кроликов наблюдалось снижение уровня кислорода после воздействия «озонированного воздуха», который «оказывал разрушительное действие». [21] [12] Сам Шенбейн сообщил, что в результате вдыхания озона возникли боли в груди, раздражение слизистых оболочек и затруднение дыхания, а мелкие млекопитающие погибли. [22] В 1911 году Леонард Хилл и Мартин Флэк заявили в Трудах Королевского общества B , что оздоровительное воздействие озона «простым повторением стало неотъемлемой частью общего убеждения; и все же точные физиологические доказательства в пользу его положительного воздействия до сих пор почти полностью отсутствовал ... Единственное, что до сих пор достигнуто, полностью достоверное знание о физиологическом действии озона состоит в том, что он вызывает раздражение и отек легких, а также смерть при вдыхании в относительно сильной концентрации в течение любого времени. " [12] [23]
Во время Первой мировой войны озон испытывался в военном госпитале Королевы Александры в Лондоне в качестве возможного дезинфицирующего средства для ран. Газ подавался непосредственно на раны на протяжении 15 минут. Это привело к повреждению как бактериальных клеток, так и тканей человека. Другие методы дезинфекции, такие как орошение антисептиками , были сочтены предпочтительными. [12] [24]
До 1920-х годов не было уверенности в том, что небольшие количества оксозона O
4, также присутствовали в пробах озона из-за сложности применения методов аналитической химии к взрывчатому концентрированному химическому веществу. [25] [26] В 1923 году Георг-Мария Шваб (работавший над докторской диссертацией под руководством Эрнста Германа Ризенфельда ) был первым, кто успешно затвердел озон и провел точный анализ, который окончательно опроверг гипотезу оксозона. [25] [26] Дальнейшие до сих пор неизмеренные физические свойства чистого концентрированного озона были определены группой Ризенфельда в 1920-х годах. [25]

Озон — бесцветный или бледно-голубой газ, мало растворимый в воде и гораздо лучше растворимый в инертных неполярных растворителях, таких как четыреххлористый углерод или фторуглероды, в которых он образует синий раствор. При 161 К (-112 ° C; -170 ° F) он конденсируется с образованием темно-синей жидкости . Опасно допускать, чтобы эта жидкость нагрелась до точки кипения, поскольку как концентрированный газообразный озон, так и жидкий озон могут взорваться. При температуре ниже 80 К (-193,2 ° C; -315,7 ° F) он образует фиолетово-черное твердое вещество . [27]
Большинство людей могут обнаружить около 0,01 мкмоль/моль озона в воздухе, который имеет очень специфический резкий запах, чем-то напоминающий хлорный отбеливатель . Воздействие от 0,1 до 1 мкмоль/моль вызывает головные боли, жжение в глазах и раздражение дыхательных путей. [28] Даже низкие концентрации озона в воздухе очень разрушительны для органических материалов, таких как латекс, пластик и легочная ткань животных.
Озон слабо диамагнитен. [29]
Согласно экспериментальным данным микроволновой спектроскопии , озон представляет собой изогнутую молекулу с симметрией C 2v (аналогично молекуле воды ). [30] Расстояния O–O составляют 127,2 пм (1,272 Å ). Угол О–О–О составляет 116,78°. [31] Центральный атом представляет собой sp² -гибридизацию с одной неподеленной парой. Озон — полярная молекула с дипольным моментом 0,53 Д. [32] Молекулу можно представить как резонансный гибрид с двумя участвующими структурами, каждая из которых имеет одинарную связь на одной стороне и двойную связь на другой. Соглашение имеет общий порядок облигаций 1,5 для обеих сторон. Он изоэлектронен нитрит -аниону . Встречающийся в природе озон может состоять из замещенных изотопов ( 16 O, 17 O, 18 O). Циклическая форма была предсказана, но не наблюдалась.

Озон – один из самых мощных известных окислителей , он гораздо сильнее O 2 . Он также нестабилен при высоких концентрациях и распадается на обычный двухатомный кислород. Период его полураспада зависит от атмосферных условий, таких как температура, влажность и движение воздуха. В лабораторных условиях период полураспада составит в среднем ~1500 минут (25 часов) в неподвижном воздухе при комнатной температуре (24 °C), нулевой влажности и нулевой смене воздуха в час. [33]
Эта реакция протекает быстрее с повышением температуры. Дефлаграция озона может быть вызвана искрой и происходить при концентрации озона 10 мас.% или выше. [34]
Озон также можно получить из кислорода на аноде электрохимической ячейки. Эта реакция может создать меньшие количества озона для исследовательских целей. [35]
Это можно наблюдать как нежелательную реакцию в газовом аппарате Гофмана при электролизе воды, когда напряжение устанавливается выше необходимого.
Озон окисляет большинство металлов (кроме золота , платины и иридия ) до оксидов металлов в их высшей степени окисления . Например:
Озон также окисляет оксид азота до диоксида азота :
Эта реакция сопровождается хемилюминесценцией . NO 2 может дополнительно окисляться до нитратного радикала :
Образующийся NO 3 может реагировать с NO 2 с образованием пятиокиси азота ( N 2 O 5 ).
Твердый перхлорат нитрония можно получить из газов NO 2 , ClO 2 и O 3 :
Озон не реагирует с солями аммония , но окисляет аммиак до нитрата аммония :
Озон реагирует с углеродом с образованием углекислого газа даже при комнатной температуре:
Озон окисляет сульфиды до сульфатов . Например, сульфид свинца(II) окисляется до сульфата свинца(II) :
Серную кислоту можно производить из озона, воды и элементарной серы или диоксида серы :
В газовой фазе озон реагирует с сероводородом с образованием диоксида серы:
Однако в водном растворе одновременно протекают две конкурирующие реакции: одна с образованием элементарной серы, а другая с образованием серной кислоты :
Алкены могут быть окислительно расщеплены озоном в процессе, называемом озонолизом , с образованием спиртов, альдегидов, кетонов и карбоновых кислот, в зависимости от второго этапа обработки.
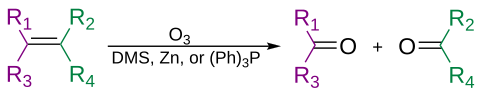
Озон также может расщеплять алкины с образованием кислотного ангидрида или дикетона . [37] Если реакция проводится в присутствии воды, ангидрид гидролизуется с образованием двух карбоновых кислот .
Обычно озонолиз проводят в растворе дихлорметана при температуре -78°С. После последовательного расщепления и перегруппировки образуется органический озонид. При восстановительной обработке (например , цинк в уксусной кислоте или диметилсульфиде ) образуются кетоны и альдегиды, при окислительной обработке (например, водная или спиртовая перекись водорода ) образуются карбоновые кислоты. [38]
Все три атома озона также могут вступать в реакцию, как при реакции хлорида олова(II) с соляной кислотой и озоном:
Перхлорат йода можно получить обработкой йода , растворенного в холодной безводной хлорной кислоте , озоном:
Озон также может реагировать с йодидом калия с образованием кислорода и газообразного йода, которые можно титровать для количественного определения: [39]
Озон можно использовать для реакций горения и горючих газов; озон обеспечивает более высокие температуры, чем сжигание диоксида кислорода ( O 2 ). Ниже представлена реакция сгорания субнитрида углерода , которая также может вызывать повышение температуры:
Озон может реагировать при криогенных температурах. При 77 К (-196,2 ° C; -321,1 ° F) атомарный водород реагирует с жидким озоном с образованием радикала супероксида водорода , который димеризуется : [40]
Озон — токсичное вещество, [41] [42] обычно встречающееся или образующееся в среде обитания человека (кабины самолетов, офисы с копировальными аппаратами, лазерными принтерами, стерилизаторы...), и его каталитическое разложение очень важно для уменьшения загрязнения. Этот тип разложения наиболее широко используется, особенно с твердыми катализаторами, и имеет множество преимуществ, таких как более высокая конверсия при более низкой температуре. Кроме того, продукт и катализатор могут быть мгновенно разделены, и таким образом катализатор может быть легко извлечен без использования какой-либо операции разделения. Более того, наиболее часто используемыми материалами при каталитическом разложении озона в газовой фазе являются благородные металлы, такие как Pt, Rh или Pd, и переходные металлы, такие как Mn, Co, Cu, Fe, Ni или Ag.
Есть две другие возможности разложения озона в газовой фазе:
Первый — это термическое разложение, при котором озон можно разложить только под действием тепла. Проблема в том, что этот тип разложения происходит очень медленно при температуре ниже 250 °C. Однако скорость разложения можно увеличить, работая при более высоких температурах, но это потребует высоких затрат энергии.
Второй — фотохимическое разложение, которое заключается в излучении озона ультрафиолетовым излучением (УФ) и приводит к образованию кислорода и радикальной перекиси. [43]
Процесс разложения озона представляет собой сложную реакцию, включающую две элементарные реакции, которые в конечном итоге приводят к образованию молекулярного кислорода, а это означает, что порядок реакции и закон скорости не могут быть определены стехиометрией подобранного уравнения.
Общая реакция:
Закон ставки (соблюдается):
Было установлено, что разложение озона следует кинетике первого порядка, и из приведенного выше закона скорости можно определить, что частичный порядок по молекулярному кислороду равен -1, а по озону - 2, поэтому глобальный порядок реакции равен 1.
Разложение озона состоит из двух элементарных стадий: первая соответствует мономолекулярной реакции, поскольку одна молекула озона распадается на два продукта (молекулярный кислород и кислород). Тогда кислород с первого этапа является промежуточным продуктом, поскольку он участвует в качестве реагента на втором этапе, который является бимолекулярной реакцией, поскольку существуют два разных реагента (озон и кислород), которые дают один продукт, соответствующий молекулярному кислороду. в газовой фазе.
Шаг 1: Мономолекулярная реакция
Шаг 2: Бимолекулярная реакция
Эти два этапа имеют разные скорости реакции: первый обратим и быстрее, чем вторая реакция, которая медленнее, поэтому это означает, что определяющим этапом является вторая реакция, и она используется для определения наблюдаемой скорости реакции. Законы скорости реакции для каждого этапа следующие:
Следующий механизм позволяет объяснить наблюдаемый экспериментально закон скорости разложения озона, а также определить порядки реакций по озону и кислороду, с помощью которых будет определяться общий порядок реакции. Более медленная стадия, бимолекулярная реакция, определяет скорость образования продукта, и, учитывая, что на этой стадии образуются две молекулы кислорода, закон скорости имеет следующий вид:
Однако это уравнение зависит от концентрации кислорода (промежуточной), которую можно определить с учетом первого шага. Поскольку первый этап протекает быстрее и обратимее, а второй — медленнее, реагенты и продукты первого этапа находятся в равновесии, поэтому концентрацию промежуточного продукта можно определить следующим образом:
Затем, используя эти уравнения, скорость образования молекулярного кислорода будет такой, как показано ниже:
Наконец, представленный механизм позволяет установить экспериментально наблюдаемую скорость с константой скорости ( K obs ) и соответствующую кинетике первого порядка следующим образом: [44]
где
Восстановление озона дает озонид- анион O−3. Производные этого аниона взрывоопасны и должны храниться при криогенных температурах. Известны озониды всех щелочных металлов . KO 3 , RbO 3 и CsO 3 можно получить из соответствующих супероксидов:
Хотя KO3 может образовываться, как указано выше, он также может образовываться из гидроксида калия и озона: [45]
NaO 3 и LiO 3 необходимо получать действием CsO 3 в жидком NH 3 на ионообменную смолу , содержащую ионы Na + или Li + : [46]
Раствор кальция в аммиаке реагирует с озоном с образованием озонида аммония , а не озонида кальция: [40]
Озон можно использовать для удаления железа и марганца из воды с образованием осадка , который можно отфильтровать:
Озон также окисляет растворенный в воде сероводород до сернистой кислоты :
Эти три реакции играют центральную роль в использовании озоновой очистки колодезной воды.
Озон также обезвреживает цианиды , превращая их в цианаты .
Озон также полностью разлагает мочевину : [47]
Озон представляет собой изогнутую трехатомную молекулу с тремя модами колебаний: симметричным растяжением (1103,157 см -1 ), изгибом (701,42 см -1 ) и антисимметричным растяжением (1042,096 см -1 ). [48] Симметричное растяжение и изгиб являются слабыми поглотителями, но антисимметричное растяжение является сильным и ответственно за то, что озон является важным второстепенным парниковым газом . Этот ИК-диапазон также используется для обнаружения окружающего и атмосферного озона, хотя измерения на основе УФ-излучения более распространены. [49]
Электромагнитный спектр озона довольно сложен. Обзор можно увидеть в спектральном атласе газообразных молекул, представляющих интерес для атмосферы, в УФ/ВИД-диапазоне MPI Mainz. [50]
Все полосы диссоциативны, что означает, что молекула распадается на O + O 2 после поглощения фотона. Наиболее важным поглощением является полоса Хартли, простирающаяся от чуть выше 300 нм до чуть выше 200 нм. Именно эта полоса отвечает за поглощение УФ-С в стратосфере.
На стороне высоких волн полоса Хартли переходит в так называемую полосу Хаггинса, которая быстро затухает, пока не исчезает на ~360 нм. Выше 400 нм, простираясь далеко в ближний ИК-диапазон, расположены полосы Чаппиуса и Вульфа. Там неструктурированные полосы поглощения полезны для обнаружения высоких концентраций озона в окружающей среде, но они настолько слабы, что не имеют большого практического эффекта.
Имеются дополнительные полосы поглощения в дальнем УФ, которые медленно увеличиваются от 200 нм до достижения максимума при ~120 нм.



Стандартный способ выразить общий уровень озона (количество озона в данном вертикальном столбце) в атмосфере — использовать единицы Добсона . Точечные измерения сообщаются в виде мольных долей в нмоль/моль (частей на миллиард, частей на миллиард) или в виде концентраций в мкг/м 3 . Изучение концентрации озона в атмосфере началось в 1920-х годах. [51]
Самые высокие уровни озона в атмосфере находятся в стратосфере , в регионе, также известном как озоновый слой, на высоте от 10 до 50 км над поверхностью (или от 6 до 31 мили). Однако даже в этом «слое» концентрация озона составляет всего от двух до восьми частей на миллион, поэтому большую часть кислорода там составляет дикислород O 2 в количестве около 210 000 частей на миллион по объему. [52]
Озон в стратосфере в основном образуется из коротковолновых ультрафиолетовых лучей с длиной волны от 240 до 160 нм. Кислород начинает слабо поглощать при 240 нм в полосах Герцберга, но большая часть кислорода диссоциирует за счет поглощения в сильных полосах Шумана-Рунге между 200 и 160 нм, где озон не поглощает. Хотя свет с более короткой длиной волны, простирающийся даже до рентгеновского предела, достаточно энергичен, чтобы диссоциировать молекулярный кислород, его относительно мало, и сильное солнечное излучение в Лайман-альфа, 121 нм, падает в точке, где молекулярный кислород впитываемость минимальна. [53]
Процесс создания и разрушения озона называется циклом Чепмена и начинается с фотолиза молекулярного кислорода.
с последующей реакцией атома кислорода с другой молекулой кислорода с образованием озона.
где «М» обозначает третье тело, уносящее избыточную энергию реакции. Молекула озона может затем поглотить фотон УФ-С и диссоциировать.
Избыточная кинетическая энергия нагревает стратосферу, когда атомы O и молекулярный кислород разлетаются и сталкиваются с другими молекулами. Это преобразование ультрафиолетового света в кинетическую энергию нагревает стратосферу. Атомы кислорода, образующиеся при фотолизе озона, затем реагируют обратно с другими молекулами кислорода, как и на предыдущем этапе, образуя больше озона. В чистой атмосфере, содержащей только азот и кислород, озон может реагировать с атомарным кислородом с образованием двух молекул O 2 :
Оценку скорости этой стадии завершения цикла превращения атомарного кислорода обратно в озон можно найти, просто взяв отношения концентраций O 2 и O 3 . Реакция обрыва катализируется присутствием определенных свободных радикалов, наиболее важными из которых являются гидроксил (OH), оксид азота (NO), а также атомарные хлор (Cl) и бром (Br). Во второй половине 20-го века было обнаружено, что количество озона в стратосфере снижается, в основном из-за увеличения концентрации хлорфторуглеродов ( CFC) и подобных хлорированных и бромированных органических молекул . Обеспокоенность по поводу последствий снижения концентрации озона для здоровья привела к Монреальскому протоколу 1987 года , запрету на производство многих химикатов , разрушающих озоновый слой , а в первом и втором десятилетии 21 века к началу восстановления концентрации стратосферного озона.

Озон в озоновом слое отфильтровывает длины волн солнечного света от УФ-лучей примерно от 200 нм до 315 нм, с пиковым поглощением озона при длине волны примерно 250 нм. [54] Это поглощение УФ-излучения озоном важно для жизни, поскольку оно расширяет поглощение УФ-излучения обычным кислородом и азотом в воздухе (которые поглощают все длины волн < 200 нм) через более низкие УФ-С (200–280 нм) и всю Диапазон УФ-В (280–315 нм). Небольшая непоглощенная часть УФ-В, которая остается после прохождения через озон, вызывает солнечные ожоги у людей и прямое повреждение ДНК в живых тканях как растений, так и животных. Влияние озона на лучи УФ-В среднего диапазона иллюстрируется его воздействием на УФ-В с длиной волны 290 нм, интенсивность излучения которого в верхних слоях атмосферы в 350 миллионов раз выше, чем на поверхности. Тем не менее, достаточное количество УФ-В-излучения аналогичной частоты достигает земли, чтобы вызвать солнечный ожог, и эти же длины волн также относятся к числу тех, которые ответственны за выработку витамина D у людей.
Озоновый слой мало влияет на более длинные волны УФ-излучения, называемые УФ-А (315–400 нм), но это излучение не вызывает солнечных ожогов или прямого повреждения ДНК. Хотя УФ-А, вероятно, действительно вызывает долгосрочное повреждение кожи у некоторых людей, оно не так опасно для растений и для здоровья поверхностных организмов на Земле в целом ( дополнительную информацию о ближнем ультрафиолете см. в разделе «Ультрафиолетовое излучение») .
Озон низкого уровня (или тропосферный озон) является загрязнителем атмосферы. [55] Он не выбрасывается непосредственно автомобильными двигателями или промышленными предприятиями, а образуется в результате реакции солнечного света на воздух, содержащий углеводороды и оксиды азота , которые реагируют с образованием озона непосредственно в источнике загрязнения или на многих километрах по ветру.
Озон напрямую реагирует с некоторыми углеводородами, такими как альдегиды , и таким образом начинает их удаление из воздуха, но эти продукты сами по себе являются ключевыми компонентами смога . Фотолиз озона под действием УФ-излучения приводит к образованию гидроксильного радикала HO•, который играет роль в удалении углеводородов из воздуха, но также является первым шагом в создании компонентов смога, таких как пероксиацилнитраты , которые могут быть мощными. раздражители глаз. Время жизни тропосферного озона в атмосфере составляет около 22 дней; его основные механизмы удаления заключаются в отложении на землю, вышеупомянутой реакции с образованием HO•, а также реакциями с OH и пероксирадикалом HO 2 •. [56]
Имеются данные о значительном снижении урожайности в сельском хозяйстве из-за увеличения приземного озона и загрязнения, которые мешают фотосинтезу и тормозят общий рост некоторых видов растений. [57] [58] Агентство по охране окружающей среды США (EPA) предложило вторичное регулирование для уменьшения ущерба урожаю в дополнение к первичному регулированию, предназначенному для защиты здоровья человека.
Определенными примерами городов с повышенными показателями содержания озона являются Денвер, Колорадо ; Хьюстон, Техас ; и Мехико , Мексика . В Хьюстоне показатель составляет около 41 нмоль/моль, тогда как в Мехико гораздо более опасен показатель около 125 нмоль/моль. [58]
Низкий уровень озона, или тропосферный озон, является наиболее тревожным типом загрязнения озоном в городских районах, и его уровень в целом увеличивается. [59] Загрязнение озоном в городских районах влияет на более плотное население и усугубляется большим количеством транспортных средств, которые выбрасывают в атмосферу загрязняющие вещества NO 2 и ЛОС , которые являются основными источниками проблемных уровней озона. [60] Загрязнение озоном в городских районах вызывает особую озабоченность в связи с повышением температуры и увеличением смертности, связанной с жарой, во время волн жары . [61] Во время волн жары в городских районах загрязнение приземного озона может быть на 20% выше, чем обычно. [62] Загрязнение озоном в городских районах достигает более высокого уровня летом и осенью, что может быть объяснено погодными условиями и характером дорожного движения. [60] Люди, живущие в нищете, в целом больше страдают от загрязнения, хотя эти группы населения с меньшей вероятностью способствуют повышению уровня загрязнения. [63]
Как упоминалось выше, Денвер, штат Колорадо, является одним из многих городов США с высоким содержанием озона. По данным Американской ассоциации легких , район Денвер-Аврора является 14-м по уровню загрязнения озоном районом в США [64]. Проблема высоких уровней озона не нова для этого региона. В 2004 году Агентство по охране окружающей среды определило Денверское метро / Норт-Фронт-Рейндж [b] как недостижимые зоны в соответствии со стандартом 8-часового озона 1997 года, [65] , но позже отложило этот статус до 2007 года. не соответствуют стандартам качества воздуха EPA. В ответ на это был разработан Колорадский план действий по озону, и в этот план были внесены многочисленные изменения. Первым крупным изменением стало то, что тестирование автомобилей на выбросы было распространено по всему штату и охватило большее количество округов, которые ранее не требовали проведения испытаний на выбросы, например, районы Лаример и округ Уэлд. Также были внесены изменения для снижения выбросов оксидов азота (NOx) и летучих органических соединений (ЛОС), что должно помочь снизить уровень озона.
Одним из крупных факторов, способствующих высокому уровню озона в этом районе, является нефтегазовая промышленность , расположенная в бассейне Денвер-Джулсбург (DJB), который пересекается с большинством городских агломераций Колорадо. Озон создается естественным путем в стратосфере Земли, но также создается в тропосфере в результате деятельности человека. Кратко упоминалось выше, NOx и ЛОС реагируют с солнечным светом, образуя озон посредством процесса, называемого фотохимией. События с повышенным уровнем озона на один час (<75 частей на миллиард) «происходят в период с июня по август, что указывает на то, что повышенный уровень озона обусловлен региональной фотохимией». [66] Согласно статье Университета Колорадо-Боулдер: «Выбросы летучих органических соединений из нефти и природного газа играют важную роль в производстве озона и могут способствовать повышению уровня O 3 в Переднем хребте Северного Колорадо (NCFR)». . [66] Используя комплексный анализ для исследования характера ветра и выбросов от крупных операций по добыче нефти и природного газа, авторы пришли к выводу, что «повышенные уровни O 3 в СКФ преимущественно коррелируют с воздушным транспортом из С-ВЮВ, которые являются наветренными секторами, где Операции по добыче нефти и газа расположены на территории месторождения Ваттенберг DJB». [66]
В Плане действий по озону Колорадо, созданном в 2008 году, существуют планы по оценке «контроля выбросов крупных промышленных источников NOx» и «требований к контролю в масштабе штата для новых резервуаров для нефти и газового конденсата и пневматических клапанов». [67] В 2011 году был опубликован Региональный план борьбы с дымкой, который включал более конкретный план по снижению выбросов NOx. Эти усилия становится все труднее реализовать, и на их реализацию уйдут многие годы. Конечно, есть и другие причины, по которым уровень озона остается высоким. К ним относятся: растущее население, что означает увеличение выбросов от автомобилей, и горы вдоль NCFR, которые могут улавливать выбросы. Если интересно, ежедневные показатели качества воздуха можно найти на веб-сайте Департамента общественного здравоохранения и окружающей среды штата Колорадо. [68] Как отмечалось ранее, Денвер по сей день продолжает испытывать высокие уровни озона. Потребуются многие годы и системный подход для борьбы с проблемой высокого уровня озона в Переднем хребте Колорадо.

Газообразный озон разрушает любой полимер, имеющий олефиновые или двойные связи в структуре цепи, например, натуральный каучук , нитриловый каучук и бутадиен-стирольный каучук. Изделия, изготовленные с использованием этих полимеров, особенно подвержены воздействию, в результате чего трещины со временем становятся длиннее и глубже, причем скорость роста трещин зависит от нагрузки, которую несет резиновый компонент, и концентрации озона в атмосфере. Такие материалы можно защитить, добавив антиозонанты , такие как воски, которые связываются с поверхностью, создавая защитную пленку, или смешиваются с материалом и обеспечивают долгосрочную защиту. Например , озоновое растрескивание раньше было серьезной проблемой для автомобильных шин [69] , но для современных шин это не проблема. С другой стороны, многие важные продукты, такие как прокладки и уплотнительные кольца , могут подвергаться воздействию озона, образующегося в системах сжатого воздуха. Топливопроводы , изготовленные из армированной резины, также подвержены воздействию, особенно в моторном отсеке, где электрические компоненты выделяют некоторое количество озона. Хранение резиновых изделий в непосредственной близости от электродвигателя постоянного тока может ускорить растрескивание озона. Коллектор двигателя генерирует искры, которые, в свою очередь, производят озон .
Хотя озон присутствовал на уровне земли до промышленной революции , пиковые концентрации сейчас намного выше, чем доиндустриальные уровни, и даже фоновые концентрации вдали от источников загрязнения существенно выше. [70] [71] Озон действует как парниковый газ , поглощая часть инфракрасной энергии, излучаемой Землей. Количественно оценить парниковый эффект озона сложно, поскольку он не присутствует в одинаковых концентрациях по всему миру. Однако наиболее широко признанные научные оценки, касающиеся изменения климата (например, Третий оценочный доклад Межправительственной группы экспертов по изменению климата ) [72] предполагают, что радиационное воздействие тропосферного озона составляет около 25% от воздействия углекислого газа .
Годовой потенциал глобального потепления тропосферного озона составляет от 918 до 1022 тонн эквивалента углекислого газа /тонну тропосферного озона. Это означает, что в расчете на одну молекулу озон в тропосфере оказывает радиационное воздействие примерно в 1000 раз сильнее, чем углекислый газ . Однако тропосферный озон — недолговечный парниковый газ, который разлагается в атмосфере гораздо быстрее, чем углекислый газ . Это означает, что за 20-летний период потенциал глобального потепления тропосферного озона намного меньше, примерно от 62 до 69 тонн эквивалента углекислого газа на тонну тропосферного озона. [73]
Из-за своей недолговечности тропосферный озон не оказывает сильного глобального воздействия, но оказывает очень сильное радиационное воздействие в региональном масштабе. Фактически, есть регионы мира, где тропосферный озон имеет радиационное воздействие до 150% углекислого газа . [74] Например, показано, что увеличение содержания озона в тропосфере ответственно за ~30% потепления внутренних частей верхней части Южного океана в период с 1955 по 2000 год. [75]
В течение последних нескольких десятилетий ученые изучали влияние острого и хронического воздействия озона на здоровье человека. Сотни исследований показывают, что озон вреден для людей на уровнях, которые в настоящее время наблюдаются в городских районах. [76] [77] Было показано, что озон влияет на дыхательную, сердечно-сосудистую и центральную нервную системы. Показано, что ранняя смертность и проблемы репродуктивного здоровья и развития также связаны с воздействием озона. [78]
Американская ассоциация легких определила пять групп населения, которые особенно уязвимы к воздействию вдыхания озона: [79]
Дополнительные данные свидетельствуют о том, что женщины, люди с ожирением и люди с низкими доходами также могут подвергаться более высокому риску воздействия озона, хотя необходимы дополнительные исследования. [79]
Острое воздействие озона варьируется от нескольких часов до нескольких дней. Поскольку озон — это газ, он напрямую влияет на легкие и всю дыхательную систему. Вдыхание озона вызывает воспаление и острые, но обратимые изменения в функции легких, а также гиперреактивность дыхательных путей. [80] Эти изменения приводят к одышке, хрипу и кашлю, которые могут усугубить заболевания легких, такие как астма или хроническая обструктивная болезнь легких (ХОБЛ), что приводит к необходимости лечения. [81] [82] Было показано, что острое и хроническое воздействие озона вызывает повышенный риск респираторных инфекций по следующему механизму. [83]
Было проведено множество исследований для определения механизма вредного воздействия озона, особенно на легкие. Эти исследования показали, что воздействие озона вызывает изменения иммунного ответа в легочной ткани, что приводит к нарушению как врожденного, так и адаптивного иммунного ответа, а также к изменению защитной функции эпителиальных клеток легких. [84] Считается, что эти изменения в иммунном ответе и связанная с ним воспалительная реакция являются факторами, которые, вероятно, способствуют повышенному риску легочных инфекций, а также ухудшению или провоцированию астмы и реактивности дыхательных путей после воздействия приземного загрязнения озоном. [84] [85]
Врожденная (клеточная) иммунная система состоит из различных химических сигналов и типов клеток, которые действуют в широком смысле и против нескольких типов патогенов, обычно бактерий или инородных тел/веществ в организме хозяина. [85] [86] Клетки врожденной системы включают фагоциты и нейтрофилы, [86] которые, как полагают, вносят вклад в механизм озоновой патологии в легких, поскольку было показано, что функционирование этих типов клеток меняется после воздействия озона. . [85] Было показано , что макрофаги, клетки, которые служат для уничтожения патогенов или инородных материалов посредством процесса «фагоцитоза», [86] изменяют уровень воспалительных сигналов, которые они выделяют в ответ на озон, либо повышая регуляцию, либо приводя к при воспалительной реакции в легких или подавлении и снижении иммунной защиты. [84] Нейтрофилы, еще один важный тип клеток врожденной иммунной системы, который в первую очередь нацелен на бактериальные патогены, [86] обнаруживаются в дыхательных путях в течение 6 часов после воздействия высоких уровней озона. Однако, несмотря на высокие уровни в тканях легких, их способность уничтожать бактерии, по-видимому, ухудшается из-за воздействия озона. [84]
Адаптивная иммунная система — это ветвь иммунитета, которая обеспечивает долговременную защиту за счет выработки антител, нацеленных на определенные патогены, а также подвержена воздействию высокого воздействия озона. [85] [86] Лимфоциты, клеточный компонент адаптивного иммунного ответа, после воздействия озона производят повышенное количество воспалительных химических веществ, называемых «цитокинами», что может способствовать гиперреактивности дыхательных путей и ухудшению симптомов астмы. [84]
Эпителиальные клетки дыхательных путей также играют важную роль в защите человека от патогенов. В нормальной ткани эпителиальный слой образует защитный барьер, а также содержит специализированные ресничные структуры, которые очищают легкие от инородных тел, слизи и болезнетворных микроорганизмов. Под воздействием озона реснички повреждаются и мукоцилиарный клиренс возбудителей снижается. Более того, эпителиальный барьер ослабевает, что позволяет патогенам преодолевать его, размножаться и распространяться в более глубокие ткани. В совокупности эти изменения в эпителиальном барьере помогают сделать людей более восприимчивыми к легочным инфекциям. [84]
Вдыхание озона влияет не только на иммунную систему и легкие, но также может повлиять на сердце. Озон вызывает кратковременный вегетативный дисбаланс, приводящий к изменению частоты сердечных сокращений и снижению вариабельности сердечного ритма; [87] и воздействие высоких доз в течение всего лишь одного часа приводит к наджелудочковой аритмии у пожилых людей, [88] оба увеличивают риск преждевременной смерти и инсульта. Озон также может приводить к вазоконстрикции, что приводит к повышению системного артериального давления, что способствует увеличению риска сердечной заболеваемости и смертности у пациентов с ранее существовавшими заболеваниями сердца. [89] [90]
Вдыхание озона в течение периодов более восьми часов в течение недель, месяцев или лет определяет хроническое воздействие. Многочисленные исследования предполагают серьезное влияние этого воздействия на здоровье различных групп населения.
Одно исследование обнаруживает значительную положительную связь между хроническим озоном и смертностью от всех причин, сердечно-сосудистых и респираторных заболеваний с увеличением риска на 2%, 3% и 12% на 10 частей на миллиард [ 91] и сообщает о связи (95% ДИ) годового содержания озона. и смертность от всех причин с коэффициентом риска 1,02 (1,01–1,04) и сердечно-сосудистой смертностью 1,03 (1,01–1,05). Аналогичное исследование обнаруживает аналогичные связи со смертностью от всех причин и даже более серьезные последствия для смертности от сердечно-сосудистых заболеваний. [92] Повышенный риск смертности от респираторных причин связан с длительным хроническим воздействием озона. [93]
Хронический озон оказывает пагубное воздействие на детей, особенно больных астмой. Риск госпитализации детей с астмой увеличивается при хроническом воздействии озона; дети младшего возраста и люди с низким доходом подвергаются еще большему риску. [94]
Взрослые, страдающие респираторными заболеваниями (астма, [95] ХОБЛ, [96] рак легких [97] ), подвергаются более высокому риску смертности и заболеваемости, а пациенты в критическом состоянии имеют повышенный риск развития острого респираторного дистресс-синдрома с хроническим воздействием озона, поскольку хорошо. [98]
Генераторы озона, продаваемые как воздухоочистители, намеренно производят газообразный озон. [42] Их часто продают для борьбы с загрязнением воздуха в помещениях, а для описания озона используют вводящие в заблуждение термины. В некоторых примерах его описывают как «активированный кислород» или «чистый воздух», предполагая, что озон является здоровым или «лучшим» видом кислорода. [42] Однако, по данным Агентства по охране окружающей среды , «есть доказательства того, что при концентрациях, не превышающих стандарты общественного здравоохранения, озон неэффективен при удалении многих вызывающих запах химикатов» и «при использовании в концентрациях, не превышающих согласно стандартам общественного здравоохранения, озон, применяемый в воздухе помещений, не эффективно удаляет вирусы, бактерии, плесень и другие биологические загрязнители». [42] Кроме того, в другом отчете говорится, что «результаты некоторых контролируемых исследований показывают, что концентрации озона, значительно превышающие эти стандарты [безопасности для человека], возможны, даже если пользователь следует инструкциям по эксплуатации производителя». [99]
У Калифорнийского совета по воздушным ресурсам есть страница со списком воздухоочистителей (многие с ионизаторами ), которые соответствуют предельному содержанию озона в помещении, равному 0,050 частей на миллион. [100] Из этой статьи:
Все портативные устройства для очистки воздуха в помещениях, продаваемые в Калифорнии, должны быть сертифицированы Калифорнийским советом по воздушным ресурсам (CARB). Чтобы получить сертификацию, воздухоочистители должны быть проверены на электрическую безопасность и выбросы озона, а также соответствовать предельной концентрации выбросов озона в 0,050 частей на миллион. Для получения дополнительной информации о правилах посетите правила воздухоочистителя.


Прекурсоры озона представляют собой группу загрязняющих веществ, преимущественно выделяющихся при сжигании ископаемого топлива . Загрязнение приземным озоном ( тропосферный озон ) создается вблизи поверхности Земли в результате воздействия ультрафиолетовых лучей дневного света на эти предшественники. Озон на уровне земли образуется в основном из прекурсоров ископаемого топлива, но естественным предшественником является метан , и очень низкий естественный фоновый уровень озона на уровне земли считается безопасным. В этом разделе рассматриваются последствия для здоровья сжигания ископаемого топлива, в результате которого содержание приземного озона значительно превышает фоновый уровень.
Существует множество доказательств того, что приземный озон может нанести вред функции легких и раздражать дыхательную систему . [55] [102] Воздействие озона (и загрязняющих веществ, которые его производят) связано с преждевременной смертью , астмой , бронхитом , сердечным приступом и другими сердечно-легочными проблемами. [103] [104]
Было доказано, что длительное воздействие озона увеличивает риск смерти от респираторных заболеваний . [42] Исследование 450 000 человек, живущих в городах США, выявило значительную корреляцию между уровнем озона и респираторными заболеваниями в течение 18-летнего периода наблюдения. Исследование показало, что у людей, живущих в городах с высоким уровнем озона, таких как Хьюстон или Лос-Анджелес, риск смерти от заболеваний легких увеличивается более чем на 30%. [105] [106]
Рекомендации по качеству воздуха, такие как рекомендации Всемирной организации здравоохранения , Агентства по охране окружающей среды США (EPA) и Европейского Союза , основаны на детальных исследованиях, направленных на определение уровней, которые могут вызвать измеримые вредные последствия для здоровья .
По мнению ученых из Агентства по охране окружающей среды, на восприимчивых людей может отрицательно повлиять уровень озона всего в 40 нмоль/моль. [104] [107] [108] В ЕС текущее целевое значение концентрации озона составляет 120 мкг/м 3 , что составляет около 60 нмоль/моль. Эта цель распространяется на все государства-члены в соответствии с Директивой 2008/50/EC. [109] Концентрация озона измеряется как максимальное среднесуточное среднее значение за 8 часов, и целевой показатель не должен превышаться более чем 25 календарных дней в году, начиная с января 2010 года. Хотя директива требует в будущем строгого соблюдения 120 мкг /м 3 (т.е. средняя концентрация озона не должна превышаться ни в один день года), для этого требования не установлена дата, и это рассматривается как долгосрочная цель. [110]
В США Закон о чистом воздухе предписывает Агентству по охране окружающей среды установить национальные стандарты качества окружающего воздуха для ряда загрязняющих веществ, включая приземный озон, а округа, не соблюдающие эти стандарты, обязаны принять меры по снижению их уровней. В мае 2008 года по постановлению суда Агентство по охране окружающей среды снизило стандарт по озону с 80 нмоль/моль до 75 нмоль/моль. Этот шаг вызвал споры, поскольку собственные ученые и консультативный совет Агентства рекомендовали снизить стандарт до 60 нмоль/моль. [104] Многие группы общественного здравоохранения и охраны окружающей среды также поддержали стандарт 60 нмоль/моль, [111] а Всемирная организация здравоохранения рекомендует 100 мкг/м 3 (51 нмоль/моль). [112]
7 января 2010 года Агентство по охране окружающей среды США (EPA) объявило о предлагаемых изменениях к Национальному стандарту качества окружающего воздуха (NAAQS) в отношении загрязняющего озона, основного компонента смога:
... EPA предлагает вместо этого установить уровень 8-часового первичного стандарта, который был установлен на уровне 0,075 мкмоль/моль в окончательном правиле 2008 года, на более низком уровне в диапазоне от 0,060 до 0,070 мкмоль/моль, чтобы обеспечить повышенную защиту детей и других групп риска от множества O
3– связанные с этим неблагоприятные последствия для здоровья, которые варьируются от снижения функции легких и усиления респираторных симптомов до серьезных показателей респираторной заболеваемости, включая обращения в отделения неотложной помощи и госпитализацию по респираторным причинам, и, возможно, сердечно-сосудистую заболеваемость, а также общую неслучайную и сердечно-легочную смертность. [113 ]
26 октября 2015 г. Агентство по охране окружающей среды опубликовало окончательное правило, вступающее в силу 28 декабря 2015 г., которое изменило 8-часовой первичный NAAQS с 0,075 частей на миллион до 0,070 частей на миллион. [114]
Агентство по охране окружающей среды разработало индекс качества воздуха (AQI), чтобы помочь широкой общественности объяснить уровни загрязнения воздуха. В соответствии с действующими стандартами среднее молярное содержание озона за восемь часов от 85 до 104 нмоль/моль описывается как «вредное для здоровья для чувствительных групп», от 105 до 124 нмоль/моль как «вредное для здоровья», а от 125 нмоль/моль до 404. нмоль/моль как «очень вредно для здоровья». [115]
Озон также может присутствовать в загрязнении воздуха внутри помещений , отчасти из-за работы электронного оборудования, такого как копировальные аппараты. Также известно, что существует связь между увеличением количества пыльцы, грибковых спор и озона, вызванным грозами, и госпитализацией больных астмой . [116]
В викторианскую эпоху один британский народный миф утверждал, что запах моря создается озоном. Фактически, характерный «запах моря» вызван диметилсульфидом , химическим веществом, вырабатываемым фитопланктоном . Британцы викторианской эпохи считали полученный запах «бодрящим». [117]
Исследование по оценке совместного воздействия озона и жары на смертность во время волн жары в Европе в 2003 году пришло к выводу, что они, по всей видимости, являются аддитивными. [118]
Озон, наряду с реактивными формами кислорода, такими как супероксид , синглетный кислород , перекись водорода и ионы гипохлорита , вырабатывается лейкоцитами и другими биологическими системами (например, корнями бархатцев ) как средство разрушения инородных тел. Озон напрямую реагирует с двойными органическими связями. Кроме того, когда озон распадается на дикислород, образуются свободные радикалы кислорода , которые обладают высокой реакционной способностью и способны повредить многие органические молекулы . Более того, считается, что мощные окислительные свойства озона могут быть фактором, способствующим воспалению . Причинно-следственная связь того, как в организме образуется озон и что он делает, все еще находится на стадии рассмотрения и по-прежнему подлежит различным интерпретациям, поскольку другие химические процессы в организме могут вызывать некоторые из тех же реакций. Имеются данные, связывающие катализируемый антителами путь окисления воды в иммунном ответе человека с выработкой озона. В этой системе озон образуется путем катализируемого антителами производства триоксидана из воды и синглетного кислорода, вырабатываемого нейтрофилами. [119]
При вдыхании озон вступает в реакцию с соединениями, выстилающими легкие, с образованием специфических метаболитов холестерина, которые, как полагают, способствуют образованию и патогенезу атеросклеротических бляшек (форма сердечно-сосудистых заболеваний ). Было подтверждено, что эти метаболиты естественным образом встречаются в атеросклеротических артериях человека и относятся к классу секостеринов, называемых атероналами , образующихся в результате озонолиза двойной связи холестерина с образованием 5,6-секостерола [120] , а также вторичного продукта конденсации посредством альдолизации. [121]
Предполагается, что озон оказывает неблагоприятное воздействие на рост растений: «... озон снижает общее количество хлорофиллов, каротиноидов и концентрацию углеводов, а также увеличивает содержание 1-аминоциклопропан-1-карбоновой кислоты (АКК) и выработку этилена. У обработанных растений Запас аскорбата в листьях был уменьшен, в то время как перекисное окисление липидов и утечка растворенных веществ были значительно выше, чем в контрольной группе, не содержащей озона. Данные показали, что озон запускает защитные механизмы против окислительного стресса в цитрусовых». [122] Исследования, в которых использовались растения перца в качестве модели, показали, что озон снижает урожайность и изменяет качество фруктов. [123] [124] Кроме того, также наблюдалось снижение уровня хлорофиллов и антиоксидантной защиты в листьях, а также повышение уровня активных форм кислорода (АФК) и повреждение липидов и белков. [123] [124]
Исследование 2022 года пришло к выводу, что Восточная Азия теряет урожай на 63 миллиарда долларов в год из-за загрязнения озоном, побочным продуктом сгорания ископаемого топлива. Китай теряет около трети своего потенциального производства пшеницы и одну четверть производства риса. [125] [126]
Из-за сильных окислительных свойств озона он является основным раздражителем, особенно поражающим глаза и дыхательную систему, и может быть опасным даже при низких концентрациях. Канадский центр по безопасности и гигиене труда сообщает, что:
Даже очень низкие концентрации озона могут быть вредны для верхних дыхательных путей и легких. Тяжесть травм зависит как от концентрации озона, так и от продолжительности воздействия. Даже очень кратковременное воздействие относительно низких концентраций может привести к тяжелому и необратимому повреждению легких или смерти» [127] .
Чтобы защитить работников, потенциально подвергающихся воздействию озона, Управление по охране труда США установило допустимый предел воздействия (PEL) 0,1 мкмоль/моль (29 CFR 1910.1000, таблица Z-1), рассчитанный как средневзвешенное значение по времени за 8 часов. Более высокие концентрации особенно опасны, и NIOSH установил предел немедленной опасности для жизни и здоровья (IDLH) 5 мкмоль/моль. [128] Рабочие помещения, где озон используется или где он может производиться, должны иметь достаточную вентиляцию, и разумно иметь монитор озона, который будет подавать сигнал тревоги, если концентрация превышает требования OSHA PEL. Непрерывные мониторы озона доступны от нескольких поставщиков.
Повышенное воздействие озона может наблюдаться на пассажирских самолетах , уровень которого зависит от высоты и атмосферной турбулентности. [129] Правила Федерального управления гражданской авиации США устанавливают предел в 250 нмоль/моль при максимальном среднем за четыре часа уровне 100 нмоль/моль. [130] Некоторые самолеты оснащены преобразователями озона в системе вентиляции для снижения воздействия на пассажиров. [129]

Генераторы озона , или озонаторы , [131] используются для производства озона для очистки воздуха или удаления запахов дыма в незанятых помещениях. Эти генераторы озона могут производить более 3 г озона в час. Озон часто образуется в природе в условиях, когда О 2 не вступает в реакцию. [28] Озон, используемый в промышленности, измеряется в мкмоль/моль (ppm, частей на миллион), нмоль/моль (ppb, частей на миллиард), мкг/м 3 , мг/ч (миллиграммы в час) или весовых процентах. Режим применяемых концентраций составляет от 1% до 5% (по воздуху) и от 6% до 14% (по кислороду) для методов старшего поколения. Новые электролитические методы позволяют достичь концентрации растворенного озона в выходящей воде от 20% до 30%.
Температура и влажность играют большую роль в том, сколько озона образуется с помощью традиционных методов генерации (таких как коронный разряд и ультрафиолетовое излучение). Методы старого поколения будут производить менее 50% номинальной мощности при работе во влажном окружающем воздухе, а не в очень сухом воздухе. Новые генераторы, использующие электролитические методы, могут достичь более высокой чистоты и растворения за счет использования молекул воды в качестве источника производства озона.

Это наиболее распространенный тип генератора озона для большинства промышленных и личных целей. Хотя существуют варианты метода получения озона с помощью коронального разряда «горячей искры», включая генераторы озона медицинского и промышленного класса, эти устройства обычно работают с помощью трубки коронного разряда или озоновой пластины. [132] [133] Они, как правило, экономически эффективны и не требуют источника кислорода, кроме окружающего воздуха, для производства озона с концентрацией 3–6%. Колебания окружающего воздуха, вызванные погодой или другими условиями окружающей среды, вызывают изменчивость производства озона. Однако они также производят оксиды азота в качестве побочного продукта. Использование осушителя воздуха может уменьшить или исключить образование азотной кислоты за счет удаления водяного пара и увеличения производства озона. При комнатной температуре азотная кислота превращается в пар, который опасен при вдыхании. Симптомы могут включать боль в груди, одышку, головные боли, сухость в носу и горле, вызывающую ощущение жжения. Использование концентратора кислорода может еще больше увеличить производство озона и еще больше снизить риск образования азотной кислоты за счет удаления не только водяного пара, но и основной массы азота.
УФ-генераторы озона, или вакуумно-ультрафиолетовые (ВУФ) генераторы озона, используют источник света, который генерирует узкополосный ультрафиолетовый свет, разновидность света, производимого Солнцем. Солнечное ультрафиолетовое излучение поддерживает озоновый слой в стратосфере Земли. [134]
УФ-генераторы озона используют окружающий воздух для производства озона, не используются системы подготовки воздуха (осушитель воздуха или концентратор кислорода), поэтому эти генераторы, как правило, дешевле. Однако УФ-генераторы озона обычно производят озон с концентрацией около 0,5% или ниже, что ограничивает потенциальную скорость производства озона. Другим недостатком этого метода является то, что он требует воздействия источника УФ-излучения на окружающий воздух (кислород) в течение более длительного периода времени, и любой газ, который не подвергается воздействию источника УФ-излучения, не будет обработан. Это делает УФ-генераторы непрактичными для использования в ситуациях, когда речь идет о быстро движущихся потоках воздуха или воды ( например, стерилизация воздуха в воздуховодах ). Производство озона является одной из потенциальных опасностей ультрафиолетового бактерицидного облучения . Генераторы озона VUV используются в плавательных бассейнах и спа- центрах с объемом воды в миллионы галлонов. Генераторы озона VUV, в отличие от генераторов коронного разряда, не производят вредных побочных продуктов азота, а также, в отличие от систем коронного разряда, генераторы озона VUV чрезвычайно хорошо работают во влажной воздушной среде. Также обычно нет необходимости в дорогостоящих механизмах удаления газов, а также нет необходимости в осушителях воздуха или концентраторах кислорода, которые требуют дополнительных затрат и обслуживания.
В методе холодной плазмы чистый газообразный кислород подвергается воздействию плазмы , создаваемой DBD . Двухатомный кислород расщепляется на отдельные атомы, которые затем воссоединяются в триплеты, образуя озон. В отрасли часто ошибочно маркируют некоторые генераторы озона DBD как генераторы коронного разряда CD. Обычно все генераторы озона с плоскими металлическими электродами производят озон методом диэлектрического барьерного разряда. Машины холодной плазмы используют чистый кислород в качестве источника входного сигнала и производят озон с максимальной концентрацией около 24%. Они производят гораздо большее количество озона за определенный период времени по сравнению с производством ультрафиолета, эффективность которого составляет около 2%. Разряды проявляются как нитевидный перенос электронов (микроразряды) в зазоре между двумя электродами. Чтобы равномерно распределить микроразряды, необходимо использовать диэлектрический изолятор для разделения металлических электродов и предотвращения образования дуги.
Электролитическая генерация озона (ЭОГ) расщепляет молекулы воды на H 2 , O 2 и O 3 . В большинстве методов EOG газообразный водород удаляется, оставляя кислород и озон в качестве единственных продуктов реакции. Таким образом, EOG может достичь более высокого растворения в воде без других конкурирующих газов, обнаруженных в методе коронного разряда, таких как газы азота, присутствующие в окружающем воздухе. Этот метод генерации позволяет достичь концентрации 20–30% и не зависит от качества воздуха, поскольку в качестве исходного материала используется вода. Производство озона электролитическим способом обычно невыгодно из-за высокого перенапряжения, необходимого для производства озона по сравнению с кислородом. Вот почему озон не образуется при обычном электролизе воды. Однако можно увеличить перенапряжение кислорода путем тщательного выбора катализатора, при котором озон преимущественно образуется при электролизе. В качестве катализаторов для этого подхода обычно выбирают диоксид свинца [135] или алмаз, легированный бором. [136]
Соотношение озона и кислорода улучшается за счет увеличения плотности тока на аноде, охлаждения электролита вокруг анода до температуры, близкой к 0 °C, использования кислого электролита (например, разбавленной серной кислоты) вместо основного раствора и применения вместо него импульсного тока. округа Колумбия. [137]
Озон нельзя хранить и транспортировать, как другие промышленные газы (поскольку он быстро распадается на двухатомный кислород), и поэтому его необходимо производить на месте. Доступные генераторы озона различаются расположением и конструкцией высоковольтных электродов. При производственных мощностях более 20 кг в час газоводяной трубчатый теплообменник может использоваться в качестве заземлителя и комплектоваться трубчатыми высоковольтными электродами на стороне газа. Режим типичного давления газа составляет около 2 бар (200 кПа ) абсолютного давления в кислороде и 3 бара (300 кПа) абсолютного давления в воздухе. На крупных объектах можно установить электроэнергию в несколько мегаватт , подаваемую в виде однофазного переменного тока частотой от 50 до 8000 Гц и пиковым напряжением от 3000 до 20 000 вольт. Приложенное напряжение обычно обратно пропорционально приложенной частоте.
Доминирующим параметром, влияющим на эффективность генерации озона, является температура газа, которая контролируется температурой охлаждающей воды и/или скоростью газа. Чем прохладнее вода, тем лучше синтез озона. Чем ниже скорость газа, тем выше концентрация (но тем меньше чистого производимого озона). В типичных промышленных условиях почти 90% эффективной мощности рассеивается в виде тепла, и его необходимо отводить достаточным потоком охлаждающей воды.
Из-за высокой реакционной способности озона можно использовать лишь некоторые материалы, такие как нержавеющая сталь (качество 316L), титан , алюминий (при отсутствии влаги), стекло , политетрафторэтилен или поливинилиденфторид . Витон можно использовать при ограничении постоянных механических сил и отсутствии влажности (ограничения по влажности применяются в зависимости от рецептуры). Гипалон можно использовать с ограничением, что с ним не контактирует вода, за исключением нормальных атмосферных уровней. Охрупчивание или усадка – распространенная причина разрушения эластомеров под воздействием озона. Растрескивание озона — распространенная причина выхода из строя эластомерных уплотнений, таких как уплотнительные кольца .
Силиконовые каучуки обычно подходят для использования в качестве прокладок при концентрациях озона ниже 1 мас.%, например, в оборудовании для ускоренного старения образцов резины.
Озон может образовываться из O
2электрическими разрядами и действием электромагнитного излучения высокой энергии . Неподавленная дуга в электрических контактах, щетках двигателя или механических переключателях разрушает химические связи атмосферного кислорода, окружающего контакты [ O
2→ 2О]. Свободные радикалы кислорода внутри и вокруг дуги рекомбинируют с образованием озона [ O
3]. [138] Определенное электрооборудование выделяет значительные уровни озона. Это особенно верно в отношении устройств, использующих высокое напряжение , таких как ионные очистители воздуха , лазерные принтеры , копировальные аппараты , электрошокеры и аппараты для дуговой сварки . Электродвигатели , использующие щетки, могут генерировать озон из-за повторяющихся искрений внутри устройства. Большие двигатели, в которых используются щетки, например те, которые используются в лифтах или гидравлических насосах, будут генерировать больше озона, чем двигатели меньшего размера.
Озон аналогичным образом образуется в результате явления грозы Кататумбо на реке Кататумбо в Венесуэле , хотя нестабильность озона делает сомнительным его влияние на озоносферу. [139] Это крупнейший в мире природный генератор озона, что дает основания для внесения его в список Всемирного наследия ЮНЕСКО . [140]

В лаборатории озон можно получить путем электролиза с использованием 9-вольтовой батареи , катода в виде карандашного графитового стержня , анода из платиновой проволоки и 3- молярного электролита из серной кислоты . [141] Происходят следующие полуклеточные реакции :
где E° представляет собой стандартный потенциал электрода .
В результате реакции три эквивалента воды превращаются в один эквивалент озона и три эквивалента водорода . Образование кислорода является конкурирующей реакцией.
Он также может быть создан дугой высокого напряжения . В своей простейшей форме высоковольтный переменный ток, такой как выход трансформатора с неоновой вывеской, подключается к двум металлическим стержням, концы которых расположены достаточно близко друг к другу, чтобы обеспечить возникновение дуги. Образующаяся дуга преобразует атмосферный кислород в озон.
Часто желательно содержать озон. Это можно сделать с помощью аппарата, состоящего из двух концентрических стеклянных трубок, герметично соединенных сверху, с газовыми отверстиями сверху и снизу внешней трубки. Во внутренний сердечник должен быть вставлен кусок металлической фольги, подключенный к одной стороне источника питания. Другая сторона источника питания должна быть подключена к другому куску фольги, обернутому вокруг внешней трубки. Источник сухого O
2применяется к нижнему порту. Когда к выводам фольги приложено высокое напряжение, электрический разряд будет разряжаться между сухим диоксидом кислорода в середине и образовывать О.
3и О
2который будет вытекать из верхнего порта. Это называется озонатор Симена. Реакцию можно резюмировать следующим образом: [28]
Наибольшее применение озон находит в производстве фармацевтических препаратов , синтетических смазочных материалов и многих других коммерчески полезных органических соединений , где он используется для разрыва углерод -углеродных связей. [28] Его также можно использовать для отбеливания веществ и для уничтожения микроорганизмов в воздухе и источниках воды. [142] Многие муниципальные системы питьевой воды убивают бактерии с помощью озона вместо более распространенного хлора . [143] Озон обладает очень высоким окислительным потенциалом . [144] Озон не образует хлорорганических соединений и не остается в воде после обработки. Озон может образовывать предполагаемый канцерогенный бромат в исходной воде с высокими концентрациями бромидов . Закон США о безопасной питьевой воде требует, чтобы эти системы вводили такое количество хлора, чтобы поддерживать в трубах минимум 0,2 мкмоль/моль остаточного свободного хлора , основываясь на результатах регулярных испытаний. Там, где имеется много электроэнергии , озон является экономически эффективным методом очистки воды, поскольку он производится по требованию и не требует транспортировки и хранения опасных химикатов. После разложения он не оставляет вкуса и запаха в питьевой воде.
Хотя рекламируется, что низкие уровни озона могут использоваться в качестве дезинфицирующего средства в жилых домах, концентрация озона в сухом воздухе, необходимая для быстрого и существенного воздействия на переносимые по воздуху патогены, превышает безопасные уровни, рекомендованные Управлением по охране труда и окружающей среды США . Агентство охраны . Контроль влажности может значительно улучшить как убойную силу озона, так и скорость его распада обратно на кислород (большая влажность обеспечивает большую эффективность). Споры большинства патогенов очень устойчивы к атмосферному озону в концентрациях, при которых у пациентов с астмой начинаются проблемы.
В 1908 году для дезинфекции воздуха было введено искусственное озонирование центральной линии лондонского метрополитена . Этот процесс был признан целесообразным, но к 1956 году он был прекращен. Однако полезный эффект сохранялся за счет озона, случайно образующегося в результате электрических разрядов двигателей поездов (см. Выше: Побочное производство). [145]
Генераторы озона были предоставлены школам и университетам Уэльса на осенний семестр 2021 года для дезинфекции классов после вспышек COVID-19 . [146]
В промышленности озон используется для:
Озон является реагентом во многих органических реакциях в лаборатории и промышленности. Озонолиз – это расщепление алкена на карбонильные соединения .
Многие больницы по всему миру используют большие генераторы озона для дезинфекции операционных залов между операциями. Помещения убираются, затем герметично закрываются, а затем заполняются озоном, который эффективно убивает или нейтрализует все оставшиеся бактерии. [152]
Озон используется в качестве альтернативы хлору или диоксиду хлора при отбеливании древесной массы . [153] Его часто используют в сочетании с кислородом и перекисью водорода, чтобы исключить необходимость использования хлорсодержащих соединений при производстве высококачественной белой бумаги . [154]
Озон можно использовать для детоксикации цианидных отходов (например, от добычи золота и серебра ) путем окисления цианида до цианата и, в конечном итоге, до углекислого газа . [155]
С момента изобретения плазменных реакторов с диэлектрическим барьерным разрядом (DBD) их стали использовать для обработки воды озоном. [156] Однако при использовании более дешевых альтернативных дезинфицирующих средств, таких как хлор, такое применение обеззараживания воды озоном DBD было ограничено высоким энергопотреблением и громоздким оборудованием. [157] [158] Несмотря на это, поскольку исследования выявили негативное воздействие обычных дезинфицирующих средств, таких как хлор, на токсичные остатки и неэффективность уничтожения определенных микроорганизмов, [159] Обеззараживание озоном на основе плазмы DBD представляет интерес для существующих доступных технологий. . Хотя озонирование воды с высокой концентрацией бромида действительно приводит к образованию нежелательных бромированных побочных продуктов дезинфекции, если только питьевая вода не производится путем опреснения, озонирование обычно можно применять, не беспокоясь об этих побочных продуктах. [158] [160] [161] [162] Преимущества озона включают высокий термодинамический окислительный потенциал, меньшую чувствительность к органическим материалам и лучшую толерантность к изменениям pH, сохраняя при этом способность убивать бактерии, грибы, вирусы, а также споры и цисты. . [163] [164] [165] Несмотря на то, что озон широко распространен в Европе на протяжении десятилетий, в США он редко используется для обеззараживания из-за ограничений, связанных с высоким энергопотреблением, громоздкой установкой и стигмой, связанной с токсичностью озона. [157] [166] Учитывая это, недавние исследовательские усилия были направлены на изучение эффективных систем очистки воды озоном. [167] Исследователи изучили легкие и компактные поверхностные реакторы DBD малой мощности, [168] [169] энергоэффективные объемные реакторы DBD [170] и микромасштабные реакторы DBD малой мощности. [171] [172] Такие исследования могут помочь проложить путь к повторному признанию обеззараживания воды озоном на основе плазмы DBD, особенно в США.
Устройства, генерирующие высокие уровни озона, некоторые из которых используют ионизацию, используются для дезинфекции и дезодорации нежилых зданий, комнат, воздуховодов, дровяных сараев, лодок и других транспортных средств.
Озонированная вода используется для стирки одежды и дезинфекции продуктов питания, питьевой воды и поверхностей в доме. По данным Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA), оно «вносит поправки в правила о пищевых добавках , чтобы обеспечить безопасное использование озона в газообразной и водной фазах в качестве противомикробного агента в пищевых продуктах, включая мясо и птицу». Исследования, проведенные в Калифорнийском политехническом университете, показали, что содержание озона в концентрации 0,3 мкмоль/моль, растворенного в фильтрованной водопроводной воде, может привести к снижению более чем на 99,99% количества таких микроорганизмов пищевого происхождения, как сальмонелла, E. coli 0157:H7 и Campylobacter . Это количество в 20 000 раз превышает рекомендованные ВОЗ пределы, указанные выше. [148] [173] Озон можно использовать для удаления остатков пестицидов из фруктов и овощей . [174] [175]
Озон используется в домах и гидромассажных ваннах для уничтожения бактерий в воде и уменьшения количества необходимого хлора или брома путем их реактивации в свободное состояние. Поскольку озон не остается в воде достаточно долго, сам по себе озон неэффективен для предотвращения перекрестного загрязнения среди купающихся, и его следует использовать в сочетании с галогенами . В воду впрыскивается газообразный озон, создаваемый ультрафиолетовым излучением или коронным разрядом. [176]
Озон также широко используется при очистке воды в аквариумах и прудах. Его использование может свести к минимуму рост бактерий, контролировать паразитов, исключить передачу некоторых заболеваний, а также уменьшить или устранить «пожелтение» воды. Озон не должен попадать на жаберные структуры рыб. Природная соленая вода (с формами жизни) обеспечивает достаточную «мгновенную потребность», чтобы контролируемые количества озона активировали бромид-ионы до бромноватистой кислоты , и озон полностью распадается за время от нескольких секунд до минут. Если используется озон с кислородным питанием, в воде будет больше растворенного кислорода, а жаберные структуры рыб атрофируются, что делает их зависимыми от воды, обогащенной кислородом.
Озонирование – процесс насыщения воды озоном – может использоваться в аквакультуре для облегчения разложения органических веществ. Озон также добавляется в рециркуляционные системы для снижения уровня нитритов [177] за счет преобразования в нитраты . Если уровень нитритов в воде высок, нитриты также будут накапливаться в крови и тканях рыб, где они препятствуют транспорту кислорода (вызывают окисление гемогруппы гемоглобина из железосодержащих ( Fe2+
) → железо ( Fe3+
), что делает гемоглобин неспособным связывать O
2). [178] Несмотря на эти очевидные положительные эффекты, использование озона в системах рециркуляции связано со снижением уровня биодоступного йода в системах с соленой водой, что приводит к таким симптомам дефицита йода, как зоб и замедление роста личинок сенегальской камбалы ( Solea senegalensis ). [179]
Озонированную морскую воду применяют для поверхностной дезинфекции икры пикши и палтуса от нодавируса. Нодавирус – это смертельный вирус, передающийся вертикально, вызывающий серьезную смертность рыб. Яйца пикши не следует обрабатывать повышенным содержанием озона, поскольку обработанные таким образом яйца не вылупляются и погибают через 3–4 дня. [180]
Применение озона на свежесрезанных ананасе и бананах показывает увеличение содержания флавоноидов и общего фенола при воздействии до 20 минут. Наблюдается снижение содержания аскорбиновой кислоты (одной из форм витамина С ), но положительное влияние на общее содержание фенолов и флавоноидов может преодолеть отрицательный эффект. [181] Помидоры при обработке озоном демонстрируют увеличение содержания β-каротина, лютеина и ликопина. [182] Однако обработка клубники озоном в предуборочный период показывает снижение содержания аскорбиновой кислоты. [183]
Озон облегчает извлечение некоторых тяжелых металлов из почвы с помощью ЭДТА . ЭДТА образует прочные водорастворимые координационные соединения с некоторыми тяжелыми металлами ( Pb , Zn ), что позволяет растворять их из загрязненной почвы. Если загрязненную почву предварительно обработать озоном, эффективность экстракции Pb , Am и Pu увеличивается на 11,0–28,9%, [184], 43,5% [185] и 50,7% [185] соответственно.
Опыление сельскохозяйственных культур является важной частью экосистемы. Озон может оказывать пагубное воздействие на взаимодействие растений и опылителей. [186] Опылители переносят пыльцу с одного растения на другое. Это важный цикл внутри экосистемы. Вызов изменений определенных атмосферных условий вокруг мест опыления или с помощью ксенобиотиков может вызвать неизвестные изменения в естественных циклах опылителей и цветковых растений. Согласно исследованию, проведенному в Северо-Западной Европе, опылители сельскохозяйственных культур подвергались большему негативному воздействию, когда уровень озона был выше. [187]
Использование озона для лечения заболеваний не подтверждается доказательствами высокого качества и обычно считается альтернативной медициной . [188]
Сноски
Цитаты
{{cite web}}: CS1 maint: unfit URL (link)