
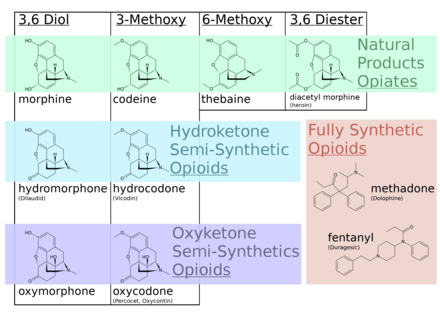
Опиат — это алкалоидное вещество , полученное из опиума (или маковой соломы ). [1] Он отличается от похожего термина опиоид тем, что последний используется для обозначения всех веществ, как природных, так и синтетических, которые связываются с опиоидными рецепторами в мозге (включая антагонисты). [2] Опиаты — это алкалоидные соединения, естественным образом встречающиеся в растении опийного мака Papaver somniferum . [3] Психоактивные соединения, обнаруженные в растении опиума, включают морфин , кодеин и тебаин (рисунок ниже неверен, тебаин — это «3,6-диметокси-»). Опиаты уже давно используются при различных медицинских состояниях, при этом свидетельства торговли опиатами и их использования для снятия боли имеются еще в восьмом веке нашей эры. [4] Большинство опиатов считаются наркотиками с умеренным или высоким потенциалом злоупотребления и включены в различные «Списки контроля за веществами» в соответствии с Единым законом о контролируемых веществах Соединенных Штатов Америки.
В 2014 году от 13 до 20 миллионов человек употребляли опиоиды в рекреационных целях (от 0,3% до 0,4% населения мира в возрасте от 15 до 65 лет). [5] По данным CDC, в этой группе населения было зарегистрировано 47 000 смертей, а общее число смертей за период с 2000 по 2014 год составило 500 000. [6] В 2016 году Всемирная организация здравоохранения сообщила, что 27 миллионов человек страдают от расстройств, связанных с употреблением опиоидов . Они также сообщили, что в 2015 году 450 000 человек умерли в результате употребления наркотиков, причем от трети до половины этого числа были отнесены к опиоидам. [7]
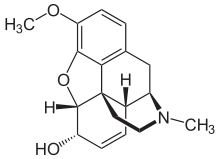
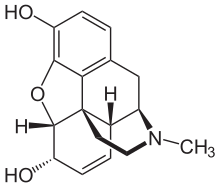
Опиаты относятся к большой биосинтетической группе бензилизохинолиновых алкалоидов и так названы, потому что они являются естественными алкалоидами, обнаруженными в опийном маке. Основными психоактивными опиатами являются морфин , кодеин и тебаин . Папаверин , носкапин и около 24 других алкалоидов также присутствуют в опиуме, но оказывают незначительное или совсем не оказывают влияние на центральную нервную систему человека . Алкалоиды, которые не оказывают влияния на центральную нервную систему, не всегда считались опиатами, но в настоящее время существует тенденция называть таковыми все алкалоиды, полученные из опиума или маковой соломы . Очень небольшие количества гидрокодона и гидроморфона обнаруживаются в пробах опиума в редких случаях; по-видимому, он вырабатывается растением при обстоятельствах и в результате процессов, которые в настоящее время не изучены. [ необходима цитата ] Дигидрокодеин , оксиморфол , оксикодон , оксиморфон , метопон Возможно, другие производные морфина и/или гидроморфона также обнаружены в следовых количествах в опиуме. [ необходима цитата ]
Несмотря на то, что морфин является наиболее значимым с медицинской точки зрения опиоидом, в медицинских целях потребляется больше кодеина, большая его часть синтезируется из морфина. Кодеин имеет большую и более предсказуемую пероральную биодоступность . Кодеин не метаболизируется в свою активную форму, морфин, с помощью CYP2D6 из-за значительного количества полиморфизма. У многих людей отсутствует какой-либо заметный метаболизм морфина, и они не испытывают никакого терапевтического эффекта (хотя у них все еще может быть тошнота/рвота или запор). Значительная часть населения является быстрыми или сверхбыстрыми метаболизаторами и может быстро развить смертельную токсичность даже от небольшого количества, присутствующего в грудном молоке, или от нескольких доз. Широко распространено мнение, что кодеин имеет меньший потенциал злоупотребления, чем морфин, несмотря на широкое злоупотребление. Его потенциал злоупотребления в значительной степени ограничен его профилем побочных эффектов. [8] Использование кодеина во многих странах снижается из-за широкого спектра метаболизма, частых побочных эффектов при терапевтических дозах (от 30 до 60 мг), а у большинства людей его анальгетическая эффективность сопоставима с терапевтической дозой ацетаминофена.

Эффекты синдрома отмены опиатов связаны с резким прекращением или сокращением длительного употребления опиатов.
Проявление зависимости от опиатов и злоупотребления ими зависит от множества факторов, включая фармакокинетические свойства опиатов и предрасположенность пользователя к зависимости. [9]
Хотя полный синтез опиоидов из нафтохинона (синтез Гейтса) или других простых органических исходных материалов возможен, это утомительные и неэкономичные процессы. Поэтому большинство анальгетиков опиатного типа , используемых сегодня, либо извлекаются из Papaver somniferum , либо синтезируются из этих опиатов, особенно тебаина . [10]
В 2015 году исследователи сообщили об успешном биосинтезе тебаина и гидрокодона с использованием генетически модифицированных дрожжей . После масштабирования для коммерческого использования процесс сократит время производства с года до нескольких дней и может снизить затраты на 90%. [ 11] [12]
Кодеин — это пролекарство , которое преобразуется в морфин и действует на μ -опиатные рецепторы. Он преобразуется в морфин путем метаболизма ферментов CYP2D6 . Лица с более низкой активностью CYP2D6 могут вообще не метаболизировать кодеин и не испытывать его анальгетического эффекта. И наоборот, лица с быстрой или сверхбыстрой активностью CYP2D6 могут слишком быстро метаболизировать препарат и испытывать побочные эффекты, связанные с дозировкой, такие как седация и фатальная дыхательная недостаточность. [13]
Фентанил — синтетический пиперидиновый опиоид, структурно схожий с арилпиперидинами. Это сильный агонист μ- рецепторов, который в 80–100 раз сильнее морфина, и имеет быстрое начало с более короткой продолжительностью действия, чем морфин, из-за перераспределения из ЦНС в жировую ткань. Когда он используется в качестве постоянного препарата (например, трансдермальные пластыри, более длительное использование внутривенного фентанила у пациентов отделения интенсивной терапии), его период полувыведения и продолжительность эффекта больше, чем у морфина. Он метаболизируется в печени ферментами CYP3A4 в соединение норфентанил. [14]
Героин, общее название диацетилморфина , является первым из нескольких полусинтетических опиоидов, полученных из морфина, компонента натурального опиума. [16] Он образуется путем ацетилирования морфина с целью повышения растворимости в липидах. [17] Героин (диацетилморфин) является пролекарством морфина ; он метаболизируется печенью в морфин после приема. Один из основных метаболитов героина, 6-моноацетилморфин (6-МАМ), также является пролекарством морфина.
Гидроморфон получают из морфина и могут использовать в качестве альтернативы ему. Он имеет высокий метаболизм первого прохода при приеме внутрь и в первую очередь глюкуронируется в печени до гидроморфон-3-глюкуронида (H3G). 75% гидроморфона выводится почками, а 7% выводится в виде исходного опиата. [14]
Меперидин — синтетический опиат, часть класса арилпиперидинов. Это сильный агонист μ- рецепторов с одной десятой силы морфина. Исторически он использовался для лечения озноба и имеет период полувыведения от трех до четырех часов. Он метаболизируется в печени до активных метаболитов нормеперидина, нормепиридиновой кислоты и медперидиновой кислоты. Нормеперидин может накапливаться до токсических уровней у пациентов с почечной недостаточностью при повторных дозах и может вызывать возбуждение ЦНС и судороги. [14]
Метадон имеет более высокую биодоступность и период полувыведения по сравнению с морфином. [18] Он метаболизируется до неактивного продукта путем N-деметилирования ферментами CYP3A4 в печени. Он имеет высокую индивидуальную вариабельность из-за различных уровней CYP3A4 у людей. [19] Он одобрен для лечения умеренной и сильной боли, а также опиоидной зависимости. [20] Из-за высокого риска взаимодействия с лекарственными средствами, токсичности для печени и вариабельности пациентов пациенты должны тщательно контролироваться в метадоновых клиниках . [21] Кроме того, существует повышенный риск смертности у пациентов, которые лечатся метадоном по сравнению с другими опиоидами, что, как полагают, связано с удлинением интервала QTc и сердечными аритмиями.
Никоморфин (вилан, морфин диникотинат), диаморфин (героин, морфин диацетат), дипропаноилморфин (морфин дипропионат), дезоморфин (пермонид, дигидродезоксиморфин), метилдезорфин , ацетилпропионилморфин , дибензоилморфин , диацетилдигидроморфин и некоторые другие также являются производными морфина. [22]
Морфин метаболизируется в печени до морфин-3-глюкуронида (M3G) и морфин-6-глюкуронида (M6G), которые выводятся почками. Он также способен проникать через гематоэнцефалический барьер в спинномозговую жидкость. M6G обладает мощной анальгетической активностью, связывается с опиоидными рецепторами и является основным фактором, способствующим терапевтическому эффекту морфина. [23] M3G не действует как анальгетик, имеет низкое сродство к опиоидным рецепторам и, возможно, может противодействовать терапевтическим эффектам морфина и M6G. Более того, высокие дозы морфина, и, следовательно, M3G, связаны с нейротоксическими побочными эффектами, такими как гипералгезия , аллодиния и миоклонус . [24]
Оксиморфон — это конгенер морфина. Он метаболизируется в 6-гидрокси-оксиморфон и оксиморфон-3-глюкуронид, и 40% выводится в виде метаболитов. 6-гидрокси-оксиморфин активен и существует в соотношении 1:1 с исходным препаратом. Активность оксиморфон-3-глюкуронида неизвестна. [14]
Опиаты с опиоидной активностью в основном используются для лечения боли с предположением, что польза как для боли, так и для функции перевесит риски для пациента. [25] Другим показанием является симптоматическое облегчение нехватки дыхания , как в острых случаях (например, отек легких ), так и у неизлечимо больных пациентов. [26] [27]
Несмотря на скудные, часто противоречивые доказательства, а иногда и исследования, не показывающие никакой пользы, опиоиды, такие как кодеин, гидрокодон и гидроморфон, традиционно использовались для лечения острого вирусного кашля (также известного как «острый бронхит»), кашля из-за обострения ХОБЛ, хронического поствирусного кашля, хронического идиопатического кашля и кашля по другим причинам. Учитывая потенциал злоупотребления, частые побочные эффекты со стороны ЖКТ и несколько исследований, не показывающих заметной пользы, рекомендации против использования опиоидов при кашле у детей. Несмотря на широкое использование, наука, поддерживающая использование опиоидов при кашле у взрослых, наиболее примечательна небольшим размером выборки, плохим дизайном исследования и неубедительными результатами, которые предполагают, что может быть небольшое уменьшение интенсивности кашля при его точном измерении. Фактические доказательства результатов, ориентированных на пациента (например, чувствуют ли пациенты себя лучше, чем при приеме плацебо), неуловимы, а использование кодеина в качестве «золотого стандарта», с которым можно сравнивать другие препараты, было поставлено под сомнение (как доказательство того, что препарат так же хорош, или, по крайней мере, не хуже, чем препарат, не приносящий никакой пользы, а имеющий только вредные побочные эффекты и потенциальную возможность злоупотребления, оставляет желать лучшего). [ необходима цитата ]
Конвертация дозы опиоидов может быть необходима при переключении лекарств, учитывая различную фармакодинамику между опиоидами. Обычно парентеральный (внутривенный или внутримышечный) морфин используется в качестве стандарта для конвертации между опиатами для достижения эквивалентных анальгетических эффектов. Эти различия в эквивалентах морфина могут различаться между формулами одного и того же лекарства и, безусловно, между пероральным и инъекционным. [28] Расчет общей суточной дозы с использованием эквивалентов морфина в миллиграммах используется для выявления пациентов с риском передозировки. [29]
Распространенные побочные эффекты, связанные с использованием опиоидов, включают: седацию , тошноту , головокружение, рвоту, запор , физическую зависимость, толерантность и потенциально фатальную дыхательную недостаточность . Из них наиболее распространенными являются запор и тошнота. Толерантность к запору не развивается. [30] Вот почему размягчители стула или слабительные (полиэтиленгликоль, докузат и сенна) часто назначают вместе с опиоидами. [31]
При передозировке, будь то преднамеренная, случайная или вызванная быстрым 2D6-превращением кодеина (или трамадола, неопиоидного опиоида, который, как и кодеин, оказывает незначительное внутреннее воздействие на μ-рецепторы, а действует скорее как пролекарство с активным метаболитом, который является μ- агонистом) .
Менее распространенные побочные эффекты включают: задержку опорожнения желудка, гипералгезию , иммунологическую и гормональную дисфункцию (гипогонадизм часто наблюдается у мужчин, принимающих хронические опиоиды, но не всегда клинически проявляется), мышечную ригидность и миоклонию . [32]
Использование опиатов для снятия боли широко распространено в системе здравоохранения. Однако долгосрочное лечение хронической боли является спорным, поскольку существует высокий риск возникновения зависимости, связанной с его использованием, что приводит к злоупотреблению и передаче другим людям даже при правильном приеме. [33] Те, кто зависим от опиатов, будут отдавать приоритет приобретению этих препаратов по сравнению с другими видами деятельности в своей жизни, что отрицательно сказывается на их профессиональных и личных отношениях. Более того, существует не так много хорошо спланированных исследований, оценивающих общую безопасность и эффективность. Многие небольшие исследования с использованием малых доз (часто половины рекомендуемой дозы) не показали большого эффекта, но на них нельзя полагаться, чтобы получить много информации о более распространенной практике пошаговой терапии и медленного повышения дозы.
Хроническое употребление опиоидов предсказуемо приводит к толерантности , и может произойти это довольно быстро (в течение нескольких дней или недель). Это происходит даже при дозах, которые считаются умеренными (например, ≥25 мг оксикодона в день). Это может привести к тому, что пациенту потребуются более высокие и/или более частые дозы препарата для получения эйфорического эффекта, хотя это может не быть фактором анальгетического эффекта, поскольку толерантность к дозе опиоида, по-видимому, не связана с потерей эффективности. [34] Толерантность связана с повышением регуляции μ-рецепторов (и, возможно, других).
Концентрационно-зависимые побочные эффекты могут варьироваться в зависимости от генетических полиморфизмов пользователя, которые могут изменять метаболизм наркотиков. Цитохром P450 (особенно CYP2D6 , но также CYP3A4 ) отвечает за метаболизм различных опиатов в активные метаболиты, а вариации активности CYP450 приводят к различным уровням наркотиков в сыворотке. [35]
Боль — это неприятное сенсорное и эмоциональное переживание, связанное с реальным или потенциальным повреждением тканей. Это важная защитная функция, при которой боль действует как сигнал тревоги, чтобы избежать или ограничить повреждение тканей. Ее нейробиология сложна и включает стимуляцию нескольких различных типов нервов. Опиоиды действуют на опиоидные рецепторы, которые связаны с ингибиторными рецепторами, связанными с G-белком (GPCR). Эти рецепторы делятся на 3 класса: μ (мю) , δ (дельта) и κ (каппа) рецепторы. [36]
Более 70% опиоидных рецепторов являются μ-рецепторами, преимущественно расположенными на центральных окончаниях ноцицепторов в заднем роге спинного мозга. Остальные 30% опиоидных рецепторов расположены постсинаптически на дендритах спиноталамических нейронов второго порядка и интернейронов. [36]
Когда опиат связывается как агонист с GPCR, будет каскад сигналов, приводящий к ингибированию аденилатциклазы и каналов ионов кальция со стимуляцией каналов ионов калия. Конечным эффектом этих изменений является снижение внутриклеточного цАМФ и гиперполяризация нейронной клетки, что снижает высвобождение нейротрансмиттера. [37] Через этот путь, когда опиаты связываются с мю-рецептором и активируют его, происходит снижение передачи болевых сигналов. Этот путь нацелен на анальгетические свойства, которые известны и используются опиатами. Другие клинически важные роли мю - это его участие в дыхательных и сердечно-сосудистых функциях, перистальтике желудочно-кишечного тракта , питании и настроении. [38] Эти другие пути важны, поскольку они объясняют побочные эффекты употребления опиатов, такие как угнетение дыхания при высоких дозах, запор при хроническом употреблении и свойства привыкания. [32]
Людям со следующими заболеваниями не следует употреблять опиоиды: [39]
Ниже приведены факторы риска злоупотребления рецептурными опиатами: [40]
По статистике, у пациентов среднего возраста с анамнезом употребления психоактивных веществ и сопутствующими психиатрическими заболеваниями наблюдается более высокий риск смертности, например, самоубийства.
Ятрогенная физиологическая и психологическая зависимость от наркотиков может возникнуть у человека с любым происхождением. Некоторые врачи более либеральны в назначении опиатов, и их пациенты становятся зависимыми от опиатов, просто следуя предписаниям своего врача. [41]
Опиат — это старый термин, который классически используется в фармакологии для обозначения препарата, полученного из опиума. В прошлом он использовался для обозначения препаратов с опиумподобным действием, но это использование устарело. Опиоид, более современный термин, используется для обозначения всех веществ, как природных, так и синтетических, которые связываются с опиоидными рецепторами (включая антагонисты).
{{cite journal}}: CS1 maint: multiple names: authors list (link)