Острый панкреатит (ОП) — это внезапное воспаление поджелудочной железы . Причины включают желчный камень, застрявший в общем желчном протоке или протоке поджелудочной железы , злоупотребление алкоголем , системное заболевание , травму , повышенный уровень кальция , гипертриглицеридемию (при этом уровень триглицеридов обычно очень высок, более 1000 мг/дл), некоторые лекарства, наследственные причины и, у детей, свинку . Острый панкреатит может быть единичным событием, он может быть рецидивирующим или может прогрессировать до хронического панкреатита и/или недостаточности поджелудочной железы (термин «дисфункция поджелудочной железы» включает случаи острого или хронического панкреатита, при которых поджелудочная железа измеримо повреждена, даже если она не отказала).
Во всех случаях острого панкреатита ранняя внутривенная гидратация жидкости и раннее энтеральное (питание, доставляемое в кишечник, либо через рот, либо через зонд ) питание связаны с более низкой смертностью и осложнениями. [2] Легкие случаи обычно успешно лечатся консервативными мерами, такими как госпитализация с внутривенным вливанием жидкости, купированием боли и ранним энтеральным питанием. Если человек не может переносить питание через рот, часто используется питание через назогастральный или назоеюнальный зонд, которые обеспечивают питание непосредственно в желудок или кишечник соответственно. [2] Тяжелые случаи часто требуют госпитализации в отделение интенсивной терапии . Тяжелый панкреатит, который по определению включает поражение органов, отличных от поджелудочной железы, связан с уровнем смертности 20%. [2] Это состояние характеризуется тем, что поджелудочная железа секретирует активные ферменты, такие как трипсин , химотрипсин и карбоксипептидаза , вместо их неактивных форм, что приводит к самоперевариванию поджелудочной железы. Кальций помогает преобразовывать трипсиноген в активный трипсин, поэтому повышенный уровень кальция (любой причины) является потенциальной причиной панкреатита. [2] В результате этого может возникнуть повреждение протоков поджелудочной железы. Долгосрочные осложнения включают диабет типа 3c (панкреатогенный диабет), при котором поджелудочная железа не может секретировать достаточное количество инсулина из-за структурного повреждения. [2] У 35% развивается экзокринная недостаточность поджелудочной железы , при которой поджелудочная железа не может секретировать пищеварительные ферменты из-за структурного повреждения, что приводит к мальабсорбции. [2]
К распространенным симптомам острого панкреатита относятся боль в животе, тошнота, рвота и лихорадка от легкой до умеренной степени. [2] [3] Боль в животе является наиболее распространенным симптомом и обычно описывается как находящаяся в левом верхнем квадранте, эпигастральной области или вокруг пупка, с иррадиацией по всему животу или в грудь или спину. [4] Боль в животе изначально может усиливаться при приеме пищи или питье, но может стать постоянной по мере прогрессирования заболевания. [2] [4] Менее распространенные симптомы включают икоту , вздутие живота и расстройство желудка. [4] Хотя это распространенные симптомы, часто они не все присутствуют; и боль в эпигастрии может быть единственным симптомом. [5]
Следующие состояния связаны с тяжелым течением заболевания:
Местно-региональные осложнения включают псевдокисту поджелудочной железы (наиболее распространенную, возникающую в 25% всех случаев, как правило, через 4–6 недель) и образование флегмоны/абсцесса, псевдоаневризмы селезеночной артерии, кровотечение из эрозий в селезеночную артерию и вену, тромбоз селезеночной вены, верхней брыжеечной вены и воротной вены (в порядке убывания частоты), непроходимость двенадцатиперстной кишки, непроходимость общего желчного протока, прогрессирование хронического панкреатита, асцит поджелудочной железы, плевральный выпот, стерильный/инфицированный некроз поджелудочной железы. [7]
Системные осложнения включают острый респираторный дистресс-синдром (ОРДС), синдром полиорганной недостаточности , диссеминированное внутрисосудистое свертывание крови (ДВС-синдром), гипокальциемию (в результате омыления жиров), гипергликемию и инсулинозависимый сахарный диабет (в результате повреждения бета -клеток, продуцирующих инсулин поджелудочной железы ), а также мальабсорбцию из-за экзокринной недостаточности.
Употребление табака, рецидивирующие эпизоды острого панкреатита, отмирание ткани поджелудочной железы, алкогольный панкреатит — все это факторы риска развития хронического панкреатита. [2]
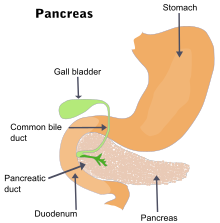
Острый панкреатит возникает при аномальной активации пищеварительных ферментов в поджелудочной железе. Это происходит из-за ненадлежащей активации неактивных предшественников ферментов, называемых зимогенами (или проферментами) внутри поджелудочной железы, в первую очередь трипсиногена . Обычно трипсиноген преобразуется в свою активную форму ( трипсин ) в первой части тонкого кишечника ( двенадцатиперстной кишке ), где фермент помогает в переваривании белков. Во время эпизода острого панкреатита трипсиноген вступает в контакт с лизосомальными ферментами (в частности, катепсином ), которые активируют трипсиноген в трипсин. Активная форма трипсина затем приводит к дальнейшей активации других молекул трипсиногена. Активация этих пищеварительных ферментов приводит к воспалению, отеку, повреждению сосудов и даже клеточной смерти. Смерть клеток поджелудочной железы происходит посредством двух основных механизмов: апоптоза , который контролируется физиологически, и некроза , который менее организован и более повреждающий. Баланс между этими двумя механизмами клеточной смерти опосредуется каспазами , которые регулируют апоптоз и выполняют важные антинекрозные функции во время панкреатита: предотвращают активацию трипсиногена, предотвращают истощение АТФ путем ингибирования полиАДФ-рибозополимеразы и ингибирования ингибиторов апоптоза (ИАП). Однако, если каспазы истощаются из-за хронического воздействия этанола или тяжелого инсульта, то некроз может преобладать.
Два типа острого панкреатита — легкий и тяжелый, которые определяются на основе того, является ли преобладающей реакцией на повреждение клеток воспаление (легкий) или некроз (тяжелый). При легком панкреатите наблюдается воспаление и отек поджелудочной железы. При тяжелом панкреатите наблюдается некроз поджелудочной железы, и могут быть повреждены близлежащие органы.
В рамках первичного повреждения наблюдается обширная воспалительная реакция, обусловленная синтезом и секрецией клетками поджелудочной железы воспалительных медиаторов: в первую очередь ФНО-альфа и ИЛ-1 . Отличительной чертой острого панкреатита является проявление воспалительной реакции, а именно привлечение нейтрофилов в поджелудочную железу. Воспалительная реакция приводит к вторичным проявлениям панкреатита: гиповолемии из-за проницаемости капилляров, острому респираторному дистресс-синдрому, диссеминированному внутрисосудистому свертыванию, почечной недостаточности, сердечно-сосудистой недостаточности и желудочно-кишечному кровотечению.
Острый панкреатит (острый геморрагический панкреонекроз) характеризуется острым воспалением и некрозом паренхимы поджелудочной железы , очаговым ферментативным некрозом жира поджелудочной железы и некрозом сосудов ( кровоизлиянием ). Они вызываются интрапанкреатической активацией ферментов поджелудочной железы. Активация липазы вызывает некроз жировой ткани в интерстиции поджелудочной железы и перипанкреатическом пространстве, а также повреждение сосудов. Некротические жировые клетки выглядят как тени, контуры клеток, лишенные ядра, розовая, мелкозернистая цитоплазма. Можно обнаружить преципитаты кальция (гематоксилинофильные). Переваривание стенок сосудов приводит к тромбозу и кровоизлиянию. Воспалительный инфильтрат богат нейтрофилами . Из-за отсутствия капсулы у поджелудочной железы воспаление и некроз могут распространяться на фасциальные слои в непосредственной близости от поджелудочной железы.
Острый панкреатит диагностируется с использованием клинической истории болезни и результатов физического обследования, подтверждающих диагноз с помощью визуализации и панкреатических ферментов (амилазы и липазы). Пересмотренная Атлантская классификация требует 2/3 из следующих результатов для постановки диагноза: боль в животе, соответствующая панкреатиту, повышенные уровни амилазы или липазы, превышающие верхнюю границу нормы более чем в 3 раза, и визуализация, соответствующая острому панкреатиту. [2] [11] Дополнительные лабораторные исследования могут использоваться для выявления недостаточности органов в прогностических целях или для определения скорости инфузионной терапии. [2] * Если уровень липазы примерно в 2,5–3 раза превышает уровень амилазы, это является признаком панкреатита, вызванного алкоголем. [12] Липаза сыворотки более чувствительна и специфична, чем амилаза сыворотки, при диагностике острого панкреатита и является предпочтительным тестом при диагностике. [13] [14]
Большинство, но не все отдельные исследования подтверждают превосходство липазы. [15] В одном крупном исследовании не было пациентов с панкреатитом, у которых была бы повышенная амилаза при нормальной липазе. [16] Другое исследование показало, что амилаза может добавить диагностическую ценность к липазе, но только если результаты двух тестов были объединены с уравнением дискриминантной функции. [17]
Было показано, что снижение клиренса липазы из-за заболеваний почек, желудочно-кишечного тракта или гепатобилиарного рака, гиперсекреции ферментов поджелудочной железы, критических заболеваний, в том числе нейрохирургического характера, приводит к повышению уровня липазы в сыворотке и может затруднить диагностику острого панкреатита. [18]
Дифференциальная диагностика включает: [19]

Что касается необходимости проведения компьютерной томографии , в практических рекомендациях указано:
КТ является важным общим инструментом первоначальной оценки острого панкреатита. Визуализация показана при первоначальном осмотре, если:
КТ рекомендуется как инструмент отсроченной оценки в следующих ситуациях:
КТ брюшной полости не следует проводить ранее, чем через 12 часов после появления симптомов, поскольку ранняя КТ (<12 часов) может привести к неоднозначным или нормальным результатам.
Результаты КТ можно классифицировать по следующим категориям для удобства запоминания:
Основная ценность КТ для лечащего врача заключается в возможности идентифицировать омертвевшие участки поджелудочной железы, которые стали некротическими из-за ишемии. Некроз поджелудочной железы можно надежно идентифицировать с помощью КТ с внутривенным контрастированием [20] , и он имеет значение, если происходит инфекция и показана хирургическая или чрескожная санация.
В то время как компьютерная томография считается золотым стандартом в диагностической визуализации острого панкреатита, [21] магнитно-резонансная томография (МРТ) становится все более ценным инструментом для визуализации поджелудочной железы, особенно скоплений панкреатической жидкости и некротизированных остатков. [22] Дополнительная полезность МРТ включает ее показание для визуализации пациентов с аллергией на контрастный материал КТ и общую большую чувствительность к кровотечению, сосудистым осложнениям, псевдоаневризмам и венозному тромбозу. [23]
Еще одним преимуществом МРТ является использование последовательностей магнитно-резонансной холангиопанкреатографии (МРХПГ). МРХПГ предоставляет полезную информацию относительно этиологии острого панкреатита, то есть наличия мелких желчных камней ( холедохолитиаз или желчнокаменная болезнь ) и аномалий протоков. [22] Клинические испытания показывают, что МРХПГ может быть таким же эффективным диагностическим инструментом для острого панкреатита с билиарной этиологией, как и эндоскопическая ретроградная холангиопанкреатография , но с преимуществами, заключающимися в меньшей инвазивности и меньшем количестве осложнений. [24] [25]

Ультразвуковое исследование менее предпочтительно в качестве диагностического теста на острый панкреатит, но его можно использовать в отдельных случаях. Абдоминальное УЗИ может быть получено, если есть опасения, что желчный камень блокирует панкреатический проток, что приводит к панкреатиту. [2]
Раннее энтеральное (питание, подаваемое непосредственно в кишечник, либо через рот, либо через зонд) питание и агрессивная внутривенная гидратация показаны при всех формах и степенях тяжести острого панкреатита и связаны с более низкой смертностью и осложнениями. [2]
Конкретная скорость внутривенного введения жидкости при остром панкреатите не установлена, но некоторые эксперты рекомендуют начальную скорость инфузии жидкости 5–10 мл внутривенных жидкостей на килограмм веса тела в час и корректировать скорость в соответствии с физиологическими параметрами, такими как частота сердечных сокращений, среднее артериальное давление , диурез и гематокрит . [2]
Изотонические кристаллоидные растворы (например, лактатный раствор Рингера ) предпочтительнее обычного физиологического раствора для инфузионной терапии и связаны с меньшим риском развития синдрома системной воспалительной реакции (ССВР). [2]
На начальных стадиях (в течение первых 12–24 часов) острого панкреатита замещение жидкости было связано со снижением заболеваемости и смертности. [26] [27] [28] [29]
Боль в животе часто является преобладающим симптомом у пациентов с острым панкреатитом и должна лечиться анальгетиками.
Опиоиды безопасны и эффективны для обеспечения контроля боли у пациентов с острым панкреатитом. [30] Адекватный контроль боли требует использования внутривенных опиатов, обычно в форме контролируемого пациентом анальгетического насоса. Гидроморфон или фентанил (внутривенно) могут использоваться для облегчения боли при остром панкреатите. Фентанил все чаще используется из-за его лучшего профиля безопасности, особенно при почечной недостаточности. Как и другие опиаты, фентанил может угнетать дыхательную функцию. Его можно вводить как в виде болюса, так и в виде постоянной инфузии. Меперидин исторически был предпочтительнее морфина из-за убеждения, что морфин вызывает увеличение давления сфинктера Одди . Однако ни одно клиническое исследование не предполагает, что морфин может усугубить или вызвать панкреатит или холецистит. [31] Кроме того, меперидин имеет короткий период полувыведения, и повторные дозы могут привести к накоплению метаболита нормеперидина, который вызывает нервно-мышечные побочные эффекты и, редко, судороги.
Острый панкреатит является катаболическим состоянием, и при гемодинамической нестабильности или сдвигах жидкости или отеках может быть снижена внутрисосудистая перфузия кишечника. Это снижение перфузии кишечника увеличивает риск некроза кишечника с бактериальной транслокацией с последующим риском сепсиса или вторичных инфекций. [2] Энтеральное питание обеспечивает необходимое потребление калорий, а также усиливает перистальтику кишечника и приток крови к кишечнику, снижая эти риски. [2] Энтеральное питание (по сравнению с парентеральным питанием , при котором питательные вещества вводятся посредством внутривенной инфузии) связано со снижением смертности, снижением риска полиорганной недостаточности и системной инфекции у пациентов с острым панкреатитом. [2] [32] У пациентов с острым панкреатитом Американская гастроэнтерологическая ассоциация (AGA) рекомендует раннее пероральное питание в течение 24 часов вместо того, чтобы держать пациента натощак (или ничего не принимать через рот). А тем, кто не может питаться перорально, AGA рекомендует энтеральное питание (через назогастральный или назоеюнальный зонд), а не парентеральное питание. [33]
У 20 процентов людей с острым панкреатитом развивается инфекция за пределами поджелудочной железы, такая как инфекции кровотока , пневмония или инфекции мочевыводящих путей . [34] Эти инфекции связаны с увеличением смертности. [35] Скопления жидкости вокруг поджелудочной железы или области внутри поджелудочной железы, в которых происходит отмирание тканей (некроз), также могут стать вторично инфицированными, что потребует применения антибиотиков. [2] При подозрении на инфекцию следует начать прием антибиотиков, пока определяется источник инфекции. Однако, если посевы отрицательные и источник инфекции не выявлен, прием антибиотиков следует прекратить.
Профилактическое применение антибиотиков не рекомендуется людям с острым панкреатитом, независимо от типа (интерстициальный или некротизирующий) или тяжести заболевания (легкая, средней тяжести или тяжелая) [11] [36]
У 30% пациентов с острым панкреатитом причина не выявлена. Эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ) с эмпирической билиарной сфинктеротомией имеет равные шансы вызвать осложнения и устранить основную причину, поэтому не рекомендуется для лечения острого панкреатита. [37] Если обнаружен желчный камень, ЭРХПГ, выполненная в течение 24–72 часов с момента обнаружения с успешным удалением камня, как известно, снижает заболеваемость и смертность. [38] Показания к ранней ЭРХПГ:
Риски ЭРХПГ заключаются в том, что она может усугубить панкреатит, привнести инфекцию в стерильный панкреатит и вызвать кровотечение.
У пациентов с легким острым панкреатитом из-за желчных камней холецистэктомия (удаление желчного пузыря) рекомендуется в больнице и связана со снижением риска рецидива панкреатита. [2] У пациентов с желчнокаменным панкреатитом, у которых наблюдается тяжелое заболевание, включая наличие скоплений перипанкреатической жидкости, холецистэктомию следует отложить, поскольку скопления жидкости вокруг поджелудочной железы делают операцию технически сложной. Перипанкреатическая жидкость также несет риск вторичного инфицирования во время операции. [2]
Хирургическое вмешательство показано при (i) инфицированном панкреонекрозе и (ii) диагностической неопределенности и (iii) осложнениях. [ необходима цитата ] Наиболее частой причиной смерти при остром панкреатите является вторичная инфекция. Инфекция диагностируется на основании 2 критериев [ необходима цитата ]
Хирургические варианты лечения инфицированного некроза включают: [ необходима цитата ]
Пациенты с острым панкреатитом выздоравливают в большинстве случаев. У некоторых может развиться абсцесс, псевдокиста или дуоденальная непроходимость. Около 20% случаев острого панкреатита являются тяжелыми, а смертность составляет около 20%. [2] Острый панкреатит можно далее разделить на легкий и тяжелый панкреатит. Было разработано несколько инструментов клинической оценки для определения прогностической информации, которые могут определять определенные области клинического ведения, такие как необходимость госпитализации в отделение интенсивной терапии. [2]
Две такие системы оценки — это критерии Рэнсона и индексы APACHE II (Оценка острого физиологии и хронического здоровья). Большинство [41] [42] , но не все [43] исследования сообщают, что оценка Apache может быть более точной. В отрицательном исследовании APACHE-II использовалась 24-часовая оценка APACHE-II, а не 48-часовая. [43] Некоторые эксперты рекомендуют использовать оценку APACHE II, а также уровень гематокрита сыворотки на ранних этапах госпитализации в качестве прогностических показателей. [13]
Шкала Рэнсона используется для прогнозирования тяжести острого панкреатита. Она была введена в 1974 году.
Критерием для назначения баллов является достижение определенной контрольной точки в любой момент в течение этого 48-часового периода, так что в некоторых ситуациях ее можно рассчитать вскоре после поступления. Это применимо как к желчнокаменной, так и к алкогольной панкреатите.
Альтернативно, панкреатит можно диагностировать при наличии любого из следующих признаков:[2]
Оценка по шкале Рэнсона ≥ 8. Органная недостаточность. Значительный некроз поджелудочной железы (не менее 30% некроза поджелудочной железы по данным КТ с контрастным усилением).
Интерпретация Если оценка ≥ 3, вероятен тяжелый панкреатит. Если оценка < 3, тяжелый панкреатит маловероятен Или
Оценка от 0 до 2: 2% смертности Оценка от 3 до 4: 15% смертности Оценка от 5 до 6: 40% смертности Оценка от 7 до 8: 100% смертности
Оценка по шкале «Острая физиология и хроническая оценка здоровья» ( APACHE II ) > 8 баллов прогнозирует смертность от 11% до 18% [13]
Разработанный в начале 1990-х годов Эмилем Дж. Бальтазаром и др. [ 44] индекс тяжести компьютерной томографии (CTSI) представляет собой систему градации, используемую для определения тяжести острого панкреатита. Числовой CTSI имеет максимум десять баллов и представляет собой сумму баллов градации Бальтазара и баллов градации панкреонекроза:
сорт Бальтазар
Оценка некроза
В ряде исследований было показано, что стадирование тяжести острого панкреатита по шкале CTSI обеспечивает более точную оценку, чем APACHE II, Ranson и уровень С-реактивного белка (СРБ). [45] [46] [47] Однако несколько исследований указывают на то, что CTSI не имеет значительной связи с прогнозом госпитализации пациентов с панкреонекрозом и не является точным предиктором тяжести ОП. [48] [49]
Шкала Глазго действительна как для панкреатита, вызванного желчными камнями, так и для панкреатита, вызванного алкоголем, тогда как шкала Рэнсона действительна только для панкреатита, вызванного алкоголем [ требуется ссылка ] . Если пациент набирает 3 или более баллов, это указывает на тяжелый панкреатит, и его следует перевести в отделение интенсивной терапии. Она оценивается с помощью мнемонического кода, PANCREAS:
Прогнозирует риск смертности при панкреатите с меньшим количеством переменных, чем критерии Рэнсона. Данные следует брать из первых 24 часов оценки состояния пациента.
Пациенты с нулевым баллом имели смертность менее одного процента, тогда как пациенты с баллом пять имели смертность 22 процента. В когорте валидации оценка BISAP имела схожие характеристики производительности теста для прогнозирования смертности с оценкой APACHE II. [50] Как и проблема многих других систем оценки, BISAP не была проверена для прогнозирования результатов, таких как продолжительность пребывания в больнице, необходимость ухода в отделении интенсивной терапии или необходимость вмешательства.
Заболеваемость острым панкреатитом во всем мире возросла с 1961 по 2016 год со средним годовым процентным приростом в 3%, рост заболеваемости наблюдался в Северной Америке и Европе. [51] Заболеваемость острым панкреатитом в Соединенных Штатах составляет 110-140 случаев на 100 000 человек. [2]
В Соединенных Штатах наиболее распространенными причинами являются камни в желчном пузыре, которые являются причиной 21–33% случаев, затем следует алкоголь (16–27%) и повышенный уровень триглицеридов (2–5%). [2]