Палладий — химический элемент ; он имеет символ Pd и атомный номер 46. Это редкий блестящий серебристо-белый металл, открытый в 1802 году английским химиком Уильямом Хайдом Волластоном . Он назвал его в честь астероида Паллада , который сам был назван в честь эпитета греческой богини Афины , полученного ею, когда она убила Палладу . Палладий, платина , родий , рутений , иридий и осмий образуют группу элементов, называемых металлами платиновой группы (МПГ). Они имеют схожие химические свойства, но палладий имеет самую низкую температуру плавления и наименее плотный из них.
Более половины запасов палладия и родственной ему платины используется в каталитических нейтрализаторах , которые преобразуют до 90% вредных газов автомобильного выхлопа ( углеводороды , окись углерода и диоксид азота ) в нетоксичные вещества ( азот , углекислый газ и диоксид азота ). водяной пар ). Палладий также используется в электронике, стоматологии , медицине , очистке водорода , химической промышленности, очистке подземных вод и ювелирных изделиях. Палладий является ключевым компонентом топливных элементов , в которых водород и кислород реагируют с образованием электричества, тепла и воды.
Рудные месторождения палладия и других МПГ встречаются редко. Наиболее обширные месторождения обнаружены в норитовом поясе Бушвельдского магматического комплекса , охватывающего бассейн Трансвааля в Южной Африке; Комплекс Стиллуотер в Монтане , США; бассейн Садбери и район Тандер-Бей в Онтарио , Канада; и Норильский комплекс в России. Переработка также является источником, в основном из списанных каталитических нейтрализаторов. Многочисленные области применения и ограниченные источники поставок приводят к значительному инвестиционному интересу.
Палладий принадлежит к 10-й группе периодической таблицы, но конфигурация крайних электронов соответствует правилу Хунда . Электроны, которые согласно правилу Маделунга должны были бы занимать 5 с , вместо этого заполняют 4 d -орбитали , поскольку энергетически более выгодно иметь полностью заполненную оболочку 4d 10 вместо конфигурации 5s 2 4d 8 . [ нужны разъяснения ]
Эта конфигурация 5s 0 , уникальная для периода 5 , делает палладий самым тяжелым элементом, имеющим только одну неполную электронную оболочку , а все оболочки над ней пусты.
Палладий имеет вид мягкого серебристо-белого металла, напоминающего платину. Он наименее плотный и имеет самую низкую температуру плавления среди металлов платиновой группы. Он мягкий и пластичный при отжиге , а при холодной обработке его прочность и твердость значительно увеличиваются. Палладий медленно растворяется в концентрированной азотной кислоте , в горячей концентрированной серной кислоте , а при тонком измельчении — в соляной кислоте . [7] Он легко растворяется при комнатной температуре в царской водке .
Палладий не вступает в реакцию с кислородом при стандартной температуре (и, следовательно, не тускнеет на воздухе ). Палладий, нагретый до 800 °C, образует слой оксида палладия (II) (PdO). Со временем он может постепенно приобретать легкую коричневатую окраску, вероятно, из-за образования поверхностного слоя его монооксида.
Пленки палладия с дефектами, полученными бомбардировкой альфа-частицами при низкой температуре, обладают сверхпроводимостью с Т с = 3,2 К [8].
Встречающийся в природе палладий состоит из семи изотопов , шесть из которых стабильны. Наиболее стабильными радиоизотопами являются 107 Pd с периодом полураспада 6,5 миллионов лет (обнаружен в природе), 103 Pd с периодом полураспада 17 дней и 100 Pd с 3,63 дня. Восемнадцать других радиоизотопов были охарактеризованы с атомным весом от 90,94948(64) u ( 91 Pd) до 122,93426 (64) u ( 123 Pd). [9] Период полураспада этих веществ составляет менее тридцати минут, за исключением 101 Pd (период полураспада: 8,47 часа), 109 Pd (период полураспада: 13,7 часа) и 112 Pd (период полураспада: 21 час). [10]
Для изотопов с единицей атомной массы меньше, чем у наиболее распространенного стабильного изотопа 106 Pd, основным способом распада является захват электрона , причем первичным продуктом распада является родий. Основным способом распада изотопов Pd с атомной массой более 106 является бета-распад , основным продуктом которого является серебро . [10]
Радиогенный 107 Ag является продуктом распада 107 Pd и был впервые обнаружен в 1978 году [11] в метеорите Санта-Клара [12] 1976 года. Первооткрыватели предполагают, что слияние и дифференциация малых планет с железным ядром могло произойти 10 миллионов лет назад. после нуклеосинтетического события. 107 Корреляции Pd и Ag, наблюдаемые в телах, расплавившихся после аккреции Солнечной системы , должны отражать присутствие короткоживущих нуклидов в ранней Солнечной системе. [13] 107
Pd также образуется в виде продукта деления при спонтанном или индуцированном делении235
У. _ Поскольку он малоподвижен в окружающей среде и имеет сравнительно низкую энергию распада ,107
Палладий обычно считается одним из наименее опасных долгоживущих продуктов деления .
Соединения палладия существуют преимущественно в степени окисления 0 и +2. Признаются и другие менее распространенные состояния. Обычно соединения палладия больше похожи на соединения платины, чем на соединения любого другого элемента.
Хлорид палладия(II) является основным исходным материалом для других соединений палладия. Он возникает при реакции палладия с хлором. Его используют для приготовления гетерогенных палладиевых катализаторов, таких как палладий на сульфате бария, палладий на угле и хлорид палладия на угле. [14] Растворы PdCl 2 в азотной кислоте реагируют с уксусной кислотой с образованием ацетата палладия(II) , также универсального реагента. PdCl 2 реагирует с лигандами (L) с образованием плоских квадратных комплексов типа PdCl 2 L 2 . Одним из примеров таких комплексов является производное бензонитрила PdCl 2 (PhCN) 2 . [15] [16]
Комплексный дихлорид бис(трифенилфосфин)палладия(II) является полезным катализатором. [17]
2.jpg/440px-Pd(OAc)2.jpg)

_Johns-Manville_Reef,_Stillwater_Complex.jpg/440px-Sulfidic_serpentintite_(platinum-palladium_ore)_Johns-Manville_Reef,_Stillwater_Complex.jpg)
Палладий образует ряд нульвалентных комплексов с формулой PdL 4 , PdL 3 и PdL 2 . Например, восстановление смеси PdCl 2 (PPh 3 ) 2 и PPh 3 дает тетракис(трифенилфосфин)палладий(0) : [18]
Другой основной комплекс палладия(0), трис(дибензилиденацетон)дипалладий(0) (Pd 2 (dba) 3 ), получают восстановлением тетрахлорпалладата натрия в присутствии дибензилиденацетона . [19]
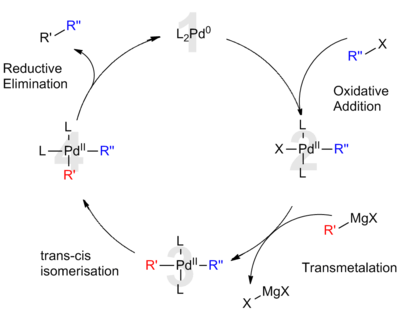
Палладий(0), а также палладий(II) являются катализаторами реакций сочетания , что было признано лауреатами Нобелевской премии по химии 2010 года Ричарду Ф. Хеку , Эйичи Негиши и Акире Судзуки . Такие реакции широко практикуются для синтеза тонких химических веществ. Выдающиеся реакции сочетания включают реакции Хека , Сузуки , сочетания Соногаширы , реакции Стилле и сочетания Кумады . Катализаторами или предкатализаторами служат ацетат палладия(II) , тетракис(трифенилфосфин)палладий(0) (Pd(PPh 3 ) 4 ) и трис(дибензилиденацетон)дипалладий(0) (Pd 2 (dba) 3 ). [20]
Хотя соединения Pd(IV) сравнительно редки, одним из примеров является гексахлорпалладат(IV) натрия Na 2 [PdCl 6 ]. Известно также несколько соединений палладия(III) . [21] Палладий(VI) был заявлен в 2002 году, [22] [23] , но впоследствии опровергнут. [24] [25]
Существуют комплексы палладия со смешанной валентностью, например, Pd 4 (CO) 4 (OAc) 4 Pd(acac) 2 образует бесконечную цепную структуру Pd с альтернативно соединенными между собой звеньями Pd 4 (CO) 4 (OAc) 4 и Pd(acac) 2 . [26]
При легировании более электроположительным элементом палладий может приобретать отрицательный заряд. Такие соединения известны как палладиды, например палладид галлия . [27] Палладиды со стехиометрией RPd 3 существуют, где R представляет собой скандий , иттрий или любой из лантаноидов . [28]
Поскольку общий объем добычи палладия в 2022 году достиг 210 000 килограммов, Россия была крупнейшим производителем с 88 000 килограммов, за ней следовали Южная Африка, Канада, США и Зимбабве. [29] Российская компания «Норильский никель» занимает первое место среди крупнейших производителей палладия в мире, на ее долю приходится 39% мирового производства. [30]
Палладий встречается в виде свободного металла в сплаве с золотом и другими металлами платиновой группы в россыпных месторождениях Урала , Австралии , Эфиопии , Северной и Южной Америки . Для производства палладия эти месторождения играют лишь незначительную роль. Важнейшими промышленными источниками являются никель - медные месторождения, обнаруженные в бассейне Садбери , Онтарио , и Норильско-Талнахские месторождения в Сибири . Другое крупное месторождение — месторождение металлов платиновой группы Риф Меренский в пределах Бушвелдского магматического комплекса Южной Африки . Магматический комплекс Стиллуотер в Монтане и рудное тело зоны Роби магматического комплекса Лак-де-Иль в Онтарио являются двумя другими источниками палладия в Канаде и США. [31] [32] Палладий содержится в редких минералах куперите [33] и полярите . [34] Известно еще много минералов Pd, но все они очень редки. [35]
Палладий также производится в ядерных реакторах деления и может быть извлечен из отработанного ядерного топлива (см. Синтез драгоценных металлов ), хотя этот источник палладия не используется. Ни одно из существующих предприятий по переработке ядерных материалов не оборудовано для извлечения палладия из высокоактивных отходов . [36] Осложнением восстановления палладия в отработавшем топливе является наличие107
Pd — слаборадиоактивный долгоживущий продукт деления . В зависимости от конечного использования радиоактивность, вносимая107
Pd может сделать восстановленный палладий непригодным для использования без дорогостоящего этапа разделения изотопов .


Сегодня наибольшее применение палладия приходится на каталитические нейтрализаторы. [37] Палладий также используется в ювелирных изделиях, стоматологии , [37] [38] производстве часов , тест-полосках для определения уровня сахара в крови, свечах зажигания самолетов , хирургических инструментах и электрических контактах . [39] Палладий также используется для изготовления некоторых профессиональных поперечных (концертных или классических) флейт . [40] Как товар, палладий в слитках имеет коды валют ISO XPD и 964. Палладий — один из четырех металлов, имеющих такие коды, остальные — золото , серебро и платина. [41] Поскольку палладий адсорбирует водород, он был ключевым компонентом в спорных экспериментах по холодному синтезу в конце 1980-х годов. [42]
Когда он тонко измельчен, как палладий на угле , палладий образует универсальный катализатор ; он ускоряет гетерогенные каталитические процессы, такие как гидрирование , дегидрирование и крекинг нефти . Палладий также необходим для катализатора Линдлара , также называемого палладием Линдлара. [43] Большое количество реакций углерод-углеродной связи в органической химии облегчаются катализаторами на основе палладия. Например:
При диспергировании на проводящих материалах палладий является отличным электрокатализатором окисления первичных спиртов в щелочных средах. [44] Палладий также является универсальным металлом для гомогенного катализа , используемым в сочетании с широким спектром лигандов для высокоселективных химических превращений.
В 2010 году Нобелевская премия по химии была присуждена «за перекрестные реакции, катализируемые палладием в органическом синтезе» Ричарду Ф. Хеку , Эйичи Негиши и Акире Судзуки . Исследование 2008 года показало, что палладий является эффективным катализатором связей углерод-фтор . [45]
Палладиевый катализ в основном используется в органической химии и промышленности, хотя его использование растет как инструмент синтетической биологии ; в 2017 году на млекопитающих была продемонстрирована эффективная каталитическая активность наночастиц палладия in vivo при лечении заболеваний. [46]
Основное применение палладия в электронике - это многослойные керамические конденсаторы [47] , в которых палладий (и сплав палладий-серебро) используется в качестве электродов. [37] Палладий (иногда в сплаве с никелем) используется или может использоваться для покрытия компонентов и разъемов бытовой электроники [48] [49] и в материалах для пайки. Согласно отчету Johnson Matthey , в 2006 году электронный сектор потреблял 1,07 миллиона тройских унций (33 тонны) палладия . [50]
Водород легко диффундирует через нагретый палладий [7] , а мембранные реакторы с Pd-мембранами используются для производства водорода высокой чистоты. [51] Палладий используется в палладий-водородных электродах в электрохимических исследованиях. Хлорид палладия (II) легко катализирует газообразный угарный газ до диоксида углерода и полезен в детекторах угарного газа . [52]
Палладий легко адсорбирует водород при комнатной температуре, образуя гидрид палладия PdH x с x меньше 1. [53] Хотя это свойство является общим для многих переходных металлов, палладий обладает уникально высокой поглощающей способностью и не теряет своей пластичности до тех пор, пока x не приблизится к 1. [54] Это свойство было исследовано при разработке эффективного и безопасного носителя для хранения водородного топлива, хотя сам палладий в настоящее время для этой цели непомерно дорог. [55] Содержание водорода в палладии можно связать с магнитной восприимчивостью , которая уменьшается с увеличением содержания водорода и становится нулевой для PdH 0,62 . При любом более высоком отношении твердый раствор становится диамагнитным . [56]
Палладий также используется для очистки водорода с помощью мембран для очистки водорода. [57] : 183–217 [58]
Палладий используется в небольших количествах (около 0,5%) в некоторых сплавах зубной амальгамы для уменьшения коррозии и увеличения металлического блеска окончательной реставрации. [59] [60]
Палладий используется в качестве драгоценного металла в ювелирных изделиях с 1939 года в качестве альтернативы платине в сплавах, называемых « белым золотом », где естественный белый цвет палладия не требует покрытия родием . Палладий, будучи гораздо менее плотным, чем платина, похож на золото в том смысле, что его можно измельчить в лист толщиной до 100 нм ( 1 ⁄ 250 000 дюйма). [7] В отличие от платины, палладий может обесцвечиваться при температуре выше 400 °C (752 °F) [61] из-за окисления, что делает его более хрупким и, следовательно, менее подходящим для использования в ювелирных изделиях; Чтобы этого не произошло, палладий, предназначенный для ювелирных изделий, нагревают в контролируемых условиях. [ нужна цитата ]
До 2004 года палладий в ювелирных изделиях использовался главным образом в производстве белого золота. Палладий — один из трех самых популярных металлов, легирующих белое золото ( также можно использовать никель и серебро). [37] Палладий-золото дороже, чем никель-золото, но редко вызывает аллергические реакции (хотя могут возникнуть определенные перекрестные аллергии с никелем). [62]
Когда во время Второй мировой войны платина стала стратегическим ресурсом, многие ювелирные браслеты изготавливались из палладия. Палладий мало использовался в ювелирном деле из-за технической сложности литья . После решения проблемы литья [63] использование палладия в ювелирных изделиях увеличилось, первоначально потому, что цена на платину выросла, а цена на палладий снизилась. [64] В начале 2004 года, когда цены на золото и платину резко выросли, Китай начал массовое производство ювелирных изделий из палладия, потребив 37 тонн в 2005 году. Последующие изменения в относительной цене платины снизили спрос на палладий до 17,4 тонны в 2009 году. [65] [66] Спрос на палладий в качестве катализатора привел к увеличению цены на палладий примерно на 50% по сравнению с ценой на платину в январе 2019 года. [67]
В январе 2010 года пробирные палаты Соединенного Королевства ввели клеймо палладия, и клеймение стало обязательным для всех ювелирных изделий, рекламирующих чистый или легированный палладий. На изделиях может быть маркировка 500, 950 или 999 частей палладия на тысячу сплава.
Перья перьевых ручек , изготовленные из золота , иногда покрываются палладием, когда требуется внешний вид серебра (а не золота). Шеффер использовал палладиевое покрытие на протяжении десятилетий либо в качестве акцента на золотых перьях, либо в качестве полного покрытия золота.
Палладий также используется люксовым брендом Hermès в качестве одного из металлов для покрытия фурнитуры своих сумок, самой известной из которых является Birkin.
В процессе платинотипной печати фотографы создают изящные черно-белые отпечатки с использованием солей платины или палладия. Палладий, часто используемый с платиной, является альтернативой серебру. [68]
Палладий представляет собой металл с низкой токсичностью по традиционным измерениям (например, LD 50 ). Недавние исследования механизма токсичности палладия предполагают высокую токсичность при измерении в течение длительного периода времени и на клеточном уровне в печени и почках. [70] Митохондрии, по-видимому, играют ключевую роль в токсичности палладия за счет коллапса потенциала митохондриальной мембраны и истощения уровня клеточного глутатиона (GSH). До этой недавней работы считалось, что палладий плохо усваивается организмом человека при попадании в организм . Такие растения, как водный гиацинт, погибают от низкого уровня солей палладия, но большинство других растений переносят это, хотя тесты показывают, что при уровнях выше 0,0003% это влияет на рост. Высокие дозы палладия могут быть ядовитыми; испытания на грызунах позволяют предположить, что он может быть канцерогенным , хотя до недавнего исследования, упомянутого выше, не было четких доказательств того, что этот элемент вредит человеку. [71]
Как и другие металлы платиновой группы , объемный Pd довольно инертен. Хотя сообщалось о контактном дерматите , данные о влиянии ограничены. Было показано, что люди с аллергической реакцией на палладий также реагируют на никель, поэтому рекомендуется избегать использования стоматологических сплавов, содержащих палладий, людям с такой аллергией. [72] [73] [74] [75] [76]
Некоторое количество палладия выбрасывается с выхлопными газами автомобилей с каталитическими нейтрализаторами . Такие автомобили выделяют от 4 до 108 нг/км частиц палладия, в то время как общее потребление с пищей оценивается менее 2 мкг на человека в день. Вторым возможным источником палладия является реставрация зубов, из которой, по оценкам, поглощение палладия составляет менее 15 мкг на человека в день. Люди, работающие с палладием или его соединениями, могут получить гораздо большее понимание. 99% растворимых соединений, таких как хлорид палладия , выводится из организма в течение трех дней. [72]
Средняя летальная доза (LD 50 ) растворимых соединений палладия у мышей составляет 200 мг/кг при пероральном введении и 5 мг/кг при внутривенном введении . [72]

Уильям Хайд Волластон отметил в своей лабораторной книге открытие нового благородного металла в июле 1802 года и в августе того же года назвал его палладием. Волластон очистил некоторое количество материала и предложил его, не называя имени первооткрывателя, в небольшом магазине в Сохо в апреле 1803 года. После резкой критики со стороны Ричарда Ченевикса , который утверждал, что палладий представляет собой сплав платины и ртути, Волластон анонимно предложил вознаграждение. 20 фунтов стерлингов за 20 гран синтетического палладиевого сплава . [77] Ченевикс получил медаль Копли в 1803 году после публикации своих экспериментов с палладием. Волластон опубликовал открытие родия в 1804 году и упоминает некоторые из своих работ по палладию. [78] [79] Он сообщил, что был первооткрывателем палладия в публикации 1805 года. [77] [80]
Он был назван Волластоном в 1802 году в честь астероида 2 Паллада , открытого двумя месяцами ранее. [7] Волластон обнаружил палладий в сырой платиновой руде из Южной Америки , растворив руду в царской водке , нейтрализовав раствор гидроксидом натрия и осаждая платину в виде хлороплатината аммония с помощью хлорида аммония . Он добавил цианид ртути , чтобы получить соединение цианид палладия (II) , которое нагревали для извлечения металлического палладия. [78]
Палладия хлорид одно время назначали для лечения туберкулеза из расчета 0,065 г в сутки (примерно один миллиграмм на килограмм массы тела). Это лечение имело множество негативных побочных эффектов и позже было заменено более эффективными препаратами. [81]
Большая часть палладия используется для каталитических нейтрализаторов в автомобильной промышленности. [72] Каталитические нейтрализаторы являются мишенью для воров, поскольку они содержат палладий и другие редкие металлы. В преддверии 2000 года поставки российского палладия на мировой рынок неоднократно задерживались и прерывались; по политическим причинам экспортная квота не была предоставлена вовремя. [82] Последовавшая за этим паника на рынке привела к тому, что в январе 2001 года цена достигла рекордного уровня в 1340 долларов за тройскую унцию (43 доллара за г ). [83] Примерно в то же время компания Ford Motor Company , опасаясь, что производство автомобилей будет нарушено Нехватка палладия привела к накоплению металла. Когда в начале 2001 года цены упали, Ford потерял почти 1 миллиард долларов США . [84]
Мировой спрос на палладий увеличился со 100 тонн в 1990 году до почти 300 тонн в 2000 году. По данным Геологической службы США , в 2006 году мировое производство палладия на рудниках составило 222 тонны . [31] Многие были обеспокоены стабильными поставками палладия после аннексии Крыма Россией , отчасти потому, что санкции могут затруднить российский экспорт палладия; Любые ограничения на экспорт палладия из России могли усугубить и без того ожидаемый большой дефицит палладия в 2014 году. [85] Эти опасения привели к тому, что цены на палладий достигли самого высокого уровня с 2001 года. [86] В сентябре 2014 года они взлетели выше 900 долларов за унцию. отметка. Однако в 2016 году палладий стоил около $614 за унцию, поскольку России удавалось поддерживать стабильные поставки. [87] В январе 2019 года фьючерсы на палладий впервые в истории поднялись выше $1344 за унцию, главным образом из-за высокого спроса со стороны автомобильной промышленности. [88] 6 января 2020 года цена палладия достигла $2024,64 за тройскую унцию ($65,094/г), впервые превысив $2000 за тройскую унцию. [89] В мае 2021 и марте 2022 года цена поднялась выше 3000 долларов за тройскую унцию. [90]

Мировые продажи палладия в 2017 году составили 8,84 миллиона тройских унций (275 тонн), [91] из которых 86% было использовано в производстве автомобильных каталитических нейтрализаторов, за которыми следовали промышленность, ювелирные изделия и инвестиции. [92] Более 75% мировой платины и 40% палладия добываются в Южной Африке . Российская горнодобывающая компания «Норильский никель » производит еще 44% палладия, а большую часть остального добывают на рудниках в США и Канаде.
Цена на палладий достигла рекордного максимума в $2981,40 за унцию 3 мая 2021 года, [93] [94] в основном из-за спекуляций о спросе на каталитические нейтрализаторы со стороны автомобильной промышленности . Палладий торгуется на спотовом рынке под кодом «XPD». При расчете в долларах США код — «XPDUSD». Более поздний избыток металла был вызван тем , что российское правительство продавало запасы советского времени в размере от 1,6 до 2 миллионов тройских унций (от 50 до 62 тонн) в год. Объем и состояние этих запасов являются государственной тайной .
Во время российско-украинской войны в марте 2022 года цены на палладий выросли на 13% с первого марта. Россия является основным поставщиком в Европу и обеспечивает 37% мирового производства. [95]
WisdomTree Physical Palladium ( LSE : PHPD) обеспечен выделенными палладиевыми слитками и является первым в мире палладиевым ETF . Она котируется на Лондонской фондовой бирже как PHPD, [96] Xetra Trading System , Euronext и Milan . ETFS Physical Palladium Shares ( NYSE : PALL) — это ETF, торгуемый на Нью-Йоркской фондовой бирже .
Традиционный способ инвестирования в палладий – покупка инвестиционных монет и слитков из палладия. Доступные палладиевые монеты включают канадский палладиевый кленовый лист , китайскую панду и американский палладиевый орел . Ликвидность прямых инвестиций в палладиевые слитки хуже, чем у золота и серебра , поскольку палладиевые монеты находятся в низком обращении. [97]
{{cite book}}: |journal=игнорируется ( помощь ){{cite book}}: CS1 maint: другие ( ссылка ){{cite book}}: CS1 maint: числовые имена: список авторов ( ссылка )