Пропионовая ацидемия , также известная как пропионовая ацидурия или дефицит пропионил-КоА-карбоксилазы ( дефицит PCC ), [1] является редким аутосомно-рецессивным метаболическим расстройством , классифицируемым как органическая ацидемия с разветвленной цепью . [2] [3]
Расстройство проявляется в раннем неонатальном периоде плохим питанием, рвотой, летаргией и отсутствием мышечного тонуса. [4] Без лечения может быстро наступить смерть из-за вторичной гипераммониемии , инфекции, кардиомиопатии или повреждения мозга. [5]
Пропионовая ацидемия может различаться по степени тяжести. [6] Тяжелая пропионовая ацидемия приводит к симптомам, которые уже наблюдаются у новорожденных. [7] Симптомы включают плохое питание, рвоту , обезвоживание , ацидоз , низкий мышечный тонус ( гипотонию ), судороги и летаргию . Последствия пропионовой ацидемии быстро становятся опасными для жизни. [ необходима цитата ]
Долгосрочные осложнения могут включать умственную отсталость, аутизм, [8] хроническую болезнь почек, [9] кардиомиопатию и удлиненный интервал QTc. [10]
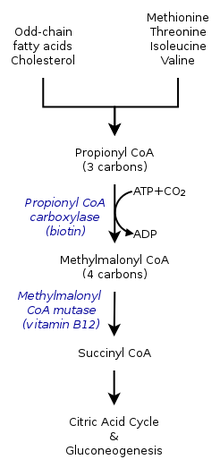

У здоровых людей фермент пропионил-КоА-карбоксилаза преобразует пропионил-КоА в метилмалонил-КоА . Это один из многих этапов в процессе преобразования определенных аминокислот и жиров в энергию. Люди с пропионовой ацидемией не могут выполнить это преобразование, поскольку фермент пропионил-КоА-карбоксилаза нефункционален. Незаменимые аминокислоты валин , метионин , изолейцин и треонин не могут быть преобразованы, и это приводит к накоплению пропионил-КоА. Вместо того, чтобы преобразовываться в метилмалонил-КоА, пропионил-КоА затем преобразуется в пропионовую кислоту , которая накапливается в кровотоке. Это, в свою очередь, вызывает накопление опасных кислот и токсинов, которые могут вызвать повреждение органов. [ необходима цитата ]
Во многих случаях пропионовая ацидемия может повредить мозг, сердце, почки, печень, вызвать судороги и задержки нормального развития, например, ходьбы или речи. Известно, что накопление пропионовой кислоты вызывает различные реакции в разных органах. Сердце и печень являются конкретными целями осложнения. Пациенту может потребоваться госпитализация, чтобы предотвратить распад белков в организме. Диетические потребности должны тщательно контролироваться. [ необходима цитата ]
Мутации в обеих копиях генов PCCA или PCCB вызывают пропионовую ацидемию. [11] Эти гены содержат инструкции по формированию альфа- и бета-субъединиц PCC, фермента, называемого пропионил-КоА-карбоксилазой. [ необходима цитата ]
PCC требуется для нормального распада незаменимых аминокислот валина, изолейцина, треонина и метионина, а также некоторых жирных кислот с нечетной цепью. Мутации в генах PCCA или PCCB нарушают функцию фермента, предотвращая метаболизм этих кислот. В результате пропионил-КоА , пропионовая кислота, кетоны , аммиак и другие токсичные соединения накапливаются в крови , вызывая признаки и симптомы пропионовой ацидемии . Гипераммониемия развивается из-за ингибирующего действия пропионил-КоА на N-ацетилглутаматсинтазу , что косвенно приводит к замедлению цикла мочевины . [12]
Повышенные метаболиты пропионовой кислоты (например, 3-гидроксипропионат, 2-метилцитрат, тиглилглицин, пропионилглицин) обнаружены в крови и моче наряду с нормальной активностью биотинидазы и нормальными уровнями метилмалоновой кислоты. [10]
Пациентам с пропионовой ацидемией следует как можно раньше начинать диету с низким содержанием белка. В дополнение к белковой смеси, лишенной метионина, треонина, валина и изолейцина, пациент должен также получать лечение L -карнитином и антибиотики 10 дней в месяц, чтобы удалить кишечную пропиогенную флору. Пациенту следует подготовить диетические протоколы с «диетой здорового дня» с низким содержанием белка, «половинной экстренной диетой», содержащей половину потребности в белке, и «экстренной диетой» без содержания белка. Эти пациенты подвержены риску тяжелой гипераммониемии во время инфекций, которые могут привести к коматозным состояниям. [13]
Трансплантация печени приобретает все большую роль в лечении таких пациентов, и небольшие серии исследований показывают улучшение качества жизни. [ необходима цитата ]
Пропионовая ацидемия наследуется по аутосомно- рецессивному типу и встречается примерно у 1 из 35 000 [11] живорожденных в Соединенных Штатах . Это состояние, по-видимому, более распространено в Саудовской Аравии , [14] с частотой около 1 из 3000. [11] Это состояние также, по-видимому, распространено среди амишей , меннонитов и других популяций с более высокой частотой кровного родства. [15]
В 1957 году родился мальчик с плохим умственным развитием, повторяющимися приступами ацидоза и высоким уровнем кетонов и глицина в крови. После диетического тестирования доктор Бартон Чайлдс обнаружил, что его симптомы ухудшались, когда ему давали аминокислоты лейцин, изолейцин, валин, метионин и треонин. В 1961 году медицинская группа в больнице Джона Хопкинса в Балтиморе , штат Мэриленд, опубликовала этот случай, назвав это расстройство кетотическим гиперглицинемией . В 1969 году, используя данные сестры исходного пациента, ученые установили, что пропионовая ацидемия является рецессивным расстройством, и что пропионовая ацидемия и метилмалоновая ацидемия вызваны дефицитом одного и того же ферментного пути. [16]