Пиррол — гетероциклическое ароматическое органическое соединение с пятичленным кольцом формулы C 4 H 4 NH . _ [3] Это бесцветная летучая жидкость, которая легко темнеет на воздухе. Замещенные производные также называют пирролами, например, N -метилпиррол, C 4 H 4 NCH 3 . Порфобилиноген , тризамещенный пиррол, является биосинтетическим предшественником многих природных продуктов, таких как гем . [4]
Пирролы являются компонентами более сложных макроциклов, включая порфириногены и продукты их переработки, в том числе порфирины гема , хлорины , бактериохлорины и хлорофиллы . [5]
Пиррол представляет собой бесцветную летучую жидкость, которая легко темнеет на воздухе и обычно очищается перегонкой непосредственно перед использованием. [6] Пиррол имеет ореховый запах. Пиррол — пятичленный ароматический гетероцикл, подобный фурану и тиофену . В отличие от фурана и тиофена он имеет диполь , у которого положительный конец лежит на стороне гетероатома, с дипольным моментом 1,58 Д. В CDCl 3 он имеет химические сдвиги 6,68 (H2, H5) и 6,22 (H3, H4). Пиррол является чрезвычайно слабым основанием для амина, с сопряженной кислотой pKa, равной -3,8 . Наиболее термодинамически стабильный катион пирролия (C 4 H 6 N + ) образуется за счет протонирования во 2-м положении. Замещение пиррола алкильными заместителями дает более основную молекулу - например, тетраметилпиррол имеет сопряженную кислоту p K a +3,7. Пиррол также является слабокислым в положении N–H с ap K a 16,5. Как кислота Льюиса с водородными связями, она классифицируется как жесткая кислота , и в модели ECW ее кислотные параметры указаны как E A = 1,38 и CA = 0,68 .
Пиррол имеет ароматический характер, поскольку неподеленные пары электронов на атоме азота частично делокализованы в кольцо, создавая ароматическую систему 4 n + 2 (см . правило Хюккеля ). По ароматичности пирролы умеренны по сравнению с бензолом , но сравнимы с родственными гетероциклами тиофеном и фураном . Резонансные энергии бензола, пиррола, тиофена и фурана составляют соответственно 152, 88, 121 и 67 кДж/моль (36, 21, 29 и 16 ккал/моль). [7] Молекула плоская.
Пиррол впервые был обнаружен Ф. Ф. Рунге в 1834 году как составная часть каменноугольной смолы . [8] В 1857 году он был выделен из пиролизата кости . Его название происходит от греческого пиррос ( πυρρός , «красноватый, огненный»), от реакции, используемой для его обнаружения — красного цвета, который он придает древесине при увлажнении соляной кислотой . [9]

Сам пиррол не встречается в природе, но многие его производные встречаются в различных кофакторах и натуральных продуктах . Обычные природные молекулы, содержащие пирролы, включают витамин B12 , желчные пигменты, такие как билирубин и биливердин , а также порфирины гема , хлорофилла , хлорины , бактериохлорины и порфириногены. [5] Другие пирролсодержащие вторичные метаболиты включают PQQ, макалувамин М, рианодин, разанилам, ламелларин, продигиозин, мирмикарин и скептрин. Синтез пирролсодержащего гемина, синтезированный Гансом Фишером, был отмечен Нобелевской премией.
Пиррол входит в состав табачного дыма и может способствовать его токсическому воздействию. [10]
Пиррол получают в промышленности обработкой фурана аммиаком в присутствии твердых кислотных катализаторов типа SiO 2 и Al 2 O 3 . [9]

Пиррол также может быть образован каталитическим дегидрированием пирролидина. [ нужна цитата ]
Описано несколько синтезов пиррольного кольца. [11] Доминируют три маршрута, [12] но существует множество других методов.
Синтез пиррола Ганча представляет собой реакцию β-кетоэфиров ( 1 ) с аммиаком (или первичными аминами) и α-галогенкетонами ( 2 ) с образованием замещенных пирролов ( 3 ). [13] [14]

Синтез пиррола Кнорра включает реакцию α-аминокетона или α-амино-β-кетоэфира с активированным метиленовым соединением. [15] [16] [17] Метод включает реакцию α- аминокетона ( 1 ) и соединения, содержащего метиленовую группу α с (связанной со следующим углеродом) карбонильной группой ( 2 ). [18]

В синтезе пиррола Паала-Кнорра 1,4-дикарбонильное соединение реагирует с аммиаком или первичным амином с образованием замещенного пиррола. [19] [20]

Пирролы по реакции Ван Лейзена получают реакцией тозилметилизоцианида (TosMIC) с еноном в присутствии основания при присоединении Михаэля . Затем в результате 5- эндоциклизации образуется 5-членное кольцо, которое реагирует с удалением тозильной группы. Последний этап — таутомеризация до пиррола. [ нужна цитата ]
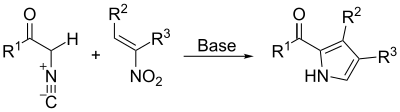
В результате синтеза Бартона-Зарда изоцианоацетат реагирует с нитроалкеном по 1,4-присоединению с последующей 5- эндо - диг- циклизацией, отщеплением нитрогруппы и таутомеризацией . [21]
Исходными материалами в синтезе пиррола Пилоти-Робинсона, названного в честь Гертруды , Роберта Робинсона и Оскара Пилоти , являются два эквивалента альдегида и гидразина . [22] [23] Продукт представляет собой пиррол с заместителями в положениях 3 и 4. Альдегид реагирует с диамином с образованием промежуточного димина ( R-C=N-N=C-R). На втором этапе между ними происходит [3,3] -сигматропная перегруппировка . Добавление соляной кислоты приводит к замыканию цикла и потере аммиака с образованием пиррола. Механизм разработали Робинсоны .
В одной модификации пропиональдегид обрабатывают сначала гидразином , а затем бензоилхлоридом при высоких температурах и с помощью микроволнового облучения : [24]
![Реакция Пилоти-Робинсона[24]](http://upload.wikimedia.org/wikipedia/commons/thumb/b/bd/Piloty-Robinson_reaction.png/400px-Piloty-Robinson_reaction.png)
Пирролы, несущие несколько заместителей, были получены реакцией мюнхнонов и алкинов . Механизм реакции включает 1,3-диполярное циклоприсоединение с последующей потерей углекислого газа по ретро -процессу Дильса-Альдера . Подобные реакции можно провести с использованием азалактонов.
Пирролы также можно получить катализируемой серебром циклизацией алкинов с изонитрилами , где R 2 — электроноакцепторная группа, а R 1 — алкан, арильная группа или сложноэфирная группа. Также было замечено, что примеры дизамещенных алкинов образуют желаемый пиррол со значительным выходом. Предполагается, что реакция протекает через промежуточный продукт ацетилида серебра . Этот метод аналогичен азид-алкиновой клик-химии , используемой для образования азолов.
Один из синтетических путей получения пиррола включает декарбоксилирование слизи аммония , аммониевой соли муциновой кислоты . Соль обычно нагревают в дистилляционной установке с глицерином в качестве растворителя . [25]

Биосинтез пиррольных колец начинается с аминолевулиновой кислоты (АЛК), которая синтезируется из глицина и сукцинил-КоА . АЛК-дегидратаза катализирует конденсацию двух молекул АЛК посредством синтеза колец типа Кнорра с образованием порфобилиногена (ПБГ). Позже он реагирует с образованием, например, гема макроциклов и хлорофилла . [26]
.
Пролин получают биосинтетически из аминокислоты L - глутамата . Глутамат-5-полуальдегид сначала образуется глутамат-5-киназой (АТФ-зависимой) и глутамат-5-полуальдегиддегидрогеназой (которая требует НАДН или НАДФН). Затем он может либо спонтанно циклизоваться с образованием 1-пирролин-5-карбоновой кислоты , которая восстанавливается до пролина пирролин-5-карбоксилатредуктазой (с использованием НАДН или НАДФН), либо превращается в орнитин с помощью орнитинаминотрансферазы с последующей циклизацией орнитинциклодеаминазой. с образованием пролина. [27]

Пролин можно использовать в качестве предшественника ароматических пирролов во вторичных натуральных продуктах, например, в продигиозинах.

Биосинтез продигиозина [28] [29] включает конвергентное соединение трех колец пиррольного типа (обозначенных A, B и C на рисунке 1) из L -пролина, L -серина, L -метионина, пирувата и 2-октеналя. .
Кольцо А синтезируется из L -пролина по пути нерибосомальной пептидсинтазы (NRPS) (рисунок 2), при котором пирролидиновое кольцо пролина дважды окисляется посредством FAD + с образованием пиррольного кольца А.
Затем кольцо А расширяется по пути поликетидсинтазы для включения L -серина в кольцо B (рисунок 3). Фрагмент кольца А переносится от белка-переносчика пептидила (PCP) к белку-ацил-переносчику (ACP) с помощью домена KS с последующим переносом на малонил-ACP посредством декарбоксилирующей конденсации Кляйзена. Затем этот фрагмент способен реагировать с замаскированным карбанионом, образующимся в результате декарбоксилирования L -серина, опосредованного PLP, который циклизуется в реакции дегидратации с образованием второго пиррольного кольца. Затем это промежуточное соединение модифицируется путем метилирования (которое включает метильную группу L -метионина в спирт в положении 6) и окисления первичного спирта до альдегида с образованием основных кольцевых структур A–B.
Из-за своего ароматического характера пиррол трудно гидрировать , он с трудом реагирует как диен в реакциях Дильса-Альдера и не вступает в обычные реакции с олефинами . Его реакционная способность аналогична реакционной способности бензола и анилина , поскольку его легко алкилировать и ацилировать. В кислых условиях пирролы легко окисляются до полипиррола [30] , поэтому многие электрофильные реагенты, используемые в химии бензола, неприменимы к пирролам. Напротив, замещенные пирролы (включая защищенные пирролы) использовались в широком диапазоне превращений. [11]
Пирролы обычно реагируют с электрофилами в α-положении (C2 или C5) из-за высочайшей степени стабильности протонированного промежуточного продукта.

Пирролы легко реагируют с нитрующими (например, HNO 3 / Ac 2 O ), сульфирующими ( Py·SO 3 ) и галогенирующими (например , NCS , NBS , Br 2 , SO 2 Cl 2 и KI / H 2 O 2 ) агентами. [31] Галогенирование обычно дает полигалогенированные пирролы, но может быть проведено и моногалогенирование. Как это типично для электрофильных присадок к пирролам, галогенирование обычно происходит в положении 2, но может также происходить и в положении 3 за счет силилирования азота. Это полезный метод для дальнейшей функционализации обычно менее реактивной 3-й позиции. [ нужна цитата ]
Ацилирование обычно происходит во 2-м положении с использованием различных методов. Ацилирование ангидридами кислот и хлорангидридами кислот может происходить с катализатором или без него. [32] 2-Ацилпирролы также получают в результате реакции с нитрилами по реакции Губена-Хеша . Пирролальдегиды могут образовываться по реакции Вильсмайера-Хаака . [33]

Протон NH в пирролах умеренно кислый с p K a 17,5. [34] Пиррол можно депротонировать сильными основаниями, такими как бутиллитий и гидрид натрия . [35] Образующийся щелочной пирролид является нуклеофильным . Обработка этого сопряженного основания электрофилом, таким как йодметан, дает N -метилпиррол.
N -Металированный пиррол может реагировать с электрофилами в положениях N или C, в зависимости от металла-координатора. Большее количество ионных связей азот-металл (например, с литием, натрием и калием) и большее количество сольватирующих растворителей приводят к N -алкилированию. Нитрофильные металлы, такие как MgX, приводят к алкилированию по C (главным образом C2) из-за более высокой степени координации с атомом азота. В случае N -замещенных пирролов металлирование атомов углерода происходит легче. Алкильные группы могут быть введены как электрофилы или посредством реакций кросс-сочетания. [ нужна цитата ]
Замещение у C3 может быть достигнуто за счет использования N -замещенного 3-бромпиррола, который можно синтезировать бромированием N -силилпиррола NBS . [ нужна цитата ]
Пирролы могут восстанавливаться до пирролидинов и пирролинов . [36] Например, восстановлением Берча эфиров пиррола и амидов были получены пирролины, региоселективность которых зависела от положения электроноакцепторной группы. [ нужна цитата ]
Пирролы с N -замещением могут вступать в реакции циклоприсоединения , такие как [4+2]-, [2+2]- и [2+1]-циклизации. Циклизация Дильса-Альдера может происходить, когда пиррол действует как диен, особенно в присутствии электроноакцепторной группы азота. Винилпирролы также могут действовать как диены. [ нужна цитата ]
Пирролы могут реагировать с карбенами , такими как дихлоркарбен , в виде [2+1]-циклоприсоединения. С дихлоркарбеном образуется промежуточный дихлорциклопропан, который распадается с образованием 3-хлорпиридина (перегруппировка Циамициана-Деннстедта). [37] [38] [39]

Полипиррол имеет некоторую коммерческую ценность. N -Метилпиррол является предшественником N -метилпирролкарбоновой кислоты, строительного материала в фармацевтической химии. [9] Пирролы также содержатся в некоторых лекарствах, включая аторвастатин , кеторолак и сунитиниб . Пирролы используются как светостойкие красные, алые и карминовые пигменты. [40] [41]
Структурные аналоги пиррола включают:
Производные пиррола включают индол , производное с конденсированным бензольным кольцом.
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ){{cite book}}: |journal=игнорируется ( помощь )