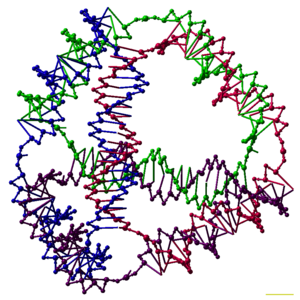
ДНК-нанотехнология — это разработка и производство структур искусственных нуклеиновых кислот для технологических целей. В этой области нуклеиновые кислоты используются как небиологические инженерные материалы для нанотехнологий , а не как носители генетической информации в живых клетках . Исследователи в этой области создали статические структуры, такие как двух- и трехмерные кристаллические решетки , нанотрубки , многогранники и произвольные формы, а также функциональные устройства, такие как молекулярные машины и ДНК-компьютеры . Эта область начинает использоваться в качестве инструмента для решения фундаментальных научных проблем в структурной биологии и биофизике , включая приложения в рентгеновской кристаллографии и спектроскопии ядерного магнитного резонанса белков для определения структур. Также исследуются потенциальные применения в электронике молекулярного масштаба и наномедицине .
Концептуальная основа ДНК-нанотехнологии была впервые заложена Надрианом Симаном в начале 1980-х годов, а широкий интерес к этой области начал привлекать в середине 2000-х годов. Такое использование нуклеиновых кислот возможно благодаря их строгим правилам спаривания оснований , которые заставляют связываться вместе только части цепей с комплементарными последовательностями оснований , образуя прочные, жесткие структуры двойной спирали . Это позволяет рационально разрабатывать базовые последовательности , которые будут избирательно собираться в сложные целевые структуры с точно контролируемыми наноразмерными характеристиками. Для создания этих структур используется несколько методов сборки, в том числе структуры на основе плиток, которые собираются из более мелких структур, складные структуры с использованием метода ДНК-оригами и динамически реконфигурируемые структуры с использованием методов смещения цепей. Название области конкретно отсылает к ДНК , но те же принципы использовались и с другими типами нуклеиновых кислот, что привело к периодическому использованию альтернативного названия « Нанотехнология нуклеиновых кислот ».
Концептуальная основа нанотехнологии ДНК была впервые заложена Надрианом Зееманом в начале 1980-х годов. [2] Первоначальной мотивацией Симана было создание трехмерной решетки ДНК для ориентации других крупных молекул, что упростило бы их кристаллографическое исследование , устранив сложный процесс получения чистых кристаллов. Эта идея, как сообщается, пришла к нему в конце 1980 года, после того как он осознал сходство между гравюрой на дереве « Глубина» М. К. Эшера и массивом шестилучевых соединений ДНК. [3] [4] В то время было известно несколько природных разветвленных структур ДНК, включая репликационную вилку ДНК и мобильное соединение Холлидея , но идея Симана заключалась в том, что неподвижные соединения нуклеиновых кислот могут быть созданы путем правильного проектирования последовательностей цепей для устранения симметрии в собранную молекулу и что эти неподвижные соединения в принципе могут быть объединены в жесткие кристаллические решетки. Первая теоретическая статья, предлагающая эту схему, была опубликована в 1982 году, а первая экспериментальная демонстрация неподвижного соединения ДНК была опубликована в следующем году. [5] [6]

В 1991 году лаборатория Симана опубликовала отчет о синтезе куба из ДНК, первой синтетической трехмерной наноструктуры нуклеиновой кислоты, за что он получил премию Фейнмана 1995 года в области нанотехнологий . За этим последовал усеченный ДНК октаэдр . Вскоре стало ясно, что эти структуры, представляющие собой многоугольные формы с гибкими соединениями в вершинах , недостаточно жесткие, чтобы образовывать протяженные трехмерные решетки. Симан разработал более жесткий структурный мотив двойного пересечения (DX) , а в 1998 году в сотрудничестве с Эриком Уинфри опубликовал создание двумерных решеток из плиток DX. [3] [2] [7] Преимущество этих структур на основе плиток заключалось в том, что они обеспечивали возможность реализации вычислений на ДНК, что было продемонстрировано Уинфри и Полом Ротемундом в их статье 2004 года об алгоритмической самосборке структуры прокладки Серпинского. и за что они разделили премию Фейнмана в области нанотехнологий 2006 года. Ключевая идея Уинфри заключалась в том, что плитки DX можно использовать как плитки Ванга , а это означает, что их сборка может выполнять вычисления. [2] Синтез трехмерной решетки был наконец опубликован Симаном в 2009 году, почти через тридцать лет после того, как он намеревался достичь этого. [8]
На протяжении 2000-х годов продолжали открываться новые способности созданных структур ДНК. Первая наномашина ДНК — мотив, который меняет свою структуру в ответ на входной сигнал — была продемонстрирована в 1999 году Симаном. Усовершенствованная система, которая стала первым устройством на основе нуклеиновых кислот, в котором использовалось смещение цепей с помощью опоры, была продемонстрирована Бернардом Юрком в 2000 году . Системы ДНК-ходок были продемонстрированы группами Симана, Найлза Пирса , Эндрю Терберфилда и Чэндэ Мао. [10] Идея использования массивов ДНК для создания шаблонов сборки других молекул, таких как наночастицы и белки, впервые предложенная Брюшом Робинсоном и Симаном в 1987 году, [11] была продемонстрирована в 2002 году Симаном, Килем и др. [12] и впоследствии многими другими группами.
В 2006 году Ротемунд впервые продемонстрировал метод ДНК-оригами , позволяющий легко и надежно формировать свернутые структуры ДНК произвольной формы. Ротемунд задумал этот метод как концептуально промежуточный между решетками DX Симана, в которых использовалось множество коротких нитей, и октаэдром ДНК Уильяма Ши, который состоял в основном из одной очень длинной нити. ДНК-оригами Ротемунда содержит длинную нить, сворачиванию которой способствуют несколько коротких нитей. Этот метод позволил сформировать гораздо более крупные структуры, чем это было возможно раньше, и которые менее технически сложны в проектировании и синтезе. [7] ДНК-оригами было на обложке журнала Nature от 15 марта 2006 года. [13] За исследованием Ротемунда, демонстрирующим двумерные структуры ДНК-оригами, последовала демонстрация твердого трехмерного ДНК-оригами Дугласом и др. в 2009 году [14] , в то время как лаборатории Йоргена Кьемса и Яна продемонстрировали полые трехмерные структуры, состоящие из двухмерных граней. [8]
Нанотехнология ДНК изначально была встречена с некоторым скептицизмом из-за необычного небиологического использования нуклеиновых кислот в качестве материалов для построения структур и проведения вычислений, а также преобладания экспериментов по доказательству принципов , которые расширяли возможности этой области, но были далеки от реального применения. Статья Симана 1991 года о синтезе куба ДНК была отклонена журналом Science после того, как один рецензент похвалил ее оригинальность, а другой раскритиковал ее за отсутствие биологической значимости. [15] К началу 2010-х годов считалось, что эта область расширила свои возможности до такой степени, что начали реализовываться приложения для фундаментальных научных исследований, а практическое применение в медицине и других областях стало считаться возможным. [8] [16] Эта область выросла с очень небольшого количества действующих лабораторий в 2001 году до как минимум 60 в 2010 году, что увеличило кадровый резерв и, следовательно, количество научных достижений в этой области за это десятилетие. [17]

Нанотехнологию часто определяют как исследование материалов и устройств с характеристиками в масштабе менее 100 нанометров . Нанотехнология ДНК, в частности, является примером молекулярной самосборки снизу вверх , при которой молекулярные компоненты спонтанно организуются в стабильные структуры; Особая форма этих структур обусловлена физическими и химическими свойствами выбранных проектировщиками компонентов. [19] В нанотехнологии ДНК компонентами материалов являются нити нуклеиновых кислот, таких как ДНК; эти нити часто являются синтетическими и почти всегда используются вне контекста живой клетки. ДНК хорошо подходит для наномасштабного конструирования, поскольку связывание между двумя нитями нуклеиновой кислоты зависит от простых правил спаривания оснований , которые хорошо понятны и образуют специфическую наноразмерную структуру двойной спирали нуклеиновой кислоты . Эти качества позволяют легко контролировать сборку структур нуклеиновой кислоты посредством дизайна нуклеиновой кислоты . Это свойство отсутствует в других материалах, используемых в нанотехнологиях, включая белки , для которых разработка белков очень сложна, и наночастицы , которые не обладают способностью к специфической сборке самостоятельно. [5]
Структура молекулы нуклеиновой кислоты состоит из последовательности нуклеотидов , отличающихся тем, какое азотистое основание они содержат. В ДНК присутствуют четыре основания: аденин (А), цитозин (С), гуанин (G) и тимин (Т). Нуклеиновые кислоты обладают свойством, заключающимся в том, что две молекулы будут связываться друг с другом, образуя двойную спираль, только если две последовательности комплементарны , что означает, что они образуют совпадающие последовательности пар оснований, при этом A связывается только с T, а C только с G. [ 5] [20] Поскольку образование правильно спаренных пар оснований энергетически выгодно , ожидается, что в большинстве случаев цепи нуклеиновой кислоты будут связываться друг с другом в конформации, которая максимизирует количество правильно спаренных оснований. Таким образом, последовательности оснований в системе нитей легко контролируемым образом определяют характер связывания и общую структуру. В нанотехнологии ДНК последовательности оснований цепей рационально разрабатываются исследователями так, что взаимодействия спаривания оснований заставляют цепи собираться в желаемую конформацию. [3] [5] Хотя ДНК является доминирующим используемым материалом, также были созданы структуры, включающие другие нуклеиновые кислоты, такие как РНК и пептид-нуклеиновая кислота (ПНК). [21] [22]
Нанотехнологию ДНК иногда делят на две пересекающиеся области: структурную нанотехнологию ДНК и динамическую нанотехнологию ДНК. Структурная нанотехнология ДНК, иногда сокращенно называемая SDN, фокусируется на синтезе и характеристике комплексов нуклеиновых кислот и материалов, которые собираются в статическое, равновесное конечное состояние. С другой стороны, нанотехнология динамической ДНК фокусируется на комплексах с полезным неравновесным поведением, например способностью реконфигурироваться на основе химического или физического стимула. Некоторые комплексы, например наномеханические устройства на основе нуклеиновых кислот, сочетают в себе черты как структурного, так и динамического подполей. [23] [24]
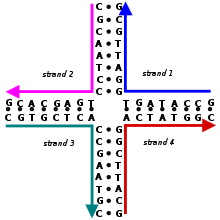
Комплексы, построенные с помощью структурной нанотехнологии ДНК, используют топологически разветвленные структуры нуклеиновых кислот, содержащие соединения. (Напротив, большая часть биологической ДНК существует в виде неразветвленной двойной спирали .) Одной из простейших разветвленных структур является соединение с четырьмя плечами, состоящее из четырех отдельных цепей ДНК, части которых комплементарны по определенному образцу. В отличие от естественных соединений Холлидея , каждое плечо в искусственном неподвижном четырехветвевом соединении имеет различную последовательность оснований , в результате чего точка соединения фиксируется в определенном положении. Множественные соединения могут быть объединены в один и тот же комплекс, например, в широко используемом структурном мотиве двойного кроссовера (DX) , который содержит два параллельных двойных спиральных домена с отдельными цепями, пересекающимися между доменами в двух точках кроссовера. Каждая точка кроссовера топологически представляет собой четырехплечевое соединение, но ограничена одной ориентацией, в отличие от гибкого одиночного четырехплечевого соединения, что обеспечивает жесткость, которая делает мотив DX подходящим в качестве структурного строительного блока для более крупных комплексов ДНК. [3] [5]
Динамическая нанотехнология ДНК использует механизм, называемый смещением цепи, опосредованным опорой, чтобы позволить комплексам нуклеиновых кислот реконфигурироваться в ответ на добавление новой цепи нуклеиновой кислоты. В этой реакции входящая цепь связывается с одноцепочечной опорной областью двухцепочечного комплекса, а затем вытесняет одну из цепей, связанных в исходном комплексе, посредством процесса миграции ветвей . Общий эффект заключается в том, что одна из нитей комплекса заменяется другой. [23] Кроме того, реконфигурируемые структуры и устройства могут быть созданы с использованием функциональных нуклеиновых кислот, таких как дезоксирибозимы и рибозимы , которые могут выполнять химические реакции, и аптамеры , которые могут связываться со специфическими белками или небольшими молекулами. [25]
Структурная нанотехнология ДНК, иногда сокращенно называемая SDN, фокусируется на синтезе и характеристике комплексов нуклеиновых кислот и материалов, сборка которых имеет статическую, равновесную конечную точку. Двойная спираль нуклеиновой кислоты имеет надежную, определенную трехмерную геометрию, которая позволяет моделировать, [26] прогнозировать и проектировать структуры более сложных комплексов нуклеиновых кислот. Создано множество таких структур, в том числе двух- и трехмерные, а также периодические, апериодические и дискретные. [24]

Небольшие комплексы нуклеиновых кислот могут быть снабжены липкими концами и объединены в более крупные двумерные периодические решетки, содержащие определенный мозаичный рисунок отдельных молекулярных плиток. [24] Самый ранний пример этого использовал комплексы двойного пересечения (DX) в качестве основных плиток, каждый из которых содержал четыре липких конца, созданных с последовательностями, которые заставляли единицы DX объединяться в периодические двумерные плоские листы, которые по сути представляют собой жесткие двумерные листы. кристаллы ДНК. [30] [31] Двумерные массивы были созданы и из других мотивов, включая ромбовидную решетку Холлидея , [32] и различные массивы на основе DX, использующие схему двойной когезии. [33] [34] На двух верхних изображениях справа показаны примеры периодических решеток на основе плиток.
Можно создать двумерные массивы, демонстрирующие апериодические структуры, сборка которых реализует определенный алгоритм, демонстрирующий одну из форм вычислений на ДНК. [17] Для плиток DX можно выбрать последовательности липких концов так, чтобы они действовали как плитки Ванга , что позволяет им выполнять вычисления. Был продемонстрирован массив DX, сборка которого кодирует операцию XOR ; это позволяет массиву ДНК реализовать клеточный автомат , который генерирует фрактал , известный как прокладка Серпинского . Третье изображение справа показывает этот тип массива. [29] Другая система имеет функцию двоичного счетчика , отображающего представление возрастающих двоичных чисел по мере их роста. Эти результаты показывают, что вычисления могут быть включены в сборку массивов ДНК. [35]
Массивы DX были созданы для формирования полых нанотрубок диаметром 4–20 нм , по сути, двумерных решеток, которые изгибаются сами по себе. [36] Эти ДНК-нанотрубки по размеру и форме несколько похожи на углеродные нанотрубки , и хотя им не хватает электропроводности углеродных нанотрубок, ДНК-нанотрубки легче модифицируются и соединяются с другими структурами. В одной из многих схем построения нанотрубок ДНК используется решетка из изогнутых плиток DX, которые закручиваются вокруг себя и замыкаются в трубку. [37] В альтернативном методе, который позволяет задавать длину окружности простым модульным способом с использованием однониточных плиток, жесткость трубки является новым свойством . [38]
Формирование трехмерных решеток ДНК было самой ранней целью ДНК-нанотехнологии, но ее оказалось одной из самых трудных для реализации. Об успехе использования мотива, основанного на концепции тенсегрити , баланса между силами растяжения и сжатия, наконец сообщили в 2009 году. [17] [39]
Исследователи синтезировали множество трехмерных комплексов ДНК, каждый из которых имеет связность многогранника , например куба или октаэдра . Это означает, что дуплексы ДНК прослеживают края многогранника с соединением ДНК в каждой вершине. [6] Самые ранние демонстрации многогранников ДНК были очень трудоемкими, требуя многократного лигирования и этапов твердофазного синтеза для создания соединенных многогранников. [40] Последующая работа привела к получению многогранников, синтез которых оказался намного проще. К ним относятся октаэдр ДНК, состоящий из длинной одиночной цепи, предназначенной для сворачивания в правильную конформацию, [41] и тетраэдр, который можно получить из четырех цепей ДНК за один этап, изображенный в верхней части этой статьи. [1]
Наноструктуры произвольной, нерегулярной формы обычно изготавливаются методом ДНК-оригами . Эти структуры состоят из длинной природной вирусной цепи в качестве «каркаса», который складывается в желаемую форму с помощью компьютерно разработанных коротких «штапельных» цепей. Преимущество этого метода заключается в простоте разработки, поскольку базовая последовательность заранее определяется последовательностью цепи каркаса, и он не требует высокой чистоты цепи и точной стехиометрии , как это делают большинство других методов нанотехнологии ДНК. ДНК-оригами было впервые продемонстрировано для двумерных фигур, таких как смайлик , грубая карта Западного полушария и картина Моны Лизы. [6] [13] [42] Твердые трехмерные структуры могут быть созданы с использованием параллельных спиралей ДНК, расположенных в виде сот, [14] а структуры с двумерными гранями могут быть сложены в полую общую трехмерную структуру. по форме напоминает картонную коробку. Их можно запрограммировать на открытие и высвобождение молекулярного груза в ответ на раздражитель, что делает их потенциально полезными в качестве программируемых молекулярных клеток . [43] [44]
Структуры нуклеиновых кислот могут быть созданы для включения молекул, отличных от нуклеиновых кислот, иногда называемых гетероэлементами, включая белки, металлические наночастицы, квантовые точки , амины [45] и фуллерены . Это позволяет создавать материалы и устройства с гораздо большим набором функциональных возможностей, чем это возможно при использовании только нуклеиновых кислот. Цель состоит в том, чтобы использовать самосборку структур нуклеиновых кислот для создания шаблона сборки размещенных на них наночастиц, контролируя их положение, а в некоторых случаях и ориентацию. [6] [46] Многие из этих схем используют схему ковалентного присоединения, используя олигонуклеотиды с амидными или тиоловыми функциональными группами в качестве химической ручки для связывания гетероэлементов. Эта схема ковалентного связывания использовалась для расположения наночастиц золота на матрице на основе DX [47] и для организации молекул белка стрептавидина в определенные структуры на матрице DX. [48] Схема нековалентного хостинга с использованием полиамидов Дервана на матрице DX использовалась для упорядочения белков стрептавидина по определенному шаблону на матрице DX. [49] Углеродные нанотрубки были размещены на массивах ДНК по образцу, позволяющему сборке действовать как молекулярное электронное устройство, полевой транзистор из углеродных нанотрубок . [50] Кроме того, существуют методы металлизации нуклеиновых кислот, при которых нуклеиновая кислота заменяется металлом, принимающим общую форму исходной структуры нуклеиновой кислоты, [51] и схемы использования наноструктур нуклеиновых кислот в качестве литографических масок, переносящих их рисунок на твердой поверхности. [52]
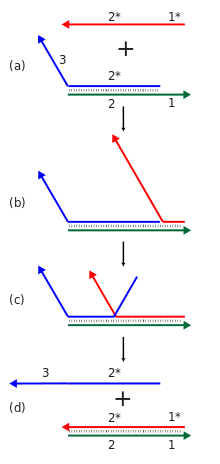
Нанотехнология динамической ДНК направлена на формирование систем нуклеиновых кислот с разработанными динамическими функциями, связанными с их общими структурами, такими как вычисления и механическое движение. Существует некоторое совпадение между структурной и динамической нанотехнологией ДНК, поскольку структуры могут быть сформированы путем отжига, а затем динамически реконфигурированы, или их можно вообще заставить формироваться динамически. [6] [10]
Были созданы комплексы ДНК, которые меняют свою конформацию под воздействием некоторых стимулов, что делает их одной из форм наноробототехники . Эти структуры изначально формируются так же, как статические структуры, созданные с помощью структурной нанотехнологии ДНК, но сконструированы так, что после первоначальной сборки возможна динамическая реконфигурация. [23] [10] Самое раннее такое устройство использовало переход между формами B-ДНК и Z-ДНК , чтобы реагировать на изменение условий буфера , совершая скручивающее движение. [53] Такая зависимость от условий буфера привела к одновременному изменению состояния всех устройств. Последующие системы могли менять состояния в зависимости от наличия цепей управления, что позволяло нескольким устройствам работать независимо друг от друга. Некоторыми примерами таких систем являются конструкция «молекулярного пинцета», имеющая открытое и закрытое состояние, [54] устройство, которое может переключаться с конформации паранемического кроссовера (PX) на конформацию (JX2) с двумя непереходными соединениями. остова ДНК, испытывающего при этом вращательное движение, [55] и двумерного массива, который может динамически расширяться и сжиматься в ответ на управляющие нити. [56] Также были созданы структуры, которые динамически открываются или закрываются, потенциально действуя как молекулярная клетка, высвобождая или раскрывая функциональный груз при открытии. [43] [57] [58] В другом примере наноструктура ДНК-оригами была соединена с РНК-полимеразой Т7 и, таким образом, могла работать как двигатель, управляемый химической энергией, который можно соединить с пассивным последователем, которым он затем управляет. [59]
ДНК-ходоки — это класс наномашин из нуклеиновых кислот, которые демонстрируют направленное движение по линейному пути. Было продемонстрировано большое количество схем. [10] Одна из стратегий заключается в управлении движением ходунка по дорожке с помощью управляющих цепочек, которые необходимо последовательно добавлять вручную. [60] [61] Также возможно контролировать отдельные шаги ДНК-ходока путем облучения светом разных длин волн. [62] Другой подход заключается в использовании ферментов рестрикции или дезоксирибозимов , чтобы расщепить нити и заставить ходунка двигаться вперед, что имеет преимущество автономного бега. [63] [64] Более поздняя система могла передвигаться по двумерной поверхности, а не по линейному пути, и продемонстрировала способность выборочно подбирать и перемещать молекулярный груз. [65] В 2018 году было показано, что цепная ДНК, которая использует транскрипцию по катящемуся кругу с помощью прикрепленной РНК-полимеразы Т7 , движется по пути ДНК, направляемый сгенерированной цепью РНК. [66] Кроме того, был продемонстрирован линейный ходунок, который выполняет синтез по шаблону ДНК по мере продвижения ходунка по дорожке, что позволяет осуществлять автономный многоэтапный химический синтез под руководством ходунка. [67] Функция синтетических ДНК-ходоков аналогична функции белков динеина и кинезина. [68]
Каскады реакций смещения цепей можно использовать как для вычислительных, так и для структурных целей. Реакция смещения отдельной цепи включает выявление новой последовательности в ответ на присутствие некоторой цепи-инициатора. Многие такие реакции могут быть связаны в каскад , где вновь выявленная выходная последовательность одной реакции может инициировать другую реакцию замещения цепи в другом месте. Это, в свою очередь, позволяет создавать сети химических реакций со многими компонентами, демонстрируя сложные вычислительные возможности и возможности обработки информации. Эти каскады становятся энергетически выгодными за счет образования новых пар оснований и увеличения энтропии в результате реакций разборки. Каскады смещения цепей позволяют выполнять изотермическую операцию сборки или вычислительный процесс, в отличие от традиционного требования сборки нуклеиновой кислоты к этапу термического отжига, на котором температура повышается, а затем медленно снижается, чтобы обеспечить правильное формирование желаемой структуры. Они также могут поддерживать каталитическую функцию инициатора, при этом менее одного эквивалента инициатора может привести к завершению реакции. [23] [69]
Комплексы смещения нитей можно использовать для создания молекулярных логических элементов , способных выполнять сложные вычисления. [70] В отличие от традиционных электронных компьютеров, которые используют электрический ток в качестве входных и выходных данных, молекулярные компьютеры используют концентрации определенных химических веществ в качестве сигналов. В случае схем смещения цепи нуклеиновой кислоты сигналом является наличие цепей нуклеиновой кислоты, которые высвобождаются или потребляются в результате событий связывания и развязывания с другими цепями в комплексах замещения. Этот подход использовался для создания логических элементов, таких как логические элементы И, ИЛИ и НЕ. [71] Совсем недавно была продемонстрирована четырехбитная схема, которая может вычислить квадратный корень из целых чисел 0–15, используя систему вентилей, содержащую 130 нитей ДНК. [72]
Другое применение каскадов смещения нитей — создание динамически собираемых структур. В них используется шпилечная структура реагентов, так что при связывании входной цепи вновь обнаруженная последовательность оказывается в той же молекуле, а не разбирается. Это позволяет добавлять в растущий комплекс новые открытые шпильки. Этот подход использовался для создания простых структур, таких как трех- и четырехветвевые соединения и дендримеры . [69]
Нанотехнология ДНК обеспечивает один из немногих способов формирования сложных структур с точным контролем над наноразмерными характеристиками. Эта область начинает находить применение для решения фундаментальных научных задач в области структурной биологии и биофизики . Самое раннее такое применение, предусмотренное в этой области, и еще находящееся в стадии разработки, относится к кристаллографии , где молекулы, которые трудно кристаллизовать изолированно, можно расположить внутри трехмерной решетки нуклеиновой кислоты, что позволяет определить их структуру. Другое применение - использование стержней ДНК-оригами для замены жидких кристаллов в экспериментах по остаточному диполярному соединению в ЯМР-спектроскопии белков ; использование ДНК-оригами выгодно, поскольку, в отличие от жидких кристаллов, они устойчивы к детергентам, необходимым для суспендирования мембранных белков в растворе. Ходоки ДНК использовались в качестве наноразмерных сборочных линий для перемещения наночастиц и прямого химического синтеза . Кроме того, структуры ДНК-оригами помогли в биофизических исследованиях функций ферментов и сворачивания белков . [24] [8]
Нанотехнологии ДНК приближаются к потенциальным практическим приложениям. Способность массивов нуклеиновых кислот организовывать другие молекулы указывает на их потенциальное применение в электронике молекулярного масштаба. Сборка структуры нуклеиновой кислоты может быть использована для создания шаблона сборки молекулярных электронных элементов, таких как молекулярные провода , обеспечивая метод нанометрового контроля размещения и общей архитектуры устройства, аналогичного молекулярному макету . [24] [6] Нанотехнологию ДНК сравнивают с концепцией программируемой материи из-за связи вычислений со свойствами ее материала. [73]
В ходе исследования, проведенного группой ученых из центров iNANO и CDNA Орхусского университета , исследователям удалось сконструировать небольшую мультипереключаемую трехмерную коробку ДНК-оригами. Предложенная наночастица была охарактеризована методами атомно-силовой микроскопии (АСМ), просвечивающей электронной микроскопии (ПЭМ) и резонансного переноса энергии Фёрстера (FRET). Было показано, что построенный ящик имеет уникальный механизм повторного закрытия, который позволяет ему неоднократно открываться и закрываться в ответ на уникальный набор ключей ДНК или РНК. Авторы предположили, что это «устройство ДНК потенциально может быть использовано для широкого спектра применений, таких как контроль функций отдельных молекул, контролируемая доставка лекарств и молекулярные вычисления». [74]
Существуют потенциальные применения нанотехнологии ДНК в наномедицине, где ее способность выполнять вычисления в биосовместимом формате может быть использована для создания «умных лекарств» для адресной доставки лекарств , а также для диагностических приложений. Одна из таких исследуемых систем использует полый ящик ДНК, содержащий белки, вызывающие апоптоз или гибель клеток, который открывается только в непосредственной близости от раковой клетки . [8] [75] Кроме того, существует интерес к экспрессии этих искусственных структур в сконструированных живых бактериальных клетках, скорее всего, с использованием транскрибируемой РНК для сборки, хотя неизвестно, способны ли эти сложные структуры эффективно сворачиваться или собираться в клеточных структурах. цитоплазма . В случае успеха это могло бы обеспечить направленную эволюцию наноструктур нуклеиновых кислот. [6] Ученые из Оксфордского университета сообщили о самосборке четырех коротких нитей синтетической ДНК в клетку, которая может проникать в клетки и сохраняться в течение как минимум 48 часов. Было обнаружено, что флуоресцентно-меченные тетраэдры ДНК остаются интактными в лабораторных культивируемых клетках почек человека , несмотря на атаку клеточных ферментов через два дня. Этот эксперимент показал возможность доставки лекарств внутрь живых клеток с использованием «клетки» ДНК. [76] [77] ДНК- тетраэдр использовался для доставки РНК-интерференции (РНКи) на мышиной модели, сообщила группа исследователей из Массачусетского технологического института . Доставка интерферирующей РНК для лечения показала некоторый успех с использованием полимера или липида , но существуют ограничения безопасности и неточное нацеливание, а также короткий срок хранения в кровотоке. Наноструктура ДНК, созданная командой, состоит из шести нитей ДНК, образующих тетраэдр, к каждому из шести ребер которого прикреплена одна нить РНК. Тетраэдр дополнительно оснащен нацеливающим белком, тремя молекулами фолата , которые приводят наночастицы ДНК к обильным рецепторам фолата, обнаруженным в некоторых опухолях. Результат показал, что экспрессия гена, на который воздействует РНКи, люцифераза , снизилась более чем вдвое. Это исследование демонстрирует перспективность использования нанотехнологии ДНК в качестве эффективного инструмента для лечения с использованием новой технологии РНК-интерференции. [78] [79] Тетраэдр ДНК также использовался в попытке преодолеть явления множественной лекарственной устойчивости . Доксорубицин(DOX) конъюгировали с тетраэдром и загружали в клетки рака молочной железы MCF-7, которые содержали насос для оттока лекарственного средства P-гликопротеина . Результаты эксперимента показали, что DOX не откачивался и был достигнут апоптоз раковых клеток. Тетраэдр без DOX был загружен в клетки для проверки его биосовместимости, и сама структура не проявила цитотоксичности. [80] Тетраэдр ДНК также использовался в качестве штрих-кода для профилирования субклеточной экспрессии и распределения белков в клетках в диагностических целях. Тетраэдрическая наноструктура продемонстрировала усиленный сигнал благодаря более высокой эффективности и стабильности мечения. [81]
Применение нанотехнологий ДНК в наномедицине также направлено на имитацию структуры и функций природных мембранных белков с помощью разработанных наноструктур ДНК. В 2012 году Лангекер и др. [82] представили структуру ДНК-оригами в форме пор, которая может самостоятельно внедряться в липидные мембраны посредством гидрофобных модификаций холестерина и индуцировать ионные токи через мембрану. За этой первой демонстрацией синтетического ионного канала ДНК последовало множество конструкций, индуцирующих поры, от одиночного дуплекса ДНК [83] до небольших структур на основе плиток [84] [85] [86] [87] [88 ] ] и большие трансмембранные порины ДНК-оригами . [89] Подобно естественным белковым ионным каналам , этот ансамбль синтетических аналогов, созданных из ДНК, таким образом, охватывает несколько порядков величины проводимости. Исследование одиночного дуплекса ДНК , встраивающего в мембрану , показало, что ток также должен течь по границе раздела ДНК-липид, поскольку в конструкции отсутствует просвет центрального канала, который позволяет ионам проходить через липидный бислой . Это указывало на то, что липидная пора, индуцированная ДНК, имеет тороидальную форму, а не цилиндрическую, поскольку головные группы липидов переориентируются в сторону встроенной в мембрану части ДНК. [83] Исследователи из Кембриджского университета и Университета Иллинойса в Урбана-Шампейн затем продемонстрировали, что такая ДНК-индуцированная тороидальная пора может способствовать быстрому переворачиванию липидов между листками липидного бислоя. Используя этот эффект, они разработали синтетический фермент, построенный на ДНК , который переворачивает липиды в биологических мембранах на несколько порядков быстрее, чем встречающиеся в природе белки, называемые скрамблазами . [90] Эта разработка подчеркивает потенциал синтетических наноструктур ДНК для персонализированных лекарств и терапии.
Наноструктуры ДНК должны быть рационально спроектированы так, чтобы отдельные цепи нуклеиновых кислот могли собираться в нужные структуры. Этот процесс обычно начинается с определения желаемой целевой структуры или функции. Затем определяется общая вторичная структура целевого комплекса с указанием расположения цепей нуклеиновой кислоты внутри структуры и того, какие части этих цепей должны быть связаны друг с другом. Последним шагом является проектирование первичной структуры , которое представляет собой спецификацию реальных последовательностей оснований каждой цепи нуклеиновой кислоты. [36] [91]
Первым шагом в разработке наноструктуры нуклеиновой кислоты является решение о том, как данная структура должна быть представлена определенным расположением нитей нуклеиновой кислоты. На этом этапе проектирования определяется вторичная структура или положение пар оснований, которые удерживают отдельные нити вместе в желаемой форме. [36] Было продемонстрировано несколько подходов:
После того, как любой из вышеперечисленных подходов будет использован для создания вторичной структуры целевого комплекса, необходимо разработать реальную последовательность нуклеотидов, которая сформируется в желаемую структуру. Дизайн нуклеиновой кислоты — это процесс присвоения конкретной последовательности оснований нуклеиновой кислоты каждой из составляющих цепей структуры так, чтобы они ассоциировались в желаемой конформации. Целью большинства методов является разработка последовательностей так, чтобы целевая структура имела наименьшую энергию и, следовательно, была наиболее термодинамически выгодной, в то время как неправильно собранные структуры имели более высокие энергии и, следовательно, были нежелательны. Это делается либо с помощью простых и быстрых эвристических методов, таких как минимизация симметрии последовательности, либо с использованием полной термодинамической модели ближайших соседей , которая более точна, но медленнее и требует больше вычислительных затрат. Геометрические модели используются для изучения третичной структуры наноструктур и обеспечения того, чтобы комплексы не были чрезмерно напряжены . [91] [93]
Дизайн нуклеиновых кислот преследует те же цели, что и дизайн белков . В обоих случаях последовательность мономеров разработана так, чтобы отдавать предпочтение желаемой целевой структуре и препятствовать другим структурам. Преимущество дизайна нуклеиновых кислот заключается в том, что он намного проще в вычислительном отношении, чем дизайн белка, поскольку простых правил спаривания оснований достаточно для прогнозирования энергетической выгодности структуры, и не требуется подробная информация об общем трехмерном сворачивании структуры. Это позволяет использовать простые эвристические методы, которые позволяют получить экспериментально надежные конструкции. Структуры нуклеиновых кислот менее универсальны, чем белки, в своих функциях из-за повышенной способности белков сворачиваться в сложные структуры и ограниченного химического разнообразия четырех нуклеотидов по сравнению с двадцатью протеиногенными аминокислотами . [93]
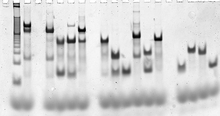
Последовательности нитей ДНК, составляющих целевую структуру, разрабатываются вычислительно с использованием программного обеспечения для молекулярного и термодинамического моделирования . [91] [93] Сами нуклеиновые кислоты затем синтезируются с использованием стандартных методов синтеза олигонуклеотидов , обычно автоматизированных в синтезаторе олигонуклеотидов , и цепи заказных последовательностей коммерчески доступны. [94] При необходимости нити можно очистить с помощью денатурирующего гель-электрофореза , [95] и определения точных концентраций с помощью любого из нескольких методов количественного определения нуклеиновых кислот с использованием спектроскопии ультрафиолетового поглощения . [96]
Полностью сформировавшиеся целевые структуры можно проверить с помощью нативного гель-электрофореза, который дает информацию о размере и форме комплексов нуклеиновых кислот. Анализ электрофоретического изменения подвижности позволяет оценить, включает ли структура все желаемые цепи. [97] Флуоресцентное мечение и резонансный перенос энергии Фёрстера (FRET) иногда используются для характеристики структуры комплексов. [98]
Структуры нуклеиновых кислот можно непосредственно визуализировать с помощью атомно-силовой микроскопии , которая хорошо подходит для расширенных двумерных структур, но менее полезна для дискретных трехмерных структур из-за взаимодействия кончика микроскопа с хрупкой структурой нуклеиновой кислоты; В этом случае часто используют просвечивающую электронную микроскопию и криоэлектронную микроскопию . Расширенные трехмерные решетки анализируются методом рентгеновской кристаллографии . [99] [100]
Общий:
Конкретные подполя: