Вирус герпеса человека 6 ( HHV-6 ) — общее собирательное название бетагерпесвируса человека 6A (HHV-6A) и бетагерпесвируса человека 6B (HHV-6B). Эти близкородственные вирусы являются двумя из девяти известных герпесвирусов , основным хозяином которых является человек. [1]
HHV-6A и HHV-6B представляют собой вирусы с двухцепочечной ДНК, относящиеся к подсемейству Betaherpesvirinae и роду Roseolovirus . ВГЧ-6А и ВГЧ-6В инфицируют почти все протестированные человеческие популяции. [2]
ВГЧ-6А был описан как более нейровирулентный [3] и поэтому чаще обнаруживается у пациентов с нейровоспалительными заболеваниями, такими как рассеянный склероз . [4] Уровни HHV-6 (и HHV-7) в мозге также повышены у людей с болезнью Альцгеймера . [5]
Первичная инфекция HHV-6B является причиной распространенного детского заболевания exanthema subitum (также известного как детская розеола или шестая болезнь). Оно передается от ребенка к ребенку. Взрослые редко заражаются этим заболеванием, поскольку большинство людей переболели им еще в детском саду, и после заражения возникает иммунитет, который предотвращает повторное заражение в будущем. Кроме того, у реципиентов трансплантатов часто встречается реактивация HHV-6B, которая может вызывать ряд клинических проявлений, таких как энцефалит , подавление функции костного мозга и пневмонит . [6]
Для обнаружения ВГЧ-6 используются различные тесты, некоторые из которых не позволяют дифференцировать эти два вида. [7]
Оба вируса могут вызывать трансплацентарную инфекцию и передаваться новорожденному. [8]
Исследование 2016 года показало, что 43% женщин с необъяснимым бесплодием дали положительный результат на ВГЧ-6А по сравнению с 0% в фертильной контрольной группе. ВГЧ-6А был обнаружен в эпителиальных клетках эндометрия женщин с необъяснимым бесплодием, но не в их крови. В контексте бесплодия это открытие подчеркивает важность целевого тестирования на ВГЧ-6А внутриутробной среды, поскольку вирус не был обнаружен в кровотоке больных людей. Таким образом, эффективная диагностика требует тестов, которые способны различать активную и латентную инфекцию ВГЧ-6А, особенно в ткани эндометрия, что подчеркивает необходимость тканеспецифичных методов обнаружения вируса для оценки и лечения бесплодия, связанного с ВГЧ-6А. [9]
Исследование 2018 года показало, что у 37% женщин, испытывающих рецидивирующую неудачу имплантации после ЭКО/ЭТ, в биоптатах эндометрия был обнаружен ВГЧ-6А по сравнению с 0% в контрольных группах. [10]
Исследование 2019 года подтвердило наличие инфекции HHV-6A у 40% женщин с идиопатическим бесплодием. Выявление влияния инфекции HHV-6A на иммунный статус эндометрия открывает новые перспективы в лечении бесплодия. Для женщин с необъяснимым бесплодием, характеризующимся ВГЧ-6А, можно выбрать противовирусную терапию и негормональные подходы, чтобы увеличить вероятность наступления беременности. [11]
В таблице ниже представлен полный обзор различных диагностических тестов, используемых для выявления вируса герпеса человека 6 (ВГЧ-6), с подробным описанием их способности различать активную и латентную инфекцию. [12] Он также включает информацию об интерпретации результатов тестов, определяет поставщиков, предлагающих эти тесты, и указывает, какие методы подходят для обнаружения ВГЧ-6А в слизистой оболочке эндометрия — важный фактор для оценки потенциальных причин бесплодия у женщин. Таблица служит руководством для медицинских работников при выборе подходящих диагностических тестов на ВГЧ-6.

В 1986 году Сайед Заки Салахуддин, Дхарам Аблаши и Роберт Галло культивировали мононуклеарные клетки периферической крови пациентов со СПИДом и лимфопролиферативными заболеваниями . Были зарегистрированы короткоживущие, крупные, рефрактильные клетки, которые часто содержали внутриядерные и/или внутрицитоплазматические тельца включения. Электронная микроскопия выявила новый вирус, который они назвали B-лимфотропным вирусом человека (HBLV). [13] [14]
Вскоре после его открытия Аблаши и др. описал пять клеточных линий, которые могут быть инфицированы недавно обнаруженным HBLV. Они опубликовали, что HSB-2, особая линия Т-клеток, очень восприимчива к инфекции. Новаторское исследование Аблаши завершилось предложением изменить название вируса с HBLV на HHV-6 в соответствии с опубликованной предварительной классификацией вирусов герпеса. [15] [16]
Спустя годы HHV-6 разделили на подтипы. Ранние исследования (1992 г.) описали два очень похожих, но уникальных варианта: HHV-6A и HHV-6B. Это различие было оправдано уникальным расщеплением эндонуклеазами рестрикции, реакциями моноклональных антител [17] и характером роста. [18]
ВГЧ-6А включает несколько штаммов, полученных от взрослых, и спектр его заболеваний четко не определен, хотя некоторые считают, что он более нейровирулентен. [19] [20] ВГЧ-6B обычно выявляется у детей с детской розеолой , поскольку он является этиологическим агентом этого заболевания. Внутри этих двух вирусов гомология последовательностей составляет 95%. [21]
В 2012 году HHV-6A и HHV-6B были официально признаны отдельными видами. [1]
ВГЧ-6А и ВГЧ-6В были признаны Международным комитетом по таксономии вирусов (ICTV) как отдельные виды в 2012 году. Розеоловирусы человека включают ВГЧ-6А, ВГЧ-6В и ВГЧ-7. [1]
Герпесвирусы были выделены как род в 1971 году в первом отчете ICTV. Этот род состоял из 23 вирусов из 4 групп. [22] В 1976 году был выпущен второй отчет ICTV, в котором этот род был возведен на уровень семейства — Herpetoviridae . Из-за возможной путаницы с вирусами, полученными от рептилий, в третьем отчете (1979) название семейства было изменено на herpesviridae . В этом отчете семейство Herpesviridae было разделено на 3 подсемейства ( alphaherpesvirinae , betaherpesvirinae и gammaherpesvirinae ) и 5 безымянных родов; Членами семейства признан 21 вирус. [23]
В 2009 году был создан отряд Herpesvirales . Это было вызвано открытием того, что вирусы герпеса рыб и моллюсков лишь отдаленно связаны с вирусами герпеса птиц и млекопитающих. Отряд Herpesvirales включает три семейства: Herpesviridae , которое содержит давно известные герпевирусы млекопитающих, птиц и рептилий, а также два новых семейства — семейство Alloherpesviridae , включающее вирусы герпеса костистых рыб и лягушек, и семейство Malacoherpesviridae , содержащее вирусы моллюски. [24]
По состоянию на 2012 год этот отряд насчитывает 3 семейства, 4 подсемейства (1 неназначенное), 18 родов (4 неназначенных) и 97 видов. [1]
Диаметр вириона HHV-6 составляет около 2000 ангстрем. [14] Внешняя часть вириона состоит из липидной двухслойной мембраны, которая содержит вирусные гликопротеины и происходит из мембраны хозяина. Под этой мембранной оболочкой находится тегумент , окружающий икосаэдрический капсид , состоящий из 162 капсомеров. Защитный капсид HHV-6 содержит двухцепочечную линейную ДНК.
Во время созревания вирионов HHV-6 мембраны клеток человека используются для формирования вирусных липидных оболочек (что характерно для всех оболочечных вирусов). Во время этого процесса HHV-6 использует липидные рафты , которые представляют собой мембранные микродомены, обогащенные холестерином , сфинголипидами и гликозилфосфатидилинозитол -заякоренными белками. [25] Ранние исследователи подозревали, что вирионы HHV-6 созревают в ядре; некоторые даже неверно опубликовали это, поскольку обобщили и применили к HHV-6 то, что было известно о других вирусах. Однако исследования, опубликованные в 2009 году, показывают, что вирус HHV-6 использует для сборки везикулы, полученные из транс-сети Гольджи. [25]
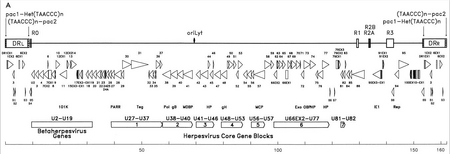
Генетический материал ВГЧ-6 состоит из линейной (круглой во время активной инфекции) двухцепочечной ДНК, которая содержит точку начала репликации , два левых и правых конца прямых повтора по 8–10 т.п.н. и уникальный сегмент размером 143–145 т.п.н. . [27]
Начало репликации (часто обозначаемое в литературе как «oriLyt») — это место, где начинается репликация ДНК. [26] Концы прямых повторов (DR L и DRR ) содержат повторяющуюся последовательность TTAGGG, идентичную последовательности теломер человека . Вариабельность числа теломерных повторов наблюдается в диапазоне 15–180. [28] [29] Эти концы также содержат сигналы расщепления и упаковки pac-1 и pac-2, которые консервативны среди герпесвирусов.
Уникальный сегмент содержит семь основных блоков ядерных генов (U27–U37, U38–U40, U41–U46, U48–U53, U56–U57, U66EX2–U77 и U81–U82) [26] , что также характерно для герпесвирусов. Эти консервативные гены кодируют белки, которые участвуют в репликации, расщеплении и упаковке вирусного генома в зрелый вирион. [28] Кроме того, они кодируют ряд иммуномодулирующих белков. Уникальный сегмент также содержит блок генов (U2–U19), консервативных среди вирусов HHV-6, HHV-7 и цитомегаловирусов (бетагерпесвирусов). Ряд уникальных генов сегментов связан, например, с семейством HCMV US22 ( InterPro : IPR003360 ). В таблице ниже приведены некоторые из их известных свойств. [26]
Когда внеклеточный вирион HHV-6 сталкивается с клетками человека, он сталкивается с кластером белков дифференцировки 46 человеческого рецептора ( CD46 ), который играет роль в регуляции системы комплемента. Белок CD46 обладает единственной вариабельной областью, образовавшейся в результате альтернативного сплайсинга . Таким образом, существует по меньшей мере четырнадцать изоформ CD46, каждая из которых связывается с HHV-6a. [33]
Внеклеточная область CD46 содержит четыре коротких консенсусных повтора примерно из 60 аминокислот, которые складываются в компактный домен бета-бочонка, окруженный гибкими петлями. [28] Как было продемонстрировано для CD46 с другими лигандами, структура белка CD46 линеаризуется при связывании HHV-6. Хотя их точное взаимодействие еще не установлено, было продемонстрировано, что второй и третий домены SCR необходимы для связывания рецептора HHV-6 и проникновения в клетку.
Мори и др. впервые идентифицировал продукт гена gQ1, гликопротеин, уникальный для HHV-6, и обнаружил, что он образует комплекс с гликопротеинами gH и gL. [17] [34] Они считали, что этот гетеротримерный комплекс служит вирусным лигандом для CD46. [27] Вскоре после этого был идентифицирован другой гликопротеин, названный gQ2, который оказался частью лигандного комплекса gH/gL/gQ1, образуя гетеротетрамер , который был положительно идентифицирован как вирусный лиганд CD46. [34] Точный процесс вступления еще не до конца понятен.
Слюнные железы были описаны как резервуар in vivo для инфекции HHV-6. [28]
Исследователи [35] провели исследование, которое показало, что Т-клетки высоко подвержены инфицированию ВГЧ-6.
В 2011 году исследователи из Национальных институтов здравоохранения попытались объяснить неизвестный тогда метод проникновения HHV-6a в нервную систему. Таким образом, они вскрыли мозг около 150 человек. Когда различные анатомические области были проанализированы на вирусную нагрузку, было обнаружено, что обонятельные ткани имеют самое высокое содержание HHV-6. Они пришли к выводу, что эти ткани являются точкой входа для HHV-6a. [21]
Приведенные выше результаты согласуются с результатами предыдущих исследований, в которых участвовал ВПГ-1 (и ряд других вирусов), который также распространяется в ЦНС через обонятельную ткань. [36]
Исследователи также предположили, что обонятельные обонятельные клетки (OEC), группа специализированных глиальных клеток, обнаруженных в полости носа, могут играть роль в инфекционности HHV-6. [21] Они подозревали эту связь в результате того, что OEC имели свойства, аналогичные свойствам астроцитов , другого типа глиальных клеток, которые ранее были идентифицированы как восприимчивые к инфекции HHV-6. [37] Исследования продолжались путем заражения ОЭК in vitro обоими типами ВГЧ-6. В конечном итоге только OEC, в которых использовался HHV-6a, дали положительный результат на признаки синтеза вируса de novo, что также характерно для астроцитов. [37]
Оказавшись внутри, были описаны два исхода: активное и неактивное заражение.
Активные инфекции включают в себя циркуляризацию линейного генома дцДНК посредством ковалентных связей от конца к концу. Впервые этот процесс был описан для вируса простого герпеса . [29] После циркуляризации HHV-6 начинает экспрессировать так называемые «непосредственно ранние» гены. Считается, что эти генные продукты являются активаторами транскрипции [7] и могут регулироваться экспрессией вирусных микроРНК . [31] Затем происходит последующая экспрессия «ранних генов», которая активирует, например, вирусные ДНК-полимеразы . Ранние гены также участвуют в последующей репликации по катящемуся кругу . [28]
Репликация HHV-6 приводит к образованию конкатемеров — длинных молекул, содержащих несколько повторов последовательности ДНК. [38] Эти длинные конкатемеры затем расщепляются между областями pac-1 и pac-2 для упаковки генома в отдельные вирионы. [29]
Не все вновь инфицированные клетки начинают репликацию по катящемуся кругу. Вирусы герпеса могут перейти в латентную стадию, неактивно заражая своего хозяина-человека. С момента открытия в 1993 году это явление было обнаружено среди всех бетагерпесвирусов . [39]
Другие бетагерпесвирусы устанавливают латентный период в виде ядерной эписомы , которая представляет собой кольцевую молекулу ДНК (аналог плазмиды ). Считается, что латентный период HHV-6 происходит исключительно за счет интеграции вирусных теломерных повторов в субтеломерные области человека. [20] Известно , что только один другой вирус, вирус болезни Марека , достигает латентного состояния таким образом. [7] Это явление возможно из-за теломерных повторов, обнаруженных на концах прямых повторов генома HHV-6.
Правый конец прямого повтора интегрируется в пределах от 5 до 41 теломерного повтора человека и преимущественно в проксимальном конце [40] хромосом 9, 17, 18, 19 и 22, но также иногда обнаруживается в хромосомах 10 и 11. [38] Предполагается, что около 70 миллионов человек являются носителями хромосомно-интегрированного вируса HHV-6. [20] [38]
Ряд генов, экспрессируемых HHV-6, уникальны для его неактивной латентной стадии. Эти гены участвуют в поддержании генома и предотвращении разрушения клетки-хозяина. [40] Например, считается, что белок U94 подавляет гены, которые участвуют в клеточном лизисе (апоптозе), а также может способствовать интеграции теломер. [28] После накопления в теломерах человека вирус периодически активируется. [40]
Конкретные триггеры реактивации недостаточно изучены. Некоторые исследователи предполагают, что причиной могут быть травмы, физический или эмоциональный стресс и гормональный дисбаланс. [41]
Исследователи в 2011 году обнаружили, что реактивация может быть положительно вызвана in vitro ингибиторами деацетилазы гистонов . Как только начинается реактивация, инициируется процесс катящегося круга и образуются конкатемеры, как описано выше. [28]
Вирус герпеса человека 6 живет в основном на людях и, хотя варианты вируса могут вызывать легкие или смертельные заболевания, они могут жить комменсально на своем хозяине. [18] Было продемонстрировано, что ВГЧ-6 способствует прогрессированию ВИЧ-1 при коинфекции Т-клеток. [42] ВГЧ-6 усиливает экспрессию первичного рецептора ВИЧ CD4, тем самым расширяя диапазон ВИЧ-чувствительных клеток. Несколько исследований также показали, что инфекция HHV-6 увеличивает выработку воспалительных цитокинов, которые усиливают экспрессию ВИЧ-1 in vitro, таких как TNF-альфа, [43] IL-1 бета и IL-8. [44] Более недавнее исследование in vivo показывает, что коинфекция HHV-6A резко ускоряет прогрессирование от ВИЧ к СПИДу у макак с косичками. [45]
Также было продемонстрировано, что HHV-6 трансактивирует вирус Эпштейна-Барр. [36]
Люди заражаются вирусом в раннем возрасте, некоторые уже в возрасте менее одного месяца. Первичные инфекции HHV-6 составляют до 20% обращений детей в отделение неотложной помощи по поводу лихорадки в США [46] [47] и связаны с несколькими более тяжелыми осложнениями, такими как энцефалит , лимфаденопатия , миокардит и миелосупрессия . Распространенность вируса в организме увеличивается с возрастом (уровень заражения наиболее высок среди младенцев в возрасте от 6 до 12 месяцев), и предполагается, что это связано с потерей у ребенка материнских антител, которые защищают его или ее от инфекций. . [18]
Существуют противоречия в корреляциях между возрастом и серопозитивностью: по некоторым данным, наблюдается снижение серопозитивности с увеличением возраста, в то время как некоторые указывают на отсутствие значительного снижения, а другие сообщают о повышении уровня серопозитивности у лиц в возрасте 62 лет и старше. После первичного заражения в слюнных железах, гемопоэтических стволовых клетках и других клетках устанавливается латентный период , который существует на протяжении всей жизни хозяина.
Известно, что вирус широко распространен по всему миру. В таких странах, как США, Великобритания, Япония и Тайвань, уровень инфицирования ВГЧ-6 составляет 64–83% к возрасту 13 месяцев. [18] [48] Исследования показали, что серологическая распространенность варьируется «примерно от 39 до 80% среди этнически разнообразного взрослого населения из Танзании, Малайзии, Таиланда и Бразилии». [18] Между этническими группами, живущими в одном и том же географическом месте, или между полами нет существенных различий. В то время как ВГЧ-6В присутствует почти во всех популяциях мира, ВГЧ-6А встречается реже в Японии, Северной Америке и Европе. [18]
Считается, что передача чаще всего происходит через попадание вирусных частиц в слюну. И HHV-6B, и HHV-7 обнаруживаются в слюне человека, причем первый встречается реже. Исследования сообщают о различных показателях распространенности ВГЧ-6 в слюне (от 3 до 90%) [18] , а также описывают слюнные железы как резервуар in vivo для ВГЧ-6. Вирус поражает слюнные железы, устанавливает латентный период и периодически реактивируется, распространяя инфекцию на других хозяев. [28]
Также была описана вертикальная передача , которая встречается примерно у 1% новорожденных в Соединенных Штатах. [7] [49] Эту форму легко идентифицировать, поскольку вирусный геном содержится в каждой клетке инфицированного человека.
Диагностика инфекции ВГЧ-6 проводится как серологическими, так и прямыми методами. Наиболее известным методом является количественное определение вирусной ДНК в крови, других жидкостях организма и органах с помощью ПЦР в реальном времени . [50]
Классическим проявлением первичной инфекции HHV-6b является субитум экзантема (ES) или «розеола», характеризующаяся высокой температурой и последующей сыпью. Однако одно исследование (1997) показало, что сыпь не является отличительным признаком инфекции ВГЧ-6, а ее частота аналогична таковой при инфекциях, не связанных с ВГЧ-6 (10–20% детей с лихорадкой в обеих группах). Инфекции ВГЧ-6 чаще проявляются высокими температурами (более 40°C), примерно у двух третей по сравнению с менее чем половиной у пациентов, не инфицированных ВГЧ-6. Столь же существенные различия наблюдались в отношении недомогания, раздражительности и воспаления барабанной перепонки. [18]
Первичная инфекция у взрослых, как правило, протекает более тяжело. [18]
Диагностика вируса, особенно HHV-6B, жизненно важна для пациента из-за побочных эффектов инфекции. Симптомы, указывающие на эту инфекцию, такие как сыпь, остаются незамеченными у пациентов, получающих антибиотики, поскольку их можно ошибочно истолковать как побочный эффект лекарства. [18] Известно, что вирус HHV-6B связан с детской болезнью розеола, а также с другими заболеваниями, вызванными этой инфекцией. К ним относятся гепатит, фебрильные судороги и энцефалит. У детей с субитальной экзантемой, вызванной инфекцией ВГЧ-6В, наблюдается лихорадка, продолжающаяся от 3 до 5 дней; сыпь на туловище, шее и лице; и иногда фебрильные судороги, однако симптомы не всегда присутствуют вместе. Первичные инфекции у взрослых встречаются редко, поскольку большинство случаев приходится на детей. Когда инфекция возникает впервые у взрослого, симптомы могут быть серьезными.
Вирус периодически вновь активируется из латентного состояния, при этом ДНК ВГЧ-6 обнаруживается у 20–25% здоровых взрослых в США. В условиях иммунокомпетентности эти повторные активации часто протекают бессимптомно, но у лиц с иммуносупрессией могут возникнуть серьезные осложнения. Реактивация HHV-6 вызывает тяжелое заболевание у реципиентов трансплантата и может привести к отторжению трансплантата, часто в сочетании с другими бетагерпесвирусами. Аналогично при ВИЧ/СПИДе реактивация HHV-6 вызывает диссеминированные инфекции, приводящие к заболеванию органов-мишеней и смерти. Хотя до 100% населения подвергаются (серопозитивному) воздействию ВГЧ-6, в большинстве случаев к 3-летнему возрасту, наблюдаются редкие случаи первичных инфекций у взрослых. В Соединенных Штатах они больше связаны с ВГЧ-6а, который считается более патогенным и более нейротропным и связан с некоторыми расстройствами, связанными с центральной нервной системой .
ВГЧ-6 был обнаружен у пациентов с рассеянным склерозом [51] и был вовлечен в качестве кофактора в ряд других заболеваний, включая синдром хронической усталости , [52] СПИД , [53] и височную эпилепсию . [54]
Рассеянный склероз (РС) — аутоиммунное воспалительное заболевание нервной системы, которое приводит к демиелинизации аксонов головного и спинного мозга. Первое исследование, специально посвященное демиелинизации, связанной с ВГЧ-6, появилось в литературе в 1996 году, когда у ранее здорового 19-месячного ребенка развилась острая энцефалопатия . Уровни основного белка миелина в спинномозговой жидкости были повышены , что позволяет предположить, что происходит демиелинизация. [55] Об этой связи почти забыли, пока четыре года спустя не было опубликовано исследование, связанное с рассеянным склерозом, которое показало распространенность ВГЧ-6 в 90% среди демиелинизированных тканей головного мозга. Для сравнения: всего лишь 13% здоровых тканей головного мозга содержали вирус. [56]
Примерно в это же время впервые появилась гипотеза молекулярной мимикрии, согласно которой Т-клетки по сути путают вирусный белок HHV-6 с основным белком миелина. На раннем этапе разработки этой гипотезы (2002 г.) итальянские исследователи использовали вариант HHV-6a вместе с основным белком бычьего миелина для создания линий перекрестно-реактивных Т-клеток. Их сравнивали с Т-клетками людей с рассеянным склерозом, а также с клетками контрольной группы, и между ними не было обнаружено существенных различий. Их ранние исследования показали, что молекулярная мимикрия не может быть механизмом, участвующим в рассеянном склерозе. [57]
За этим последовало еще несколько подобных исследований. Исследование, проведенное в октябре 2014 года, подтвердило роль длительной инфекции ВГЧ-6 с демиелинизацией в прогрессирующих неврологических заболеваниях. [58]
Синдром хронической усталости (СХУ) — изнурительное заболевание [59] , причина которого неизвестна. Пациенты с СХУ имеют аномальные неврологические, иммунологические и метаболические показатели.
У многих, но не у всех пациентов, соответствующих критериям СХУ, заболевание начинается с острого инфекционноподобного синдрома. Случаи СХУ могут быть следствием хорошо документированных инфекций, вызванных несколькими инфекционными агентами. [60] В исследовании 259 пациентов с «СХУ-подобным» заболеванием, опубликованном вскоре после открытия ВГЧ-6, использовались первичные культуры лимфоцитов для выявления людей с активной репликацией ВГЧ-6. Такая активная репликация была обнаружена у 70% пациентов по сравнению с 20% контрольной группы ( ). [61] Вопрос, поднятый, но не получивший ответа в этом исследовании, заключался в том, вызвала ли болезнь тонкий иммунодефицит, который привел к реактивации ВГЧ-6, или же реактивация ВГЧ-6 привела к появлению симптомов заболевания.
Последующие исследования, в которых использовались только серологические методы, которые не отличают активную инфекцию от латентной, дали неоднозначные результаты: большинство, но не все, обнаружили связь между СХУ и инфекцией ВГЧ-6. [60] [62] [63]
В других исследованиях использовались анализы, которые могут выявить активную инфекцию: первичная культура клеток, ПЦР сыворотки или плазмы или анализ антител к раннему антигену IgM. Большинство этих исследований показали связь между СХУ и активной инфекцией ВГЧ-6, [62] [64] [65] [66] [67] [68], хотя некоторые этого не сделали. [63] [69]
Таким образом, активная инфекция ВГЧ-6 присутствует у значительной части пациентов с СХУ. Более того, известно, что ВГЧ-6 инфицирует клетки нервной системы и иммунной системы, а также систем органов с очевидными нарушениями при СХУ. Несмотря на эту связь, остается недоказанным, что реактивированная инфекция ВГЧ-6 является причиной СХУ.
Тиреоидит Хашимото является наиболее распространенным заболеванием щитовидной железы и характеризуется обильной лимфоцитарной инфильтрацией и поражением щитовидной железы. Недавние исследования предполагают потенциальную роль ВГЧ-6 (возможно, варианта А) в развитии или возникновении тиреоидита Хашимото. [70]
Изучена роль ВГЧ-6 во время беременности, приводящая к воспалению в амниотической полости . [71]
ДНК ВГЧ-6А была обнаружена в эндометрии почти у половины группы бесплодных женщин, но ни у одной из фертильных контрольных групп. Естественные клетки-киллеры , специфичные для HHV-6A, и высокие уровни некоторых цитокинов в матке также были обнаружены в эндометрии бесплодных женщин, положительных на HHV-6A. Авторы предполагают, что HHV-6A может оказаться важным фактором женского бесплодия . [72]
Идентифицировано множество онкогенных вирусов человека. Например, HHV-8 связан с саркомой Капоши , [73] вирус Эпштейна -Барра с лимфомой Беркитта , а ВПЧ с раком шейки матки . Фактически, по оценкам Всемирной организации здравоохранения (2002 г.), 17,8% случаев рака у человека были вызваны инфекцией. [74] Типичные методы, с помощью которых вирусы инициируют онкогенез, включают подавление иммунной системы хозяина, вызывание воспаления или изменение генов.
ВГЧ-6 обнаруживается при лимфомах , лейкозах , раке шейки матки и опухолях головного мозга . [19] Было продемонстрировано, что различные клеточные линии медуллобластомы , а также клетки других опухолей головного мозга экспрессируют рецептор CD46. Вирусная ДНК также была обнаружена во многих других непатологических тканях мозга, но ее уровни ниже. [19]
Белок P53 человека действует как супрессор опухоли. Лица, которые не производят этот белок должным образом, чаще заболевают раком — явление, известное как синдром Ли-Фраумени . Один из продуктов гена HHV-6, белок U14, связывает P53 и включает его в вирионы . Другой генный продукт, белок ORF-1, также может связывать и инактивировать P53. Было даже показано, что клетки, экспрессирующие ген ORF-1, производят фибросаркомы при инъекции мышам. [19]
Было показано, что другой продукт HHV-6, ранний белок U95, связывает ядерный фактор каппа B. Дерегуляция этого фактора связана с раком. [19]
Трижды сообщалось о воспалении глаз, индуцированном HHV-6. Все три случая были зарегистрированы у пожилых людей: два в 2007 году и один в 2011 году. Первые два были зарегистрированы в Японии и Франции, а последний – в Японии. [75] [76] [77]
Считалось, что это произошло в результате реактивации, поскольку уровни антител IgM против HHV-6 были низкими. [77]
Эпилепсия медиальной височной доли связана с инфекцией HHV-6. В этой области мозга существуют три структуры: миндалевидное тело , гиппокамп и парагиппокампальная извилина . Мезиальная височная эпилепсия (MTLE) является наиболее распространенной формой хронической эпилепсии, и ее основной механизм до конца не изучен. [78]
Исследователи постоянно сообщают об обнаружении ДНК ВГЧ-6 в тканях, взятых у пациентов с MTLE. Исследования продемонстрировали склонность HHV-6 к агрегации в височной доле [79] с самыми высокими концентрациями в астроцитах гиппокампа. [78]
Однако одна группа исследователей в конечном итоге пришла к выводу, что HHV-6 может не участвовать в MTLE, связанном с мезиальным височным склерозом. [80]
Вирус является частой причиной дисфункции печени и острой печеночной недостаточности у реципиентов трансплантата печени, а недавно его связали с перипортальным сливным некрозом. Более того, ДНК ВГЧ-6 часто обнаруживается только в тканях биопсии, поскольку в стойких случаях уровень ДНК падает ниже уровня обнаружения в крови. [81]
Не существует фармацевтических препаратов, одобренных специально для лечения инфекции ВГЧ-6, хотя использование лечения цитомегаловирусом ( валганцикловир , ганцикловир , [82] цидофовир и фоскарнет ) показало некоторый успех. [7] Эти препараты назначаются с целью ингибирования правильной полимеризации ДНК путем конкуренции с дезокситрифосфатными нуклеотидами [82] или специфической инактивации вирусных ДНК-полимераз. [2]
Найти лечение может быть сложно, если реактивация HHV-6 происходит после операции по трансплантации, поскольку препараты для трансплантации включают иммунодепрессанты. [83]
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ){{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка )