Кремнийорганическая химия — это изучение металлоорганических соединений, содержащих связи углерод - кремний , поэтому их называют кремнийорганическими соединениями . Большинство кремнийорганических соединений похожи на обычные органические соединения, будучи бесцветными, горючими, гидрофобными и устойчивыми на воздухе. Карбид кремния — неорганическое соединение.
В 1863 году Чарльз Фридель и Джеймс Крафтс создали первое органохлорсилановое соединение. [1] В том же году они также описали «эфир поликремниевой кислоты» при получении этил- и метил-о-кремниевой кислоты. [1] Обширные исследования в области кремнийорганических соединений были начаты в начале 20-го века Фредериком С. Киппингом . [2] Он также ввел термин «силикон» (напоминающий кетоны , хотя это ошибочно) [3] [4] : 286 по отношению к этим материалам в 1904 году. В знак признания достижений Киппинга компания Dow Chemical Company учредила в 1960-х годах премию, которая присуждается за значительный вклад в химию кремния. [5] В своих работах Киппинг отметился применением реактивов Гриньяра для получения алкилсиланов и арилсиланов , а также получением впервые силиконовых олигомеров и полимеров. [2]
В 1945 году Эжен Г. Рохов также внес значительный вклад в химию кремнийорганических соединений, впервые описав процесс Мюллера-Рохова . [6]

Кремнийорганические соединения широко распространены в коммерческих продуктах. Наиболее распространенными являются пеногасители, герметики (герметики), клеи и покрытия из силиконов . Другие важные применения включают сельскохозяйственные и растительные адъюванты, обычно используемые в сочетании с гербицидами и фунгицидами . [7]
Связи углерод-кремний отсутствуют в биологии , однако ферменты были использованы для искусственного создания связей углерод-кремний в живых микробах. [8] [9] [10] Силикаты , с другой стороны, известны своим существованием в диатомовых водорослях . [11] Силафлуофен — это кремнийорганическое соединение, которое действует как пиретроидный инсектицид . Несколько кремнийорганических соединений были исследованы в качестве фармацевтических препаратов. [12] [13]
В подавляющем большинстве кремнийорганических соединений Si является четырехвалентным с тетраэдрической молекулярной геометрией . По сравнению со связями углерод-углерод, связи углерод-кремний длиннее и слабее. [7] [15]
Связь C–Si несколько поляризована в сторону углерода из-за большей электроотрицательности углерода (C 2,55 против Si 1,90), а одинарные связи от Si до электроотрицательных элементов очень прочны. [14] Таким образом, кремний восприимчив к нуклеофильной атаке O − , Cl − , или F − ; энергия связи Si–O в частности поразительно высока. Эта особенность используется во многих реакциях, таких как реакция Сакураи , перегруппировка Брука , окисление Флеминга-Тамао и олефинирование Петерсона . [16]
Связь Si–C (1,89 Å) значительно длиннее типичной связи C–C (1,54 Å), что говорит о том, что силильные заместители имеют меньшие стерические требования, чем их органильные аналоги. Когда геометрия позволяет, кремний проявляет отрицательное гиперконъюгирование , обращая обычную поляризацию на соседних атомах. [ необходима цитата ]
Первое кремнийорганическое соединение, тетраэтилсилан, было получено Чарльзом Фриделем и Джеймсом Крафтсом в 1863 году путем реакции тетрахлорсилана с диэтилцинком .
Основная часть кремнийорганических соединений происходит из кремнийорганических хлоридов (CH
3)
4-хSiCl
х. Эти хлориды производятся по " Прямому процессу ", который подразумевает реакцию метилхлорида с кремний-медным сплавом. Основным и наиболее востребованным продуктом является диметилдихлорсилан :
Получают множество других продуктов, включая триметилсилилхлорид и метилтрихлорсилан . Ежегодно этим путем получают около 1 миллиона тонн кремнийорганических соединений. Этот метод также может быть использован для фенилхлорсиланов. [17]
Другим основным методом образования связей Si-C является гидросилилирование (также называемое гидросилированием). [18] В этом процессе соединения со связями Si-H ( гидросиланы ) присоединяются к ненасыщенным субстратам. С коммерческой точки зрения основными субстратами являются алкены . Другие ненасыщенные функциональные группы — алкины , имины , кетоны и альдегиды — также участвуют, но эти реакции имеют небольшую экономическую ценность. [19]

Для гидросилилирования требуются металлические катализаторы, особенно на основе металлов платиновой группы .
В родственном силилметаллировании металл заменяет атом водорода.
Гексаметилдисилан реагирует с метиллитием, образуя триметилсилиллитий: [20]
Аналогично, трис(триметилсилил)силиллитий получается из тетракис(триметилсилил)силана : [21]
Кремний является компонентом многих функциональных групп. Большинство из них аналогичны органическим соединениям. Исключением является редкость множественных связей с кремнием, что отражено в правиле двойной связи .
Силанолы являются аналогами спиртов. Их обычно получают гидролизом силилхлоридов: [22]
Реже силанолы получают окислением силилгидридов, реакцией, в которой используется металлический катализатор:
Было выделено много силанолов, включая (CH
3)
3SiOH и (C
6ЧАС
5)
3SiOH . Они примерно в 500 раз более кислотны, чем соответствующие спирты. Силоксиды являются депротонированными производными силанолов: [22]
Силанолы имеют тенденцию к дегидратации с образованием силоксанов :
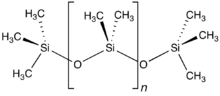
Полимеры с повторяющимися силоксановыми связями называются силиконами . Соединения с двойной связью Si=O, называемые силанонами, крайне нестабильны.
Силиловые эфиры имеют связь Si-OC. Обычно их получают реакцией спиртов с силилхлоридами:
Силиловые эфиры широко используются в качестве защитных групп для спиртов .
Используя прочность связи Si-F, источники фторида, такие как фторид тетра-н-бутиламмония (TBAF), применяются для снятия защиты с силиловых эфиров:
Органосилилхлориды являются важными товарными химикатами. Они в основном используются для производства силиконовых полимеров, как описано выше. Особенно важными силилхлоридами являются диметилдихлорсилан ( Me
2SiCl
2), метилтрихлорсилан ( MeSiCl
3) и триметилсилилхлорид ( Me
3SiCl ) производятся прямым способом . Более специализированные производные, которые находят коммерческое применение, включают дихлорметилфенилсилан, трихлор(хлорметил)силан, трихлор(дихлорфенил)силан, трихлорэтилсилан и фенилтрихлорсилан.
Хотя пропорционально небольшой выход, кремнийорганические соединения широко используются в органическом синтезе . В частности, триметилсилилхлорид Me
3SiCl является основным силилирующим агентом. Один классический метод, называемый реакцией Флуда, для синтеза этого класса соединений заключается в нагревании гексаалкилдисилоксанов R
3SiOSiR
3с концентрированной серной кислотой и галогенидом натрия . [23]

Связь кремния с водородом длиннее, чем связь C–H (148 по сравнению с 105 пм) и слабее (299 по сравнению с 338 кДж/моль). Водород более электроотрицателен , чем кремний, отсюда и название силилгидридов . Обычно наличие гидрида не упоминается в названии соединения. Триэтилсилан имеет формулу Et
3SiH . Фенилсилан — это PhSiH
3. Исходное соединение SiH
4называется силаном .
Кремнийорганические соединения, в отличие от своих углеродных аналогов, не имеют богатой химии двойных связей . [25] Соединения со связями силена Si=C (также известные как алкилиденсиланы ) являются лабораторными диковинками, такими как аналог кремниевого бензола силабензол . В 1967 году Гусельников и Флауэрс представили первые доказательства существования силенов в результате пиролиза диметилсилациклобутана . [26] Первый стабильный (кинетически экранированный) силен был описан в 1981 году Бруком. [27] [28]
Дисилены имеют двойные связи Si=Si, а дисилины являются кремниевыми аналогами алкина. Первый силин (с тройной связью кремния с углеродом) был описан в 2010 году. [29]

Силолы , также называемые силациклопентадиенами , являются членами более крупного класса соединений, называемых металлолами . Они являются кремниевыми аналогами циклопентадиенов и представляют в настоящее время академический интерес из-за их электролюминесценции и других электронных свойств. [30] [31] Силолы эффективны в электронном транспорте. Они обязаны своим низколежащим LUMO благоприятному взаимодействию между антисвязывающей сигма -орбиталью кремния с антисвязывающей пи-орбиталью фрагмента бутадиена .
В отличие от углерода, соединения кремния могут быть также координированы с пятью атомами в группе соединений, начиная от так называемых силатранов , таких как фенилсилатран , до уникально стабильного пентаорганосиликата: [32]
Стабильность гипервалентного кремния является основой реакции Хиямы , реакции связывания, используемой в некоторых специализированных органических синтетических приложениях. Реакция начинается с активации связи Si-C фторидом :
В общем, почти любая связь кремний-гетероатом чувствительна к воде и будет спонтанно гидролизоваться. [33] Ненапряженные связи кремний-углерод, однако, очень прочны и расщепляются только в небольшом количестве экстремальных условий. Сильные кислоты будут протодесилатировать арилсиланы и, в присутствии катализатора кислоты Льюиса, алкилсиланы. Большинство нуклеофилов слишком слабы, чтобы вытеснить углерод из кремния: исключениями являются фторид -ионы и алкоксиды , хотя последние часто депротонируют органосилан до кремниевого илида вместо этого. [34]
Как источник ковалентного гидрида , гидросиланы являются хорошими восстановителями .
Некоторые аллилсиланы могут быть получены из аллиловых эфиров , таких как 1 и моносилилмедных соединений, которые образуются in situ в результате реакции дисилилцинкового соединения 2 с иодидом меди в: [35] [36]
В этом типе реакции полярность кремния меняется на противоположную в химической связи с цинком и происходит формальное аллильное замещение в бензоилоксигруппе .
Ненасыщенные силаны, подобные вышеперечисленным, подвержены электрофильному замещению .
Кремнийорганические соединения влияют на иммунную систему пчел (и других насекомых), делая их более восприимчивыми к вирусной инфекции. [13] [37]
{{cite book}}: CS1 maint: другие ( ссылка ){{cite web}}: CS1 maint: неподходящий URL ( ссылка )