
Toxoplasma gondii ( / ˈ t ɒ k s ə ˌ p l æ z m ə ˈ ɡ ɒ n d i . aɪ , -iː / ) — паразитическое простейшее (в частности, апикомплексан ) , вызывающее токсоплазмоз . [3] Обнаруженный во всем мире T. gondii способен заражать практически всех теплокровных животных , [4] : 1 , но кошачьи являются единственными известными окончательными хозяевами , у которых паразит может подвергаться половому размножению. [5] [6]
У грызунов T. gondii изменяет поведение таким образом, что увеличивается вероятность того , что грызуны станут жертвами кошачьих. [7] [8] [9] Поддержка этой «гипотезы манипуляции» основана на исследованиях, показывающих, что крысы, инфицированные T. gondii , имеют меньшее отвращение к кошачьей моче , в то время как инфекция у мышей снижает общую тревожность , усиливает исследовательское поведение и увеличивает потерю отвращение к хищникам в целом. [7] [10] Поскольку кошки являются одними из немногих хозяев, внутри которых T. gondii может размножаться половым путем, такие поведенческие манипуляции считаются эволюционными адаптациями , которые увеличивают репродуктивный успех паразита, поскольку грызуны, которые не избегают кошачьих жилищ, с большей вероятностью станут кошачья добыча. [7] Основные механизмы вызванных T. gondii поведенческих изменений у грызунов происходят посредством эпигенетического ремоделирования нейронов, которые управляют соответствующим поведением (например, гипометилирование генов , связанных с аргинин-вазопрессином , в медиальной миндалевидном теле , что значительно снижает отвращение к хищникам). [11] [12]
У людей, особенно у младенцев и людей с ослабленным иммунитетом , инфекция T. gondii обычно протекает бессимптомно, но может привести к серьезному случаю токсоплазмоза . [13] [4] T. gondii может первоначально вызывать легкие гриппоподобные симптомы в первые несколько недель после заражения, но в остальном у здоровых взрослых людей симптомы не наблюдаются. [14] [13] [4] Это бессимптомное состояние инфекции называется латентной инфекцией , и оно связано с многочисленными тонкими поведенческими, психиатрическими и личностными изменениями у людей. [14] [15] [16] Поведенческие изменения, наблюдаемые между инфицированными и неинфицированными людьми, включают снижение отвращения к кошачьей моче (но с разными траекториями в зависимости от пола) и повышенный риск некоторых психических расстройств , особенно шизофрении и биполярного расстройства . [17] Предварительные данные свидетельствуют о том, что инфекция T. gondii может вызывать некоторые из тех же изменений в мозге человека , что и у грызунов. [18] [19] [9] [20] [21] [22] Многие из этих ассоциаций активно обсуждаются, а новые исследования показали их слабость и пришли к выводу: [23]
В целом было мало доказательств того, что T. gondii связан с повышенным риском психических расстройств, плохим контролем импульсов, личностными аберрациями или нейрокогнитивными нарушениями.
T. gondii — один из наиболее распространенных паразитов в развитых странах; [24] [25] по оценкам серологических исследований, до 50% мирового населения подвергалось воздействию и может быть хронически инфицировано T. gondii ; хотя уровень заражения значительно различается от страны к стране. [14] [26] По оценкам, по состоянию на 2018 год самая высокая распространенность серотипа IgG наблюдалась в Эфиопии - 64,2%. [27]

T. gondii содержит органеллы, называемые роптриями и микронемами , а также другие органеллы.

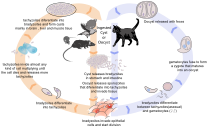
Жизненный цикл T. gondii можно в общих чертах разделить на два компонента: половой компонент, который встречается только у кошек (кошачьих, диких или домашних), и бесполый компонент, который может встречаться практически у всех теплокровных животных, включая человека и кошек. , и птицы. [28] : 2 Поскольку T. gondii может размножаться половым путем только внутри кошек, кошки, следовательно, являются окончательными хозяевами T. gondii . Все остальные хозяева, у которых может происходить только бесполое размножение, являются промежуточными хозяевами .
Когда кошка заражается T. gondii (например, в результате употребления в пищу инфицированной мыши, несущей тканевые кисты паразита), паразит выживает при прохождении через желудок , в конечном итоге заражая эпителиальные клетки тонкой кишки кошки. [28] : 39 Внутри этих кишечных клеток паразиты подвергаются половому развитию и размножению, образуя миллионы толстостенных цист, содержащих зиготы , известных как ооцисты. Кошки являются единственным окончательным хозяином, поскольку в их кишечнике отсутствует экспрессия фермента дельта-6-десатуразы (D6D). Этот фермент преобразует линолевую кислоту ; отсутствие экспрессии способствует системному накоплению линолевой кислоты. Недавние данные показали, что этот избыток линолевой кислоты необходим для полового размножения T. gondii . [6]

Инфицированные эпителиальные клетки в конечном итоге разрываются и высвобождают ооцисты в просвет кишечника , после чего они выделяются с фекалиями кошки. [4] : 22 Ооцисты могут затем распространиться на почву, воду, пищу или что-либо еще, потенциально загрязненное фекалиями. Обладая высокой устойчивостью, ооцисты могут выживать и оставаться инфекционными в течение многих месяцев в холодном и сухом климате. [29]
Проглатывание ооцист человеком или другими теплокровными животными является одним из распространенных путей заражения. [30] Люди могут подвергнуться воздействию ооцист, например, потребляя немытые овощи или загрязненную воду, или контактируя с фекалиями (подстилкой) инфицированной кошки. [28] : 2 [31] Хотя кошки также могут заразиться при проглатывании ооцист, они гораздо менее чувствительны к заражению ооцистами, чем промежуточные хозяева. [32] [4] : 107
Обнаруженные промежуточные хозяева включают свиней, кур, коз, овец [28] :2 и Macropus rufus по Moré et al. 2010. [33] : 162 Крупный рогатый скот и лошади устойчивы и считаются неспособными к серьезному заражению. [28] : 11 Считается, что T. gondii имеет три стадии заражения; тахизоитная стадия быстрого деления, брадизоитная стадия медленного деления внутри тканевых кист и стадия окружающей среды ооцисты. [34] Тахизоиты также известны как «тахизоиты» и брадизоиты как «брадизоиты». [35] Когда ооциста или тканевая киста проглатывается человеком или другим теплокровным животным, упругая стенка кисты растворяется протеолитическими ферментами в желудке и тонкой кишке, высвобождая спорозоиты из ооцисты. [30] [34] Паразиты сначала проникают в клетки эпителия кишечника и вокруг него, а внутри этих клеток паразиты дифференцируются в тахизоиты, подвижную и быстро размножающуюся клеточную стадию T. gondii . [28] : 39 Тканевые кисты в тканях, таких как мозговая и мышечная ткань, образуются примерно через 7–10 дней после первоначального заражения. [34] Хотя наблюдалась тяжелая инфекция M. rufus , неизвестно, является ли это обычным явлением. [33]
Внутри клеток-хозяев тахизоиты реплицируются внутри специализированных вакуолей (называемых паразитофорными вакуолями ), образующихся из мембраны клетки-хозяина во время инвазии в клетку. [28] : 23–39 Тахизоиты размножаются внутри этой вакуоли до тех пор, пока клетка-хозяин не погибнет и не разорвется, высвобождая и распространяя тахизоиты через кровоток во все органы и ткани тела, включая мозг . [28] : 39–40
Паразита можно легко выращивать в монослоях клеток млекопитающих, поддерживаемых in vitro в культуре тканей . Он легко проникает и размножается в самых разных клеточных линиях фибробластов и моноцитов . В инфицированных культурах паразит быстро размножается, тысячи тахизоитов вырываются из инфицированных клеток и проникают в соседние клетки, со временем разрушая монослой. Затем новые монослои можно заразить, используя каплю этой инфицированной культуральной жидкости, и паразит будет поддерживаться в течение неопределенного времени без необходимости использования животных.
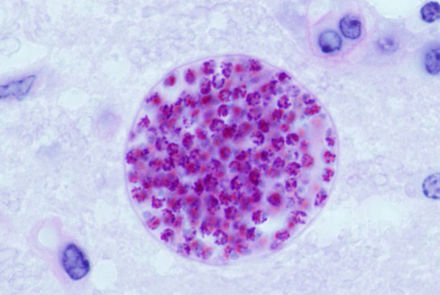
После начального периода инфекции, характеризующегося пролиферацией тахизоитов по всему организму, давление со стороны иммунной системы хозяина заставляет тахизоиты T. gondii превращаться в брадизоиты, полуспящую , медленно делящуюся клеточную стадию паразита. [36] Внутри клеток-хозяев скопления этих брадизоитов известны как тканевые кисты. Стенка кисты образована мембраной паразитофорной вакуоли. [28] : 343 Хотя тканевые кисты, содержащие брадизоиты, могут образовываться практически в любом органе, тканевые кисты преимущественно формируются и сохраняются в головном мозге, глазах и поперечно -полосатых мышцах (включая сердце). [28] : 343 Однако специфические тропизмы тканей могут различаться у разных видов промежуточных хозяев; у свиней большинство тканевых кист обнаруживается в мышечной ткани, тогда как у мышей большинство кист обнаруживается в головном мозге. [28] : 41
Размер кист обычно варьируется от пяти до 50 мкм в диаметре [37] (при этом 50 мкм составляют примерно две трети ширины среднего человеческого волоса). [38]
Поедание тканевых цист мяса является одним из основных способов заражения T. gondii как для людей, так и для мясоедов, теплокровных животных. [28] : 3 Люди потребляют тканевые кисты при употреблении в пищу сырого или недоваренного мяса (особенно свинины и баранины). [39] Поедание тканевых кист также является основным способом заражения кошек. [4] : 46
На выставке в Музее естественной истории Сан-Диего говорится, что городские стоки с кошачьими фекалиями переносят Toxoplasma gondii в океан, которая может убить каланов. [40]
Тканевые кисты могут сохраняться в тканях хозяина на протяжении всей жизни животного. [28] : 580 Однако постоянное присутствие кист, по-видимому, обусловлено периодическим процессом разрыва и повторного инцистирования кисты, а не постоянной продолжительностью жизни отдельных кист или брадизоитов. [28] : 580 В любой момент времени у хронически инфицированного хозяина происходит разрыв очень небольшого процента кист, [28] : 45 хотя точная причина разрыва этой тканевой кисты по состоянию на 2010 год еще не известна. [4] : 47
Теоретически T. gondii может передаваться между промежуточными хозяевами неопределенно долго посредством цикла потребления тканевых цист мяса. Однако жизненный цикл паразита начинается и завершается только тогда, когда паразит передается кошачьему хозяину, единственному хозяину, внутри которого паразит может снова подвергаться половому развитию и размножению. [30]
В 2006 году исследователи рассмотрели доказательства того, что T. gondii имеет необычную структуру популяции, в которой доминируют три клональные линии, называемые типами I, II и III, которые встречаются в Северной Америке и Европе, несмотря на наличие половой фазы в его жизненном цикле. Они подсчитали, что общий предок существовал около 10 000 лет назад. [41] Авторы последующего и более масштабного исследования 196 изолятов из различных источников, включая T. gondii у белоголового орлана, серого волка, песца и калана, также обнаружили, что штаммы T. gondii , заражающие дикую природу Северной Америки, имеют ограниченное генетическое разнообразие с появление лишь нескольких основных клональных типов. Они обнаружили, что 85% штаммов в Северной Америке принадлежали к одному из трех широко распространенных генотипов II, III и Типа 12. Таким образом, T. gondii сохранил способность к сексу в Северной Америке на протяжении многих поколений, производя в основном клональные популяции, а спаривания порождали небольшое генетическое разнообразие. [42]
В разные периоды своего жизненного цикла отдельные паразиты превращаются в различные клеточные стадии, причем каждая стадия характеризуется различной клеточной морфологией , биохимией и поведением. Эти стадии включают тахизоиты, мерозоиты, брадизоиты (обнаруживаются в тканевых цистах) и спорозоиты (обнаруживаются в ооцистах).
Некоторые стадии подвижны , а некоторые кальций-зависимые протеинкиназы (TgCDPK s) участвуют в подвижности этого паразита. [43] [44] Гаджи и др. 2015 находкаTgCDPK3 необходим для начала действия подвижности, поскольку он фосфорилирует миозин А T. gondii (ТгМИОА ). [43] [44] TgCDPK3 является функциональным ортологом CDPK1 у этого паразита. [44]

Подвижные и быстро размножающиеся тахизоиты ответственны за расширение популяции паразита в организме хозяина. [45] [28] : 19 Когда хозяин потребляет тканевую кисту (содержащую брадизоиты) или ооцисту (содержащую спорозоиты), брадизоиты или спорозоиты постепенно превращаются в тахизоиты при инфицировании кишечного эпителия хозяина. [28] : 359 В начальный острый период инфекции тахизоиты распространяются по организму через кровоток. [28] : 39–40 На более поздних, латентных (хронических) стадиях инфекции тахизоиты превращаются в брадизоиты с образованием тканевых кист.

Как и тахизоиты, мерозоиты быстро делятся и отвечают за увеличение популяции паразита в кишечнике кошки перед половым размножением. [28] : 19 Когда окончательный хозяин из семейства кошачьих потребляет тканевую кисту (содержащую брадизоиты), брадизоиты превращаются в мерозоиты внутри эпителиальных клеток кишечника. После непродолжительного периода быстрого роста популяции в кишечном эпителии мерозоиты превращаются в неинфекционные половые стадии паразита для полового размножения, что в конечном итоге приводит к образованию ооцист, содержащих зиготы. [28] : 306
Брадизоиты — это медленно делящаяся стадия паразита, образующая тканевые кисты. Когда неинфицированный хозяин поглощает тканевую кисту, брадизоиты, выделяющиеся из кисты, заражают эпителиальные клетки кишечника, прежде чем перейти в пролиферативную стадию тахизоитов. [28] : 359 После начального периода пролиферации по всему телу хозяина тахизоиты затем превращаются обратно в брадизоиты, которые размножаются внутри клеток-хозяев, образуя тканевые кисты у нового хозяина.
Спорозоиты — это стадия паразита, обитающего в ооцистах. Когда человек или другой теплокровный хозяин потребляет ооцисту, из нее высвобождаются спорозоиты, заражающие эпителиальные клетки перед переходом в пролиферативную стадию тахизоитов. [28] : 359
Первоначально инфекция T. gondii стимулирует выработку IL-2 и IFN-γ врожденной иммунной системой. [36] Непрерывное производство IFN-γ необходимо для контроля как острой, так и хронической инфекции T. gondii . [36] Эти два цитокина вызывают CD4+ и CD8+ Т-клеточный иммунный ответ. [36] Таким образом, Т-клетки играют центральную роль в иммунитете против токсоплазменной инфекции. Т-клетки распознают антигены токсоплазмы , которые им представлены молекулами собственного главного комплекса гистосовместимости (MHC). Специфическая генетическая последовательность конкретной молекулы MHC резко различается у разных людей, поэтому эти молекулы участвуют в отторжении трансплантата. Лица, несущие определенные генетические последовательности молекул MHC, гораздо чаще заражаются токсоплазмой . Одно исследование с участием более 1600 человек показало, что токсоплазменная инфекция особенно распространена среди людей, у которых экспрессируются определенные аллели MHC (HLA-B*08:01, HLA-C*04:01, HLA-DRB 03:01, HLA-DQA*05: 01 и HLA-DQB*02:01). [46]
IL-12 вырабатывается во время инфекции T. gondii для активации естественных клеток-киллеров (NK) . [36] Триптофан является незаменимой аминокислотой для T. gondii, которую он удаляет из клеток-хозяев. IFN-γ индуцирует активацию индоламин-2,3-диоксигеназы (IDO) и триптофан-2,3-диоксигеназы (TDO), двух ферментов, ответственных за расщепление триптофана. [47] Иммунное давление в конечном итоге приводит к тому, что паразит образует кисты, которые обычно откладываются в мышцах и мозге хозяев. [36]
Активация IDO и TDO, опосредованная IFN-γ, представляет собой эволюционный механизм, который заставляет паразита голодать, но может привести к истощению триптофана в мозгу хозяина. IDO и TDO расщепляют триптофан до N-формилкинуренин . Введение L-кинуренина способно индуцировать депрессивно-подобное поведение у мышей. [47] Было продемонстрировано, что инфекция T. gondii повышает уровень кинуреновой кислоты (KYNA) в мозге инфицированных мышей и в мозгу людей, страдающих шизофренией. [47] Низкий уровень триптофана и серотонина в мозге уже был связан с депрессией. [48]
Следующие факторы были идентифицированы как факторы риска заражения T. gondii у людей и теплокровных животных:
Распространенный аргумент в дебатах о том, является ли владение кошкой этичным, включает вопрос о передаче Toxoplasma gondii людям. [60] Несмотря на то, что «жизнь в доме с кошкой, которая пользовалась лотком, была сильно связана с инфекцией» [31] и что проживание с несколькими котятами или любой кошкой в возрасте до одного года имеет определенное значение, [50] несколько другие исследования утверждают, что показали, что проживание в доме с кошкой не является значимым фактором риска заражения T. gondii . [51] [61]
Конкретные векторы передачи также могут различаться в зависимости от географического положения. «Считается, что морская вода в Калифорнии загрязнена ооцистами T. gondii , которые происходят из кошачьих фекалий, выживают или обходят очистку сточных вод и перемещаются к побережью через речные системы. T. gondii была идентифицирована в калифорнийской мидии с помощью полимеразной цепной реакции. и секвенирование ДНК. В свете потенциального присутствия T. gondii беременные женщины и люди с ослабленным иммунитетом должны знать об этом потенциальном риске, связанном с употреблением в пищу сырых устриц, мидий и моллюсков». [50]
Было также показано , что у теплокровных животных, таких как коричневые крысы , овцы и собаки, T. gondii также передается половым путем. [62] [63] [64] Хотя T. gondii может заражать, передаваться и размножаться бесполым путем в организме человека и практически всех других теплокровных животных, паразит может размножаться половым путем только в кишечнике представителей семейства кошачьих ( кошачьи) . [30] Таким образом, кошачьи являются окончательными хозяевами T. gondii ; все остальные хозяева (например, человек или другие млекопитающие) являются промежуточными хозяевами .
Следующие меры предосторожности рекомендуются для предотвращения или значительного снижения вероятности заражения T. gondii . Эта информация была адаптирована с веб-сайтов Центров США по контролю и профилактике заболеваний [65] и клиники Мэйо . [66]
Основные правила техники безопасности при обращении с пищевыми продуктами могут предотвратить или снизить вероятность заражения T. gondii , например мытье немытых фруктов и овощей и отказ от сырого или недоваренного мяса, птицы и морепродуктов. Другие небезопасные практики, такие как употребление непастеризованного молока или неочищенной воды, могут увеличить вероятность заражения. [65] Поскольку T. gondii обычно передается при проглатывании микроскопических кист в тканях инфицированных животных, мясо, не подготовленное для их уничтожения, представляет риск заражения. Замораживание мяса в течение нескольких дней при минусовой температуре (0 ° F или -18 ° C) перед приготовлением может разрушить все цисты, поскольку они редко выдерживают такие температуры. [4] : 45 Во время приготовления целые куски красного мяса следует готовить при внутренней температуре не менее 145 °F (63 °C). Мясо средней прожарки обычно готовят при температуре от 130 до 140 °F (от 55 до 60 °C), [67] , поэтому рекомендуется готовить мясо как минимум до средней температуры . После приготовления перед употреблением следует дать возможность отдохнуть в течение 3 минут. Однако фарш следует готовить при внутренней температуре не менее 160 °F (71 °C) без периода выдержки. Всю домашнюю птицу следует готовить при внутренней температуре не ниже 165 °F (74 °C). После приготовления перед употреблением следует дать возможность отдохнуть в течение 3 минут.
Ооцистам в кошачьих фекалиях требуется как минимум день, чтобы образовать споры (чтобы они стали заразными после того, как они были выделены), поэтому ежедневная утилизация кошачьего туалета значительно снижает вероятность развития инфекционных ооцист. Поскольку они могут распространяться и сохраняться в окружающей среде в течение нескольких месяцев, людям следует носить перчатки при работе в саду или при работе с почвой и сразу мыть руки после выбрасывания кошачьего туалета. Эти меры предосторожности относятся к открытым песочницам/песочницам для игр, которые следует накрывать, когда они не используются. Кошачьи фекалии ни в коем случае нельзя смывать в унитаз.
Беременные женщины подвергаются более высокому риску передачи паразита своему будущему ребенку, а люди с ослабленным иммунитетом - заражения затяжной инфекцией. По этой причине им не следует менять или трогать кошачьи туалеты. В идеале кошек следует держать в помещении и кормить только пищей, которая имеет низкий или нулевой риск переноса ооцист, например, коммерческий корм для кошек или хорошо приготовленный столовый корм.
Против Toxoplasma gondii не существует одобренной вакцины для человека . [68] Исследования вакцин для человека продолжаются. [69]
Для овец одобренная живая вакцина, продаваемая под названием Toxovax (от MSD Animal Health ), обеспечивает пожизненную защиту. [70]
У людей активный токсоплазмоз можно лечить комбинацией таких препаратов, как пириметамин и сульфадиазин , а также фолиниевой кислоты . Пациентам с ослабленным иммунитетом может потребоваться непрерывное лечение до тех пор, пока их иммунная система не восстановится. [71]
Во многих частях мира, где имеется высокая популяция диких кошек, существует повышенный риск для местной дикой природы из-за увеличения заражения Toxoplasma gondii . Было обнаружено, что концентрации T. gondii в сыворотке диких животных повышаются там, где имеется большое количество популяций кошек. Это создает опасную среду для организмов, которые не эволюционировали в условиях совместного проживания с кошачьими и их паразитами. [72]
Токсоплазмоз является одним из факторов смертности южных каланов , особенно в районах с большими городскими стоками. [73] В своей естественной среде обитания каланы контролируют популяцию морских ежей и, таким образом, косвенно контролируют леса морских водорослей. Обеспечивая рост морских водорослей, вы защищаете другие морские популяции, а выбросы CO 2 сокращаются благодаря способности водорослей поглощать атмосферный углерод. [74] Обследование 105 пляжных выдр показало, что 38,1% из них имели паразитарные инфекции, а 28% указанных инфекций привели к смерти от протозойного менингоэнцефалита. [73] Было обнаружено, что Toxoplasma gondii является основной причиной 16,2% этих смертей, в то время как 6,7% смертей были вызваны близкородственным простейшим паразитом, известным как Sarcocystis Neurona . [73]
Норки, ведущие полуводный образ жизни, также восприимчивы к инфекции и имеют антитела к Toxoplasma gondii . [75] Норки могут следовать той же диете, что и выдры, и питаться ракообразными, рыбой и беспозвоночными, таким образом, путь передачи инфекции аналогичен выдрам. Из-за способности норки чаще пересекать землю и часто рассматриваться как инвазивный вид, норки представляют собой большую угрозу при транспортировке T. gondii к другим видам млекопитающих, чем выдры, у которых более ограниченный ареал. [75]
Несмотря на то, что популяции пингвинов недостаточно изучены, особенно те, которые живут в одной среде с человеческой популяцией, они подвергаются риску из-за паразитарных инфекций, главным образом токсоплазмоза гондии . К основным подвидам пингвинов, зараженных T. gondii , относятся дикие Магеллановы и Галапагосские пингвины, а также голубые и африканские пингвины, содержащиеся в неволе. [76] В одном исследовании в 57 (43,2%) из 132 образцов сыворотки магеллановых пингвинов был обнаружен T. gondii . Известно, что на острове Магдалены, на котором находится пингвин, нет популяции кошек, но очень часто встречается популяция людей, что указывает на возможность передачи инфекции. [76]
При обследовании черноногих пингвинов, больных токсоплазмозом, обнаруживают гепатомегалию, спленомегалию, черепные кровоизлияния и некроз почек. [77] Альвеолярная и печеночная ткань содержит большое количество иммунных клеток, таких как макрофаги, содержащие тахизоиты T. gondii. [77] Гистопатологические особенности у других животных, пораженных токсоплазмозом, имели тахизоиты в структурах глаза, таких как сетчатка, что приводило к слепоте. [77]
Передача ооцист неизвестна, хотя зарегистрировано множество случаев заражения морских видов. Исследователи обнаружили, что ооциты T. gondii могут выживать в морской воде не менее 6 месяцев, при этом концентрация соли не влияет на их жизненный цикл. Исследований способности жизненного цикла ооцист T. gondii в пресноводной среде не проводилось, хотя инфекции все еще присутствуют. Одна из возможных гипотез передачи – через виды амеб, особенно виды Acanthamoeba , виды, которые встречаются во всех водных средах (пресная, солоноватая и насыщенная морская вода). Обычно амебы действуют как естественный фильтр, фагоцитируя питательные вещества и бактерии, находящиеся в воде. Однако некоторые патогены использовали это в своих целях и эволюционировали, чтобы избежать разрушения и, таким образом, выживать, заключенные в амебу – к ним относятся, среди прочего, Holosporaceae, Pseudomonaceae, Burkholderiacceae. [78] В целом, это помогает возбудителю при транспортировке, а также защищает от лекарств и стерилизаторов, которые в противном случае могли бы привести к гибели возбудителя. [79] Исследования показали, что ооцисты T. gondii могут жить внутри амеб после поглощения в течение как минимум 14 дней без существенного уничтожения паразита. [80] Способность микроорганизма выживать in vitro зависит от самого микроорганизма, но существует несколько всеобъемлющих механизмов. Было обнаружено, что ооцисты T. gondii устойчивы к кислому pH и, таким образом, защищены подкислением, обнаруживаемым в эндоцитарных вакуолях и лизосомах. [80] Фагоцитоз дополнительно усиливается, если на амебах расположена богатая углеводами поверхностная мембрана. [81] Возбудитель может высвобождаться либо путем лизиса амеб, либо путем экзоцитоза, но этот вопрос недостаточно изучен [82]
Почти все виды птиц, проверенные на Toxoplasma gondii, дали положительный результат. Единственным видом птиц, у которого не зарегистрированы клинические симптомы токсоплазмоза, являются дикие утки, а о домашних утках было обнаружено только одно сообщение в 1962 году. [83] Виды с устойчивостью к T. gondii включают домашних индеек, [84] сов, краснохвостые ястребы и воробьи, в зависимости от штамма T. gondii . [85] T. gondii значительно более серьезен у голубей, особенно у коронованных голубей, декоративных голубей и голубей, происходящих из Австралии и Новой Зеландии. Типичное начало быстрое и обычно приводит к смерти. Те, кто выживает, часто страдают хроническими заболеваниями энцефалита и неврита. [85] Аналогичным образом, канарейки оказываются такими же тяжелыми, как и голуби, но клинические симптомы более аномальны по сравнению с другими видами. В большинстве случаев инфекция поражает глаза, вызывая слепоту, поражения сосудистой оболочки, конъюнктивит, атрофию глаза, блефарит и хориоретинит [85] . В большинстве случаев инфекция приводит к смерти.
Урбанизация и глобальное потепление чрезвычайно влияют на передачу T. gondii . [86] Температура и влажность являются важными факторами на стадии споруляции: низкая влажность всегда губительна для ооцист, и они также уязвимы к экстремальным температурам. [86] Осадки также являются важным фактором выживания болезнетворных микроорганизмов, передающихся через воду. Поскольку увеличение количества осадков напрямую увеличивает скорость стока в реках, объем стока в прибрежные районы также увеличивается. Это может привести к распространению болезнетворных микроорганизмов, передающихся через воду, на большие территории.
Эффективной вакцины против T. gondii не существует , и исследования живой вакцины продолжаются. Кормление кошек коммерчески доступной пищей, а не сырым, недоваренным мясом, предотвращает превращение кошек в хозяев ооцист, поскольку более высокая распространенность наблюдается в районах, где кормят сырым мясом. [87] Исследователи также предполагают, что владельцы запрещают кошкам жить в помещении и подвергать их стерилизации или стерилизации, чтобы уменьшить популяцию бездомных кошек и уменьшить взаимодействие с промежуточными хозяевами. Предлагается ежедневно собирать фекалии из туалетных лотков, помещать их в закрывающийся пакет и выбрасывать в мусор, а не смывать в унитаз, чтобы ограничить загрязнение воды. [88]
Исследования показали, что водно-болотные угодья с высокой плотностью растительности снижают концентрацию ооцист в воде за счет двух возможных механизмов. Во-первых, растительность снижает скорость потока, что приводит к большему осаждению из-за увеличения времени транспортировки. [88] Во-вторых, растительность может удалять ооцисты благодаря своей способности механически напрягать воду, а также посредством процесса адгезии (т.е. прикрепления к биопленкам). Было обнаружено, что зоны эрозии и разрушения прибрежных водно-болотных угодий являются местом обитания повышенных концентраций ооцист T. gondii , которые затем попадают в открытые прибрежные воды. Доказано, что современные физические и химические методы лечения, обычно используемые на водоочистных сооружениях, неэффективны против T. gondii . Исследования показали, что дезинфекция УФ-С воды, содержащей ооцисты, приводит к их инактивации и возможной стерилизации. [89]
Секвенированы геномы более 60 штаммов T. gondii . Большинство из них имеют размер 60–80 МБ и состоят из 11–14 хромосом . [90] [91] Основные штаммы кодируют 7 800–10 000 белков , из которых около 5 200 консервативны в RH, GT1, ME49, VEG. [90] Была создана база данных ToxoDB для документирования геномной информации о токсоплазме . [92] [93] [94]
В 1908 году, работая в Институте Пастера в Тунисе , Шарль Николь и Луи Мансо обнаружили простейший организм в тканях хомякоподобного грызуна, известного как гунди , Ctenodactylus Gundi . [30] Хотя Николь и Мансо первоначально считали, что этот организм принадлежит к роду Leishmania , который они описали как «Leishmania gondii» , вскоре они поняли, что открыли совершенно новый организм; они переименовали его в Toxoplasma gondii . Новое название рода Toxoplasma является отсылкой к его морфологии: Toxo , от греческого τόξον ( токсон , «дуга, лук») и πλάσμα ( плазма , «форма, форма») и хозяина, у которого он был обнаружен, гунди ( гондии). [95] В том же году Николь и Мансо обнаружили T. gondii , Альфонсо Сплендоре идентифицировал тот же организм у кролика в Бразилии . Однако он не дал ему названия. [30] В 1914 году итальянский тропицист Альдо Кастеллани «первым заподозрил, что токсоплазмоз может поражать человека». [96]
Первая убедительная идентификация T. gondii у людей была сделана у девочки, родившейся в срок с помощью кесарева сечения 23 мая 1938 года в детской больнице в Нью-Йорке . [30] В трехдневном возрасте у девочки начались судороги , и врачи выявили поражения пятен обоих ее глаз . Когда она умерла в возрасте одного месяца, было проведено вскрытие . Было обнаружено, что в повреждениях , обнаруженных в ее мозге и тканях глаз, обнаружены как свободные, так и внутриклеточные T. gondii' . [30] Инфицированную ткань девочки гомогенизировали и инокулировали внутримозгово кроликам и мышам; затем у них развился энцефалит . Позже врожденная передача была подтверждена у многих других видов, особенно у зараженных овец и грызунов.
Возможность передачи T. gondii через употребление недоваренного мяса была впервые предложена Д. Вейнманом и А. Х. Чандлером в 1954 году. [30] В 1960 году было показано, что соответствующая стенка кисты растворяется под действием протеолитических ферментов, обнаруженных в желудке, высвобождая инфекционные агенты. брадизоиты в желудок (которые переходят в кишечник). Гипотеза о передаче инфекции через употребление недоваренного мяса была проверена в приюте в Париже в 1965 году; заболеваемость T. gondii выросла с 10% до 50% после года добавления двух порций приготовленной редкой говядины или конины в ежедневный рацион многих сирот, и до 100% среди тех, кого кормили приготовленными редко приготовленными бараньими отбивными. [30]
Исследование, проведенное в Мумбаи в 1959 году , показало, что распространенность этого заболевания среди строгих вегетарианцев аналогична распространенности среди невегетарианцев. Это повысило вероятность третьего основного пути заражения, помимо врожденного и плотоядного мяса, приготовленного некачественно. [30]
В 1970 году ооцисты были обнаружены в фекалиях кошек. Показан фекально-оральный путь заражения через ооцисты . [30] В 1970-х и 1980-х годах фекалии широкого спектра инфицированных видов животных были проверены на предмет наличия в них ооцист — по крайней мере 17 видов кошачьих выделяют ооцисты, но не было доказано, что ни один некошачий не допускает полового размножения T. gondii. (приводит к отторжению ооцист). [30]
В 1984 году Элмер Р. Пфефферкорн опубликовал свое открытие о том, что обработка человеческих фибробластов человеческим рекомбинантным гамма-интерфероном блокирует рост T. gondii . [97]
Есть много случаев, когда у грызунов с T. gondii наблюдались изменения в поведении . Замеченные изменения заключались в уменьшении врожденной неприязни к кошкам, что облегчило кошкам охоту на грызунов. В эксперименте, проведенном Бердой и его коллегами, инфицированные крысы отдавали предпочтение области с запахом кошки, а не области с запахом кролика, что облегчило паразиту сделать последний шаг к окончательному хозяину из семейства кошачьих. [7] Это пример концепции расширенного фенотипа , то есть идеи о том, что поведение инфицированного животного меняется, чтобы максимизировать выживаемость генов, которые увеличивают хищничество промежуточного хозяина-грызуна. [98]
Различия в зависимом от пола поведении, наблюдаемые у инфицированных хозяев по сравнению с неинфицированными людьми, можно объяснить различиями в уровне тестостерона. Зараженные мужчины имели более высокий уровень тестостерона, в то время как инфицированные женщины имели значительно более низкие уровни по сравнению с их неинфицированными эквивалентами. [99] Исследования на людях с использованием опросника Кеттелла «16 личностных факторов» показали, что инфицированные мужчины набрали более низкие баллы по фактору G (сила суперэго/сознание правил) и выше по фактору L (бдительность), в то время как у инфицированных женщин наблюдалась противоположная картина. [100] Такие мужчины чаще игнорировали правила, были более расчетливыми, подозрительными и ревнивыми. С другой стороны, женщины были более сердечными, общительным, добросовестными и моралистическими. [100] Мыши, инфицированные T. gondii, имеют худшие двигательные способности, чем неинфицированные мыши. [101] [102] Таким образом, как инфицированным, так и неинфицированным взрослым был проведен компьютерный простой тест на реакцию. Было обнаружено, что инфицированные взрослые работали гораздо хуже и быстрее теряли концентрацию, чем контрольная группа . Однако эффект инфекции объясняет лишь менее 10% изменчивости показателей [100] (т. е. могут быть и другие мешающие факторы). Также наблюдалась корреляция между серологической распространенностью T. gondii у людей и повышенным риском дорожно-транспортных происшествий. У инфицированных риск попасть в дорожно-транспортное происшествие в 2,65 раза выше. [103] Турецкое исследование подтвердило, что это справедливо и для водителей. [104] Этот паразит связан со многими неврологическими расстройствами, такими как шизофрения . В метаанализе 23 исследований, соответствующих критериям включения, серологическая распространенность антител к T. gondii у людей с шизофренией значительно выше, чем в контрольной популяции (OR=2,73, P<0,000001). [105] Обзор исследований 2009 года показал, что у лиц, пытающихся совершить самоубийство, было гораздо больше показательных антител (IgG), чем у пациентов психиатрических стационаров без попыток самоубийства. [106] Также было показано, что инфекция связана с самоубийством у женщин старше 60 лет (P<0,005) [107]
Как упоминалось ранее, эти результаты увеличения доли людей, серопозитивных к паразиту в случаях этих неврологических расстройств, не обязательно указывают на причинную связь между инфекцией и заболеванием. Также важно отметить, что в 2016 году было проведено репрезентативное исследование возрастной когорты с целью проверки гипотезы о том, что токсоплазмоз связан с нарушениями в мозге и поведении, измеряемыми по ряду фенотипов, включая нервно-психические расстройства, плохой контроль импульсов, личностные и психические расстройства. нейрокогнитивные дефициты. Результаты этого исследования не подтвердили результаты ранее упомянутых исследований, более чем незначительно. Ни одно из значений P не показало значимости для какого-либо показателя результата. Таким образом, согласно этому исследованию, наличие антител к T. gondii не коррелирует с увеличением восприимчивости к какому-либо фенотипу поведения (за исключением, возможно, более высокого уровня неудачных попыток самоубийства). Эта группа не обнаружила какой-либо значимой связи между серопозитивностью T. gondii и шизофренией . Команда отмечает, что нулевые результаты могут быть ложноотрицательными из-за низкой статистической мощности из-за небольших размеров выборки, но с учетом этих весов их установка должна избегать некоторых возможностей ошибок в примерно 40 исследованиях, которые действительно показали положительную корреляцию. Они пришли к выводу, что необходимо провести дальнейшие исследования. [108] Другое репрезентативное исследование населения с участием 7440 человек в Соединенных Штатах показало, что токсоплазменная инфекция в 2,4 раза чаще встречается у людей, у которых в анамнезе были симптомы маниакального и депрессивного расстройства (биполярное расстройство типа 1), по сравнению с населением в целом. [109]
Исследования связи между инфекцией T. gondii и предпринимательским поведением показали, что студенты с положительным результатом теста на воздействие T. gondii в 1,4 раза чаще выбирают специальность «бизнес» и в 1,7 раза чаще делают упор на «менеджмент и предпринимательство». Среди 197 участников предпринимательских мероприятий заражение T. gondii коррелировало с вероятностью открытия собственного бизнеса в 1,8 раза выше. [110]
Опубликованные исследования также показали, что инфекция T. gondii потенциально может способствовать изменениям в политических убеждениях и ценностях человека. Те, кто заражен паразитом, как правило, демонстрируют более высокую степень мышления «мы против них». [111] [112] [113]
Механизм изменений в поведении частично объясняется усилением метаболизма дофамина, [114] который можно нейтрализовать препаратами-антагонистами дофамина. [115] T. gondii имеет два гена, которые кодируют бифункциональную фенилаланин и тирозингидроксилазу , два важных и ограничивающих скорость этапа биосинтеза дофамина. Один из генов экспрессируется конститутивно, а другой вырабатывается только во время развития кисты. [116] [117] В дополнение к дополнительному производству дофамина, инфекция T. gondii также вызывает у животных долговременные эпигенетические изменения, которые увеличивают экспрессию вазопрессина , что является вероятной причиной изменений, которые сохраняются после устранения инфекции. [118]
В 2022 году опубликованное в журнале Nature исследование хорошо документированной популяции волков, изучавшейся на протяжении всей их жизни, показало, что T. gondii также может оказывать существенное влияние на их поведение. Было высказано предположение, что заражение этим паразитом придало инфицированным волкам смелости к поведению, которое определяло лидерские роли и влияло на рискованное поведение, возможно, даже мотивируя создание новых независимых стай, которые они создавали и возглавляли, модели поведения которых отличались от моделей поведения стай, в которые они входили. рожденный. Исследование показало, что иногда зараженный волк становился единственным размножающимся самцом в стае, [119] что приводило к значительному воздействию T. gondii на другой вид .
Токсоплазмоз становится глобальной угрозой для здоровья, поскольку им заражается 30–50% населения мира.
Клинически пожизненное присутствие паразита в тканях большинства инфицированных обычно считается бессимптомным.
Однако ряд исследований показывает, что эта «бессимптомная инфекция» может привести и к развитию других патологий человека.
... Серораспространенность токсоплазмоза коррелировала с бременем различных заболеваний.
Статистические связи не обязательно означают причинно-следственную связь.
Однако принцип предосторожности предполагает, что возможная роль токсоплазмоза как пускового фактора, ответственного за развитие ряда клинических форм, заслуживает гораздо большего внимания и финансовой поддержки как в повседневной медицинской практике, так и в будущих клинических исследованиях.