В органической химии ароматичность — это химическое свойство, описывающее способ, которым сопряженное кольцо ненасыщенных связей , неподеленных пар или пустых орбиталей демонстрирует стабилизацию более сильную, чем можно было бы ожидать, стабилизируя только сопряжение. Самое раннее использование этого термина было в статье Августа Вильгельма Хофмана в 1855 году. [1] Не существует общей связи между ароматичностью как химическим свойством и обонятельными свойствами таких соединений.
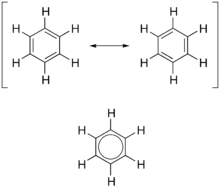
Ароматичность можно также считать проявлением циклической делокализации и резонанса . [2] [3] [4] Обычно считается, что это происходит потому, что электроны могут свободно вращаться вокруг кругового расположения атомов , которые попеременно связаны одинарной и двойной связью друг с другом. Эти связи можно рассматривать как гибрид одинарной и двойной связи, причем каждая связь в кольце идентична любой другой. Эта широко распространенная модель ароматических колец, а именно идея о том, что бензол образуется из шестичленного углеродного кольца с чередующимися одинарными и двойными связями (циклогексатриен), была развита Кекуле ( см. Раздел «История» ниже). Модель бензола состоит из двух резонансных форм, что соответствует наложению двойных и одинарных связей, образующему шесть полуторных связей. Бензол — более стабильная молекула, чем можно было бы ожидать без учета делокализации заряда.
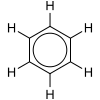
Как это стандартно для резонансных диаграмм , двусторонняя стрелка используется для обозначения того, что две структуры не являются отдельными объектами, а просто гипотетическими возможностями. Это также не является точным представлением фактического соединения , которое лучше всего представлено гибридом (средним) этих структур, который можно увидеть справа. Связь AC=C короче, чем связь C-C, но бензол идеально шестиугольный — все шесть связей углерод-углерод имеют одинаковую длину , промежуточную между длиной одинарной и двойной связью .
Лучшим представлением является круговая π-связь ( внутренний цикл Армстронга ), в которой электронная плотность равномерно распределяется через π-связь выше и ниже кольца. Эта модель более правильно отражает расположение электронной плотности внутри ароматического кольца.
Одинарные связи образуются с электронами, расположенными между ядрами углерода — они называются σ-связями . Двойные связи состоят из σ-связи и π-связи. π-связи образуются в результате перекрытия атомных p-орбиталей выше и ниже плоскости кольца. На следующей диаграмме показаны положения этих p-орбиталей:
Поскольку они находятся вне плоскости атомов, эти орбитали могут свободно взаимодействовать друг с другом и становиться делокализованными. Это означает, что каждый электрон не связан с одним атомом углерода, а принадлежит всем шести в кольце. Таким образом, электронов недостаточно для образования двойных связей на всех атомах углерода, но «лишние» электроны одинаково укрепляют все связи в кольце. Полученная молекулярная орбиталь имеет π-симметрию.
Первое известное использование слова «ароматический» в качестве химического термина, а именно применительно к соединениям, содержащим фенильный радикал , встречается в статье Августа Вильгельма Хофмана в 1855 году. [1] Если это действительно самое раннее введение Любопытно, что Гофман ничего не говорит о том, почему он ввел прилагательное, указывающее на обонятельный характер, для обозначения группы химических веществ, лишь некоторые из которых обладают заметным ароматом. Кроме того, многие из наиболее пахучих известных органических веществ представляют собой терпены , которые не являются ароматическими в химическом смысле. Но терпены и бензооидные вещества имеют общую химическую характеристику, а именно более высокие индексы ненасыщенности, чем многие алифатические соединения , и Хофманн, возможно, не проводил различия между этими двумя категориями.
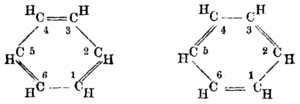
В XIX веке химики сочли загадкой, что бензол может быть настолько нереактивным в реакциях присоединения, учитывая его предполагаемую высокую степень ненасыщенности. Циклогексатриеновая структура бензола была впервые предложена Августом Кекуле в 1865 году. В течение следующих нескольких десятилетий большинство химиков с готовностью приняли эту структуру, поскольку она объясняет большинство известных изомерных связей ароматической химии.
Между 1897 и 1906 годами Дж. Дж. Томсон , первооткрыватель электрона, предположил, что между каждым атомом углерода в бензоле есть три эквивалентных электрона.
Объяснение исключительной стабильности бензола традиционно приписывают сэру Роберту Робинсону , который, по-видимому, первым (в 1925 году) [6] ввёл термин «ароматический секстет» как группу из шести электронов, устойчивых к разрушению.
Фактически, эту концепцию можно проследить еще дальше, от Эрнеста Крокера в 1922 году [7] до Генри Эдварда Армстронга , который в 1890 году написал, что «(шесть) центрических сродств действуют внутри цикла... бензол может быть представлен двойным кольцо ( так в оригинале ) ... и когда образуется аддитивное соединение, внутренний цикл сродства нарушается, смежные атомы углерода, к которым ничего не было присоединено, неизбежно приобретают этиленовое состояние». [8] [ нужна проверка ]
Здесь Армстронг описывает как минимум четыре современные концепции. Во-первых, его «сродство» сегодня более известно как электрон , который должен был быть открыт всего семь лет спустя Дж. Дж. Томсоном. Во-вторых, он описывает электрофильное ароматическое замещение , происходящее (третий) через промежуточный продукт Уиланда , при котором (четвертый) разрывается сопряжение кольца. Он ввел символ C с центром в кольце как сокращение внутреннего цикла , предвосхищая тем самым обозначения Эриха Клара . Утверждается, что он также предвосхитил природу волновой механики , поскольку осознал, что его сродства имели направление, а не просто были точечными частицами, а в совокупности имели распределение, которое можно было изменить путем введения заместителей в бензольное кольцо ( так же, как распределение электрический заряд тела изменяется при приближении его к другому телу ).
Квантово -механические причины этой стабильности, или ароматичности, были впервые смоделированы Хюкелем в 1931 году. Он был первым, кто разделил связывающие электроны на сигма- и пи-электроны.
Ароматическое (или арильное ) соединение содержит набор ковалентно связанных атомов со специфическими характеристиками:
В то время как бензол является ароматическим (6 электронов от 3 двойных связей), циклобутадиен - нет, поскольку число π-делокализованных электронов равно 4, что, конечно, кратно 4. Однако циклобутадиенидный ион (2-) является ароматическим ( 6 электронов). Атом ароматической системы может иметь другие электроны, не входящие в состав системы, и поэтому игнорируются правилом 4n + 2. В фуране атом кислорода находится в состоянии sp²-гибридизации. Одна неподеленная пара находится в π-системе, а другая — в плоскости кольца (аналогично связи CH в остальных положениях). Имеется 6 π-электронов, поэтому фуран ароматический.
Ароматические молекулы обычно демонстрируют повышенную химическую стабильность по сравнению с аналогичными неароматическим молекулами. Молекула, которая может быть ароматической, будет стремиться изменить свою электронную или конформационную структуру, чтобы оказаться в такой ситуации. Эта дополнительная стабильность меняет химический состав молекулы. Ароматические соединения подвергаются реакциям электрофильного ароматического замещения и нуклеофильного ароматического замещения , но не реакциям электрофильного присоединения , как это происходит с двойными углерод-углеродными связями.
Многие из самых ранних известных примеров ароматических соединений, таких как бензол и толуол, имеют характерный приятный запах. Это свойство привело к появлению термина «ароматические» для этого класса соединений и, следовательно, к термину «ароматика» для обозначения обнаруженного в конечном итоге электронного свойства.
Циркулирующие π-электроны в ароматической молекуле создают кольцевые токи , которые противодействуют приложенному магнитному полю в ЯМР . [9] Сигнал ЯМР протонов в плоскости ароматического кольца сдвинут существенно дальше в слабое поле, чем сигнал неароматических sp²-углеродов. Это важный способ определения ароматичности. По такому же механизму смещаются в большую сторону поля сигналы протонов, расположенных вблизи оси кольца.
Ароматические молекулы способны взаимодействовать друг с другом в так называемой π-π-стекинге : π-системы образуют два параллельных кольца, перекрывающихся в ориентации «лицом к лицу». Ароматические молекулы также способны взаимодействовать друг с другом в ориентации «край к лицу»: небольшой положительный заряд заместителей на атомах кольца одной молекулы притягивается к небольшому отрицательному заряду ароматической системы на другой молекуле.
Плоские моноциклические молекулы, содержащие 4n π-электронов, называются антиароматическими и, как правило, дестабилизированы. Молекулы, которые могут быть антиароматическими , будут стремиться изменить свою электронную или конформационную структуру, чтобы избежать этой ситуации, тем самым становясь неароматическим. Например, циклооктатетраен (COT) искажает свою планарность, нарушая π-перекрытие между соседними двойными связями. Относительно недавно было обнаружено, что циклобутадиен принимает асимметричную прямоугольную конфигурацию, в которой действительно чередуются одинарные и двойные связи; резонанса нет, а одинарные связи заметно длиннее двойных, что уменьшает неблагоприятное перекрытие р-орбиталей. Это снижение симметрии снимает вырождение двух ранее несвязывающих молекулярных орбиталей, что по правилу Хунда вынуждает два неспаренных электрона перейти на новую, слабосвязывающую орбиталь (а также создает слабо разрыхляющую орбиталь). Следовательно, циклобутадиен неароматичен; напряжение асимметричной конфигурации перевешивает антиароматическую дестабилизацию, которая могла бы повлиять на симметричную квадратную конфигурацию.
Ароматические соединения играют ключевую роль в биохимии всех живых существ. Каждая из четырех ароматических аминокислот гистидин , фенилаланин , триптофан и тирозин служит одним из 20 основных строительных блоков белков. Далее, все 5 нуклеотидов ( аденин , тимин , цитозин , гуанин и урацил ), составляющие последовательность генетического кода в ДНК и РНК, являются ароматическими пуринами или пиримидинами . Молекула гема содержит ароматическую систему с 22 π-электронами. Хлорофилл также имеет аналогичную ароматическую систему.
Ароматические соединения имеют важное значение в промышленности. Ключевыми ароматическими углеводородами , представляющими коммерческий интерес, являются бензол , толуол , орто -ксилол и пара -ксилол . Ежегодно во всем мире производится около 35 миллионов тонн. Их извлекают из сложных смесей, полученных при переработке нефти или перегонке каменноугольной смолы, и используют для производства ряда важных химикатов и полимеров, включая стирол , фенол , анилин , полиэстер и нейлон .
Подавляющее большинство ароматических соединений представляют собой соединения углерода, но они не обязательно должны быть углеводородами.
Бензол , а также большинство других аннуленов ( за исключением циклодекапентаена ) с формулой C n H n , где n — четное число, например циклотетрадекагептаен .
В гетероциклических ароматических соединениях ( гетероароматы ) один или несколько атомов ароматического кольца принадлежат не углероду, а другому элементу. Это может уменьшить ароматичность кольца и, таким образом (как в случае с фураном ), повысить его реакционную способность. Другие примеры включают пиридин , пиразин , имидазол , пиразол , оксазол , тиофен и их бензаннулированные аналоги ( например, бензимидазол ).
Полициклические ароматические углеводороды — это молекулы, содержащие два или более простых ароматических колец, слитых вместе за счет двух соседних атомов углерода (см. также простые ароматические кольца ). Примерами являются нафталин , антрацен и фенантрен .
Многие химические соединения представляют собой ароматические кольца с присоединенными другими функциональными группами . Примеры включают тринитротолуол (ТНТ), ацетилсалициловую кислоту (аспирин), парацетамол и нуклеотиды ДНК .
Ароматичность обнаружена и у ионов : циклопропенильного катиона (система 2е), циклопентадиенильного аниона (система 6е), иона тропилия (6е) и циклооктатетраендианиона (10е). Ароматические свойства приписывают небензеноидным соединениям, таким как тропон . Ароматические свойства проверяются до предела в классе соединений, называемых циклофанами .
Особый случай ароматичности обнаруживается в гомоароматичности , когда сопряжение прерывается одним sp 3- гибридным атомом углерода.
Когда углерод в бензоле заменяется другими элементами в солях борабензола , силабензола , германабензола , оловобензола , фосфорина или пирилия , ароматичность все еще сохраняется. Ароматичность также возникает в соединениях, которые вообще не основаны на углероде. Синтезированы неорганические шестичленные соединения, аналогичные бензолу. Гексасилабензол (Si 6 H 6 ) и боразин (B 3 N 3 H 6 ) структурно аналогичны бензолу, с замещением атомов углерода другим элементом или элементами. В боразине атомы бора и азота чередуются по кольцу. Совсем недавно методом ЯМР твердого тела Li была экспериментально подтверждена ароматичность плоских колец Si 5 6- , находящихся в фазе Цинтла Li 12 Si 7 . [10]
Считается, что металлическая ароматичность присутствует в некоторых металлических кластерах алюминия. [ нужна цитата ]
Ароматичность Мёбиуса возникает, когда циклической системе молекулярных орбиталей, образованной из p π атомных орбиталей и населенной в замкнутой оболочке 4n (n — целое число) электронами, придается одиночный полуповорот, соответствующий ленте Мёбиуса . π-система с 4n электронами в плоском (нескрученном) кольце была бы антиароматической и, следовательно, очень нестабильной из-за симметрии комбинаций p-атомных орбиталей. При скручивании кольца симметрия системы меняется и становится разрешенной ( подробности см. Также в концепции Мёбиуса – Хюккеля ). Поскольку поворот может быть левым или правым , полученные ароматические соединения Мёбиуса являются асимметричными или хиральными . По состоянию на 2012 год нет никаких доказательств того, что ароматическая молекула Мёбиуса была синтезирована. [11] [12] Ароматики с двумя полуповоротами, соответствующими парадромным топологиям, были впервые предложены Иоганном Листингом . [13] В карбобензоле кольцевые связи расширены алкиновыми и алленовыми группами.
Y-ароматика — это концепция, которая была разработана для объяснения необычайной стабильности и высокой основности катиона гуанидиния . Гуанидиний не имеет кольцевой структуры, но имеет шесть π-электронов, делокализованных по молекуле. Однако эта концепция противоречива, и некоторые авторы подчеркивают разные эффекты. [14] [15] [16]
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ){{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ){{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ){{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка )