Эстрадиол ( Е2 ), также называемый эстрадиол , представляет собой стероидный гормон эстрогена и основной женский половой гормон . Он участвует в регуляции женских репродуктивных циклов , таких как эстральный и менструальный циклы . Эстрадиол отвечает за развитие женских вторичных половых признаков , таких как грудь , расширение бедер и женский тип распределения жира . Он также важен для развития и поддержания женских репродуктивных тканей , таких как молочные железы , матка и влагалище, в период полового созревания , зрелого возраста и беременности . [7] Он также оказывает важное воздействие на многие другие ткани , включая кости , жир , кожу , печень и мозг .
Хотя уровень эстрадиола у мужчин намного ниже, чем у женщин, эстрадиол играет важную роль и у мужчин. Помимо человека и других млекопитающих , эстрадиол также обнаружен у большинства позвоночных и ракообразных , насекомых , рыб и других видов животных . [8] [9]
Эстрадиол вырабатывается главным образом в фолликулах яичников , а также в других тканях, включая яички , надпочечники , жир, печень , молочные железы и мозг. Эстрадиол вырабатывается в организме из холестерина посредством ряда реакций и промежуточных продуктов . [10] Основной путь включает образование андростендиона , который затем преобразуется ароматазой в эстрон и впоследствии превращается в эстрадиол. Альтернативно, андростендион может быть преобразован в тестостерон , который затем может быть преобразован в эстрадиол. При наступлении менопаузы у женщин выработка эстрогенов яичниками прекращается, а уровень эстрадиола снижается до очень низкого уровня.
Помимо своей роли естественного гормона, эстрадиол используется в качестве лекарства , например, в менопаузальной гормональной терапии и феминизирующей гормональной терапии для трансгендерных женщин ; Информацию об эстрадиоле как о лекарстве см. в статье об эстрадиоле (лекарстве) .
Развитие вторичных половых признаков у женщин обусловлено эстрогенами, а именно эстрадиолом. [11] [12] Эти изменения начинаются в период полового созревания , большинство из них усиливаются в репродуктивном возрасте и становятся менее выраженными при снижении поддержки эстрадиола после менопаузы . Таким образом, эстрадиол способствует развитию груди и отвечает за изменения формы тела , влияя на кости, суставы и отложение жира . [11] [12] У женщин эстрадиол вызывает развитие груди, расширение бедер , распределение женского жира (при этом жир откладывается, в частности, на груди, бедрах, бедрах и ягодицах), а также созревание влагалища и вульвы . опосредует скачок пубертатного роста (опосредованно через повышенную секрецию гормона роста ) [13] и закрытие эпифизов (тем самым ограничивая окончательный рост ) у обоих полов. [11] [12]
У женщин эстрадиол действует как гормон роста тканей репродуктивных органов, поддерживая слизистую оболочку влагалища , шейные железы, эндометрий и слизистую оболочку маточных труб. Усиливает рост миометрия . Эстрадиол, по-видимому, необходим для поддержания яйцеклеток в яичнике . Во время менструального цикла эстрадиол, вырабатываемый растущими фолликулами, через систему положительной обратной связи запускает гипоталамо-гипофизарные события, которые приводят к выбросу лютеинизирующего гормона , вызывая овуляцию. В лютеиновой фазе эстрадиол в сочетании с прогестероном подготавливает эндометрий к имплантации . Во время беременности уровень эстрадиола увеличивается за счет выработки плаценты . Эффект эстрадиола вместе с эстроном и эстриолом при беременности менее ясен. Они могут способствовать маточному кровотоку, росту миометрия, стимулировать рост груди, а в доношенном возрасте способствовать размягчению шейки матки и экспрессии рецепторов окситоцина в миометрии . [ нужна цитата ] У павианов блокирование выработки эстрогена приводит к потере беременности, что позволяет предположить, что эстрадиол играет роль в поддержании беременности. Исследования изучают роль эстрогенов в процессе начала родов . Действие эстрадиола необходимо до воздействия прогестерона в лютеиновую фазу. [ нужна цитата ]
Влияние эстрадиола (и эстрогенов в целом) на мужскую репродукцию является сложным. Эстрадиол вырабатывается под действием ароматазы главным образом в клетках Лейдига семенников млекопитающих , а также в некоторых половых клетках и клетках Сертоли неполовозрелых млекопитающих. [14] Он действует ( in vitro ) для предотвращения апоптоза мужских сперматозоидов . [15] Хотя некоторые исследования в начале 1990-х годов утверждали о связи между глобальным снижением количества сперматозоидов и воздействием эстрогена в окружающей среде, [16] более поздние исследования не обнаружили ни такой связи, ни доказательств общего снижения количества сперматозоидов. [17] [18] Подавление выработки эстрадиола в субпопуляции мужчин с субфертильностью может улучшить анализ спермы . [19]
Мужчины с определенными генетическими заболеваниями половых хромосом , такими как синдром Клайнфельтера , будут иметь более высокий уровень эстрадиола. [20]
Эстрадиол оказывает глубокое воздействие на кости. Лица без него (или других эстрогенов) станут высокими и евнухоидными , поскольку закрытие эпифизов задерживается или может не произойти. [21] Также влияет плотность костей , что приводит к ранней остеопении и остеопорозу . [22] Низкий уровень эстрадиола также может предсказать переломы, причем у женщин в постменопаузе самая высокая частота переломов костей . [23] Женщины после менопаузы испытывают ускоренную потерю костной массы из-за относительного дефицита эстрогена. [24]
Рецептор эстрогена , как и рецептор прогестерона , обнаружен в коже , в том числе в кератиноцитах и фибробластах . [25] [26] В период менопаузы и после нее снижение уровня женских половых гормонов приводит к атрофии , истончению и усилению морщинистости кожи, а также к снижению эластичности , упругости и прочности кожи. [25] [26] Эти изменения кожи представляют собой ускорение старения кожи и являются результатом снижения содержания коллагена , нарушений морфологии эпидермальных клеток кожи , уменьшения основного вещества между волокнами кожи , а также уменьшения капилляров и кровотока . [25] [26] Кожа также становится более сухой во время менопаузы, что связано с уменьшением гидратации кожи и поверхностных липидов (выработка кожного сала). [25] Наряду с хронологическим старением и фотостарением, дефицит эстрогенов в период менопаузы является одним из трех основных факторов, преимущественно влияющих на старение кожи. [25]
Заместительная гормональная терапия , состоящая из системного лечения эстрогеном отдельно или в сочетании с прогестагеном, имеет хорошо документированные и значительные положительные эффекты на кожу женщин в постменопаузе. [25] [26] Эти преимущества включают увеличение содержания коллагена в коже, увеличение толщины и эластичности кожи, а также увлажнение кожи и поверхностных липидов. [25] [26] Было обнаружено, что эстроген при местном применении оказывает аналогичное благотворное воздействие на кожу. [25] Кроме того, исследование показало, что местный крем с 2% прогестерона значительно повышает эластичность и упругость кожи, а также заметно уменьшает морщины у женщин в пери- и постменопаузе. [26] С другой стороны, гидратация кожи и поверхностные липиды существенно не изменились при местном применении прогестерона. [26] Эти результаты показывают, что прогестерон, как и эстроген, также оказывает благотворное воздействие на кожу и может независимо защищать ее от старения. [26]
Эстрогены могут вырабатываться в мозге из предшественников стероидов. Было обнаружено, что как антиоксиданты они обладают нейропротекторной функцией. [27]
Петли положительной и отрицательной обратной связи менструального цикла включают эстрадиол яичников как связующее звено с гипоталамо-гипофизарной системой, регулирующее гонадотропины . [28]
Считается, что эстроген играет важную роль в психическом здоровье женщин, при этом предполагается связь между уровнем гормонов, настроением и самочувствием. Внезапные падения или колебания или длительные периоды устойчивого низкого уровня эстрогена могут быть связаны со значительным снижением настроения. Было показано, что клиническое выздоровление от депрессии после родов, перименопаузы и постменопаузы эффективно после стабилизации и/или восстановления уровня эстрогена. [29] [30]
Было обнаружено, что объемы сексуально диморфных структур мозга у трансгендерных женщин изменяются и приближаются к типичным женским структурам мозга при воздействии эстрогена одновременно с андрогенной депривацией в течение нескольких месяцев, что позволяет предположить, что эстроген и/или андрогены играют значительную роль. в половой дифференциации мозга как пренатально , так и в более позднем возрасте.
Есть также свидетельства того, что программирование сексуального поведения взрослых самцов у многих позвоночных во многом зависит от эстрадиола, вырабатываемого во время внутриутробного развития и в раннем детстве. [32] Пока неизвестно, играет ли этот процесс значительную роль в сексуальном поведении человека, хотя данные, полученные от других млекопитающих, указывают на связь. [33]
Было обнаружено, что эстроген увеличивает секрецию окситоцина и усиливает экспрессию его рецептора , рецептора окситоцина , в мозге . [34] Было обнаружено, что у женщин однократной дозы эстрадиола достаточно для повышения концентрации циркулирующего окситоцина. [35]
Эстрадиол связан с развитием и прогрессированием таких видов рака, как рак молочной железы, рак яичников и рак эндометрия. Эстрадиол влияет на ткани-мишени главным образом путем взаимодействия с двумя ядерными рецепторами, называемыми рецептором эстрогена α (ERα) и рецептором эстрогена β (ERβ). [36] [37] Одной из функций этих рецепторов эстрогена является модуляция экспрессии генов . Как только эстрадиол связывается с ЭР, рецепторные комплексы затем связываются со специфическими последовательностями ДНК , что может вызвать повреждение ДНК и увеличение деления клеток и репликации ДНК . Эукариотические клетки реагируют на поврежденную ДНК, стимулируя или ослабляя фазы G1, S или G2 клеточного цикла, чтобы инициировать восстановление ДНК . В результате происходит клеточная трансформация и пролиферация раковых клеток. [38]
Эстроген влияет на определенные кровеносные сосуды . Улучшение артериального кровотока было продемонстрировано в коронарных артериях . [39] 17-бета-эстрадиол (Е2) считается самым мощным эстрогеном, обнаруженным у человека. Е2 влияет на функцию сосудов, апоптоз и повреждение во время ишемии и реперфузии сердца. E2 может защитить сердце и отдельные кардиомиоциты от повреждений, связанных с ишемией. После сердечного приступа или длительных периодов гипертонии Е2 подавляет побочные эффекты патологического ремоделирования сердца. [40]
Во время беременности высокий уровень эстрогенов, а именно эстрадиола, увеличивает свертываемость крови и риск венозной тромбоэмболии .
Эстрадиол оказывает комплексное воздействие на печень . Он влияет на выработку множества белков , включая липопротеины , связывающие белки и белки, ответственные за свертывание крови . [ нужна цитация ] В больших количествах эстрадиол может привести к холестазу , например, холестазу беременности .
Определенные гинекологические состояния зависят от эстрогена, такие как эндометриоз , лейомиома матки и маточное кровотечение . [ нужна цитата ]
Эстрадиол действует главным образом как агонист рецептора эстрогена (ER), ядерного рецептора стероидных гормонов . Существует два подтипа ER: ERα и ERβ , и эстрадиол мощно связывается и активирует оба этих рецептора. Результатом активации ER является модуляция транскрипции и экспрессии генов в клетках , экспрессирующих ER , что является преобладающим механизмом, с помощью которого эстрадиол опосредует свои биологические эффекты в организме. Эстрадиол также действует как агонист мембранных рецепторов эстрогена (mER), таких как GPER (GPR30), недавно обнаруженный неядерный рецептор эстрадиола, посредством которого он может опосредовать множество быстрых негеномных эффектов . [42] В отличие от ER, GPER, по-видимому, селективен в отношении эстрадиола и демонстрирует очень низкое сродство к другим эндогенным эстрогенам, таким как эстрон и эстриол . [43] Дополнительные mER, помимо GPER, включают ER-X , ERx и Gq - mER . [44] [45]
ERα/ERβ находятся в неактивном состоянии и захвачены мультимолекулярными шаперонными комплексами, организованными вокруг белка теплового шока 90 (HSP90), содержащего белок p23, и иммунофилина, и локализованы в основном в цитоплазме и частично в ядре. По классическому пути E2 или классическому пути эстрогена эстрадиол попадает в цитоплазму , где взаимодействует с ЭР. После связывания E2 ER диссоциируют от комплексов молекулярных шаперонов и становятся способными димеризоваться, мигрировать в ядро и связываться со специфическими последовательностями ДНК ( элемент ответа на эстроген , ERE), что обеспечивает транскрипцию генов, которая может происходить в течение часов и дней.
При подкожной инъекции мышам эстрадиол примерно в 10 раз более эффективен, чем эстрон, и примерно в 100 раз более эффективен, чем эстриол. [46] [47] [48] Таким образом, эстрадиол является основным эстрогеном в организме, хотя считается, что роль эстрона и эстриола как эстрогенов не является незначительной. [48]

Эстрадиол, как и другие стероидные гормоны , образуется из холестерина . После расщепления боковой цепи и использования пути Δ5 или Δ4- андростендион является ключевым посредником. Часть андростендиона превращается в тестостерон, который, в свою очередь, под действием ароматазы превращается в эстрадиол. Альтернативным путем андростендион ароматизируется в эстрон , который впоследствии превращается в эстрадиол с помощью 17β-гидроксистероиддегидрогеназы (17β-HSD). [50]
В репродуктивном возрасте большая часть эстрадиола у женщин вырабатывается гранулезными клетками яичников путем ароматизации андростендиона (продуцируемого в клетках теки фолликулов) в эстрон с последующим превращением эстрона в эстрадиол с помощью 17β-HSD. Меньшие количества эстрадиола также вырабатываются корой надпочечников , а у мужчин - яичками. [ нужна медицинская ссылка ]
Эстрадиол вырабатывается не только в гонадах ; в частности, жировые клетки производят активные предшественники эстрадиола и будут продолжать делать это даже после менопаузы. [51] Эстрадиол также вырабатывается в головном мозге и стенках артерий .
У мужчин примерно от 15 до 25% циркулирующего эстрадиола вырабатывается в яичках . [52] [53] Остальное синтезируется посредством периферической ароматизации тестостерона в эстрадиол и андростендиона в эстрон (который затем трансформируется в эстрадиол через периферический 17β-HSD). [52] [53] Эта периферическая ароматизация происходит преимущественно в жировой ткани , но также встречается и в других тканях, таких как кости , печень и мозг . [52] У мужчин вырабатывается примерно от 40 до 50 мкг эстрадиола в день. [52]
В плазме эстрадиол в значительной степени связан с ГСПГ и альбумином . Лишь около 2,21% (±0,04%) эстрадиола является свободным и биологически активным. Процент остается постоянным на протяжении всего менструального цикла . [54]
Инактивация эстрадиола включает преобразование в менее активные эстрогены, такие как эстрон и эстриол. Эстриол является основным метаболитом мочи . [ нужна цитация ] Эстрадиол конъюгируется в печени с образованием конъюгатов эстрогена, таких как сульфат эстрадиола , глюкуронид эстрадиола , и, как таковой, выводится через почки . Некоторые из водорастворимых конъюгатов выводятся через желчные протоки и частично реабсорбируются после гидролиза из кишечного тракта . Эта энтерогепатическая циркуляция способствует поддержанию уровня эстрадиола.
Эстрадиол также метаболизируется посредством гидроксилирования в катехол-эстрогены . В печени он неспецифически метаболизируется CYP1A2 , CYP3A4 и CYP2C9 посредством 2-гидроксилирования в 2-гидроксиэстрадиол , а также CYP2C9 , CYP2C19 и CYP2C8 посредством 17β-гидроксидегидрирования в эстрон [55] с различными другими цитохромами P450. (CYP) ферменты и метаболические преобразования также участвуют. [56]
Эстрадиол дополнительно конъюгируется со сложным эфиром в липоидные формы эстрадиола, такие как пальмитат эстрадиола и стеарат эстрадиола, в определенной степени; эти эфиры хранятся в жировой ткани и могут действовать как очень длительный резервуар эстрадиола. [57] [58]
Эстрадиол выводится с мочой в виде глюкуронидных и сульфатных эстрогеновых конъюгатов . После внутривенного введения меченого эстрадиола женщинам почти 90% выводится с мочой и калом в течение 4–5 дней. [59] [60] Энтерогепатическая рециркуляция вызывает задержку выведения эстрадиола. [59]

Уровни эстрадиола у женщин в пременопаузе сильно варьируются на протяжении менструального цикла, а референтные диапазоны широко варьируются от источника к источнику. [62] Уровни эстрадиола минимальны и, по данным большинства лабораторий, колеблются от 20 до 80 пг/мл во время ранней и средней фолликулярной фазы (или первой недели менструального цикла, также известной как менструация). [63] [64] Уровни эстрадиола постепенно повышаются в это время и в середине и конце фолликулярной фазы (или второй недели менструального цикла) до предовуляторной фазы. [62] [63] Во время предовуляции (период примерно от 24 до 48 часов) уровни эстрадиола ненадолго повышаются и достигают самых высоких концентраций в любое другое время менструального цикла. [62] В это время уровни циркулирующих крови обычно составляют от 130 до 200 пг/мл, но у некоторых женщин могут достигать 300–400 пг/мл, а верхний предел референтного диапазона некоторых лабораторий даже выше (для например, 750 пг/мл). [62] [63] [65] [66] [67] После овуляции (или в середине цикла) и во второй половине менструального цикла или лютеиновой фазы уровень эстрадиола выходит на плато и колеблется между 100 и 150 пг/мл. во время ранней и средней лютеиновой фазы, а также во время поздней лютеиновой фазы или за несколько дней до менструации достигают минимума около 40 пг/мл. [62] [64] В разных источниках сообщается, что средние интегрированные уровни эстрадиола в течение полного менструального цикла составляют 80, 120 и 150 пг/мл. [64] [68] [69] Хотя существуют противоречивые сообщения, одно исследование показало, что средние интегральные уровни эстрадиола составляют 150 пг/мл у молодых женщин, тогда как средние интегральные уровни варьируются от 50 до 120 пг/мл у женщин старшего возраста. [69]
В репродуктивный период у женщин уровень эстрадиола несколько выше, чем уровень эстрона, за исключением ранней фолликулярной фазы менструального цикла; таким образом, эстрадиол можно считать преобладающим эстрогеном в репродуктивный период у женщин с точки зрения абсолютных уровней в сыворотке и эстрогенной активности. [ нужна цитата ] Во время беременности эстриол становится преобладающим циркулирующим эстрогеном, и это единственный раз, когда эстрол появляется в организме, тогда как во время менопаузы преобладает эстрон (оба основаны на уровнях сыворотки). [ нужна цитата ] Эстрадиол, вырабатываемый мужчинами из тестостерона, присутствует на уровнях сыворотки, примерно сопоставимых с уровнями у женщин в постменопаузе (14–55 против <35 пг/мл соответственно). [ нужна цитация ] Также сообщалось, что если концентрации эстрадиола у 70-летнего мужчины сравнить с концентрациями у 70-летней женщины, уровни у мужчины примерно в 2-4 раза выше. [70]
У женщин уровень эстрадиола в сыворотке крови измеряется в клинической лаборатории и отражает прежде всего активность яичников. Анализ крови на эстрадиол измеряет количество эстрадиола в крови. [77] Применяется для проверки функции яичников, плаценты, надпочечников. [77] Это позволяет выявить исходный уровень эстрогена у женщин с аменореей или менструальной дисфункцией, а также выявить состояние гипоэстрогенности и менопаузы. Кроме того, мониторинг эстрогена во время терапии бесплодия позволяет оценить рост фолликулов и полезен при мониторинге лечения. Эстрогенпродуцирующие опухоли будут демонстрировать стойкие высокие уровни эстрадиола и других эстрогенов. При преждевременном половом созревании уровень эстрадиола неадекватно повышается.
Результаты отдельных лабораторных исследований всегда следует интерпретировать с использованием диапазонов, предоставленных лабораторией, проводившей тест.
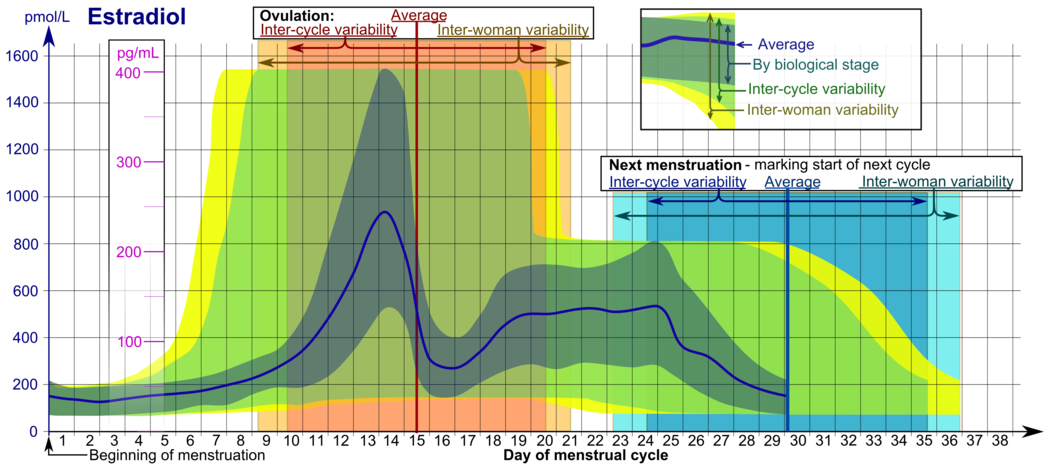
В нормальном менструальном цикле уровень эстрадиола обычно составляет <50 пг/мл во время менструации, повышается по мере развития фолликула (пик: 200 пг/мл), кратковременно падает при овуляции и снова повышается во время лютеиновой фазы, достигая второго пика. В конце лютеиновой фазы уровень эстрадиола падает до менструального уровня, если только не наступила беременность.
Во время беременности уровень эстрогена, включая эстрадиол, неуклонно повышается по мере приближения срока беременности. Источником этих эстрогенов является плацента , которая ароматизирует прогормоны, вырабатываемые в надпочечниках плода.
Эстрадиол используется в качестве лекарства , в первую очередь в гормональной терапии симптомов менопаузы , а также в феминизирующей гормональной терапии для трансгендеров. [82]
Эстрадиол – это стероид эстрана . [82] Он также известен как 17β-эстрадиол (в отличие от 17α-эстрадиола ) или как эстра-1,3,5(10)-триен-3,17β-диол. Он имеет две гидроксильные группы , одну в положении C3, а другую в положении 17β, а также три двойные связи в кольце A. Из-за наличия двух гидроксильных групп эстрадиол часто обозначают сокращенно E2. Структурно родственные эстрогены: эстрон (Е1), эстриол (Е3) и эстетрол (Е4) имеют одну, три и четыре гидроксильные группы соответственно.
В рандомизированном двойном слепом плацебо-контролируемом исследовании было показано, что эстрадиол оказывает гендерно-специфическое влияние на чувствительность к справедливости. В целом, когда разделение определенной суммы денег было представлено как справедливое или несправедливое в модифицированной версии игры- ультиматума , эстрадиол повышал уровень принятия справедливых предложений среди мужчин и снижал его среди женщин. Однако в группе плацебо «простая вера в получение лечения эстрадиолом значительно увеличила принятие несправедливо оформленных предложений у обоих полов», указывая на то, что так называемые «окружающие» факторы играли роль в организации ответов на эти представления игра ультиматум . [83]
Открытие эстрогена обычно приписывают американским ученым Эдгару Аллену и Эдварду А. Дойзи . [84] [85] В 1923 году они заметили, что инъекция жидкости из фолликулов яичников свиней вызывала изменения пубертатного периода и эструса (включая изменения влагалища , матки и молочных желез , а также сексуальную восприимчивость ) у половозрелых мышей и крыс с удаленными яичниками. [84] [85] [86] Эти результаты продемонстрировали существование гормона , который вырабатывается яичниками и участвует в половом созревании и размножении . [84] [85] [86] На момент открытия Аллен и Дойзи не давали названия гормону, а просто называли его «гормоном яичников» или «фолликулярным гормоном»; [85] другие называли его по-разному: феминин , фолликулин , менформон , теликинин и эмменин . [87] [88] В 1926 году Паркс и Беллерби ввели термин «эстрин» для описания гормона на основании того, что он вызывает течку у животных. [89] [87] Эстрон был выделен и очищен независимо Алленом, Дойзи и немецким ученым Адольфом Бутенандтом в 1929 году, а эстриол был выделен и очищен Маррианом в 1930 году; они были первыми идентифицированными эстрогенами. [85] [90] [91]
Эстрадиол, самый мощный из трех основных эстрогенов, был идентифицирован последним. [85] [89] Он был открыт Швенком и Хильдебрантом в 1933 году, которые синтезировали его путем восстановления эстрона. [85] Эстрадиол был впоследствии выделен и очищен из яичников свиноматок Дойзи в 1935 году, при этом его химическая структура была определена одновременно [92] и называлась по-разному: дигидротелин , дигидрофолликулин , дигидрофолликулярный гормон и дигидроксиэстрин . [85] [93] [94] В 1935 году название эстрадиол и термин эстроген были официально установлены Комитетом по половым гормонам Организации здравоохранения Лиги Наций ; это последовало за названиями эстрон (который первоначально назывался теелин, прогинон, фолликулин и кетогидроксиэстрин) и эстриол (первоначально назывался теелол и тригидроксиэстрин), которые были установлены в 1932 году на первом заседании Международной конференции по стандартизации половых гормонов в Лондоне . [89] [95] После его открытия частичный синтез эстрадиола из холестерина был разработан Инхоффеном и Хольвегом в 1940 году, а полный синтез был разработан Аннером и Мишером в 1948 году. [85]
Название эстрадиол происходит от слова эстра- , греч. οἶστρος ( oistros , буквально означает «воодушевление или вдохновение»), [96] который относится к кольцевой системе стероидов эстрана , и -диол , химический термин и суффикс, указывающий на то, что соединение представляет собой тип спирта, несущего две гидроксильные группы .
Уровни эстрадиола минимальны в первые дни фолликулярной фазы, но по мере созревания фолликула его концентрация увеличивается в общем кровообращении. Самые высокие уровни достигаются примерно за 24–48 часов до пика ЛГ. Фактически, предовуляторный пик эстрадиола представляет собой его самую высокую концентрацию в течение всего менструального цикла. Концентрации в сыворотке крови в это время обычно составляют около 130–200 пг/мл, но у некоторых женщин могут достигаться концентрации до 300–400 пг/мл. После временного снижения, связанного с овуляцией, секреция эстрадиола восстанавливается за счет продукции желтого тела во время лютеиновой фазы. Плато уровня около 100–150 пг/мл (Abraham, 1978; Thorneycroft et al., 1971) чаще всего наблюдается в период от -10 до -5 дней до начала менструации. По мере регрессии желтого тела уровень эстрадиола падает постепенно у некоторых женщин и резко у других в течение последних нескольких дней лютеиновой фазы. Это приводит к наступлению менструации и отторжению эндометрия. Уровень эстрадиола в сыворотке крови во время менструации составляет примерно 30–50 пг/мл. (Источник.)
В большинстве лабораторий уровни эстрадиола в сыворотке колеблются от 20 до 80 пг/мл в раннюю и среднюю фолликулярную фазу менструального цикла и достигают пика от 200 до 500 пг/мл во время предовуляторного всплеска. В среднелютеиновую фазу уровни эстрадиола в сыворотке колеблются от 60 до 200 пг/мл.
Уровни эстрадиола в плазме колеблются от 40 до 80 пг/мл в течение 1-й недели овариального цикла (ранняя фолликулярная фаза) и от 80 до 300 пг/мл в течение 2-й недели (средняя и поздняя фолликулярная фаза, включая периовуляторный пик). Затем в течение 3-й и 4-й недель уровень эстрадиола колеблется от 100–150 пг/мл (ранняя и средняя лютеиновая фаза) до 40 пг/мл за несколько дней до менструации (поздняя лютеиновая фаза). Средний уровень интегрированного эстрадиола в течение полного 28-дневного нормального цикла составляет около 80 пг/мл.
Середина цикла: 150–750 пг/мл.
Середина цикла: 110–330 пг/мл.
Овуляторный: 200-400 пг/мл
[...] после менопаузы уровень циркулирующего эстрадиола снижается со среднего значения в пременопаузе, составляющего 120 пг/мл, до всего лишь 13 пг/мл.
[...] [пременопаузальная] средняя концентрация [эстрадиола] 150 пг/мл [...]