Врожденные лимфоидные клетки ( ILC ) — это последнее открытое семейство врожденных иммунных клеток, происходящее из общих лимфоидных предшественников (CLP). В ответ на патогенное повреждение тканей ILC способствуют иммунитету посредством секреции сигнальных молекул и регуляции как врожденных, так и адаптивных иммунных клеток. ILC представляют собой преимущественно тканерезидентные клетки, обнаруживаемые как в лимфоидных (иммуносвязанных), так и в нелимфоидных тканях и редко в крови. Они особенно распространены на поверхности слизистых оболочек, играя ключевую роль в иммунитете слизистой оболочки и гомеостазе . Характеристики, позволяющие их дифференцировать от других иммунных клеток, включают регулярную лимфоидную морфологию , отсутствие реаранжированных антигенных рецепторов, обнаруженных на Т-клетках и В-клетках (из-за отсутствия гена RAG ), а также фенотипические маркеры, обычно присутствующие на миелоидных или дендритных клетках . [1]
На основании различий в путях развития, фенотипе и образующихся сигнальных молекулах в 2013 году ILC были разделены на три группы: 1, 2 и 3, однако после дальнейшего исследования их теперь разделили на пять групп: NK-клетки , ILC1, ILC2 , ILC3 и клетки-индукторы лимфоидной ткани (LTi). [2] ILC участвуют во многих физиологических функциях, включая тканевый гомеостаз , морфогенез , метаболизм , восстановление и регенерацию. Многие из их ролей аналогичны Т-клеткам , поэтому предполагается, что они являются врожденными аналогами Т-клеток. [3] Нарушение регуляции ILC может привести к иммунной патологии, такой как аллергия , бронхиальная астма и аутоиммунные заболевания . [4]
Развитие ILC инициируется в ответ на присутствие факторов транскрипции, которые включаются из-за присутствия факторов окружающего микроокружения, таких как цитокины , Notch-лиганды и циркадный ритм (встроенные поведенческие изменения после суточного цикла). После созревания ILC высвобождают цитокины. Таким образом, классификация ILC основана на различиях в профилях транскрипционных факторов и цитокинов, связанных с развитием и функцией различных подтипов ILC. [5]
Линии ILC1 и NK-клеток расходятся на ранних этапах своего развития и могут быть различены по их различию в зависимости от факторов транскрипции , их цитотоксичности и экспрессии их резидентных маркеров. NK-клетки представляют собой цитотоксические клетки, циркулирующие в кровотоке и убивающие инфицированные вирусом и опухолевые клетки. ILC1 представляют собой нецитотоксичные или слабоцитотоксичные тканевые резидентные клетки, функционирующие в целях защиты от инфекций, вызываемых вирусами и некоторыми бактериями .
Из-за того, что ILC1 и NK-клетки имеют как общие, так и необщие характеристики, классификация ILC1 человека является проблематичной. Оба типа клеток продуцируют IFN-γ в качестве основного цитокина и для этого требуют транскрипционного фактора T-bet . [6] Обе клетки также могут продуцировать IFN-γ, когда цитокины IL-15 или IL-12 активируются в тканях после инфекции или повреждения, и секретируют TGFβ1 в тандеме с IFN-γ при стимуляции. Это способствует ремоделированию эпителия кишечника и внеклеточного матрикса. [7] Совместная стимуляция IL-18 также значительно повышает уровни IFN-γ. [8] Высвобождение IFN-γ стимулирует макрофаги и другие мононуклеарные фагоциты , вызывая противомикробный эффект и искореняя внутриклеточные инфекции. Кислородные радикалы , вырабатываемые обоими типами клеток, также помогают искоренить инфекцию. ILC1 и NK-клетки также могут продуцировать TNF-α , внося дополнительный вклад в воспалительную реакцию, в зависимости от экспрессии их молекул.
Существуют различия в зависимости от факторов транскрипции между NK-клетками и ILC1. Хотя оба типа клеток используют T-bet для развития, было обнаружено, что NK-клетки присутствуют у хозяев с дефицитом T-bet, но ILC1 полностью зависят от его присутствия. [6] Однако развитие NK-клеток полностью зависит от присутствия транскрипционного фактора Eomes, тогда как ILC1 могут развиваться независимо от его присутствия. [6] Это означает, что Eomes обычно можно использовать в качестве маркера NK-клеток, предполагая, что зрелые NK-клетки представляют собой Tbet + Eomes +, а ILC1 представляют собой Tbet + Eomes -. [9]
ILC1 и NK-клетки имеют некоторые общие фенотипические маркеры, в том числе: NK1.1 у мышей и рецепторы NK-клеток (NCR), такие как NKp44 и NKp46, как у людей, так и у мышей. [10] [6] Они также имеют различия в фенотипических маркерах, включая экспрессию CD127 на ILC1 человека, которая присутствует не на всех NK-клетках. Кроме того, NKp80, маркер NK-клеток человека, не экспрессируется на ILC1. Было показано , что у мышей CD200R отличает NK-клетки от ILC1. [11] Отношения между линиями ILC1 и NK-клеток все еще остаются неясными из-за отсутствия этих характерных маркеров, присутствующих на некоторых клетках NK/ILC1 в определенных тканях или после определенных событий инфекции/воспаления. Это подтверждает теорию тканеспецифических функций. [10] Например, CD127 , хотя и экспрессируется большинством ILC1, отсутствует в резидентных ILC1 слюнных желез, которые также обладают способностью экспрессировать Eomes , фундаментальную особенность NK-клеток. [12]
Из-за продукции гранзимов и перфорина NK-клетки считаются врожденными аналогами цитотоксических CD8+ Т-клеток , тогда как ILC1 считаются врожденными аналогами Т-хелперных клеток из-за продукции единственного IFN-γ без цитотоксической активности. [13]
ILC2 являются резидентными в тканях и участвуют во врожденной реакции на паразитов, таких как инфекция гельминтов, помогая восстанавливать повреждения тканей. Их много в тканях кожи, [14] [15] легких, печени и кишечника. [6] [16] Они характеризуются выработкой амфирегулина и цитокинов 2 типа, включая IL-4 , IL-5 и IL-13 , в ответ на IL-25 , TSLP и IL-33 . [6] Благодаря своей цитокиновой сигнатуре они считаются врожденными аналогами клеток Th2 .
Они экспрессируют характерные поверхностные маркеры и рецепторы хемокинов , которые участвуют в распределении лимфоидных клеток по определенным участкам органов. У людей ILC2 экспрессируют CRTH2 , KLRG1 , SST2 , CD161 и CD25 . [3] У мышей ILC2 экспрессируют CD44 , но не CD161 . [3]
ILC2 для своего развития требуют IL-7 , активирующего фундаментальные факторы транскрипции RORα и GATA3 . GATA3 также необходим для поддержания функции ILC2, при этом лишение GATA3 подавляет развитие и функцию клеток.
Хотя ILC2 считаются гомогенными, их можно разделить на субпопуляции естественных ILC2 (nILC2) и воспалительных ILC2 (iILC2) в зависимости от их чувствительности к IL-33 и IL-25. [3] nILC2 — это те, которые реагируют на IL-33 в тканях, находящихся в естественном иммунном состоянии, тогда как iILC2 реагируют на IL-25 или гельминтов-паразитов. [3] nILC2 экспрессируют больше Thy1 и ST2 и снижают уровень KLRG1 . [3] iILC2 экспрессируют больше KLRG1 и снижают уровень Thy1 и ST2. [3] В дополнение к этим субпопуляциям, еще одна популяция, названная клетками ILC210, характеризуется способностью продуцировать IL-10 . [3]
ILC3 участвуют во врожденном иммунном ответе на внеклеточные бактерии и грибы. Они играют ключевую роль в гомеостазе кишечных бактерий и в регуляции ответов клеток Th17 . [17] ILC3 взрослого человека в основном обнаруживаются в собственной пластинке кишечника и миндалинах, однако они также обнаруживаются в селезенке , эндометрии , децидуальной оболочке и коже. [18]
ILC3 в своем развитии и функционировании зависят от транскрипционного фактора RORγt . [19] Они экспрессируют RORγt в ответ на IL-1β и IL-23 или патогенные сигналы. [20] IL-22 является основным цитокином, продуцируемым ILC3, и играет фундаментальную роль в поддержании гомеостаза кишечника. Однако ILC3 продуцируют множество других цитокинов, включая IL-17, IL-22, IFN-γ и GM-CSF , в зависимости от стимулов окружающей среды. [21]
Существует две подгруппы ILC3: NCR- и NCR+ ILC3, причем NCR, отображаемый на ILC3 мышей, представляет собой NKp46, по сравнению с NKp44, отображаемым на ILC3 человека. [21] NKp44+ ILC3 высоко обогащены миндалинами и кишечником, являясь исключительным источником IL-22. [21] Некоторые ILC3 могут также экспрессировать другие маркеры NK-клеток, включая NKp30 и CD56 . [22] NCR-ILC3 в основном продуцируют IL-17A и IL-17F, а при определенных обстоятельствах и IL-22. [23] NCR-ILC3 могут дифференцироваться в NCR+ при увеличении уровня экспрессии T-bet. [5] Несмотря на экспрессию маркеров NK-клеток, ILC3 сильно отличаются от NK-клеток разными путями развития и эффекторными функциями.

Клетки LTi считаются отдельной линией из-за их уникального пути развития, однако их часто считают частью группы ILC3 из-за многих схожих характеристик. Как и ILC3, клетки LTi зависят от RORγt. Они участвуют в формировании вторичных лимфатических узлов и пейеровых бляшек, способствуя развитию лимфоидной ткани, что они осуществляют посредством действия лимфотоксина , члена суперсемейства TNF . [6] Они имеют решающее значение как на эмбриональной, так и на взрослой стадии развития иммунной системы, и поэтому клетки LTi присутствуют в органах и тканях на ранних стадиях эмбрионального развития. [6] Они играют ключевую роль в организации первичной и вторичной лимфоидной ткани, а также во взрослой лимфоидной ткани, регулируя адаптивный иммунный ответ и поддерживая структуры вторичной лимфоидной ткани. [25]
Их продукцию стимулируют ретиноевая кислота , CXCL13, RANK-L и цитокины IL-1B, IL-23 и IL-6. [26] Они экспрессируют c-Kit , CCR6 , CD25 , CD127 и CD90 , однако не содержат NCR. [6] Экспрессия OX40L является еще одним хорошим маркером клеток LTi у взрослых мышей и людей. [24] Это могут быть CD4+/-. Как и ILC3, после активации клетки LTi в основном продуцируют IL-17A , IL-17F и IL-22. [23] Они опосредуются RANK, TNF , IL-17 и IL-22.
Клетки LTi индуцируют экспрессию AIRE , аутоиммунного регуляторного гена, обеспечивая развитие эмбриональных эпителиальных клеток тимуса. [24] Они делают это посредством передачи сигналов лимфотоксина α4β7 и RANK-L. [24] Клетки LTi также обеспечивают выживание CD4+ Т-клеток памяти и, следовательно, иммунных ответов памяти в вновь сформированных лимфатических узлах. [24] Они делают это через членов суперсемейства TNF OX40L и CD30L , которые передают сигнал CD4+ Т-клеткам. [24] Эту роль можно использовать для предотвращения аутоиммунитета и улучшения реакций памяти после вакцинации. [24]
Наше понимание путей, участвующих в развитии ILC, стало ясным только в последние несколько лет, при этом наши знания в основном основаны на путях мыши. [6] CLP обладают способностью дифференцироваться в ряд различных типов клеток, включая Т-клетки, B-клетки и ILC, в зависимости от присутствующих клеточных сигналов. За исключением NK-клеток, всем ILC для выживания необходима передача сигналов IL-7. Репрессор транскрипции ID2, по-видимому, противодействует дифференцировке В- и Т-клеток , образуя ID2-зависимый предшественник, который может далее дифференцироваться с помощью специфичных для линии транскрипционных факторов. [4]
ILC не зависят от гена, активирующего рекомбинацию (RAG), вместо этого они полагаются на передачу сигналов цитокинов через общую гамма-цепь цитокинов-рецепторов и путь киназы JAK3 для своего развития. [27]
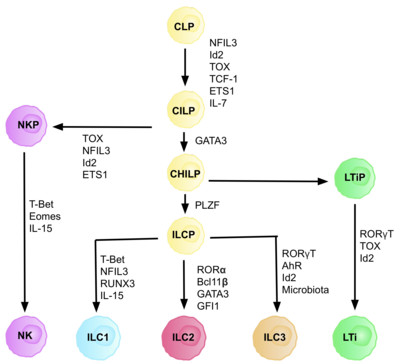
ILC происходят из общих врожденных лимфоидных предшественников (CILP), которые происходят из CLP, которые обладают способностью дифференцироваться в ряд различных типов лимфоидных клеток, включая Т- и В-клетки. [6] CILP могут затем дифференцироваться в предшественников NK-клеток (NKP) или в недавно описанные общие хелперные врожденные лимфоидные предшественники (CHILP). [6] CHILP могут затем дифференцироваться в предшественники индукторов лимфоидной ткани (LTiP) и предшественники врожденных лимфоидных клеток (ILCP). Факторы, присутствующие в микроокружении, определяют прогрессирование CLP в сторону конкретных подтипов ILC, включая лиганды notch, цитокины, циркадный ритм и экспрессию факторов транскрипции. [ нужна цитата ]
Развитие CLP в CILP и далее в ILC требует транскрипционного фактора ID2 , чтобы опосредовать подавление судьбы лимфоидных клеток, генерирующих Т- и В-клетки. [27] Это происходит за счет снижения активности факторов транскрипции E-box ( E2A , E2-2 и HEB ), имеющих решающее значение для развития B- и T-клеток. [27] Первоначально предполагалось, что ID2 необходим для того, чтобы CLP дифференцировались во все подмножества ILC, однако исследования показали, что нокаут ID2 во время развития CLP наносит вред развитию всех подмножеств ILC, кроме предшественников NK-клеток, которые не зависит от наличия Id2. [28] Благодаря этому осознанию была идентифицирована группа клон-негативных клеток (требуется любая истинная клетка-предшественник), которые полностью зависели от присутствия ID2 и экспрессировали другие ключевые маркеры ILC, с фенотипом: Lin-ID2. +IL7Ra+CD25-α4β7+, которые теперь известны как общие помощники, подобные врожденным лимфоидным предшественникам CHILP. [28] Их называют «общими хелперами» из-за их сходства с судьбами Т-хелперных эффекторных клеток.
Каждая стадия дифференцировки зависит от экспрессии различных факторов транскрипции, включая: NFIL3 , TCF-1 , ETS1 , GATA3, PLZF, T-bet, Eomes, RUNX3 , RORα, Bcl11b , Gfi1, RORγt и AhR . [6] Скоординированная экспрессия этих специфических факторов транскрипции активирует или подавляет гены-мишени, имеющие решающее значение для дифференцировки подпопуляций лимфоцитов. [27] В частности, Nfil3, экспрессия которого регулируется цитокинами, контролирует дифференцировку ILC через транскрипционные факторы Id2, RORγt, Eomes и Tox . [29] Это доказывает, что тканевые сигналы играют ключевую роль в принятии решений о судьбе в линиях ILC.
Исследования показывают, что первичным местом развития ILC является печень у плода и костный мозг у взрослых, поскольку именно здесь были обнаружены CLP, NKP и CHILP. [27] Затем клетки выходят и циркулируют в крови, пока не достигнут назначенных им тканей, кодируемых молекулами адгезии и хемокинами . [27] Однако также было показано, что созревание ILCs может происходить за пределами первичных лимфоидных тканей, подобно созреванию наивных Т-хелперных клеток.
Предшественники NK-клеток и предшественники ILC3 были обнаружены в миндалинах человека, а ILCP плода присутствуют в кишечнике мыши и накапливаются в пейеровых бляшках. [30] [31] Ретиноевая кислота, вырабатываемая многими типами клеток, такими как нервные клетки, дендритные клетки и стромальные клетки , способствует дифференцировке ILC3, а не ILC2, и необходима для их полного созревания. [27] Кроме того, AhR, который может запускаться с помощью лигандов, образующихся после катаболизма пищи, необходим для поддержания функции и экспрессии кишечных ILC3. [30]
ILCs участвуют в нашем иммунном ответе на патогены во всех органах, особенно на слизистых оболочках. [13] Они играют ключевую роль во врожденном иммунном ответе благодаря своей способности быстро секретировать иммунорегуляторные цитокины, однако они также играют роль в формировании адаптивного ответа, взаимодействуя с другими иммунными клетками. Микроокружение ткани, в которой они находятся, определяет и тонко настраивает экспрессию разнообразных профилей ILC, способствуя их взаимодействию в выполнении множества эффекторных функций.
Стратегическое расположение и глубокое укоренение ILC в тканях позволяют им поддерживать гомеостаз и, следовательно, здоровое функционирование тканей. Однако ILCs также играют вредную роль в различных участках слизистой оболочки. [32]
Поскольку функция ILCs связана с их специфической тканевой локализацией, определение сигналов, участвующих в их локализации и моделях миграции, будет иметь важное значение для выявления новых путей лечения заболеваний. [21]
Фундаментальное свойство иммунитета 2-го типа и, следовательно, клеток ILC2, заключается в борьбе с слишком крупными организмами, которые не могут быть переварены, например, с гельминтами . [33] В кишечнике в ответ на гельминтную инфекцию эпителиальные клетки секретируют высокие уровни IL-25, активируя клетки ILC2. ILC2 продуцируют IL-13, который управляет дифференцировкой дополнительных эпителиальных клеток посредством сигнальных путей Notch. Эта инструкция позволяет ремоделировать ткань для изгнания гельминта-паразита и других крупных патогенов.
IL-13 также активирует Т-клетки, вызывая дальнейшие физиологические реакции по изгнанию паразита. [34] Т-клетки стимулируют секрецию слизи бокаловидными клетками, сокращение гладких мышц и секретируют сигналы, рекрутирующие тучные клетки и эозинофилы в это место, стимулируя пролиферацию В-клеток. [34]
Инфекция может привести к повреждению тканей вследствие миграции гельминта. ILC2 играют ключевую роль в восстановлении повреждений тканей после инфекции, продуцируя лиганды, такие как AREG , для рецепторов эпителиальных факторов роста, что облегчает дифференцировку эпителиальных клеток для восстановления тканей. [6] Это может способствовать усилению барьерной функции эпителия и замедлению проникновения патогенов. [34]

Во многих тканевых нишах ILCs связаны с негематопоэтическими клетками, такими как стромальные клетки. В легких ILC2 имеют четкую локализацию в стромальных клетках, которые выделяют IL-33 и TSLP, способствуя гомеостазу ILC2 как в устойчивом состоянии, так и в ответ на инфекцию гельминтов, после того как гельминт развился в кишечнике и мигрировал. в легкие через кровь. [35]
ILC2 легких расположены близко к кровеносным сосудам, что позволяет рекрутировать эозинофилы из крови. Они также располагаются в дыхательных путях, где могут накапливаться потенциальные патогены. Это означает, что они находятся в тесном контакте с нейроэндокринными клетками , которые активируют ILC2 посредством высвобождения пептида, связанного с геном кальцитонина . [36] Другие исследования также подтверждают регуляцию функции ILC через нейронные цепи .
Кроме того, ILC1 и ILC3 выделяют кислородные радикалы и смертельно повреждающие ферменты в ответ на патогенную инфекцию, вызывая повреждение тканей хозяина. Реакции на восстановление ткани координируются иммунным ответом 2-го типа после того, как ILC3 и ILC1 очистили ткань от микробов и мусора.
Кишечные ILC подвергаются воздействию пищевых, микробных и эндогенных метаболитов. Возвращение ILC в тонкую кишку опосредовано интегрином α4β7 и рецептором CCR9. ILC2 экспрессируют CCR9 в костном мозге, поэтому могут напрямую попадать в кишечник, однако для обеспечения экспрессии CCR9 на ILC1 и ILC3 необходима ретиноевая кислота.
ILC способствуют поддержанию целостности барьера в кишечнике, защищая от различных бактерий и вирусных инфекций. ILC3 являются наиболее многочисленной субпопуляцией, присутствующей как в кишечнике взрослого, так и в кишечнике плода. [37] Распределение ILCs в кишечнике меняется в процессе развития, и они неравномерно распределяются по сегментам желудочно-кишечного тракта. Это распределение по различным нишам кишечника опосредовано различными сигнальными каскадами. [38] У человека примерно 70% кишечных ILC являются NCR+, а 15% — NCR-. [39]

ILC3 напрямую взаимодействуют с бактериальной флорой , создавая сеть между микробиотой и хозяином, способствуя гомеостазу. ILC3 ограничивают колонизацию множества вредных бактерий в кишечнике посредством секреции IL-22, стимулируя эпителиальные клетки вырабатывать антимикробные пептиды. [40] Производство IL-22 индуцируется за счет производства IL-23 и IL-1β макрофагами и ДК, что способствует заживлению слоя слизистой оболочки. [3] Например, IL-22 может способствовать восстановлению повреждений кишечника после химиотерапии или лучевой терапии . ILC3 регулируют удержание комменсальных бактерий в просвете, позволяя им подвергаться воздействию фагоцитов собственной пластинки, что приводит к праймированию Т-клеток. Хотя они могут представлять антигены через рецепторы MHC класса II , у ILC отсутствуют костимулирующие молекулы , и поэтому они играют роль в анергии Т-клеток , способствуя толерантности к полезным комменсалам. [39] Таким образом, связь между ILC3 и Т-клетками в кишечнике имеет решающее значение для поддержания гомеостаза, поскольку в отсутствие ILC3 может происходить неконтролируемая активация Т-клеток. Кроме того, микробиота играет роль в точной настройке продукции IL-22 с помощью ILC3, например, сегментированные нитчатые бактерии в подвздошной кишке регулируют выработку IL-22 и обеспечивают дифференцировку клеток Th17. [41] [42]
ILC3 взаимодействуют с кишечной нервной системой для поддержания гомеостаза кишечника, поскольку в ответ на бактерии глиальные клетки собственной пластинки секретируют нейротрофические факторы , которые через нейрорегуляторный рецептор RET индуцируют выработку IL-22 ILC3. [43] Дендритные клетки также могут продуцировать IL-23 во время стресса, вызванного патогеном, также активируя ILC3, позволяя производить IL-22. Одним из механизмов, с помощью которых IL-22 регулирует микробиоту, присутствующую в кишечнике, является механизм гликозилирования эпителиальных клеток. [44] Экспрессия IL-22 и лимфотоксина с помощью ILC3 контролирует экспрессию фукозилтрансферазы 2, которая обеспечивает фукозилирование эпителиальных клеток, обеспечивая источник питательных веществ для люминальных бактерий. [44]
Лиганды AHR из рациона или микробиоты распознаются иммунными клетками, регулируя развитие ILC и функции NK-клеток в кишечнике. В ответ на метаболиты триптофана передача сигналов AhR поддерживает экспрессию IL-22 и гомеостаз кишечника. [6] Ретиноевая кислота, продуцируемая дендритными клетками, способствует экспрессии рецепторов самонаведения кишечника на ILC1 и ILC3, а также усиливает функцию ILC3 за счет повышения регуляции RORγt и IL-22. [6] Также существует перекрестное взаимодействие между макрофагами и ILC3 через RORγt-индуцированное производство GM-CSF, которое зависит от микробной передачи сигналов, и производство IL-1β макрофагами. [39] Дефицит витамина А в пище приводит к аномально малому количеству ILC3 и, следовательно, к снижению выработки IL-22 и более высокой восприимчивости к инфекциям. И наоборот, ретиноевая кислота подавляет пролиферацию ILC2 за счет снижения регуляции IL-7Ra , а лишение витамина А, как было показано, повышает опосредованную ILC2 устойчивость к гельминтной инфекции у мышей. [39] Таким образом, ILC3 образуют сеть взаимодействий для поддержания гомеостаза кишечника между микробиомом , кишечным эпителием, нейроглиальными клетками и другими иммунными клетками.
Клетки LTi присутствуют в пейеровых бляшках и лимфоидных фолликулах , взаимодействуя с В-клетками, облегчая выработку IgA , что способствует комменсализму хозяина с местной микробиотой. [45] ILC1 и NK-клетки производят IFN-γ для борьбы с внутриклеточными патогенами. При заражении C. dificile ILC1 и ILC3 взаимодействуют для борьбы с инфекцией. [46] ILC2 индуцируют дифференцировку бокаловидных клеток и выработку слизи в кишечнике для защиты тканей от повреждения при паразитарной инфекции.
Различные группы врожденных лимфоидных клеток обладают способностью влиять на онкогенез несколькими способами. [47] [48]
ILC группы 1 представляют собой популяцию ILC с наиболее значимым противоопухолевым потенциалом, при этом NK-клетки обладают способностью распознавать недостающие MHC класса I на поверхности опухолевых клеток. [49] Таким образом, они действуют комплементарно с цитотоксическими Т-клетками, которые распознают и убивают опухолевые клетки, которые представляют чужеродный антиген в MHC класса I. [50] [51] NK-клетки экспрессируют ряд клеточных поверхностей, активирующих NK. клеточные рецепторы со специфичностью к лигандам, индуцированным стрессом, сверхэкспрессируемым на опухолевых клетках. Дополнительную информацию о NK-клетках при наблюдении за опухолями см . на странице «Естественные клетки-киллеры» .
ILC1 влияют на микроокружение опухоли путем выработки цитокинов IFN-γ и TNF-α, которые в начале иммунного ответа поляризуют другие иммунные клетки, такие как макрофаги M1 , дендритные клетки и цитотоксические Т-клетки , в этом месте, создавая воспалительную реакцию. среда. [52] В случае успеха привлечение этих клеток убьет онкогенные клетки, однако в некоторых случаях IFN-γ и TNF-α могут играть роль в индукции иммуносупрессивных иммунных клеток, таких как MDSC , и, следовательно, противовоспалительных. цитокины, создающие иммунную среду, из которой опухолевые клетки могут выйти . [53] [54] [48]
Роль ILC2 и ILC3 в наблюдении за опухолями зависит от микроокружения, встречающегося в их резидентных тканях.
ILC2 продуцируют цитокины, которые способствуют противовоспалительному иммунному ответу, например IL-13, IL-4, амфирегулин, способствующие росту опухоли. [55] Однако в некоторых случаях ILC2 могут продуцировать IL-5, стимулируя цитотоксический ответ эозинофилов и, следовательно, противоопухолевый ответ. [56] [57]
ILC3 также могут участвовать в про- или противоопухолевых средах. Производство IL-17 может поддерживать рост опухолей и метастазирование, поскольку он индуцирует проницаемость кровеносных сосудов, однако усиление экспрессии MHC класса II на их поверхности может стимулировать CD4+ Т-клетки, оказывая противоопухолевое действие. [58] Кроме того, сообщалось, что ILC3 способствуют образованию третичных лимфоидных структур при раке легких, играя защитную роль. [59]

Все подгруппы ILC присутствуют в печени и регулируют иммунный ответ, защищая ткань от вирусной и бактериальной инфекции. [60] ILC1 являются доминирующей подгруппой ILC, присутствующей в печени. Продукция ими IFN-γ способствует выживанию гепатоцитов . [61] Продукция IFN-γ ILC1 зависит от экспрессии рецептора NK-клеток CD226 . [61] Управляемое IL-12 производство IFN-γ с помощью ILC1 ускоряется внеклеточным АТФ , а IFN-γ активирует молекулы выживания Bcl-2 и Bcl-xL в гепатоцитах. [61]
NK-клетки играют роль в иммунном ответе против вирусного гепатита B и C , ограничивая фиброз печени и рак печени . Они уничтожают печеночные клетки при фиброзе печени посредством TRAIL и/или NKG2D .
ILCs играют важную роль в поддержании пищевого стресса и метаболического гомеостаза. Продукция метаболитов триптофана заставляет транскрипционный фактор AhR индуцировать экспрессию IL-22, поддерживая количество присутствующих ILC3 и, следовательно, гомеостаз кишечника. [6] Метаболит витамина А, ретиноевая кислота, также усиливает экспрессию IL-22, и, следовательно, отсутствие сигнального пути AhR и ретиноевой кислоты приводит к снижению иммунитета к бактериальным инфекциям, таким как желудочно-кишечная инфекция Citrobacter Rodentium. . [6] Ретиноевая кислота также усиливает экспрессию маркеров кишечника на ILC1 и ILC3. Таким образом, доступность пищевых питательных веществ изменяет иммунный ответ ILC на инфекцию и воспаление, подчеркивая важность сбалансированного и здорового питания.
ILC2 поддерживают иммунную среду 2-го типа в жировой ткани посредством продукции IL-5, IL-4 и IL-13. Это регулирует ожирение, резистентность к инсулину и расход калорий. [6] Нарушение этой регуляции вызывает стойкое воспаление 1 типа, приводящее к ожирению . ILC2 способствуют образованию адипоцитов и, следовательно, увеличению затрат энергии. Следовательно, снижение ответов ILC2 в тканях является характеристикой ожирения, поскольку это прерывает их решающую роль в энергетическом гомеостазе, что приводит к снижению затрат энергии и увеличению ожирения. [62] В дополнение к ILC2, ILC1 способствуют гомеостазу макрофагов жировой ткани как при худом, так и при ожирении, составляя 5-10% резидентной популяции лимфоцитов в отложениях тощей жировой ткани человека. [10] Диета с высоким содержанием жиров увеличивает количество ILC1 и активацию жировой ткани, повышая уровни IFN-γ и TNF-α. ILC1 продуцируют хемоаттрактант макрофагов CCL2, и, следовательно, передача сигналов ILC1-макрофагами является ключевым регулятором жировой ткани. [63] Этот путь может быть потенциальной мишенью для лечения пациентов с заболеваниями печени .
ILC2 способствуют пролиферации эпителиальных и бокаловидных клеток и, следовательно, выработке слизи в дыхательных путях. Эти функции способствуют восстановлению и поддержанию целостности эпителия. ILC2 обеспечивают защиту от гельминтных инфекций в легких посредством продукции AhR, IL-9 и IL-13. [64] Считается, что эти ILC2 возникают в кишечнике и мигрируют в легкие для борьбы с гельминтной инфекцией. [65]
ILC1 и NK-клетки секретируют IFN-γ в ответ на вирусную инфекцию легких, включая риновирус и респираторно-синцитиальный вирус (РСВ). [3]
ILC3 также участвуют в легочных инфекциях посредством секреции IL-17 и IL-22, например, при инфекции S. pneumoniae . Необходимы дальнейшие исследования, чтобы расшифровать роль ILC в респираторных инфекциях человека. [66]

Данные показывают, что ILC3 и ILC2 рекрутируются в поврежденную дерму как у мышей, так и у людей посредством эпидермальной передачи сигналов Notch1. [39] ILC3 секретируют IL-17F, который играет роль в иммунных и эпителиальных клеточных реакциях во время заживления ран, путем привлечения макрофагов к этому месту. Экспрессия TNF также играет роль в заживлении ран, поскольку направляет локализацию ILC3 в поврежденный эпидермис кожи. [39] В ответ на высвобождение эпидермисом IL-33 ILC2 секретируют высокие уровни амфирегулина, критического эпидермального фактора роста, тем самым способствуя заживлению кожных ран. [39]
Слизистая оболочка полости рта колонизируется комменсалами и подвергается воздействию пищевых антигенов и патогенов. ILC в слизистой оболочке полости рта помогают поддерживать барьер и защищать от инфекций. ILC3 и внутриэпителиальные ILC1 были первоначально идентифицированы в миндалинах и обнаружены в деснах человека. Примерно 10–15% лимфоцитов были идентифицированы как ILC, большинство из них продуцируют ILC1 IFN-γ. ILC3 в ротоглотке защищают от инфекции Candida albicans, продуцирующей IL-17A и IL-17F, индуцированной IL-23. Мыши, у которых отсутствуют ILC3 из-за делеции или истощения RORγt, перенесли тяжелые инфекции, вызванные Candida albicans. [67]
Было показано, что ILC могут секретировать нейротрансмиттеры и нейропептиды в легкие. ILC2 взаимодействуют с нейронами дыхательных путей благодаря близости к нервным волокнам, а резидентные ILC2, продуцирующие IL-5, обнаруживаются в богатых коллагеном регионах вблизи места слияния кровеносных сосудов среднего размера и дыхательных путей. Кроме того, ILC2, продуцирующие IL-5, обнаруживаются в легочных нейроэндокринных клетках в местах соединения ветвей дыхательных путей, где концентрируются частицы, попадающие в дыхательные пути. Локализация ILC2 в дыхательных путях позволяет предположить, что резидентность ILC2 определяется микроокружением в разных зонах ткани. [68]
Взаимодействие циркадных часов и ILC было продемонстрировано путем изучения регуляции главных часов гена Arntl. Его удаление привело к нарушению регуляции ILC3, вызванному эпигенетическими изменениями, что привело к экспрессии IL-22 и способствовало изменению микробиома, эпителиальных клеток и нарушению поглощения липидов в кишечнике. С другой стороны, удаление Nr1d1, белка, участвующего в регуляции циркадных метаболических реакций, приводило к снижению NCR+ ILC3 и увеличению продукции IL-17, но не влияло на LTi-подобный ILC3. [69]

Было подтверждено, что ILC2 играют патогенную роль при воспалении легких. Эпителиальные клетки легких экспрессируют цитокины IL-33 и IL-25, или TSLP, в ответ на различные аллергены , грибы и вирусы. Эти цитокины активируют ILC2, и, следовательно, у пациентов с аллергической астмой присутствует повышенное количество ILC2 и цитокинов типа 2 (IL-4/5/13). [3] Они секретируют IL-13, инициируя аллергическое воспаление легких, и дополнительно способствуют дифференцировке Th2, увеличивая выработку IL-13 и, следовательно, усиливая аллергический ответ. [70]
Продукция IL-5 ILC2 в легких приводит к привлечению эозинофилов, а известно, что другие популяции клеток взаимодействуют и формируют присутствие ILC2 в легких при воспалении дыхательных путей у пациентов с астмой. Кроме того, они также способствуют пролиферации В-клеток. Считается, что увеличение присутствия ILC2 коррелирует с тяжестью заболевания, и данные подтверждают, что некоторые «испытанные аллергенами» ILC2 сохраняются после разрешения первоначального воспаления, демонстрируя сходство с Т-клетками памяти. Наличие ILC2, «испытывающих аллергены», может быть причиной того, что пациенты с астмой часто становятся сенсибилизированными к различным аллергенам. [39]
Этот аллергический иммунный ответ, по-видимому, не зависит от Т- и В-клеток, причем данные подтверждают, что аллергические реакции, напоминающие астматические симптомы, могут быть вызваны у мышей, у которых отсутствуют Т- и В-клетки, с помощью IL-33. [71] [72]
Как другие ILC влияют на астму, менее ясно, однако исследования показывают корреляцию между количеством ILC3, продуцирующих IL-17, и тяжестью заболевания. На мышах было показано, что NK-клетки и ILC1 ингибируют экспансию ILC2 за счет продукции IFN-γ и, следовательно, могут помочь контролировать заболевание. Необходимы дальнейшие исследования на людях, чтобы определить, как баланс между различными подгруппами влияет на астму. [73]
NK-клетки экспрессируют множество рецепторов на клеточной поверхности, которые могут быть активирующими, ингибирующими, адгезионными, цитокиновыми или хемотаксическими. Интеграция информации, собранной с помощью этих многочисленных входных данных, позволяет NK-клеткам поддерживать аутотолерантность и распознавать сигналы стресса собственных клеток. [74] Если тонкая динамическая регуляция активации NK-клеток становится несбалансированной в пользу атаки собственных клеток, это патология аутоиммунного заболевания. Нарушение регуляции NK-клеток вовлечено в ряд аутоиммунных заболеваний, включая рассеянный склероз , системную красную волчанку и сахарный диабет I типа . [75]
Имеющиеся данные свидетельствуют о том, что нацеливание на ILC может быть полезным при разработке терапии аутоиммунных заболеваний. Поскольку ILC и Т-клетки имеют множество дублирующих функций, лучшим вариантом может быть нацеливание и нейтрализация их эффекторных цитокинов. В качестве альтернативы в качестве подхода к лечению воспалительных заболеваний можно использовать воздействие на их вышестоящие активирующие медиаторы (IL-23, IL-1B или IL-6) или их факторы выживания (IL-7). [21]

Также было обнаружено, что частота ILC2 повышена в других тканях с аллергическими симптомами, таких как полипы носа у пациентов с хроническим риносинуситом , а также у пациентов с обострением респираторного заболевания аспирином . [3] Концентрация ILC2 положительно коррелирует с тяжестью заболевания.
ILC2 активируются благодаря присутствию TSLP и IL-4, продуцируемых эпителиальными клетками и эозинофилами соответственно. Затем они производят IL-4, IL-5 и IL-13, дополнительно активируя эозинофилы в петле положительной обратной связи , способствуя воспалению. Разрыв этой петли может стать потенциальным средством лечения ринита. NK-клетки, по-видимому, играют полезную роль, их меньше у пациентов с аллергическим ринитом. [76]
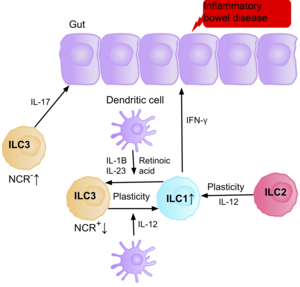
Исследования показывают, что IL-17, продуцирующий NCR-ILC3 , способствует патофизиологии ВЗК из-за их повышенного содержания в кишечнике пациентов с болезнью Крона . [39] Кроме того, количество ILC1 в слизистой оболочке кишечника у пациентов с болезнью Крона увеличивается примерно с 10% до 40% от общего числа присутствующих ILC. [39] Увеличение количества ILC коррелирует с тяжестью заболевания. Имеющиеся данные свидетельствуют о том, что пластичность между ILC3 и ILC1 в кишечнике является важным фактором болезни Крона, при этом ILC3 дифференцируются в ILC1 при воздействии IL-12, продуцируемого дендритными клетками. [39] Однако IL-23, IL-1B и ретиноевая кислота, присутствующие в кишечнике, могут стимулировать дифференцировку ILC1 обратно в ILC3. [39] Данные также свидетельствуют о способности ILC2 приобретать провоспалительный фенотип, при этом ILC2, продуцирующие IFN-γ, присутствуют в кишечнике пациентов с болезнью Крона в ответ на определенные факторы окружающей среды, такие как цитокины. [39]
Пациенты с ВЗК имеют повышенный риск развития рака кишечника из-за хронического воспаления, когда ILC3 приобретают провоспалительный фенотип ILC1 во время хронического воспаления. Поскольку ILC накапливаются в кишечнике пациентов с воспалительными заболеваниями кишечника, считается, что они могут играть протуморогенную роль. В подтверждение этого исследования показывают увеличение количества эффекторных цитокинов IL-23, IL-17 и IL-22 в микроокружении опухоли при раке кишечника. [77] [78] [79]
NK-клетки секретируют IFN-γ, обладающий противоопухолевым действием. Многочисленные исследования показывают снижение частоты присутствия NK-клеток и IFN-γ в кишечнике или периферической крови пациентов с раком кишечника. [80] [81] Необходимы дальнейшие исследования для определения их точной роли в развитии рака кишечника.
Печеночные ILC1 способствуют патогенезу хронического гепатита B за счет продукции IFN-γ и TNF-α. Нарушение эпителия, выстилающего печеночные желчные протоки, часто наблюдается в ответ на хроническое воспаление печени, а повышенная пролиферация этих протоков связана с раком печени. [60] Данные свидетельствуют о том, что усиленная пролиферация запускается IL-13, который продуцируется IL-33-индуцированной продукцией клеток ILC2. Также было показано, что ILC2 усиливают прогрессирование фиброза печени, что, в свою очередь, способствует развитию рака печени. [60]
Доступность определенных пищевых питательных веществ может влиять на иммунный гомеостаз ILC, изменяя энергию, запасаемую в жировой ткани. Жировая ткань поддерживает гомеостаз метаболизма и в настоящее время считается полностью иммунокомпетентным органом. Недоедание и обжорство могут нарушать регуляцию реакций ILC через изменения в пищевых питательных веществах, оказывая прямое влияние на энергию, запасаемую в жировой ткани. [10] Ожирение связано с изменениями желудочно-кишечной флоры, увеличением притока свободных жирных кислот из жировой ткани в печень и увеличением проницаемости кишечника. [10] Тесная анатомическая близость желудочно-кишечного тракта и печени означает, что транспорт бактериальных метаболитов через воротную вену запускает воспаление, воздействуя на клетки врожденного иммунитета, включая ILC1, поэтому играя важную роль в активации воспалительного состояния в печени. . Следовательно, воспаление, связанное с ожирением, может влиять на прогрессирование заболевания печени из-за развития резистентности к инсулину и метаболической дисрегуляции. [10] Таким образом, ILC1 являются ключевым регулятором воспаления жировой ткани и являются потенциальной терапевтической мишенью для лечения людей с заболеваниями печени или метаболическим синдромом .
ILC2 также были идентифицированы в белой жировой ткани человека и мыши , что способствует развитию ожирения. При нарушении регуляции гомеостаза в жировой ткани снижение ответов ILC2 является характеристикой ожирения, поскольку это прерывает их решающую роль в энергетическом гомеостазе, что приводит к снижению затрат энергии и увеличению ожирения. [62]
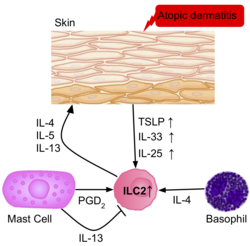
Частота ILC2 выше в воспаленной коже больных атопическим дерматитом, чем у здоровых пациентов. [39] ILC2 из кожи пациентов вызывали активацию рецепторов IL-25, IL-33, TSLP и PGD2, что указывает на их роль в активации ILC2. Базофилы и тучные клетки также присутствуют в этих поражениях кожи, продуцируя IL-4 и PGD2 , дополнительно активируя ILC2.

Псориаз , другое воспалительное заболевание кожи, вызывает утолщение эпидермиса, образуя бляшки, которые в основном населены Т-клетками и дендритными клетками. Т-клетки представляют собой иммунный ответ 1 типа; однако считается, что утолщение и воспаление эпидермиса вызваны продукцией IL-22, IL-17A и IL-17F другими Т-клетками, такими как Th17 или γδ Т-клетки . [39] Однако более поздние данные свидетельствуют о том, что ILC3 на самом деле продуцируют большое количество этих цитокинов с увеличением количества ILC3 в периферической крови пациентов с псориазом. [39]
ILC были изучены в барьерах слизистой оболочки и их взаимодействии с адаптивным иммунитетом, что позволяет предположить их причастность к аутоиммунным заболеваниям. При артрите, характеризующемся наличием аутоантител, в выработке этих антител участвуют нарушенные перекрестные помехи между Tfh и B-клетками. Интересно, что было высказано предположение, что воспалительные реакции Th17 и Tfh генерируются в желудочно-кишечном тракте и что микробиота может усиливать этот ответ. Таким образом, развитие ILC, участвующих в регуляции иммунного ответа против микробиоты кишечника, связано с артритом. В случае ILC2 играет важную роль в регуляции воспалительных реакций путем производства IL-4, IL-9 и IL-13. [82]
В случае ILC3 при рассеянном склерозе эти клетки вовлечены в третичные лимфоидные агрегаты в головном мозге пациентов с прогрессирующим заболеванием. Кроме того, увеличение LTi-подобного ILC3 коррелировало с наличием аутоантител в мозговой жидкости. [82]
Наша классификация ILC на подмножества обеспечивает упрощенную структуру, однако, несмотря на вышеуказанную систему классификации, некоторые исследования предполагают, что их развитие и фенотипическое поддержание гораздо сложнее, с высоким уровнем пластичности между подмножествами. Исследования подтвердили способность некоторых подгрупп ILC превращаться в другую подгруппу в присутствии специфических цитокинов. [13] [47] Это также общая особенность Т-клеток, и считается, что эта пластичность имеет решающее значение для того, чтобы наша иммунная система могла точно настроить ответы на такое количество различных патогенов. [13] Для пластичности ILC необходимы рецепторы цитокинов, их факторы транскрипции и доступ определенных областей хроматина к факторам транскрипции, однако до сих пор остается неясным, где эти цитокины продуцируются и где происходит дифференцировка in Vivo. [6]

ILC, присутствующие у пациентов с хронической обструктивной болезнью легких (ХОБЛ), являются типичным примером пластичности ILC. Исследования как на людях, так и на мышах показали, что резидентные ILC2 в легких приобретают фенотип ILC1 во время ХОБЛ, увеличивая секрецию IFN-γ и, следовательно, воспаление. [83] Различные триггеры, включая сигаретный дым, вызывают секрецию IL-12 и IL-18, вызывая дифференцировку ILC2 в ILC1. GATA3 регулируется вниз, а экспрессия T-bet регулируется вверх. [83] Таким образом, у пациентов наблюдается более высокое соотношение ILC1:ILC2 в крови, при этом обилие присутствующих ILC1 коррелирует с тяжестью заболевания. [83]
Способность ILC3 превращаться в ILC1-подобные клетки была показана in vitro и in vivo. [84] [85] [47] Когда ILC3 культивируются с IL-2 и IL-15, это вызывает усиление T-bet и рецептора IL-12 (IL-12R) β2, что позволяет конвертировать ILC3. к ILC1. Кроме того, исследования показывают, что IL-23 может способствовать превращению ILC1 в ILC3. [85]
Появляется все больше доказательств того, что ILC2 также обладают определенной степенью пластичности, при этом исследования подтверждают их способность превращаться в ILC1 и ILC3 при воздействии специфических стимулов окружающей среды, таких как цитокины или Notch-лиганды. [86] [47]
Передача сигналов, индуцированная цитокинами, регулирует пластичность между ILC3 и ILC1, индуцируя экспрессию T-bet. У пациентов с болезнью Крона повышение ILC1 за счет ILC3 возможно за счет продукции IL-2 Т-регуляторными клетками, что приводит к патогенному состоянию и воспалительным явлениям. Хотя пластичность является обратимой, во время дифференцировки NKp46+ ILC3 в ILC1 модуляция экспрессии T-bet зависит от IL-23, IL-2 и IL-1b и улучшается ретиноевой кислотой. Следовательно, пластичность ILC3 по отношению к ILC1 зависит от дендритных клеток, которые продуцируют эти цитокины. Хотя взаимная конверсия ILC1 и ILC3 модулируется дифференциальной экспрессией RORγt и T-bet, остаются различные вопросы, которые необходимо объяснить, чтобы понять воспаление, вызываемое этими клетками. [87]
В случае ILC2 активность Gata3 может подавляться из-за воздействия инфекционных агентов, таких как вирус гриппа, респираторно-синцитиальный вирус и Staphylococcus aureus, что приводит к увеличению экспрессии IL12Rb2, IL-18Ra и T-bet. Дифференцировка ILC2 в ILC1 также может быть обратимой, хотя механизм пока не ясен. [87]
В определенных условиях, таких как воспаление, хроническое заболевание или опухолевое микроокружение, активированные NK-клетки могут начать экспрессировать CD49a и CXCR6 , общие маркеры ILC1, усиливая их пластические свойства. [88] [89]
Определение степени пластичности ILC во время заболевания может быть полезно, чтобы позволить нам предотвратить или усилить их конверсию в другие подмножества, которые могут способствовать патогенности. [47] [90]
Исторически различие между врожденной и адаптивной иммунной системой основывалось на неспецифической природе врожденной системы и отсутствии памяти. [91] По мере появления информации о функциях NK-клеток и других ILC как эффекторов и организаторов адаптивного иммунного ответа это различие стало менее ясным. Некоторые исследователи предполагают, что в этом определении следует больше сосредоточиться на кодировании зародышевой линии рецепторов врожденной иммунной системы, а не на перестроенных рецепторах адаптивной иммунной системы. [74]