Рифампицин , также известный как рифампицин , представляет собой ансамициновый антибиотик , используемый для лечения нескольких типов бактериальных инфекций , включая туберкулез (ТБ), комплекс Mycobacterium avium , проказу и болезнь легионеров . [2] Он почти всегда используется вместе с другими антибиотиками, за двумя заметными исключениями: когда он назначается в качестве «предпочтительного лечения, которое настоятельно рекомендуется» [3] при латентной туберкулезной инфекции; и при использовании в качестве постконтактной профилактики для предотвращения Haemophilus influenzae типа b и менингококковой инфекции у людей, подвергшихся воздействию этих бактерий. [2] Прежде чем лечить человека в течение длительного периода времени, рекомендуется измерить ферменты печени и показатели крови. [2] Рифампицин можно назначать перорально или внутривенно. [2]
Общие побочные эффекты включают тошноту, рвоту, диарею и потерю аппетита. [2] Моча, пот и слезы часто окрашиваются в красный или оранжевый цвет. [2] Могут возникнуть проблемы с печенью или аллергические реакции. [2] Это часть рекомендуемого лечения активного туберкулеза во время беременности, хотя его безопасность во время беременности неизвестна. [2] Рифампицин относится к группе антибиотиков рифамицина . [2] Он работает за счет уменьшения производства РНК бактериями. [2]
Рифампицин был открыт в 1965 году, поступил на рынок в Италии в 1968 году и одобрен в США в 1971 году. [4] [5] [6] Он включен в Список основных лекарственных средств Всемирной организации здравоохранения . [7] Всемирная организация здравоохранения классифицирует рифампицин как критически важный для медицины человека препарат. [8] Он доступен в виде непатентованного лекарства . [2] Рифампицин производится почвенной бактерией Amycolatopsis rifamycinica . [6]

Рифампицин используется для лечения туберкулеза в сочетании с другими антибиотиками, такими как пиразинамид , изониазид и этамбутол . [9] Для лечения туберкулеза его вводят ежедневно в течение не менее шести месяцев. [10] Комбинированная терапия используется для предотвращения развития резистентности и сокращения продолжительности лечения. [11] Резистентность микобактерий туберкулеза к рифампицину развивается быстро, когда он используется без другого антибиотика, при этом лабораторные оценки уровня резистентности составляют от 10 -7 до 10 -10 на одну туберкулезную бактерию на поколение. [12] [13]
Рифампицин можно использовать отдельно у пациентов с латентной туберкулезной инфекцией, чтобы предотвратить или задержать развитие активного заболевания, поскольку в нем присутствует лишь небольшое количество бактерий. Кокрейновский обзор не выявил различий в эффективности между 3-4-месячным режимом лечения рифампицином и 6-месячным режимом лечения изониазидом для профилактики активного туберкулеза у пациентов, не инфицированных ВИЧ, а у пациентов, получавших рифампицин, наблюдался более низкий уровень гепатотоксичности . [14] Однако качество доказательств было признано низким. [14] Ранее рекомендовался более короткий двухмесячный курс рифампицина и пиразинамида, но он больше не рекомендуется из-за высоких показателей гепатотоксичности. [15]
Рифампицин следует принимать натощак, запивая стаканом воды. Обычно его принимают по крайней мере за час до еды или через два часа после еды. [16]
Рифампицин также используется для лечения нетуберкулезных микобактериальных инфекций, включая проказу (болезнь Хансена) и Mycobacterium kansasii . [17]
При комбинированной терапии, используемой в качестве стандартного лечения болезни Хансена, рифампицин всегда используется в сочетании с дапсоном и клофазимином , чтобы избежать развития лекарственной устойчивости. [ нужна цитата ]
Он также используется при лечении инфекций Mycobacterium elastics , связанных с язвой Бурули , обычно в сочетании с кларитромицином или другими антибиотиками. [18]
В 2008 году предварительные данные показали, что рифампицин может быть полезен при лечении метициллин-резистентного золотистого стафилококка ( MRSA ) в сочетании с другими антибиотиками, в том числе при трудно поддающихся лечению инфекциях, таких как остеомиелит и инфекции протезных суставов. [19] По состоянию на 2012 год было неясно, полезна ли комбинированная терапия рифампицином при гнойном остеомиелите позвонков. [20] Мета-анализ пришел к выводу, что добавление рифампицина к β-лактаму или ванкомицину может улучшить результаты лечения бактериемии, вызванной золотистым стафилококком. [21] Однако более недавнее исследование не выявило никакой пользы от дополнительного применения рифампицина. [22]
Он также используется в качестве профилактического лечения против инфекций Neisseria meningitidis ( менингококковых ). Рифампицин также рекомендуется в качестве альтернативного лечения инфекций, вызванных клещевыми возбудителями Borrelia burgdorferi и Anaplasma phagocytophilum, когда лечение доксициклином противопоказано, например, у беременных женщин или у пациентов с аллергией на тетрациклиновые антибиотики в анамнезе. [23] [24]
Его также иногда используют для лечения инфекций, вызванных видами Listeria , Neisseria gonorrhoeae , Haemophilus influenzae и Legionella pneumophila . При таких нестандартных показаниях перед началом терапии рифампицином следует провести тестирование на чувствительность к противомикробным препаратам (если возможно). [ нужна цитата ]
Виды Enterobacteriaceae , Acinetobacter и Pseudomonas обладают внутренней устойчивостью к рифампицину . [ нужна цитата ]
Он использовался вместе с амфотерицином B в практически безуспешных попытках лечения первичного амебного менингоэнцефалита, вызванного Naegleria fowleri . [ нужна цитата ]
Рифампицин можно использовать в качестве монотерапии в течение нескольких дней для профилактики менингита, однако при длительном лечении активных инфекций быстро развивается резистентность , поэтому препарат всегда применяют против активных инфекций в сочетании с другими антибиотиками. [25]
Рифампицин относительно неэффективен против спирохет , что привело к его использованию в качестве селективного агента, способного изолировать их из материалов, культивируемых в лабораториях. [26]
Рифампицин обладает некоторой эффективностью против вируса коровьей оспы . [27] [28]
Минимальные ингибирующие концентрации рифампицина для некоторых значимых с медицинской точки зрения патогенов составляют:
Рифампицин используется для лечения зуда , вызванного первичным билиарным холангитом . Связанные с лечением побочные эффекты включают гепатотоксичность , нефротоксичность , гемолиз и взаимодействие с другими лекарственными средствами. [31] По этим причинам, а также из-за некоторых этических проблем, связанных с использованием антибиотиков не по назначению, рифампицин как очень эффективный антибиотик для профилактики менингита не считается подходящим для лечения зуда. [32] [33] [34]
Рифампицин с клиндамицином использовался для лечения кожного заболевания гнойного гидраденита . [35]
Наиболее серьезным побочным эффектом является гепатотоксичность, и люди, получающие его, часто проходят базовые и частые тесты функции печени для выявления раннего поражения печени. [36]
Наиболее распространенные побочные эффекты включают лихорадку, желудочно-кишечные расстройства, сыпь и иммунологические реакции. Прием рифампицина обычно приводит к тому, что некоторые жидкости организма, такие как моча, пот и слезы, приобретают оранжево-красный цвет – доброкачественный побочный эффект, который, тем не менее, может быть пугающим, если его не ожидать. Это также можно использовать для мониторинга эффективности всасывания препарата (если цвет препарата не виден в моче, пациент может захотеть перенести дозу препарата дальше во времени от приема пищи или молока). Изменение цвета пота и слез не заметно непосредственно, но пот может окрасить светлую одежду в оранжевый цвет, а слезы могут навсегда испачкать мягкие контактные линзы. Поскольку рифампицин может выделяться с грудным молоком, во время его приема следует избегать грудного вскармливания. [ нужна цитата ]
Другие побочные эффекты включают в себя:
Рифампицин представляет собой поликетид , принадлежащий к химическому классу соединений, называемых ансамицинами , названным так из-за их гетероциклической структуры, содержащей нафтохиноновое ядро, охватываемое алифатической анса-цепью. Нафтохиноновый хромофор придает рифампицину характерный красно-оранжевый кристаллический цвет. [ нужна цитата ]
Критическими функциональными группами рифампицина при его ингибировании связывания бактериальной РНК-полимеразы являются четыре критические гидроксильные группы анса-мостика и нафтолового кольца, которые образуют водородные связи с аминокислотными остатками белка. [39]
Рифампицин представляет собой 3-(4-метил-1-пиперазинил)иминометильное производное рифамицина SV . [40]
Рифампицин является наиболее мощным известным индуктором ферментной системы цитохрома P450 печени , включая изоферменты CYP2B6 , CYP2C8 , CYP2C9 , CYP2C19 , CYP3A4 , CYP3A5 и CYP3A7 . [41] Он увеличивает метаболизм многих лекарств [42] и, как следствие, может сделать их менее эффективными или даже неэффективными за счет снижения их уровня. [43] Например, пациентам, проходящим длительную антикоагулянтную терапию варфарином, необходимо увеличить дозу варфарина и часто проверять время свертывания крови, поскольку несоблюдение этого требования может привести к неадекватной антикоагулянтной терапии, что приведет к серьезным последствиям тромбоэмболии. [44]
Рифампицин может снижать эффективность противозачаточных таблеток или других гормональных контрацептивов за счет индукции системы цитохрома Р450 до такой степени, что у женщин, использующих пероральные контрацептивы и принимавших рифампицин даже очень короткими курсами (например, в качестве профилактики), возникали нежелательные беременности . против заражения бактериальным менингитом). [ нужна цитата ]
Другие взаимодействия включают снижение уровня и меньшую эффективность антиретровирусных препаратов , эверолимуса , аторвастатина , росиглитазона , пиоглитазона , целекоксиба , кларитромицина , каспофунгина , вориконазола и лоразепама . [45]
Рифампицин является антагонистом микробиологического действия антибиотиков гентамицина и амикацина. Активность рифампицина против некоторых видов микобактерий может усиливаться изониазидом (за счет ингибирования синтеза миколата) [46] и амброксолом (за счет воздействия на хозяина при аутофагии и фармакокинетике). [47]
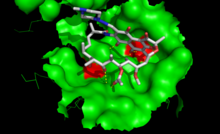
Рифампицин ингибирует бактериальный ДНК-зависимый синтез РНК путем ингибирования бактериальной ДНК-зависимой РНК-полимеразы . [48]
Данные о кристаллической структуре и биохимические данные позволяют предположить, что рифампицин связывается с карманом β-субъединицы РНК-полимеразы внутри канала ДНК/РНК, но вдали от активного центра. [39] Ингибитор предотвращает синтез РНК, физически блокируя элонгацию и, таким образом, предотвращая синтез бактериальных белков-хозяев. Посредством этого механизма «стерической окклюзии» рифампицин блокирует синтез второй или третьей фосфодиэфирной связи между нуклеотидами в основной цепи РНК, предотвращая удлинение 5'-конца транскрипта РНК более чем на 2 или 3 нуклеотида. [39] [49]
В недавнем исследовании было показано, что рифампицин связывается с редуктазой цитохрома P450 и изменяет ее конформацию, а также активность, поддерживая метаболизм прогестерона через CYP21A2 . [50]
Устойчивость к рифампицину возникает в результате мутаций, которые изменяют остатки сайта связывания рифампицина на РНК-полимеразе, что приводит к снижению сродства к рифампицину. [49] Мутации резистентности связаны с геном rpoB , кодирующим бета-субъединицу РНК-полимеразы. Большинство мутаций устойчивости у E. coli находятся в 3 кластерах на rpoB . [12] Кластер I представляет собой аминокислоты с 509 по 533, кластер II представляет собой аминокислоты с 563 по 572, а кластер III представляет собой аминокислоту 687 .
При описании мутаций rpoB у других видов обычно используют соответствующий номер аминокислоты в E. coli . У Mycobacterium Tuberculosis большинство мутаций, приводящих к устойчивости к рифампицину, находится в кластере I, в центральной области горячей точки размером 81 п.о., называемой RRDR, что означает «область, определяющая устойчивость к рифампицину». [51] Изменение аминокислоты 531 с серина на лейцин , возникающее в результате изменения последовательности ДНК TCG на TTG, является наиболее распространенной мутацией. [12] Устойчивость к туберкулезу также возникает из-за мутаций в N-концевой области rpoB и кластере III. [12]
Альтернативный механизм резистентности заключается в катализируемом Arr АДФ-рибозилировании рифампицина. С помощью фермента Arr, продуцируемого возбудителем Mycobacterium smegmatis , АДФ-рибоза добавляется к рифампицину по одной из его гидроксигрупп анса-цепи, тем самым инактивируя препарат. [52]
Микобактериальная устойчивость к рифампицину может возникать отдельно или вместе с устойчивостью к другим противотуберкулезным препаратам первого ряда. Раннее выявление такого туберкулеза с множественной лекарственной устойчивостью или широкой лекарственной устойчивостью имеет решающее значение для улучшения результатов лечения пациентов за счет введения соответствующих методов лечения второй линии, а также для снижения передачи туберкулеза с лекарственной устойчивостью. [53] Традиционные методы выявления резистентности включают посев микобактерий и тестирование на чувствительность к лекарственным средствам, результаты которых могут занять до 6 недель. Анализ Xpert MTB/RIF — это автоматизированный тест, который позволяет выявить устойчивость к рифампицину, а также диагностировать туберкулез. Кокрейновский обзор, обновленный в 2014 и 2021 годах, пришел к выводу, что для выявления устойчивости к рифампицину Xpert MTB/RIF является точным, то есть (95%) чувствительным и (98%) специфичным. [54]
При пероральном приеме рифампицин достигает максимальной концентрации в плазме примерно через 2–4 часа. 4-аминосалициловая кислота (еще один противотуберкулезный препарат) значительно снижает абсорбцию рифампицина [55] , и пиковые концентрации могут быть ниже. Если эти два препарата необходимо применять одновременно, их следует назначать раздельно с интервалом от 8 до 12 часов между приемами. [ нужна цитата ]
Рифампицин легко всасывается из желудочно- кишечного тракта; его сложноэфирная функциональная группа быстро гидролизуется в желчи и катализируется высоким pH и субстрат-специфическими эстеразами . Примерно через 6 часов практически весь препарат деацетилируется. Даже в этой деацетилированной форме рифампицин по-прежнему остается мощным антибиотиком; однако он больше не может реабсорбироваться в кишечнике и выводится из организма. Лишь около 7% введенного препарата выводится с мочой в неизмененном виде, хотя на выведение с мочой приходится лишь около 30% выведения препарата. Около 60–65% выводится с калом. [ нужна цитата ]
Период полувыведения рифампицина колеблется от 1,5 до 5,0 часов, однако при печеночной недостаточности он значительно увеличивается. Потребление пищи препятствует его всасыванию из желудочно-кишечного тракта, и препарат выводится быстрее. Когда рифампицин принимают во время еды, его максимальная концентрация в крови снижается на 36%. Антациды не влияют на его всасывание. [56] Снижения всасывания рифампицина с пищей иногда бывает достаточно, чтобы заметно повлиять на цвет мочи, который можно использовать в качестве маркера того, эффективно ли всасывается доза препарата. [ нужна цитата ]
Распределение препарата по организму высокое, эффективные концентрации достигаются во многих органах и жидкостях организма, включая спинномозговую жидкость . Поскольку само вещество красного цвета, такое высокое распределение является причиной оранжево-красного цвета слюны, слез, пота, мочи и кала. Около 60–90% препарата связывается с белками плазмы. [57]
Рифампицин ингибирует бактериальную РНК-полимеразу и обычно используется для ингибирования синтеза бактериальных белков хозяина во время экспрессии рекомбинантных белков в бактериях. РНК, кодирующая рекомбинантный ген, обычно транскрибируется с ДНК вирусной РНК-полимеразой Т7 , на которую не влияет рифампицин. [ нужна цитата ]
В 1957 году образец почвы из соснового леса на Французской Ривьере был доставлен для анализа в исследовательскую лабораторию Lepetit Pharmaceuticals в Милане , Италия. Там исследовательская группа под руководством Пьеро Сенси [58] и Марии Терезы Тимбал обнаружила новую бактерию. Этот новый вид произвел новый класс молекул с антибиотической активностью. Поскольку Сенси, Тимбал и исследователи особенно любили французскую криминальную историю «Рифифи» (о краже драгоценностей и конкурирующих бандах), [59] они решили назвать эти соединения рифамицинами . После двух лет попыток получить более стабильные полусинтетические продукты в 1965 году была получена новая молекула с высокой эффективностью и хорошей переносимостью, получившая название рифампицин. [4]
Рифампицин впервые был продан в Италии в 1968 году и был одобрен FDA в 1971 году. [4]
В августе 2020 года Управлению по контролю за продуктами и лекарствами США (FDA) стало известно о примесях нитрозаминов в некоторых образцах рифампина. [60] FDA и производители изучают происхождение этих примесей в рифампицине, а агентство разрабатывает методы тестирования для регулирующих органов и промышленности для обнаружения 1-метил-4-нитрозопиперазина (MNP). [60] МНП принадлежит к классу соединений нитрозаминов, некоторые из которых классифицируются как вероятные или возможные канцерогены для человека (вещества, которые могут вызывать рак), на основании лабораторных испытаний, таких как исследования канцерогенности на грызунах. [60] Хотя данные для прямой оценки канцерогенного потенциала МНЧ отсутствуют, имеющаяся информация о близкородственных соединениях нитрозаминов была использована для расчета пределов воздействия МНЧ на протяжении всей жизни. [60]
По состоянию на январь 2021 года FDA продолжает расследование присутствия 1-метил-4-нитрозопиперазина (MNP) в рифампине или 1-циклопентил-4-нитрозопиперазина (CPNP) в рифапентине, одобренном для продажи в США. [61]
Рифампицину присвоено МНН и ЗАПРЕЩЕНО , а рифампицину присвоено обозначение USAN . Рифампицин может обозначаться сокращенно R, RMP, RA, RF или RIF (США). [ нужна цитата ]
Рифампицин также известен как рифалдазин, [62] [63] рофакт и рифампицин в США также как рифамицин SV. [64]
Его химическое название — 5,6,9,17,19,21-гексагидрокси-23-метокси-2,4,12,16,18,20,22-гептаметил-8-[N-(4-метил-1- пиперазинил)формимидоил]-2,7-(эпоксипентадека[1,11,13]триенимино)-нафто[2,1-b]фуран-1,11(2H)-дион-21-ацетат. [ нужна цитата ]
Рифампицин доступен под многими торговыми марками по всему миру. [65]