Убиквитинлигаза (также называемая убиквитинлигазой E3 ) представляет собой белок , который рекрутирует убиквитин-конъюгирующий фермент E2 , который загружен убиквитином , распознает белковый субстрат и помогает или непосредственно катализирует перенос убиквитина от E2 к белковому субстрату. . Проще говоря, лигаза обеспечивает перемещение убиквитина от носителя убиквитина к другому объекту (субстрату) посредством некоторого механизма. Убиквитин , достигнув места назначения, в конечном итоге присоединяется изопептидной связью к остатку лизина , который является частью целевого белка. [2] Лигазы Е3 взаимодействуют как с белком-мишенью, так и с ферментом Е2 и, таким образом, придают Е2 субстратную специфичность. Обычно E3 полиубиквитинируют свой субстрат с помощью Lys48-связанных цепей убиквитина, нацеливаясь на субстрат для разрушения протеасомой . Однако возможны многие другие типы связей, которые изменяют активность, взаимодействия или локализацию белка. Убиквитинирование лигазами E3 регулирует различные области, такие как транспорт клеток, репарация ДНК и передача сигналов, и имеет огромное значение в клеточной биологии. Лигазы Е3 также играют ключевую роль в контроле клеточного цикла, опосредуя деградацию циклинов , а также белков -ингибиторов циклин-зависимых киназ . [3] Геном человека кодирует более 600 предполагаемых лигаз E3, что обеспечивает огромное разнообразие субстратов. [4]
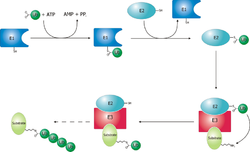
Убиквитинлигаза называется Е3 и действует совместно с ферментом, активирующим убиквитин Е1 , и ферментом, конъюгирующим убиквитин Е2 . Существует один основной фермент E1, общий для всех убиквитинлигаз, который использует АТФ для активации убиквитина для конъюгации и переноса его на фермент E2. Фермент Е2 взаимодействует со специфическим партнером Е3 и переносит убиквитин на целевой белок . Е3, который может представлять собой мультибелковый комплекс , в целом отвечает за нацеливание убиквитинирования на специфические белки -субстраты . [ нужна цитата ]
Реакция убиквитилирования протекает в три или четыре стадии в зависимости от механизма действия убиквитинлигазы Е3. На консервативном первом этапе остаток цистеина E1 атакует АТФ-активируемый С-концевой глицин на убиквитине, что приводит к образованию тиоэфирного комплекса Ub-S-E1. Энергия гидролиза АТФ и дифосфата способствует образованию этого реакционноспособного тиоэфира, а последующие этапы термонейтральны. Затем происходит реакция транстиолирования, в которой остаток цистеина Е2 атакует и заменяет Е1. Лигазы типа E3 домена HECT будут иметь еще одну реакцию транстиолирования для переноса молекулы убиквитина на E3, тогда как гораздо более распространенные лигазы типа домена RING Finger переносят убиквитин непосредственно от E2 к субстрату. [5] Последним этапом первого события убиквитилирования является атака целевого белка аминогруппы лизина, которая удаляет цистеин и образует стабильную изопептидную связь. [6] Заметным исключением из этого правила является белок p21 , который, по-видимому, убиквитилируется с использованием N-концевого амина, образуя таким образом пептидную связь с убиквитином. [7]
По оценкам, у людей имеется 500–1000 лигаз Е3, которые придают субстратную специфичность Е1 и Е2. [8] Лигазы Е3 подразделяются на четыре семейства: HECT, RING-finger, U-box и PHD-finger. [8] Лигазы E3 RING-finger являются самым большим семейством и содержат такие лигазы, как комплекс, способствующий анафазе (APC) и комплекс SCF ( белковый комплекс Skp1 - Cullin -F-box). Комплексы SCF состоят из четырех белков: Rbx1, Cul1, Skp1, которые инвариантны среди комплексов SCF, и белка F-box, который варьируется. Идентифицировано около 70 белков F-бокса человека. [9] Белки F-box содержат F-box, который связывает остальную часть комплекса SCF, и домен, связывающий субстрат, который придает E3 его субстратную специфичность. [8]

Передача сигналов убиквитина зависит от разнообразия тегов убиквитина, обеспечивающего специфичность его сообщения. Белок может быть помечен одной молекулой убиквитина (моноубиквитилирование) или множеством различных цепей молекул убиквитина (полиубиквитилирование). [11] Е3-убиквитинлигазы катализируют события полиубиквитинирования во многом так же, как и одиночный механизм убиквитинирования, используя вместо этого остаток лизина из молекулы убиквитина, присоединенный в настоящее время к белку-субстрату, для атаки С-конца новой молекулы убиквитина. [6] [11] Например, обычная метка 4-убиквитина, связанная через лизин в положении 48 (K48), привлекает меченый белок к протеасоме и последующей деградации. [11] Однако все семь остатков лизина убиквитина (K6, K11, K27, K29, K33, K48 и K63), а также N-концевой метионин используются в цепях in vivo. [11]
Моноубиквитинирование связано с путями эндоцитоза мембранных белков . Например, фосфорилирование тирозина в положении 1045 рецептора эпидермального фактора роста (EGFR) может рекрутировать лигазу E3 c-Cbl типа RING через домен SH2 . C-Cbl моноубиквитилирует EGFR, сигнализируя о его интернализации и транспортировке в лизосому. [12]
Моноубиквитинирование также может регулировать локализацию цитозольного белка. Например, лигаза E3 MDM2 убиквитилирует p53 либо для деградации (полиубиквитиновая цепь K48), либо для ядерного экспорта (монобиквитилирование). Эти события происходят в зависимости от концентрации, что позволяет предположить, что модуляция концентрации лигазы E3 является стратегией клеточной регуляции для контроля гомеостаза и локализации белка. [13]
Убиквитинлигазы являются последним и потенциально наиболее важным фактором, определяющим субстратную специфичность при убиквитинировании белков . [14] Лигазы должны одновременно отличать свой белковый субстрат от тысяч других белков в клетке , а также от других (неактивных по убиквитинированию) форм того же белка. Этого можно достичь с помощью различных механизмов, большинство из которых включают распознавание дегронов : специфических коротких аминокислотных последовательностей или химических мотивов на субстрате. [15]
Протеолитическое расщепление может привести к обнажению остатков на N-конце белка. Согласно правилу N-конца , разные N-концевые аминокислоты (или N-дегроны) распознаются в разной степени соответствующей убиквитинлигазой (N-рекогнин), что влияет на период полураспада белка . [16] Например, положительно заряженные ( Arg , Lys , His ) и объемистые гидрофобные аминокислоты ( Phe , Trp , Tyr , Leu , Ile ) распознаются преимущественно и, таким образом, считаются дестабилизирующими дегронами , поскольку они способствуют более быстрой деградации их белков. [17]

Дегрон может быть преобразован в активную форму путем посттрансляционной модификации [19] , такой как фосфорилирование остатка тирозина , серина или треонина . [20] В этом случае убиквитинлигаза распознает исключительно фосфорилированную версию субстрата благодаря стабилизации внутри сайта связывания . Например, FBW7 , единица распознавания субстрата F-box убиквитинлигазы SCF FBW7 , стабилизирует фосфорилированный субстрат путем связывания водородом его остатков аргинина с фосфатом, как показано на рисунке справа. В отсутствие фосфата остатки FBW7 отталкивают субстрат. [18]
Присутствие кислорода или других небольших молекул может влиять на распознавание дегрона. [18] Белок фон Хиппель-Линдау (VHL) (часть распознавания субстрата специфической лигазы E3), например, распознает индуцируемый гипоксией фактор альфа (HIF-α) только в нормальных условиях кислорода , когда его пролин гидроксилирован . С другой стороны, при гипоксии HIF-a не гидроксилируется, избегает убиквитинирования и, таким образом, действует в клетке в более высоких концентрациях, которые могут инициировать транскрипционный ответ на гипоксию. [21] Другим примером низкомолекулярного контроля деградации белка является фитогормон ауксин в растениях. [22] Ауксин связывается с TIR1 (домен распознавания субстрата убиквитинлигазы SCF TIR1 ), увеличивая сродство TIR1 к его субстратам ( репрессоры транскрипции : Aux/IAA) и способствуя их деградации.
Помимо распознавания аминокислот, убиквитинлигазы могут также обнаруживать необычные особенности субстратов, которые служат сигналами к их разрушению. [14] Например, San1 (антагонист Sir 1), контроль качества ядерного белка в дрожжах , имеет неупорядоченный домен связывания субстрата , что позволяет ему связываться с гидрофобными доменами неправильно свернутых белков . [14] С другой стороны, неправильно свернутые или избыточно несобранные гликопротеины пути ERAD распознаются Fbs1 и Fbs2, белками F-бокса млекопитающих лигаз E3 SCF Fbs1 и SCF Fbs2 . [23] Эти домены распознавания имеют небольшие гидрофобные карманы, позволяющие им связывать гликаны , содержащие высокое содержание маннозы .
Помимо линейных дегронов , лигаза Е3 в некоторых случаях может также распознавать структурные мотивы на субстрате. [14] В этом случае 3D-мотив может позволить субстрату напрямую связать свою биохимическую функцию с убиквитинированием . Эту связь можно продемонстрировать на примере белка TRF1 (регулятор длины теломер человека ), который распознается соответствующей ему лигазой E3 ( FBXO4 ) посредством межмолекулярного взаимодействия бета-листов . TRF1 не может быть убиквинизирован, пока он связан с теломерами, вероятно, потому, что тот же домен TRF1, который связывается с его лигазой E3, также связывается с теломерами. [14]
Убиквитинлигазы E3 регулируют гомеостаз, клеточный цикл и пути восстановления ДНК, и в результате ряд этих белков участвует в различных видах рака, включая известные MDM2, BRCA1 и опухолевый супрессор фон Хиппеля-Линдау . [24] Например, мутация MDM2 была обнаружена при раке желудка , [25] почечно-клеточной карциноме , [26] и раке печени [27] (среди прочих) для нарушения регуляции концентрации MDM2 за счет увеличения сродства его промотора к транскрипции Sp1. фактор , вызывающий усиление транскрипции мРНК MDM2. [25] Для идентификации пар убиквитинлигаза-субстрат E3 доступно несколько экспериментальных методов, основанных на протеомике, [28] таких как идентификация биотина, зависящая от близости (BioID), захват убиквитинлигазы-субстрата и тандемные убиквитин-связывающие объекты (TUBE).