

Антинуклеарные антитела ( ANA , также известные как антинуклеарный фактор или ANF ) [2] представляют собой аутоантитела , которые связываются с содержимым ядра клетки . У нормальных людей иммунная система вырабатывает антитела к чужеродным белкам ( антигенам ), но не к белкам человека ( аутоантигенам ). В некоторых случаях вырабатываются антитела к человеческим антигенам. [3]
Существует множество подтипов ANA, таких как антитела против Ro , антитела против La , антитела против Sm , антитела против nRNP , антитела против Scl-70 , антитела против дцДНК , антитела против гистонов , антитела к комплексам ядерных пор. , антицентромерные антитела и антитела против sp100 . Каждый из этих подтипов антител связывается с различными белками или белковыми комплексами внутри ядра. Они обнаруживаются при многих заболеваниях, включая аутоиммунитет , рак и инфекции , с разной распространенностью антител в зависимости от состояния. Это позволяет использовать АНА в диагностике некоторых аутоиммунных заболеваний, в том числе системной красной волчанки , синдрома Шегрена , [4] склеродермии , [5] смешанного заболевания соединительной ткани , [6] полимиозита , дерматомиозита , аутоиммунного гепатита [7] и лекарственного гепатита. индуцированная волчанка . [8]
Тест ANA обнаруживает аутоантитела, присутствующие в сыворотке крови человека . Обычными тестами, используемыми для обнаружения и количественного определения АНА, являются непрямая иммунофлуоресценция и иммуноферментный анализ (ИФА). При иммунофлуоресценции уровень аутоантител определяют в виде титра . Это наибольшее разведение сыворотки, при котором еще обнаруживаются аутоантитела. Положительные титры аутоантител в разведении, равном или превышающем 1:160, обычно считаются клинически значимыми. Положительные титры менее 1:160 наблюдаются у 20% здорового населения, особенно у пожилых людей. Хотя положительные титры 1:160 и выше тесно связаны с аутоиммунными заболеваниями, они также обнаруживаются у 5% здоровых людей. [9] [10] Скрининг аутоантител полезен при диагностике аутоиммунных заболеваний, а мониторинг уровней помогает предсказать прогрессирование заболевания. [8] [11] [12] Положительный тест на АНА редко бывает полезен, если отсутствуют другие клинические или лабораторные данные, подтверждающие диагноз. [13]
Организм человека имеет множество защитных механизмов против болезнетворных микроорганизмов , одним из которых является гуморальный иммунитет . Этот защитный механизм вырабатывает антитела (большие гликопротеины ) в ответ на иммунный стимул. Для этого процесса необходимы многие клетки иммунной системы, включая лимфоциты ( Т-клетки и В-клетки ) и антигенпредставляющие клетки . Эти клетки координируют иммунный ответ при обнаружении чужеродных белков ( антигенов ), продуцируя антитела, которые связываются с этими антигенами. В нормальной физиологии лимфоциты, распознающие человеческие белки ( аутоантигены ), либо подвергаются запрограммированной гибели клеток ( апоптоз ), либо становятся нефункциональными. Эта аутотолерантность означает, что лимфоциты не должны вызывать иммунный ответ против клеточных антигенов человека. Однако иногда этот процесс нарушается, и против человеческих антигенов вырабатываются антитела, что может привести к аутоиммунному заболеванию. [3]
АНА обнаруживаются при многих заболеваниях, а также у некоторых здоровых людей. К этим заболеваниям относятся: системная красная волчанка (СКВ), ревматоидный артрит , синдром Шегрена , склеродермия , полимиозит , дерматомиозит , первичный билиарный цирроз печени , лекарственная волчанка , аутоиммунный гепатит , рассеянный склероз , дискоидная волчанка , заболевания щитовидной железы , антифосфолипидный синдром , ювенильный идиопатический артрит , псориатический артрит , ювенильный дерматомиозит , идиопатическая тромбоцитопеническая пурпура , инфекции и рак . Эти антитела можно подразделить в зависимости от их специфичности, и каждая подгруппа имеет различную склонность к конкретным заболеваниям. [8] [14]
Экстрагируемые ядерные антигены (ENA) представляют собой группу аутоантигенов , которые первоначально были идентифицированы как мишени антител у людей с аутоиммунными заболеваниями. Их называют ЭНА, потому что их можно извлечь из ядра клетки с помощью физиологического раствора. [8] [15] ЭНА состоят из рибонуклеопротеинов и негистоновых белков, названных либо по имени донора, предоставившего прототип сыворотки (Sm, Ro, La, Jo), либо по названию заболевания, при котором обнаружены антитела (SS-A, SS-B, Scl-70). [16]

Антитела анти-Ro и анти-La , также известные как SS-A и SS-B соответственно, обычно обнаруживаются при первичном синдроме Шегрена , аутоиммунном заболевании , поражающем экзокринные железы . Наличие обоих антител обнаруживается в 30–60% случаев синдрома Шегрена, одни анти-Ro антитела обнаруживаются в 50–70% случаев синдрома Шегрена и в 30% случаев СКВ с поражением кожи, а анти-La антитела редко обнаруживаются изолированно. . [11] [17] Антитела против La также обнаруживаются при СКВ; однако обычно также присутствует синдром Шегрена. [18] Антитела против Ro также реже обнаруживаются при других заболеваниях, включая аутоиммунные заболевания печени, целиакию , аутоиммунные ревматические заболевания, сердечную неонатальную красную волчанку и полимиозит . [19] [20] Во время беременности антитела против Ro могут проникать через плаценту и вызывать блокаду сердца [21] [22] и неонатальную волчанку у младенцев. [23] При синдроме Шегрена анти-Ro и анти-La антитела коррелируют с ранним началом, увеличением продолжительности заболевания, увеличением околоушных желез , поражением вне желез и инфильтрацией желез лимфоцитами. [12] Антитела против Ro специфичны к компонентам комплекса Ro-RNP, включающего белки массой 45 кДа, 52 кДа, 54 кДа и 60 кДа и РНК . ДНК /РНК-связывающий белок массой 60 кДа и регуляторный белок Т-клеток массой 52 кДа являются наиболее охарактеризованными антигенами антител против Ro. В совокупности эти белки являются частью рибонуклеопротеинового комплекса (РНП), который связывается с Y-РНК человека hY1-hY5. La-антиген представляет собой фактор терминации транскрипции массой 48 кДа РНК-полимеразы III , который связывается с комплексом Ro-RNP. [16] [17] [24] [25]
Механизм выработки антител при синдроме Шегрена до конца не изучен, но апоптоз (запрограммированная гибель клеток) и молекулярная мимикрия могут играть определенную роль. [12] Антигены Ro и La экспрессируются на поверхности клеток, подвергающихся апоптозу, и могут вызывать воспаление внутри слюнной железы при взаимодействии с клетками иммунной системы. Антитела также можно получать посредством молекулярной мимикрии, при которой перекрестно-реактивные антитела связываются как с вирусными, так и с человеческими белками. Это может произойти с одним из антигенов, Ro или La, и впоследствии может привести к образованию антител к другим белкам посредством процесса, известного как распространение эпитопа . Ретровирусный белок gag имеет сходство с белком La и предлагается в качестве возможного примера молекулярной мимикрии при синдроме Шегрена. [12] [20]
Антитела Анти-Смита (Anti-Sm) являются очень специфичным маркером СКВ. Примерно у 99% людей без СКВ отсутствуют антитела против Sm, но только у 20% людей с СКВ они есть. Они связаны с поражением центральной нервной системы , заболеванием почек , фиброзом легких и перикардитом при СКВ, но не связаны с активностью заболевания. Антигены антител против Sm представляют собой основные единицы малых ядерных рибонуклеопротеинов (мяРНП), называемых от A до G, и связываются с мяРНП U1, U2, U4, U5 и U6. Чаще всего антитела специфичны к единицам B, B' и D. [26] [27] Молекулярные и эпидемиологические исследования показывают, что антитела против Sm могут индуцироваться молекулярной мимикрией, поскольку белок демонстрирует некоторое сходство с белками вируса Эпштейна-Барра . [28] [29]
Антитела к ядерному рибонуклеопротеину (анти-нРНП) , также известные как антитела к U1-РНП, обнаруживаются в 30–40% случаев СКВ. Их часто обнаруживают вместе с антителами против Sm, но они могут быть связаны с различными клиническими ассоциациями. Помимо СКВ, эти антитела тесно связаны со смешанными заболеваниями соединительной ткани . Антитела против нРНП распознают основные единицы А и С мяРНП и поэтому в первую очередь связываются с U1-мяРНП. [26] [30] Иммунный ответ на РНП может быть вызван презентацией ядерных компонентов на клеточной мембране в виде апоптотических пузырей. Молекулярная мимикрия также была предложена в качестве возможного механизма продукции антител к этим белкам из-за сходства между полипептидами U1-RNP и полипептидами вируса Эпштейна-Барра. [31]
Антитела против Scl-70 связаны со склеродермией . [32] Чувствительность антител к склеродермии составляет примерно 34%, но выше для случаев с диффузным поражением кожи (40%) и ниже для ограниченного поражения кожи (10%). Специфичность антител составляет 98% и 99,6% при других ревматических заболеваниях и нормальных людях соответственно. [8] [33] Помимо склеродермии, эти антитела обнаруживаются примерно у 5% больных СКВ. [34] Антигенной мишенью антител против Scl-70 является топоизомераза I. [35]
Хотя антитела против Jo-1 часто включаются в состав ANA, на самом деле они представляют собой антитела к цитоплазматическому белку, гистидил-тРНК-синтетазе – аминоацил-тРНК-синтетазе, необходимой для синтеза тРНК, нагруженной гистидином. [15] Они тесно связаны с полимиозитом и дерматомиозитом и редко встречаются при других заболеваниях соединительной ткани. Около 20–40% случаев полимиозита являются положительными по антителам Jo-1, и у большинства из них наблюдаются интерстициальные заболевания легких, маркеры HLA-DR3 и HLA-DRw52 человеческого лейкоцитарного антигена (HLA); известный под общим названием синдром Джо-1. [26] [36]

Антитела против двухцепочечной ДНК (анти-дцДНК) тесно связаны с СКВ. Они являются очень специфичным маркером заболевания, причем некоторые исследования указывают почти на 100%. [8] Данные о чувствительности колеблются от 25 до 85%. Уровни антител против дцДНК, известные как титры, коррелируют с активностью заболевания при СКВ; высокие уровни указывают на более активную волчанку. Наличие антител против дцДНК также связано с волчаночным нефритом, и есть доказательства, что они являются его причиной. Некоторые антитела против дцДНК перекрестно реагируют с другими антигенами, обнаруженными на базальной мембране клубочков (GBM) почек, такими как гепарансульфат , коллаген IV, фибронектин и ламинин . Связывание этих антигенов в почках может вызвать воспаление и фиксацию комплемента , что приводит к повреждению почек. Было показано , что наличие высокого уровня связывания ДНК и низкого уровня C3 имеет чрезвычайно высокую прогностическую ценность (94%) для диагностики СКВ. [37] Также возможно, что антитела против дцДНК интернализуются клетками, когда они связывают мембранные антигены, а затем отображаются на поверхности клетки. Это может способствовать воспалительной реакции Т-клеток в почках. Важно отметить, что не все антитела против дцДНК связаны с волчаночным нефритом и что при их отсутствии этот симптом могут вызывать и другие факторы. Антиген антител против дцДНК представляет собой двухцепочечную ДНК . [38] [39]
Антигистоновые антитела обнаруживаются в сыворотке до 75–95% людей с лекарственной волчанкой и у 75% идиопатической СКВ. В отличие от антител против дцДНК при СКВ, эти антитела не фиксируют комплемент. [ нужна цитация ] Хотя они чаще всего встречаются при лекарственной волчанке, они также обнаруживаются в некоторых случаях СКВ, склеродермии , ревматоидного артрита и недифференцированных заболеваний соединительной ткани . Известно, что многие лекарства вызывают лекарственную волчанку и образуют различные антигенные мишени внутри нуклеосомы, которые часто перекрестно реагируют с несколькими гистоновыми белками и ДНК. Прокаинамид вызывает форму лекарственной волчанки, при которой вырабатываются антитела к комплексу гистонов H2A и H2B. [40] [41]
Как антитела к гликопротеину-210 (анти-gp210), так и антитела к нуклеопорину 62 (анти-p62) представляют собой антитела к компонентам ядерной мембраны и обнаруживаются при первичном билиарном циррозе печени (ПБЦ). Каждое антитело присутствует примерно в 25–30% ПБЦ. Антигены обоих антител являются составляющими ядерной мембраны . gp210 представляет собой белок массой 200 кДа, участвующий в прикреплении компонентов ядерной поры к ядерной мембране. Антиген p62 представляет собой комплекс ядерных пор массой 60 кДа. [42] [43]
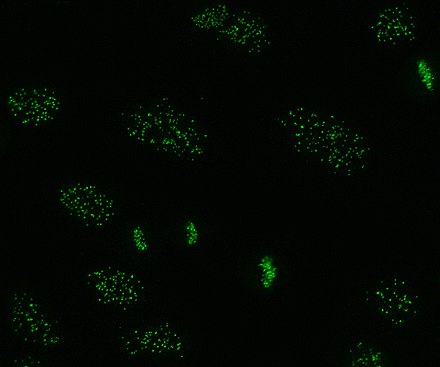
Антицентромерные антитела связаны с ограниченным кожным системным склерозом, также известным как синдром CREST , первичным билиарным циррозом печени и проксимальной склеродермией. [44] Известно шесть антигенов, все из которых связаны с центромерой ; CENP-A – CENP-F. CENP-A представляет собой белок, подобный гистону H3, массой 17 кДа . CENP-B представляет собой ДНК-связывающий белок массой 80 кДа, участвующий в сворачивании гетерохроматина . CENP-C представляет собой белок массой 140 кДа, участвующий в сборке кинетохор . CENP-D представляет собой белок массой 50 кДа с неизвестной функцией, но может быть гомологичен другому белку, участвующему в конденсации хроматина , RCC1 . CENP-E представляет собой белок массой 312 кДа из семейства моторных белков кинезина . CENP-F представляет собой белок ядерного матрикса массой 367 кДа, который связывается с кинетохорой в поздней фазе G2 во время митоза. Антитела CENP-A, B и C встречаются чаще всего (16–42% случаев системной склеродермии) и связаны с феноменом Рейно, телеангиэктазиями , поражением легких и ранним началом системной склеродермии. [33] [45] [46]
Антитела против sp100 обнаруживаются примерно в 20–30% случаев первичного билиарного цирроза печени (ПБЦ). Они обнаруживаются у немногих людей без ПБЦ и поэтому являются очень специфичным маркером заболевания. Антиген sp100 находится в ядерных тельцах; большие белковые комплексы в ядре, которые могут играть роль в росте и дифференцировке клеток. [47]
Антитела против PM-Scl обнаруживаются почти в 50% случаев синдрома перекрытия полимиозита/системной склеродермии (PM/SSc) . Около 80% людей, у которых в сыворотке крови присутствуют антитела, страдают этим заболеванием. Присутствие антител связано с ограниченным поражением кожи при синдроме перекрытия ПМ/ССД. Антигенными мишенями антител являются компоненты экзосомного комплекса РНК -процессинга в ядрышке . [33] В этот комплекс входят десять белков, и антитела к восьми из них обнаруживаются с разной частотой; PM/Scl-100 (70–80%), PM/Scl-75 (46–80%), hRrp4 (50%), hRrp42 (21%), hRrp46 (18%), hCs14 (14%), hRrp41 ( 10%) и hRrp40 (7%). [48]
Антитела против DFS70 образуют плотный мелкий пятнистый рисунок при непрямой иммунофлуоресценции и обнаруживаются в норме и при различных состояниях, но не связаны с системной аутоиммунной патологией. Следовательно, их можно использовать, чтобы исключить такие состояния у ANA-позитивных людей. У значительного числа пациентов диагностируется системная красная волчанка или недифференцированное заболевание соединительной ткани, в основном на основании положительного АНА. В случае, если определенные аутоантитела не обнаружены (например, антитела против ENA), для подтверждения диагноза рекомендуется тестирование антител против DFS70. Тесты на антитела к DFS70 доступны в виде тестов с маркировкой CE. До сих пор не существует одобренного FDA анализа. [49]


Наличие АНА в крови можно подтвердить с помощью скринингового теста. Хотя существует множество тестов для выявления АНА, наиболее распространенными тестами, используемыми для скрининга, являются непрямая иммунофлуоресценция и иммуноферментный анализ (ИФА). [50] После обнаружения ANA определяются различные подтипы. [8]
Непрямая иммунофлуоресценция является одним из наиболее часто используемых тестов на АНА. Обычно клетки HEp-2 используются в качестве субстрата для обнаружения антител в сыворотке человека. Предметные стекла микроскопа покрыты клетками HEp-2, и сыворотка инкубируется с клетками. Если указанные и нацеленные антитела присутствуют, они будут связываться с антигенами на клетках; в случае ANA антитела связываются с ядром. Их можно визуализировать, добавив античеловеческое антитело с флуоресцентной меткой (обычно FITC или родопсин B), которое связывается с антителами. Молекула будет флуоресцировать, когда на нее светит свет определенной длины волны, что можно увидеть под микроскопом. В зависимости от антитела, присутствующего в сыворотке человека, и локализации антигена в клетке, на клетках HEp-2 будут наблюдаться различные образцы флуоресценции. [51] [52] Уровни антител анализируются путем разведения сыворотки крови. Тест на АНА считается положительным, если флуоресценция наблюдается при титре 1:40/1:80. Более высокие титры более клинически значимы, поскольку низкие положительные результаты (<1:160) обнаруживаются у 20% здоровых людей, особенно у пожилых людей. Лишь около 5% здорового населения имеют титры АНА 1:160 или выше. [8] [53]

Примерно до 1975 года, когда были введены клетки HEp-2, ткани животных использовались в качестве стандартного субстрата для иммунофлуоресценции. [11] Клетки HEp-2 в настоящее время являются одним из наиболее распространенных субстратов для обнаружения ANA методом иммунофлуоресценции. [54]
Первоначально возникший штамм карциномы гортани, клеточная линия была загрязнена и вытеснена клетками HeLa , и теперь ее идентифицируют как клетки HeLa. [55]
Они превосходят ранее использовавшиеся ткани животных из-за большого размера и высокой скорости митоза (деление клеток) в клеточной линии . Это позволяет обнаруживать антитела к митоз-специфичным антигенам, например центромерные антитела. Они также позволяют идентифицировать антитела против Ro, поскольку для фиксации клеток используется ацетон (другие фиксаторы могут вымыть антиген). [56]
На клетках HEp-2 наблюдается множество моделей ядерного окрашивания: гомогенное, крапчатое, ядрышковое, ядерно-мембранозное, центромерное, ядерное точечное и плеоморфное. Гомогенная картина наблюдается при окрашивании конденсированных хромосом и интерфазного хроматина . Этот паттерн связан с антителами против дцДНК , антителами к нуклеосомным компонентам и антителами против гистонов. Есть два крапчатых узора: мелкий и грубый. Мелкий крапчатый рисунок имеет мелкое ядерное окрашивание с неокрашенным метафазным хроматином, который связан с антителами против Ro и против La. Грубая картина окрашивания имеет грубое зернистое ядерное окрашивание, вызванное антителами против U1-RNP и против Sm. Характер ядрышкового окрашивания связан со многими антителами, включая анти-Scl-70, анти-PM-Scl, анти-фибрилларин и анти-Th/To. Окрашивание ядерной мембраны проявляется в виде флуоресцентного кольца вокруг ядра клетки и вызывается антителами анти-gp210 и анти-p62. На рисунке центромеры показаны множественные ядерные точки в интерфазных и митотических клетках, что соответствует количеству хромосом в клетке. На рисунках ядерных точек в интерфазных клетках имеется от 13 до 25 ядерных точек , которые продуцируются антителами против sp100 . Плеоморфный паттерн обусловлен наличием антител к ядерному антигену пролиферирующей клетки . [26] [53] [57] [58] Было показано, что непрямая иммунофлуоресценция немного превосходит ELISA при обнаружении ANA в клетках HEp-2. [54]

Crithidia luciliae — гемофлагеллатные одноклеточные протисты . Их используют в качестве субстрата в иммунофлуоресценции для обнаружения антител против дцДНК. Они обладают органеллой , известной как кинетопласт , которая представляет собой большую митохондрию с сетью взаимосвязанных кольцевых молекул дцДНК. После инкубации с сывороткой, содержащей антитела против дцДНК и флуоресцентно-меченные античеловеческие антитела, кинетопласт будет флуоресцировать. Отсутствие других ядерных антигенов в этой органелле означает, что использование C. luciliae в качестве субстрата позволяет специфично выявлять антитела против дцДНК. [8] [59] [60]
В иммуноферментном анализе (ИФА) для обнаружения АНА используются покрытые антигеном микротитровальные планшеты . [61] Каждая лунка микротитровального планшета покрыта либо одним антигеном, либо несколькими антигенами для обнаружения специфических антител или для скрининга ANA, соответственно. Антигены происходят либо из клеточных экстрактов, либо из рекомбинантных. Сыворотка крови инкубируется в лунках планшета и отмывается. Если присутствуют антитела, связывающиеся с антигеном, они останутся после промывания. Добавляют вторичное античеловеческое антитело, конъюгированное с таким ферментом, как пероксидаза хрена . Ферментативная реакция приведет к изменению цвета раствора, пропорциональному количеству антител, связанных с антигеном. [11] [52] [62] Существуют значительные различия в обнаружении АНА с помощью иммунофлуоресценции и различных наборов ИФА, и между ними существует лишь незначительное согласие. Врач должен быть знаком с различиями, чтобы оценить результаты различных анализов. [61]
В следующей таблице указана чувствительность различных типов АНА к различным заболеваниям.
Некоторые ANA появляются при нескольких типах заболеваний, что приводит к снижению специфичности теста. Например, было показано, что IgM- ревматоидный фактор (IgM-RF) перекрестно реагирует с ANA, вызывая ложноположительную иммунофлюоресценцию . [64] Положительные ANA, а также антитела против ДНК были зарегистрированы у пациентов с аутоиммунным заболеванием щитовидной железы . [65] [66] ANA может иметь положительный результат теста у до 45% людей с аутоиммунными заболеваниями щитовидной железы или ревматоидным артритом и до 15% людей с ВИЧ или гепатитом С. [66] [67] [68] [69] По данным Lupus Foundation of America , «около 5% населения в целом будут иметь положительный ANA. Однако по крайней мере 95% людей с положительным ANA не имеют волчанка. Положительный результат теста на АНА иногда может наблюдаться в семьях, даже если у членов семьи нет признаков волчанки». [10] С другой стороны, они говорят, что хотя 95% пациентов с волчанкой на самом деле имеют положительный тест на ANA, «лишь небольшой процент имеет отрицательный ANA, и у многих из них есть другие антитела (например, антифосфолипидные антитела). , анти-Ro, анти-SSA) или их ANA, преобразованная из положительной в отрицательную под воздействием стероидов , цитотоксических препаратов или уремии (почечной недостаточности)». [10]

Клетка LE была обнаружена в костном мозге в 1948 году Харгрейвсом и соавт. [70] В 1957 г. Холборов и др. впервые продемонстрировал АНА с помощью непрямой иммунофлуоресценции. [71] Это было первым признаком того, что за СКВ ответственны процессы, затрагивающие клеточное ядро. В 1959 году было обнаружено, что сыворотка больных СКВ содержит антитела, которые осаждаются с помощью солевых экстрактов ядер, известные как экстрагируемые ядерные антигены (ЭНА). Это привело к характеристике антигенов ENA и соответствующих им антител. Так, антитела против Sm и против RNP были открыты в 1966 и 1971 годах соответственно. В 1970-х годах были открыты антитела анти-Ro/анти-SS-A и анти-La/анти-SS-B. Антитело Scl-70 было известно как специфическое антитело против склеродермии в 1979 году, однако антиген (топоизомераза-I) не был охарактеризован до 1986 года. Антиген и антитело Jo-1 были охарактеризованы в 1980 году. [8] [20]