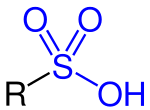
В органической химии сульфоновая кислота (или сульфоновая кислота ) относится к члену класса сероорганических соединений с общей формулой R-S(=O) 2 -OH , где R представляет собой органическую алкильную или арильную группу, а S(= О) 2 (ОН) группа сульфонилгидроксида . [1] В качестве заместителя он известен как сульфогруппа . Сульфоновую кислоту можно рассматривать как серную кислоту , в которой одна гидроксильная группа заменена органическим заместителем . Исходное соединение (с органическим заместителем, замененным водородом) представляет собой исходную сульфоновую кислоту HS (=O) 2 (OH) , таутомер сернистой кислоты S(=O)(OH) 2 . [а] Соли или эфиры сульфоновых кислот называются сульфонатами .
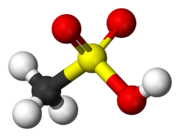
Арилсульфоновые кислоты производятся процессом сульфирования . Обычно сульфирующим агентом является триоксид серы . Широкомасштабным применением этого метода является производство алкилбензолсульфоновых кислот :
В этой реакции триоксид серы является электрофилом , а арен — нуклеофилом. Реакция является примером электрофильного ароматического замещения . [1]
Алкилсульфокислоты можно получить многими методами. При сульфоксидировании алканы облучаются смесью сернистого газа и кислорода . Эта реакция используется в промышленности для производства алкилсульфоновых кислот, которые используются в качестве поверхностно-активных веществ . [2]
Прямая реакция алканов с триоксидом серы обычно не пригодна, за исключением превращения метансульфоновой кислоты в метандисульфоновую кислоту .
Многие алкансульфокислоты можно получить присоединением бисульфита к концевым алкенам. Бисульфит также может быть алкилирован алкилгалогенидами : [2 ]
Сульфоновые кислоты можно получить окислением тиолов :
Этот путь лежит в основе биосинтеза таурина .
Многие сульфоновые кислоты получают гидролизом сульфонилгалогенидов и родственных предшественников. Таким образом, перфтороктансульфоновую кислоту получают гидролизом сульфонилфторида, который, в свою очередь, образуется в результате электрофторирования октансульфоновой кислоты. Аналогичным образом сульфонилхлорид, полученный из полиэтилена, гидролизуется до сульфоновой кислоты. Эти сульфонилхлориды производятся в результате свободнорадикальных реакций хлора, диоксида серы и углеводородов с использованием реакции Рида .
Винилсульфокислота получается гидролизом карбилсульфата ( C 2 H 4 (SO 3 ) 2 ), который, в свою очередь, получается присоединением триоксида серы к этилену .
Сульфоновые кислоты являются сильными кислотами. Обычно говорят, что они примерно в миллион раз сильнее, чем соответствующая карбоновая кислота. Например, п -толуолсульфоновая кислота и метансульфоновая кислота имеют значения p K a -2,8 и -1,9 соответственно, а бензойной кислоты и уксусной кислоты - 4,20 и 4,76 соответственно. Однако из-за их сильной кислотности значения p K a не могут быть измерены напрямую, и обычно приводимые значения следует рассматривать как косвенные оценки со значительной неопределенностью. Например, в различных источниках сообщается, что p K a метансульфоновой кислоты достигает -0,6 [3] или всего -6,5. [4] Известно, что сульфоновые кислоты реагируют с твердым хлоридом натрия ( солью ) с образованием сульфоната натрия и хлористого водорода. [5] Это свойство подразумевает кислотность в пределах двух или трех порядков от кислотности HCl (g) , чье p K a недавно было точно определено (p K a aq = -5,9). [ нужна цитата ]
Из-за своей полярности сульфоновые кислоты обычно представляют собой кристаллические твердые вещества или вязкие, высококипящие жидкости. Они также обычно бесцветны и не окисляются, [6] что делает их пригодными для использования в качестве кислотных катализаторов в органических реакциях. Их полярность в сочетании с высокой кислотностью делает сульфоновые кислоты с короткой цепью водорастворимыми, тогда как сульфоновые кислоты с более длинной цепью проявляют свойства моющих средств.
Строение сульфокислот иллюстрируется прототипом — метансульфоновой кислотой . Группа сульфоновой кислоты RSO 2 OH имеет тетраэдрический центр серы, что означает, что сера находится в центре четырех атомов: трех атомов кислорода и одного углерода. Общая геометрия серного центра напоминает форму серной кислоты .
Известны как алкил-, так и арилсульфокислоты, большинство масштабных применений связано с ароматическими производными.
Моющие средства и поверхностно-активные вещества представляют собой молекулы, которые сочетают в себе сильно неполярные и сильно полярные группы. Традиционно мыло является популярным поверхностно-активным веществом, полученным из жирных кислот . С середины 20-го века в развитых обществах использование сульфоновых кислот превзошло использование мыла. Например, ежегодно для различных целей производится около 2 миллиардов килограммов алкилбензолсульфонатов . Сульфонаты лигнина, получаемые путем сульфирования лигнина , являются компонентами буровых растворов и добавками в некоторые виды бетона . [7]
Многие, если не большая часть антрахиноновых красителей производятся или перерабатываются посредством сульфирования. [8] Сульфоновые кислоты имеют тенденцию прочно связываться с белками и углеводами . По этой причине большинство «смываемых» красителей представляют собой сульфоновые кислоты (или содержат функциональную сульфонильную группу). п-Крезидинсульфоновая кислота используется для изготовления пищевых красителей.
Будучи сильными кислотами, сульфокислоты также используются в качестве катализаторов . Простейшими примерами являются метансульфоновая кислота , CH 3 SO 2 OH и п -толуолсульфоновая кислота , которые регулярно используются в органической химии как кислоты, являющиеся липофильными (растворимыми в органических растворителях). Полимерные сульфоновые кислоты также полезны. Смола Dowex представляет собой сульфокислотное производное полистирола и используется в качестве катализаторов и для ионного обмена ( умягчения воды ). Нафион , фторированная полимерная сульфоновая кислота, является компонентом протонообменных мембран топливных элементов . [9]

Сульфамидные препараты , класс антибактериальных средств, производятся из сульфоновых кислот.
В сульфитном процессе изготовления бумаги лигнин удаляют из лигноцеллюлозы путем обработки древесной щепы растворами сульфит- и бисульфит-ионов. Эти реагенты расщепляют связи между компонентами целлюлозы и лигнина и особенно внутри самого лигнина. Лигнин превращается в лигносульфонаты , полезные иономеры , которые растворимы и могут быть отделены от целлюлозных волокон.
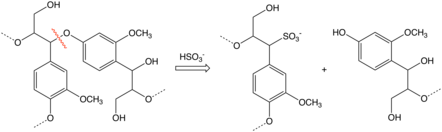
Арилсульфоновые кислоты подвержены гидролизу, обратному реакции сульфирования. Хотя бензолсульфоновая кислота гидролизуется при температуре выше 200 ° C, большинство родственных производных гидролизуются легче. Таким образом, при нагревании арилсульфоновых кислот в водной кислоте образуется исходный арен. Эта реакция используется в нескольких сценариях. В некоторых случаях сульфоновая кислота служит водорастворимой защитной группой, как показано на примере очистки пара-ксилола через его производное сульфоновой кислоты. При синтезе 2,6-дихлорфенола фенол превращается в его производное 4-сульфоновой кислоты, которое затем избирательно хлорируется в положениях, фланкирующих фенол. При гидролизе высвобождается группа сульфоновой кислоты. [10]
Сульфоновые кислоты можно превратить в сложные эфиры . Этот класс органических соединений имеет общую формулу R-SO 2 -OR. Сульфоновые эфиры, такие как метилтрифлат , считаются хорошими алкилирующими агентами в органическом синтезе . Такие сложные эфиры сульфонат часто получают алкоголизом сульфонилхлоридов :
Сульфонилгалогенидные группы возникают, когда сульфонильная функциональная группа одинарно связана с атомом галогена. Они имеют общую формулу R-SO 2 -X, где X представляет собой галогенид, обычно хлорид или фторид. Хлориды получают хлорированием сульфокислот с использованием тионилхлорида . Сульфонилфториды можно получить обработкой сульфоновых кислот тетрафторидом серы : [11]
Несмотря на свою прочность, связь (арил)C-SO 3 - может быть разорвана нуклеофильными реагентами. Историческое и непреходящее значение имеет α-сульфонирование антрохинона с последующим замещением сульфонатной группы другими нуклеофилами, которое невозможно установить напрямую. [8] Ранний метод получения фенола включал базовый гидролиз бензолсульфоната натрия , который можно легко получить из бензола. [12]
Однако условия для этой реакции суровы: для получения самой бензолсульфоновой кислоты требуется «плавленная щелочь» или расплавленный гидроксид натрия при 350 ° C. [13] В отличие от механизма конденсонно-щелочного гидролиза хлорбензола, протекающего по принципу отщепления-присоединения ( бензиновый механизм), бензолсульфокислота претерпевает аналогичную конверсию по механизму S N Ar, что выявлено при мечении 14 С, несмотря на отсутствие стабилизирующие заместители. [14] Сульфоновые кислоты с электроноакцепторными группами (например, с заместителями NO 2 или CN) подвергаются этому превращению гораздо легче.
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка )