
Аденозинтрифосфат ( АТФ ) представляет собой нуклеотид [2] , который обеспечивает энергию для управления и поддержки многих процессов в живых клетках , таких как сокращение мышц , распространение нервных импульсов , растворение конденсата и химический синтез . АТФ, обнаруженная во всех известных формах жизни , часто называют «молекулярной денежной единицей » внутриклеточной передачи энергии . [3] При потреблении в метаболических процессах он превращается либо в аденозиндифосфат (АДФ), либо в аденозинмонофосфат (АМФ). Другие процессы восстанавливают АТФ. Он также является предшественником ДНК и РНК и используется в качестве кофермента . Взрослый человек ежедневно перерабатывает около 50 кг АТФ. [4]
С точки зрения биохимии АТФ классифицируется как нуклеозидтрифосфат , что указывает на то, что она состоит из трех компонентов: азотистого основания ( аденина ), сахарной рибозы и трифосфата .
АТФ состоит из аденина , присоединенного 9-атомом азота к 1'- атому углерода сахара ( рибозы ), который, в свою очередь, присоединен к 5'-атому углерода сахара к трифосфатной группе. Во многих реакциях, связанных с обменом веществ, адениновая и сахарная группы остаются неизменными, но трифосфат превращается в ди- и монофосфат, давая соответственно производные АДФ и АМФ . Три фосфорильные группы обозначены как альфа (α), бета (β) и, для терминального фосфата, гамма (γ). [5]
В нейтральном растворе ионизированный АТФ существует в основном в виде АТФ 4- с небольшой долей АТФ 3- . [6]
Будучи полианионом и обладая потенциально хелатирующей полифосфатной группой, АТФ связывает катионы металлов с высоким сродством. Константа связывания Mg _2+есть ( 9 554 ). [7] Связывание двухвалентного катиона , почти всегда магния , сильно влияет на взаимодействие АТФ с различными белками. Благодаря силе взаимодействия АТФ-Mg2 + АТФ существует в клетке преимущественно в виде комплекса с Mg2+ .2+
связаны с фосфатными кислородными центрами. [6] [8]
Второй ион магния имеет решающее значение для связывания АТФ в киназном домене. [9] Присутствие Mg 2+ регулирует активность киназы. [10] С точки зрения мира РНК интересно, что АТФ может переносить ион Mg, который катализирует полимеризацию РНК. [ нужна цитата ]
Соли АТФ можно выделить в виде бесцветных твердых веществ. [11]

АТФ стабилен в водных растворах с pH от 6,8 до 7,4 в отсутствие катализаторов. При более экстремальных значениях pH он быстро гидролизуется до АДФ и фосфата. Живые клетки поддерживают соотношение АТФ и АДФ на уровне десяти порядков от равновесия, при этом концентрации АТФ в пять раз превышают концентрацию АДФ. [12] [13] В контексте биохимических реакций связи POP часто называют высокоэнергетическими связями . [14]
Гидролиз АТФ до АДФ и неорганического фосфата.
высвобождает 20,5 килоджоулей на моль (4,9 ккал/моль) энтальпии , однако выделение энтальпии может несколько отличаться в физиологических условиях, если реагент и продукты не находятся точно в этих состояниях ионизации. [15] Значения свободной энергии, высвобождаемой при отщеплении фосфатного (Pi ) или пирофосфатного (PPi ) звена от АТФ при стандартных концентрациях 1 моль/л при pH 7, составляют: [16]
Эти сокращенные уравнения при pH около 7 можно записать более явно (R = аденозил ):
В цитоплазматических условиях, когда соотношение АДФ/АТФ находится на 10 порядков от равновесия, ΔG составляет около -57 кДж/моль. [12]
Наряду с pH изменение свободной энергии гидролиза АТФ также связано с концентрацией Mg 2+ : от ΔG°' = -35,7 кДж/моль при нулевой концентрации Mg 2+ до ΔG°' = -31 кДж/моль при [Mg 2+ ] = 5 мМ. Более высокие концентрации Mg 2+ уменьшают свободную энергию, выделяющуюся в реакции за счет связывания ионов Mg 2+ с отрицательно заряженными атомами кислорода АТФ при pH 7. [17]
Типичная внутриклеточная концентрация АТФ может составлять 1–10 мкмоль на грамм ткани у различных эукариот. [18] Дефосфорилирование АТФ и рефосфорилирование АДФ и АМФ происходят неоднократно в ходе аэробного метаболизма. [19]
АТФ может вырабатываться рядом различных клеточных процессов; Тремя основными путями у эукариот являются (1) гликолиз , (2) цикл лимонной кислоты / окислительное фосфорилирование и (3) бета-окисление . Общий процесс окисления глюкозы до углекислого газа , комбинация путей 1 и 2, известный как клеточное дыхание , производит около 30 эквивалентов АТФ из каждой молекулы глюкозы. [20]
Производство АТФ нефотосинтезирующими аэробными эукариотами происходит главным образом в митохондриях , которые составляют около 25% объема типичной клетки. [21]
При гликолизе глюкоза и глицерин метаболизируются до пирувата . При гликолизе образуются два эквивалента АТФ посредством фосфорилирования субстрата, катализируемого двумя ферментами: фосфоглицераткиназой (PGK) и пируваткиназой . Также образуются два эквивалента никотинамидадениндинуклеотида (НАДН), которые могут окисляться через цепь переноса электронов и приводить к образованию дополнительного АТФ с помощью АТФ-синтазы . Пируват, образующийся в качестве конечного продукта гликолиза, является субстратом цикла Кребса . [22]
Гликолиз рассматривается как состоящий из двух фаз по пять стадий в каждой. На этапе 1, «подготовительной фазе», глюкоза превращается в 2-d-глицеральдегид-3-фосфат (g3p). Один АТФ вкладывается в этап 1, а другой АТФ вкладывается в этап 3. Этапы 1 и 3 гликолиза называются «этапами прайминга». На этапе 2 два эквивалента g3p превращаются в два пирувата. На этапе 7 производятся два АТФ. Кроме того, на этапе 10 производятся еще два эквивалента АТФ. На этапах 7 и 10 АТФ генерируется из АДФ. В цикле гликолиза образуется сеть из двух АТФ. Путь гликолиза позже связан с циклом лимонной кислоты, который производит дополнительные эквиваленты АТФ. [ нужна цитата ]
При гликолизе гексокиназа непосредственно ингибируется ее продуктом, глюкозо-6-фосфатом, а пируваткиназа ингибируется самой АТФ. Основной контрольной точкой гликолитического пути является фосфофруктокиназа (ФФК), которая аллостерически ингибируется высокими концентрациями АТФ и активируется высокими концентрациями АМФ. Ингибирование ПФК АТФ необычно, поскольку АТФ также является субстратом реакции, катализируемой ПФК; активная форма фермента представляет собой тетрамер , существующий в двух конформациях, только одна из которых связывает второй субстрат фруктозо-6-фосфат (F6P). Белок имеет два сайта связывания АТФ: активный сайт доступен в любой конформации белка, но связывание АТФ с сайтом-ингибитором стабилизирует конформацию, которая плохо связывает F6P. [22] Ряд других небольших молекул могут компенсировать вызванный АТФ сдвиг равновесной конформации и реактивировать ПФК, включая циклический АМФ , ионы аммония , неорганический фосфат и фруктозо-1,6- и -2,6-бифосфат. [22]
В митохондриях пируват окисляется пируватдегидрогеназным комплексом до ацетильной группы, которая полностью окисляется до углекислого газа в ходе цикла лимонной кислоты (также известного как цикл Кребса ). Каждый «виток» цикла лимонной кислоты производит две молекулы углекислого газа, один эквивалент АТФ- гуанозинтрифосфата (ГТФ) посредством фосфорилирования на уровне субстрата, катализируемого сукцинил-КоА-синтетазой , поскольку сукцинил-КоА превращается в сукцинат, три эквивалента НАДН. и один эквивалент FADH 2 . НАДН и ФАДН 2 перерабатываются (в НАД + и ФАД соответственно) путем окислительного фосфорилирования , генерируя дополнительный АТФ. Окисление НАДН приводит к синтезу 2–3 эквивалентов АТФ, а окисление одного ФАДН 2 дает 1–2 эквивалента АТФ. [20] Большая часть клеточного АТФ вырабатывается в результате этого процесса. Хотя сам цикл лимонной кислоты не включает молекулярный кислород , это обязательно аэробный процесс, поскольку O 2 используется для переработки НАДН и ФАДН 2 . При отсутствии кислорода цикл лимонной кислоты прекращается. [21]
Генерация АТФ митохондриями из цитозольного НАДН осуществляется за счет малат-аспартатного челнока (и в меньшей степени глицерин-фосфатного челнока ), поскольку внутренняя мембрана митохондрий непроницаема для НАДН и НАД + . Вместо переноса образовавшегося НАДН фермент малатдегидрогеназа превращает оксалоацетат в малат , который перемещается в митохондриальный матрикс. Другая реакция, катализируемая малатдегидрогеназой, происходит в противоположном направлении, образуя оксалоацетат и НАДН из вновь транспортированного малата и внутренних запасов НАД + в митохондриях . Трансаминаза превращает оксалоацетат в аспартат для транспортировки обратно через мембрану в межмембранное пространство. [21]
При окислительном фосфорилировании прохождение электронов от НАДН и ФАДН 2 через цепь переноса электронов высвобождает энергию для перекачки протонов из митохондриального матрикса в межмембранное пространство. Эта накачка генерирует движущую силу протонов , которая является итоговым эффектом градиента pH и градиента электрического потенциала на внутренней митохондриальной мембране. Поток протонов вниз по этому градиенту потенциала, то есть из межмембранного пространства в матрикс, дает АТФ с помощью АТФ-синтазы. [23] За ход производится три АТФ.
Хотя потребление кислорода является фундаментальным для поддержания движущей силы протонов, в случае нехватки кислорода ( гипоксии ) внутриклеточный ацидоз (опосредованный повышенными скоростями гликолиза и гидролизом АТФ ) способствует увеличению мембранного потенциала митохондрий и непосредственно управляет синтезом АТФ. [24]
Большая часть АТФ, синтезируемая в митохондриях, будет использована для клеточных процессов в цитозоле; таким образом, он должен быть экспортирован из места синтеза в митохондриальном матриксе. Движению АТФ наружу благоприятствует электрохимический потенциал мембраны, поскольку цитозоль имеет относительно положительный заряд по сравнению с относительно отрицательным матриксом. Каждый вывезенный АТФ стоит 1 H + . Производство одной АТФ обходится примерно в 3 Н + . Следовательно, для производства и экспорта одного АТФ требуется 4Н +. Внутренняя мембрана содержит антипортер , транслоказу АДФ/АТФ, который представляет собой интегральный мембранный белок, используемый для обмена вновь синтезированного АТФ в матриксе на АДФ в межмембранном пространстве. [25] Эта транслоказа управляется мембранным потенциалом, поскольку она приводит к перемещению около 4 отрицательных зарядов через митохондриальную мембрану в обмен на 3 отрицательных заряда, перемещенных внутрь. Однако транспортировать фосфат в митохондрии также необходимо; фосфатный носитель перемещает протон с каждым фосфатом, частично рассеивая протонный градиент. После завершения гликолиза, цикла лимонной кислоты, цепи переноса электронов и окислительного фосфорилирования на одну глюкозу образуется примерно 30–38 молекул АТФ. [ нужна цитата ]
Цикл лимонной кислоты регулируется главным образом наличием ключевых субстратов, в частности соотношением НАД + и НАДН, а также концентрацией кальция , неорганического фосфата, АТФ, АДФ и АМФ. Цитрат – ион, давший название циклу – является ингибитором цитратсинтазы по принципу обратной связи , а также ингибирует ПФК, обеспечивая прямую связь между регуляцией цикла лимонной кислоты и гликолизом. [22]
В присутствии воздуха и различных кофакторов и ферментов жирные кислоты превращаются в ацетил-КоА . Этот путь называется бета-окислением . Каждый цикл бета-окисления укорачивает цепь жирной кислоты на два атома углерода и производит по одному эквиваленту ацетил-КоА, НАДН и ФАДН 2 . Ацетил-КоА метаболизируется в цикле лимонной кислоты с образованием АТФ, тогда как НАДН и ФАДН 2 используются в результате окислительного фосфорилирования для образования АТФ. Десятки эквивалентов АТФ образуются в результате бета-окисления одной длинной ацильной цепи. [26]
При окислительном фосфорилировании ключевым контрольным моментом является реакция, катализируемая цитохром-с-оксидазой , которая регулируется наличием ее субстрата – восстановленной формы цитохрома-с . Количество доступного восстановленного цитохрома с напрямую связано с количеством других субстратов:
из которого непосредственно следует это уравнение:
Таким образом, высокое соотношение [НАДН] к [НАД + ] или высокое соотношение [АДФ] [P i ] к [АТФ] подразумевает большое количество восстановленного цитохрома с и высокий уровень активности цитохром с оксидазы. [22] Дополнительный уровень регуляции обеспечивается скоростью транспорта АТФ и НАДН между митохондриальным матриксом и цитоплазмой. [25]
Кетоновые тела можно использовать в качестве топлива, образуя 22 молекулы АТФ и 2 молекулы ГТФ на молекулу ацетоацетата при окислении в митохондриях. Кетоновые тела транспортируются из печени в другие ткани, где ацетоацетат и бета -гидроксибутират могут быть повторно преобразованы в ацетил-КоА с образованием восстанавливающих эквивалентов (НАДН и ФАДН 2 ) посредством цикла лимонной кислоты. Кетоновые тела не могут использоваться печенью в качестве топлива, поскольку в печени отсутствует фермент β-кетоацил-КоА-трансфераза, также называемый тиолазой . Ацетоацетат в низких концентрациях поглощается печенью и подвергается детоксикации по метилглиоксальному пути, который заканчивается лактатом. Ацетоацетат в высоких концентрациях поглощается клетками, отличными от клеток печени, и поступает другим путем через 1,2-пропандиол . Хотя этот путь проходит через другую серию этапов, требующих АТФ, 1,2-пропандиол можно превратить в пируват. [27]
Брожение – это обмен органических соединений в отсутствие воздуха. Он включает фосфорилирование на уровне субстрата при отсутствии дыхательной цепи транспорта электронов . Уравнение реакции глюкозы с образованием молочной кислоты :
Анаэробное дыхание – это дыхание в отсутствие О.2. Прокариоты могут использовать множество акцепторов электронов. К ним относятся нитраты , сульфаты и углекислый газ.
АТФ также может быть синтезирован посредством нескольких так называемых реакций «пополнения», катализируемых семейством ферментов нуклеозиддифосфаткиназ (NDK), которые используют другие нуклеозидтрифосфаты в качестве высокоэнергетического донора фосфата, и семейством АТФ:гуанидо-фосфотрансферазы . [ нужна цитата ]
У растений АТФ синтезируется в тилакоидной мембране хлоропласта . Этот процесс называется фотофосфорилированием . «Машина» аналогична таковой в митохондриях, за исключением того, что энергия света используется для перекачки протонов через мембрану и создания протондвижущей силы. Затем происходит АТФ-синтаза точно так же, как при окислительном фосфорилировании. [28] Некоторая часть АТФ, вырабатываемого в хлоропластах, потребляется в цикле Кальвина , в результате которого образуются триозные сахара.
Общее количество АТФ в организме человека составляет около 0,1 моль/л . [29] Большая часть АТФ перерабатывается из АДФ в результате вышеупомянутых процессов. Таким образом, в любой момент времени общее количество АТФ + АДФ остается довольно постоянным.
Энергия, используемая клетками человека у взрослого человека, требует ежедневного гидролиза от 100 до 150 моль/л АТФ, а это означает, что человек обычно использует количество АТФ, соответствующее весу его тела, в течение дня. [30] Каждый эквивалент АТФ перерабатывается 1000–1500 раз в течение одного дня ( 150/0,1 = 1500 ), [29] примерно со скоростью 9×10 20 молекул/с. [29]
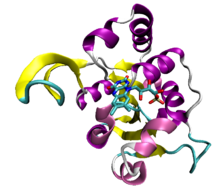
АТФ участвует в передаче сигнала , служа субстратом для киназ — ферментов, переносящих фосфатные группы. Киназы являются наиболее распространенными АТФ-связывающими белками. У них есть небольшое количество общих складок. [31] Фосфорилирование белка киназой может активировать каскад, такой как митоген-активируемый протеинкиназный каскад. [32]
АТФ также является субстратом аденилатциклазы , чаще всего в путях передачи сигнала рецептора, связанного с G-белком , и трансформируется во второй мессенджер , циклический АМФ, который участвует в запуске сигналов кальция путем высвобождения кальция из внутриклеточных запасов. [33] Эта форма передачи сигнала особенно важна для функции мозга, хотя она участвует в регуляции множества других клеточных процессов. [34]
АТФ — один из четырех мономеров, необходимых для синтеза РНК . Процессу способствуют РНК-полимеразы . [35] Аналогичный процесс происходит при образовании ДНК, за исключением того, что АТФ сначала преобразуется в дезоксирибонуклеотид dATP. Как и многие реакции конденсации в природе, репликация и транскрипция ДНК также потребляют АТФ.
Ферменты аминоацил-тРНК- синтетазы потребляют АТФ в месте прикрепления тРНК к аминокислотам, образуя комплексы аминоацил-тРНК. Аминоацилтрансфераза связывает АМФ-аминокислоту с тРНК. Реакция сочетания протекает в две стадии:
Аминокислота связана с предпоследним нуклеотидом на 3'-конце тРНК (буква А в последовательности CCA) посредством сложноэфирной связи (перевернутая на иллюстрации).
Транспортировка химических веществ из клетки против градиента часто связана с гидролизом АТФ. Транспорт осуществляется АТФ-связывающими кассетными переносчиками . Геном человека кодирует 48 транспортеров ABC, которые используются для экспорта лекарств, липидов и других соединений. [36]
Клетки секретируют АТФ для связи с другими клетками в процессе, называемом пуринергической передачей сигналов . АТФ служит нейротрансмиттером во многих частях нервной системы, модулирует биение ресничек, влияет на снабжение сосудов кислородом и т. д. АТФ либо секретируется непосредственно через клеточную мембрану через канальные белки [37] [38] , либо перекачивается в пузырьки [39] , которые затем сливаются с мембраной. Клетки обнаруживают АТФ с помощью белков- пуринергических рецепторов P2X и P2Y.
Недавно было предложено действовать как биологический гидротроп АТФ [40] и было показано, что он влияет на растворимость во всем протеоме. [41]
Ацетилфосфат (AcP), предшественник АТФ, может быть легко синтезирован с умеренными выходами из тиоацетата при pH 7 и 20 °C и pH 8 и 50 °C, хотя ацетилфосфат менее стабилен при более высоких температурах и щелочных условиях, чем в более холодных условиях. и от кислой до нейтральной среды. Однако он не способен способствовать полимеризации рибонуклеотидов и аминокислот и способен только к фосфорилированию органических соединений. Было показано, что он может способствовать агрегации и стабилизации АМФ в присутствии Na + , агрегация нуклеотидов может способствовать полимеризации выше 75°C, однако она может происходить только в отсутствие Na + . Возможно, что полимеризация, стимулируемая AcP, может происходить на минеральных поверхностях. [42] Было показано, что АДФ может фосфорилироваться до АТФ только с помощью AcP, а другие нуклеозидтрифосфаты не фосфорилируются с помощью AcP. Это может объяснить, почему все формы жизни используют АТФ для запуска биохимических реакций. [43]
Биохимические лаборатории часто используют исследования in vitro для изучения АТФ-зависимых молекулярных процессов. Аналоги АТФ также используются в рентгеновской кристаллографии для определения структуры белка в комплексе с АТФ, часто вместе с другими субстратами. [ нужна цитата ]
Ингибиторы АТФ-зависимых ферментов, такие как киназы , необходимы для изучения сайтов связывания и переходных состояний , участвующих в АТФ-зависимых реакциях. [ нужна цитата ]
Большинство полезных аналогов АТФ не могут подвергаться гидролизу, как это происходит с АТФ; вместо этого они удерживают фермент в структуре, тесно связанной с АТФ-связанным состоянием. Аденозин-5'-(γ-тиотрифосфат) представляет собой чрезвычайно распространенный аналог АТФ, в котором один из атомов кислорода гамма-фосфата заменен атомом серы ; этот анион гидролизуется значительно медленнее, чем сам АТФ, и действует как ингибитор АТФ-зависимых процессов. В кристаллографических исследованиях переходные состояния гидролиза моделируются связанным ионом ванадата .
Следует с осторожностью интерпретировать результаты экспериментов с аналогами АТФ, поскольку некоторые ферменты могут гидролизовать их с заметной скоростью при высоких концентрациях. [44]
АТФ используется внутривенно при некоторых заболеваниях сердца. [45]
АТФ была открыта в 1929 году Карлом Ломанном [46] и Ендрассиком [47] и независимо Сайрусом Фиске и Йеллапрагадой Субба Рао из Гарвардской медицинской школы [48] . Обе команды соревновались друг с другом в поиске метода определения фосфора.
Фриц Альберт Липманн в 1941 году предположил, что он является посредником между энерговыделяющими и энергозатратными реакциями в клетках. [49]
Впервые он был синтезирован в лаборатории Александром Тоддом в 1948 году [50] , частично за эту работу он был удостоен Нобелевской премии по химии в 1957 году.
Нобелевская премия по химии 1978 года была присуждена Питеру Деннису Митчеллу за открытие хемиосмотического механизма синтеза АТФ.
Нобелевская премия по химии 1997 года была разделена: половина совместно Пола Д. Бойера и Джона Э. Уокера «за объяснение ферментативного механизма, лежащего в основе синтеза аденозинтрифосфата (АТФ)», а другая половина — Йенса К. Скоу . за первое открытие фермента, переносящего ионы, Na + , K + -АТФазы». [51]