Атом – основная частица химических элементов . Атом состоит из ядра , состоящего из протонов и обычно нейтронов , окруженного электромагнитно связанным роем электронов . Химические элементы отличаются друг от друга количеством протонов, находящихся в их атомах. Например, любой атом, содержащий 11 протонов, — это натрий , а любой атом, содержащий 29 протонов, — медь . Атомы с одинаковым числом протонов, но разным числом нейтронов называются изотопами одного и того же элемента.
Атомы чрезвычайно малы, обычно около 100 пикометров в поперечнике. Человеческий волос имеет ширину около миллиона атомов углерода. Это меньше, чем самая короткая длина волны видимого света, а это означает, что люди не могут видеть атомы в обычные микроскопы. Атомы настолько малы, что точно предсказать их поведение с помощью классической физики невозможно из-за квантовых эффектов .
Более 99,94% массы атома находится в ядре. Протоны имеют положительный электрический заряд , а нейтроны не имеют заряда, поэтому ядро заряжено положительно. Электроны заряжены отрицательно, и именно этот противоположный заряд связывает их с ядром. Если числа протонов и электронов равны, как это обычно бывает, то атом в целом электрически нейтрален. Если в атоме больше электронов, чем протонов, то он имеет общий отрицательный заряд и называется отрицательным ионом (или анионом). И наоборот, если у него больше протонов, чем электронов, он имеет положительный заряд и называется положительным ионом (или катионом).
Электроны атома притягиваются к протонам атомного ядра электромагнитной силой . Протоны и нейтроны в ядре притягиваются друг к другу ядерной силой . Эта сила обычно сильнее электромагнитной силы, которая отталкивает положительно заряженные протоны друг от друга. При определенных обстоятельствах отталкивающая электромагнитная сила становится сильнее ядерной силы. В этом случае ядро распадается и оставляет после себя разные элементы . Это форма ядерного распада .
Атомы могут присоединяться к одному или нескольким другим атомам химическими связями, образуя химические соединения , такие как молекулы или кристаллы . Способность атомов присоединяться и отделяться друг от друга ответственна за большинство физических изменений, наблюдаемых в природе. Химия – наука, изучающая эти изменения.
Основная идея о том, что материя состоит из мельчайших неделимых частиц, — это старая идея, появившаяся во многих древних культурах. Слово « атом» происходит от древнегреческого слова «атомос» , [а] , что означает «неразрезаемый». Эта древняя идея была основана на философских рассуждениях, а не на научных рассуждениях. Современная теория атома не основана на этих старых концепциях. [1] [2] В начале 19 века учёный Джон Дальтон заметил, что химические вещества, по-видимому, объединяются друг с другом в дискретных и последовательных единицах веса, и он решил использовать слово « атом» для обозначения этих единиц. [3]

В начале 1800-х годов английский химик Джон Дальтон обобщил экспериментальные данные, собранные им и другими учеными, и открыл закономерность, ныне известную как « закон множественных пропорций ». Он заметил, что в химических соединениях, содержащих два конкретных химических элемента, содержание элемента А на единицу элемента Б будет различаться в этих соединениях на небольшие целые числа. Эта закономерность предполагала, что элементы объединяются друг с другом посредством дискретных единиц веса, и Дальтон решил назвать эти единицы «атомами». [4]
Например, существует два типа оксида олова : один представляет собой серый порошок, состоящий из 88,1% олова и 11,9% кислорода, а другой — белый порошок, состоящий из 78,7% олова и 21,3% кислорода. Поправляя эти цифры, в сером порошке на каждые 100 г олова приходится около 13,5 г кислорода, а в белом порошке — около 27 г кислорода на каждые 100 г олова. 13,5 и 27 образуют соотношение 1:2. Дальтон пришел к выводу, что в этих оксидах на каждый атом олова приходится соответственно один или два атома кислорода ( SnO и SnO 2 ). [5] [6]
Дальтон также проанализировал оксиды железа . Существует один тип оксида железа — черный порошок, состоящий из 78,1% железа и 21,9% кислорода; и есть еще один оксид железа, представляющий собой красный порошок, состоящий на 70,4% из железа и на 29,6% из кислорода. Поправляя эти цифры, в черном порохе на каждые 100 г железа приходится около 28 г кислорода, а в красном порохе — около 42 г кислорода на каждые 100 г железа. 28 и 42 образуют соотношение 2:3. Дальтон пришел к выводу, что в этих оксидах на каждые два атома железа приходится соответственно два или три атома кислорода ( Fe 2 O 2 и Fe 2 O 3 ). [б] [7] [8]
Последний пример: закись азота состоит из 63,3% азота и 36,7% кислорода, оксид азота — 44,05% азота и 55,95% кислорода, а диоксид азота — 29,5% азота и 70,5% кислорода. Скорректировав эти цифры, в закиси азота на каждые 140 г азота приходится 80 г кислорода, в оксиде азота — около 160 г кислорода на каждые 140 г азота, а в диоксиде азота — 320 г кислорода на каждые 140 г. г азота. 80, 160 и 320 образуют соотношение 1:2:4. Соответствующие формулы этих оксидов: N 2 O , NO и NO 2 . [9] [10]
Ученые обнаружили, что некоторые вещества имеют одинаковый химический состав, но разные свойства. Например, в 1827 году Фридрих Вёлер обнаружил, что гремучее серебро и цианат серебра состоят из 107 частей серебра, 12 частей углерода, 14 частей азота и 16 частей кислорода (теперь мы знаем их формулы как AgCNO). В 1830 году Йенс Якоб Берцелиус ввел для описания этого явления термин изомерия . В 1860 году Луи Пастер выдвинул гипотезу, что молекулы изомеров могут иметь один и тот же набор атомов, но в разном расположении. [11]
В 1874 году Якобус Хенрикус ван 'т Хофф предположил, что атом углерода связан с другими атомами в тетраэдрическом расположении. Основываясь на этом, он объяснил структуру органических молекул таким образом, что мог предсказать, сколько изомеров может иметь соединение. Рассмотрим, например, пентан (C 5 H 12 ). В методе моделирования молекул Ван 'т Хоффа существуют три возможные конфигурации пентана, и ученые все же открыли три и только три изомера пентана. [12] [13]
В 1870 году Дмитрий Менделеев заметил, что, когда он располагал элементы в ряд по их атомному весу, в их свойствах наблюдалась определенная периодичность. [14] Например, второй элемент, литий , имел свойства, подобные девятому элементу, натрию , и шестнадцатому элементу, калию — период семь. Точно так же бериллий , магний и кальций были похожи и все они находились на семи позициях друг от друга в таблице Менделеева. Используя эти закономерности, Менделеев предсказал существование и свойства новых элементов, которые позже были открыты в природе: скандия , галлия и германия . [15] Более того, таблица Менделеева могла бы предсказать, со сколькими атомами других элементов может связаться атом — например, атом углерода и атом германия объединятся с двумя атомами кислорода, и эти элементы находятся в одной группе. Менделеев обнаружил, что эти закономерности подтверждают теорию атома, поскольку они показывают, что элементы можно классифицировать по их атомному весу.
В 1897 году Дж. Дж. Томсон обнаружил, что катодные лучи не являются электромагнитными волнами, а состоят из частиц, поскольку они могут отклоняться электрическими и магнитными полями. Он измерил, что эти частицы в 1800 раз легче водорода (самого легкого атома). Томсон пришел к выводу, что эти частицы произошли от атомов внутри катода — это были субатомные частицы. Он назвал эти новые частицы корпускулами , но позже их переименовали в электроны . Томсон также показал, что электроны идентичны частицам, испускаемым фотоэлектрическими и радиоактивными материалами. [16] Вскоре было признано, что электроны — это частицы, которые переносят электрический ток в металлических проводах. [17] Томсон пришел к выводу, что эти электроны возникли из самих атомов катода в его приборах, а это означало, что атомы не являются неделимыми, как думал Дальтон.
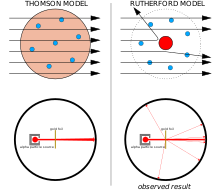
Дж. Дж. Томсон считал, что отрицательно заряженные электроны распределены по всему атому в виде моря положительного заряда, распределенного по всему объему атома. [18] Эту модель иногда называют моделью сливового пудинга .
Между 1908 и 1913 годами Эрнест Резерфорд и его коллеги Ганс Гейгер и Эрнест Марсден провели серию экспериментов, в которых они бомбардировали тонкую металлическую фольгу альфа-частицами. Они сделали это, чтобы измерить характер рассеяния альфа-частиц. Они заметили, что альфа-частицы отклоняются на углы более 90°. Это не должно было быть возможным согласно модели атома Томсона, заряды которого были слишком разбросаны, чтобы создавать достаточно сильное электрическое поле. Резерфорд предположил, что положительный заряд атома не распределен по всему объему атома, как считал Томсон, а сконцентрирован в крошечном ядре в центре. Только такая интенсивная концентрация заряда могла создать достаточно сильное электрическое поле, чтобы отклонить альфа-частицы, как это наблюдалось. [19]

В 1913 году физик Нильс Бор предложил модель, в которой предполагалось, что электроны атома вращаются вокруг ядра, но могут делать это только по конечному набору орбит и могут прыгать между этими орбитами только при дискретных изменениях энергии, соответствующих поглощению. или излучение фотона. [20] Это квантование использовалось для объяснения того, почему орбиты электронов стабильны (учитывая, что в классической физике заряды при ускорении, включая круговое движение, теряют кинетическую энергию, которая испускается в виде электромагнитного излучения) и почему элементы поглощают и излучают электромагнитное излучение в дискретные спектры. [21]
Позже в том же году Генри Мозли предоставил дополнительные экспериментальные доказательства в пользу теории Нильса Бора . Эти результаты усовершенствовали модель Эрнеста Резерфорда и Антониуса ван ден Брука , которые предполагали, что атом содержит в своем ядре количество положительных ядерных зарядов , равное его (атомному) номеру в периодической таблице. До этих экспериментов атомный номер не был известен как физическая и экспериментальная величина. То, что он равен атомному ядерному заряду, остается общепринятой моделью атома и сегодня. [22]
Химические связи между атомами были объяснены Гилбертом Ньютоном Льюисом в 1916 году как взаимодействие между составляющими их электронами. [23] Поскольку было известно, что химические свойства элементов в значительной степени повторяются в соответствии с периодическим законом , [24] в 1919 году американский химик Ирвинг Ленгмюр предположил, что это можно объяснить, если электроны в атоме связаны или сгруппированы в некоторые группы. образом. Считалось, что группы электронов занимают набор электронных оболочек вокруг ядра. [25]
Модель атома Бора была первой полной физической моделью атома. Он описал общую структуру атома, то, как атомы связываются друг с другом, и предсказал спектральные линии водорода. Модель Бора не была идеальной и вскоре была заменена более точной моделью Шрёдингера, но этого было достаточно, чтобы развеять все оставшиеся сомнения в том, что материя состоит из атомов. Для химиков идея атома была полезным эвристическим инструментом, но у физиков были сомнения относительно того, действительно ли материя состоит из атомов, поскольку никто еще не разработал полную физическую модель атома.
В 1917 году Резерфорд бомбардировал газообразный азот альфа -частицами и наблюдал испускание ядер водорода из газа (Резерфорд распознал их, поскольку ранее он получил их, бомбардируя водород альфа-частицами и наблюдая ядра водорода в продуктах) . Резерфорд пришел к выводу, что ядра водорода возникли из ядер самих атомов азота (по сути, он расщепил азот). [26]
Из своей собственной работы и работ своих учеников Бора и Генри Мозли Резерфорд знал, что положительный заряд любого атома всегда можно приравнять к целому числу ядер водорода. Это, в сочетании с атомной массой многих элементов, примерно эквивалентной целому числу атомов водорода, которые тогда считались самыми легкими частицами, привело его к выводу, что ядра водорода являются единичными частицами и основной составляющей всех атомных ядер. Он назвал такие частицы протонами . Дальнейшие эксперименты Резерфорда показали, что ядерная масса большинства атомов превышает массу имеющихся в них протонов; он предположил, что эта избыточная масса состоит из ранее неизвестных нейтрально заряженных частиц, которые предварительно назвали « нейтронами ».
В 1928 году Уолтер Боте заметил, что бериллий испускает высокопроникающее электрически нейтральное излучение при бомбардировке альфа-частицами. Позже было обнаружено, что это излучение может выбивать атомы водорода из парафина . Первоначально считалось, что это высокоэнергетическое гамма-излучение , поскольку гамма-излучение оказывает аналогичное воздействие на электроны в металлах, но Джеймс Чедвик обнаружил, что эффект ионизации слишком силен, чтобы его можно было объяснить электромагнитным излучением, пока энергия и импульс сохранялись при взаимодействии. В 1932 году Чедвик подверг различные элементы, такие как водород и азот, таинственному «бериллиевому излучению» и, измерив энергию отталкивающихся заряженных частиц, пришел к выводу, что это излучение на самом деле состоит из электрически нейтральных частиц, которые не могут быть безмассовыми. как гамма-лучи, но вместо этого они должны были иметь массу, подобную массе протона. Чедвик теперь назвал эти частицы нейтронами Резерфорда. [27] За открытие нейтрона Чедвик получил Нобелевскую премию в 1935 году. [28]
Открытие нейтрона объяснило существование изотопов , которые представляют собой атомы одного и того же элемента, имеющие немного разные массы из-за того, что они имеют разное количество нейтронов, но одинаковое количество протонов.
В 1925 году Вернер Гейзенберг опубликовал первую последовательную математическую формулировку квантовой механики ( матричную механику ). [22] Годом ранее Луи де Бройль предположил, что все частицы в некоторой степени ведут себя как волны, [29] а в 1926 году Эрвин Шредингер использовал эту идею для разработки уравнения Шредингера , математической модели атома, которая описывала электроны как трехмерные формы сигналов , а не точки в пространстве. [30]
Следствием использования форм сигналов для описания частиц является то, что математически невозможно получить точные значения положения и импульса частицы в данный момент времени. Это стало известно как принцип неопределенности , сформулированный Вернером Гейзенбергом в 1927 году. [22] В этой концепции для заданной точности измерения положения можно было получить только диапазон вероятных значений импульса, и наоборот. [31] Эта модель смогла объяснить наблюдения за поведением атомов, которые не могли объяснить предыдущие модели, например, определенные структурные и спектральные закономерности атомов, больших, чем водород. Таким образом, планетарная модель атома была отвергнута в пользу той, которая описывала зоны атомных орбит вокруг ядра, где наиболее вероятно наблюдать данный электрон. [32] [33]
Хотя слово « атом» первоначально обозначало частицу, которую нельзя разрезать на более мелкие частицы, в современном научном использовании атом состоит из различных субатомных частиц . Составляющими частицами атома являются электрон , протон и нейтрон .
Электрон является наименее массивной из этих частиц на четыре порядка при9,11 × 10–31 кг , с отрицательным электрическим зарядом и размером , слишком малым для измерения с помощью доступных методов. [34] Это была самая легкая частица с положительной массой покоя, измеренная до открытия массы нейтрино . В обычных условиях электроны связаны с положительно заряженным ядром притяжением, создаваемым противоположными электрическими зарядами. Если атом имеет больше или меньше электронов, чем его атомный номер, то он в целом становится соответственно отрицательно или положительно заряженным; заряженный атом называется ионом . Электроны известны с конца 19 века, главным образом благодаря Дж. Дж. Томсону ; подробности см . в истории субатомной физики .
Протоны имеют положительный заряд и массу1,6726 × 10-27 кг . _ Число протонов в атоме называется его атомным номером . Эрнест Резерфорд (1919) заметил, что азот под бомбардировкой альфа-частицами выбрасывает то, что казалось ядрами водорода. К 1920 году он признал, что ядро водорода является отдельной частицей внутри атома, и назвал его протоном .
Нейтроны не имеют электрического заряда и имеют массу1,6749 × 10-27 кг . _ [35] [36] Нейтроны являются самыми тяжелыми из трех составляющих частиц, но их масса может быть уменьшена за счет энергии связи ядра . Нейтроны и протоны (вместе называемые нуклонами ) имеют сравнимые размеры — порядка2,5 × 10–15 м , хотя «поверхность» этих частиц четко не выражена. [37] Нейтрон был открыт в 1932 году английским физиком Джеймсом Чедвиком .
В Стандартной модели физики электроны — это действительно элементарные частицы без внутренней структуры, тогда как протоны и нейтроны — это составные частицы, состоящие из элементарных частиц , называемых кварками . В атомах есть два типа кварков, каждый из которых имеет дробный электрический заряд. Протоны состоят из двух ап-кварков (каждый с зарядом +2/3) и один нижний кварк (с зарядом —1/3). Нейтроны состоят из одного верхнего и двух нижних кварков. Это различие объясняет разницу в массе и заряде между двумя частицами. [38] [39]
Кварки удерживаются вместе сильным взаимодействием (или сильной силой), которое осуществляется глюонами . Протоны и нейтроны, в свою очередь, удерживаются друг с другом в ядре ядерной силой , которая является остатком сильного взаимодействия и имеет несколько иные свойства радиуса действия (подробнее см. В статье о ядерной силе). Глюон — член семейства калибровочных бозонов , которые представляют собой элементарные частицы, передающие физические силы. [38] [39]

Все связанные протоны и нейтроны в атоме составляют крошечное атомное ядро и вместе называются нуклонами . Радиус ядра примерно равен фемтометру , где – общее число нуклонов. [40] Это намного меньше радиуса атома, который составляет порядка 10 5 Фм. Нуклоны связаны друг с другом короткодействующим потенциалом притяжения, называемым остаточной сильной силой . На расстояниях менее 2,5 фм эта сила намного мощнее, чем электростатическая сила , которая заставляет положительно заряженные протоны отталкивать друг друга. [41]
Атомы одного и того же элемента имеют одинаковое количество протонов, называемое атомным номером . В пределах одного элемента количество нейтронов может различаться, что определяет изотоп этого элемента. Суммарное число протонов и нейтронов определяет нуклид . Число нейтронов по отношению к протонам определяет стабильность ядра, при этом некоторые изотопы подвергаются радиоактивному распаду . [42]
Протон, электрон и нейтрон классифицируются как фермионы . Фермионы подчиняются принципу Паули , который запрещает идентичным фермионам, таким как несколько протонов, занимать одно и то же квантовое состояние одновременно. Таким образом, каждый протон в ядре должен занимать квантовое состояние, отличное от всех других протонов, и то же самое относится ко всем нейтронам ядра и ко всем электронам электронного облака. [43]
Ядро, в котором количество протонов отличается от количества нейтронов, потенциально может перейти в более низкое энергетическое состояние в результате радиоактивного распада, в результате которого количество протонов и нейтронов будет более точно совпадать. В результате атомы с одинаковым количеством протонов и нейтронов более устойчивы к распаду, но с увеличением атомного номера взаимное отталкивание протонов требует увеличения доли нейтронов для поддержания стабильности ядра. [43]
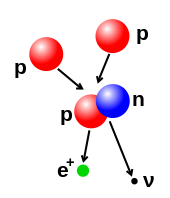
Число протонов и нейтронов в атомном ядре можно изменить, хотя для этого могут потребоваться очень высокие энергии из-за сильного взаимодействия. Ядерный синтез происходит, когда несколько атомных частиц объединяются, образуя более тяжелое ядро, например, в результате энергетического столкновения двух ядер. Например, в ядре Солнца протонам требуется энергия от 3 до 10 кэВ, чтобы преодолеть взаимное отталкивание — кулоновский барьер — и слиться в одно ядро. [44] Деление ядра — это противоположный процесс, вызывающий разделение ядра на два меньших ядра — обычно в результате радиоактивного распада. Ядро также можно модифицировать путем бомбардировки субатомными частицами или фотонами высокой энергии. Если это изменяет количество протонов в ядре, атом превращается в другой химический элемент. [45] [46]
Если масса ядра после реакции синтеза меньше суммы масс отдельных частиц, то разница между этими двумя значениями может быть выделена как тип полезной энергии (например, гамма- лучи или кинетическая энергия). бета - частицы ), как описано в формуле эквивалентности массы и энергии Альберта Эйнштейна , e =mc 2 , где m — потеря массы, а c — скорость света . Этот дефицит является частью энергии связи нового ядра, и именно невосполнимая потеря энергии заставляет слитые частицы оставаться вместе в состоянии, требующем этой энергии для разделения. [47]
Слияние двух ядер, в результате которого образуются более крупные ядра с меньшими атомными номерами, чем у железа и никеля (общее число нуклонов около 60), обычно представляет собой экзотермический процесс , который выделяет больше энергии, чем требуется для их соединения. [48] Именно этот процесс высвобождения энергии делает ядерный синтез в звездах самоподдерживающейся реакцией. Для более тяжелых ядер энергия связи, приходящаяся на нуклон , начинает уменьшаться. Это означает, что процесс термоядерного синтеза, в котором образуется ядро с атомным номером выше примерно 26 и массовым числом выше примерно 60, является эндотермическим процессом . Таким образом, более массивные ядра не могут подвергаться реакции синтеза с выделением энергии, которая может поддерживать гидростатическое равновесие звезды. [43]

Электроны в атоме притягиваются к протонам в ядре электромагнитной силой . Эта сила связывает электроны внутри электростатической потенциальной ямы, окружающей меньшее ядро, а это означает, что для выхода электрона необходим внешний источник энергии. Чем ближе электрон к ядру, тем больше сила притяжения. Следовательно, электронам, связанным вблизи центра потенциальной ямы, требуется больше энергии для выхода, чем электронам, находящимся на большем расстоянии.
Электроны, как и другие частицы, обладают свойствами как частицы, так и волны . Электронное облако — это область внутри потенциальной ямы, где каждый электрон образует своего рода трехмерную стоячую волну — форму волны, которая не движется относительно ядра. Такое поведение определяется атомной орбиталью — математической функцией, которая характеризует вероятность того, что электрон окажется в определенном месте, когда его положение измерено. [49] Вокруг ядра существует только дискретный (или квантованный) набор этих орбиталей, поскольку другие возможные волновые модели быстро распадаются в более стабильную форму. [50] Орбитали могут иметь одну или несколько кольцевых или узловых структур и отличаться друг от друга размером, формой и ориентацией. [51]

Каждая атомная орбиталь соответствует определенному энергетическому уровню электрона. Электрон может изменить свое состояние на более высокий энергетический уровень, поглотив фотон с достаточной энергией, чтобы перевести его в новое квантовое состояние. Аналогичным образом, в результате спонтанной эмиссии электрон с более высоким энергетическим состоянием может перейти в более низкое энергетическое состояние, излучая при этом избыточную энергию в виде фотона. Эти характерные значения энергии, определяемые различиями в энергиях квантовых состояний, ответственны за атомные спектральные линии . [50]
Количество энергии, необходимое для удаления или добавления электрона ( энергия связи электрона) , намного меньше энергии связи нуклонов . Например, для отрыва электрона в основном состоянии атома водорода требуется всего 13,6 эВ по сравнению с 2,23 миллиона эВ для расщепления ядра дейтерия . [53] Атомы электрически нейтральны, если они имеют одинаковое количество протонов и электронов. Атомы, имеющие либо дефицит, либо избыток электронов, называются ионами . Электроны, находящиеся дальше всего от ядра, могут передаваться другим близлежащим атомам или распределяться между атомами. Благодаря этому механизму атомы могут соединяться в молекулы и другие типы химических соединений, такие как кристаллы с ионной и ковалентной сетью . [54]
По определению, любые два атома с одинаковым числом протонов в ядрах принадлежат одному и тому же химическому элементу . Атомы с одинаковым количеством протонов, но разным количеством нейтронов — это разные изотопы одного и того же элемента. Например, все атомы водорода содержат ровно один протон, но существуют изотопы без нейтронов ( водород-1 , безусловно, самая распространенная форма, [55] также называемая протием), один нейтрон ( дейтерий ), два нейтрона ( тритий ) и более . чем два нейтрона . Известные элементы образуют набор атомных номеров, от однопротонного элемента водорода до 118-протонного элемента оганессона . [56] Все известные изотопы элементов с атомными номерами больше 82 радиоактивны, хотя радиоактивность элемента 83 ( висмута ) настолько мала, что практически незначительна. [57] [58]
Около 339 нуклидов встречаются на Земле в природе , [59] из которых 251 (около 74%) не распадаются и называются « стабильными изотопами ». Только 90 нуклидов теоретически стабильны , а распад еще 161 (в результате чего общее количество достигло 251) не наблюдался, хотя теоретически это энергетически возможно. Они также формально классифицируются как «стабильные». Еще 35 радиоактивных нуклидов имеют период полураспада более 100 миллионов лет и достаточно долгоживущие, чтобы присутствовать с момента зарождения Солнечной системы . Эта коллекция из 286 нуклидов известна как первичные нуклиды . Наконец, известно, что еще 53 короткоживущих нуклида встречаются в природе как дочерние продукты распада первичных нуклидов (например, радий из урана ) или как продукты естественных энергетических процессов на Земле, таких как бомбардировка космическими лучами (например, углерод -14). [60] [примечание 1]
Для 80 химических элементов существует по крайней мере один стабильный изотоп . Как правило, для каждого из этих элементов существует лишь несколько стабильных изотопов, в среднем 3,1 стабильного изотопа на элемент. Двадцать шесть « моноизотопных элементов » имеют только один стабильный изотоп, в то время как наибольшее количество стабильных изотопов, наблюдаемых для любого элемента, равно десяти, для элемента олово . Элементы 43 , 61 и все элементы с номерами 83 и выше не имеют стабильных изотопов. [61] : 1–12
На стабильность изотопов влияет соотношение протонов к нейтронам, а также наличие определенных «магических чисел» нейтронов или протонов, которые представляют собой замкнутые и заполненные квантовые оболочки. Эти квантовые оболочки соответствуют набору энергетических уровней внутри оболочечной модели ядра; заполненные оболочки, такие как заполненная оболочка из 50 протонов для олова, придают нуклиду необычную стабильность. Из 251 известного стабильного нуклида только четыре имеют как нечетное число протонов , так и нечетное число нейтронов: водород-2 ( дейтерий ), литий-6 , бор-10 и азот-14 . ( Тантал-180m является нечетно-нечетным и стабильным по наблюдениям, но, по прогнозам, он распадается с очень длительным периодом полураспада.) Кроме того, только четыре встречающихся в природе радиоактивных нечетно-нечетных нуклида имеют период полураспада более миллиарда лет: калий -180m. 40 , ванадий-50 , лантан-138 и лютеций-176 . Большинство нечетно-нечетных ядер очень нестабильны по отношению к бета-распаду , поскольку продукты распада четно-четные и, следовательно, более прочно связаны из-за эффектов спаривания ядер . [62]
Подавляющая часть массы атома состоит из протонов и нейтронов, из которых он состоит. Общее число этих частиц (называемых «нуклонами») в данном атоме называется массовым числом . Это целое положительное число, безразмерное (вместо измерения массы), поскольку оно выражает количество. Примером использования массового числа является «углерод-12», который имеет 12 нуклонов (шесть протонов и шесть нейтронов).
Фактическая масса покоящегося атома часто выражается в дальтонах (Да), также называемых единой атомной единицей массы (u). Эта единица определяется как двенадцатая часть массы свободного нейтрального атома углерода -12 , что примерно равно1,66 × 10-27 кг . _ [63] Водород-1 (самый легкий изотоп водорода, который также является нуклидом с наименьшей массой) имеет атомный вес 1,007825 Да. [64] Значение этого числа называется атомной массой . Данный атом имеет атомную массу, примерно равную (в пределах 1%) его массовому числу, умноженному на атомную единицу массы (например, масса азота-14 составляет примерно 14 Да), но это число не будет точно целым числом, за исключением ( по определению) в случае углерода-12. [65] Самый тяжелый стабильный атом — свинец-208, [57] с массой207,976 6521 Да . [66]
Поскольку даже самые массивные атомы слишком легки, чтобы с ними можно было работать напрямую, химики вместо этого используют единицу измерения молей . В одном моле атомов любого элемента всегда содержится одинаковое количество атомов (около6,022 × 10 23 ). Это число было выбрано таким образом, что если элемент имеет атомную массу 1 u, то моль атомов этого элемента имеет массу, близкую к одному грамму. Из-за определения единой атомной единицы массы каждый атом углерода-12 имеет атомную массу ровно 12 Да, поэтому моль атомов углерода-12 весит ровно 0,012 кг. [63]
У атомов нет четко выраженной внешней границы, поэтому их размеры обычно описывают в терминах атомного радиуса . Это мера расстояния, на которое электронное облако простирается от ядра. [67] Это предполагает, что атом имеет сферическую форму, которая соблюдается только для атомов в вакууме или свободном пространстве. Атомные радиусы могут быть получены из расстояний между двумя ядрами, когда два атома соединены химической связью . Радиус варьируется в зависимости от положения атома на атомной диаграмме, типа химической связи, количества соседних атомов ( координационного числа ) и квантово-механического свойства, известного как спин . [68] В периодической таблице элементов размер атома имеет тенденцию увеличиваться при движении вниз по столбцу, но уменьшаться при перемещении по строкам (слева направо). [69] Следовательно, самый маленький атом — это гелий с радиусом 32 пм , а один из самых крупных — цезий с радиусом 225 пм. [70]
Под воздействием внешних сил, таких как электрические поля , форма атома может отклоняться от сферической симметрии . Деформация зависит от величины поля и типа орбит электронов внешней оболочки, как показывают теоретико-групповые соображения. Асферические отклонения могут возникать, например, в кристаллах , где большие кристаллические электрические поля могут возникать в узлах решетки с низкой симметрией . [71] [72] Было показано, что значительные эллипсоидальные деформации возникают для ионов серы [73] и ионов халькогена [74] в соединениях типа пирита .
Размеры атомов в тысячи раз меньше длин волн света (400–700 нм ), поэтому их нельзя увидеть с помощью оптического микроскопа , хотя отдельные атомы можно наблюдать с помощью сканирующего туннельного микроскопа . Чтобы представить себе мельчайшие размеры атома, представьте, что типичный человеческий волос имеет ширину около 1 миллиона атомов углерода. [75] В одной капле воды содержится около 2 секстиллионов (2 × 10 21 ) атомов кислорода и вдвое больше атомов водорода. [76] Бриллиант в один карат массойВ 2 × 10-4 кг содержится около 10 секстиллионов (10 22 ) атомов углерода . [примечание 2] Если бы яблоко было увеличено до размеров Земли, то атомы в яблоке были бы примерно такого же размера, как исходное яблоко. [77]

Каждый элемент имеет один или несколько изотопов, ядра которых нестабильны и подвержены радиоактивному распаду, в результате чего ядро испускает частицы или электромагнитное излучение. Радиоактивность может возникнуть, когда радиус ядра велик по сравнению с радиусом сильного взаимодействия, которое действует только на расстояниях порядка 1 фм. [78]
Наиболее распространенными формами радиоактивного распада являются: [79] [80]
Другие, более редкие типы радиоактивного распада включают выброс нейтронов, протонов или кластеров нуклонов из ядра или более одной бета-частицы . Аналогом гамма-излучения, который позволяет возбужденным ядрам терять энергию другим способом, является внутренняя конверсия — процесс, в результате которого образуются высокоскоростные электроны, не являющиеся бета-лучами, с последующим образованием фотонов высокой энергии, не являющихся гамма-лучами. Несколько крупных ядер взрываются на два или более заряженных фрагмента различной массы плюс несколько нейтронов в результате распада, называемого спонтанным ядерным делением .
Каждый радиоактивный изотоп имеет характерный период распада — период полураспада , который определяется количеством времени, необходимым для распада половины образца. Это экспоненциальный процесс распада , который постепенно уменьшает долю оставшегося изотопа на 50% за каждый период полураспада. Следовательно, по прошествии двух периодов полураспада присутствует только 25% изотопа и так далее. [78]
Элементарные частицы обладают внутренним квантовомеханическим свойством, известным как спин . Это аналогично угловому моменту объекта, который вращается вокруг своего центра масс , хотя, строго говоря, эти частицы считаются точечными и нельзя сказать, что они вращаются. Спин измеряется в единицах приведенной постоянной Планка (ħ), при этом электроны, протоны и нейтроны имеют спин 1 ⁄ 2 ħ, или «спин- 1 ⁄ 2 ». В атоме электроны, движущиеся вокруг ядра , помимо спина обладают орбитальным угловым моментом , тогда как само ядро обладает угловым моментом, обусловленным его ядерным спином. [81]
Магнитное поле , создаваемое атомом, — его магнитный момент — определяется этими различными формами углового момента, точно так же, как вращающийся заряженный объект классически создает магнитное поле, но наиболее доминирующий вклад вносит спин электрона. Из-за того, что электроны подчиняются принципу запрета Паули , согласно которому никакие два электрона не могут находиться в одном и том же квантовом состоянии , связанные электроны образуют пары друг с другом, причем один член каждой пары находится в состоянии со спином вверх, а другой - в состоянии. противоположное, состояние со спином вниз. Таким образом, эти спины нейтрализуют друг друга, сводя общий магнитный дипольный момент к нулю в некоторых атомах с четным числом электронов. [82]
В ферромагнитных элементах, таких как железо, кобальт и никель, нечетное количество электронов приводит к образованию неспаренного электрона и суммарному магнитному моменту. Орбитали соседних атомов перекрываются, и более низкое энергетическое состояние достигается, когда спины неспаренных электронов выравниваются друг с другом - спонтанный процесс, известный как обменное взаимодействие . Когда магнитные моменты ферромагнитных атомов выстраиваются в ряд, материал может создавать измеримое макроскопическое поле. Парамагнетики содержат атомы с магнитными моментами, которые выстраиваются в случайных направлениях при отсутствии магнитного поля, но магнитные моменты отдельных атомов выстраиваются в линию в присутствии поля. [82] [83]
Ядро атома не будет иметь спина, если оно имеет четное количество нейтронов и протонов, но в других случаях нечетного числа ядро может иметь спин. Обычно ядра со спином ориентированы в случайных направлениях из-за теплового равновесия , но для некоторых элементов (таких как ксенон-129 ) можно поляризовать значительную часть ядерных спиновых состояний так, чтобы они были выровнены в одном направлении — условие называется гиперполяризацией . Это имеет важное применение в магнитно-резонансной томографии . [84] [85]
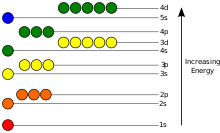
Потенциальная энергия электрона в атоме отрицательна по сравнению с тем, когда расстояние от ядра стремится к бесконечности ; ее зависимость от положения электрона достигает минимума внутри ядра, примерно обратно пропорционально расстоянию. В квантово-механической модели связанный электрон может занимать только набор состояний с центром в ядре, и каждое состояние соответствует определенному энергетическому уровню ; теоретическое объяснение см. в независимом от времени уравнении Шредингера . Уровень энергии можно измерить по количеству энергии, необходимой для отделения электрона от атома, и обычно выражается в единицах электронвольт (эВ). Состояние с самой низкой энергией связанного электрона называется основным состоянием, т.е. стационарным состоянием , а переход электрона на более высокий уровень приводит к возбужденному состоянию. [86] Энергия электрона увеличивается вместе с n , потому что (среднее) расстояние до ядра увеличивается. Зависимость энергии от ℓ обусловлена не электростатическим потенциалом ядра, а взаимодействием между электронами.
Чтобы электрон мог перейти между двумя разными состояниями , например, из основного состояния в первое возбужденное состояние , он должен поглотить или испустить фотон с энергией, соответствующей разнице потенциальной энергии этих уровней, согласно модели Нильса Бора , что может быть точно рассчитывается по уравнению Шредингера . Электроны перепрыгивают между орбиталями подобно частицам. Например, если одиночный фотон сталкивается с электронами, только один электрон меняет состояние в ответ на фотон; см. свойства электрона .
Энергия испускаемого фотона пропорциональна его частоте , поэтому эти конкретные энергетические уровни проявляются как отдельные полосы в электромагнитном спектре . [87] Каждый элемент имеет характерный спектр, который может зависеть от заряда ядра, подоболочек, заполненных электронами, электромагнитных взаимодействий между электронами и других факторов. [88]

Когда непрерывный спектр энергии проходит через газ или плазму, некоторые фотоны поглощаются атомами, заставляя электроны менять свой энергетический уровень. Те возбужденные электроны, которые остаются связанными со своим атомом, спонтанно излучают эту энергию в виде фотона, путешествующего в случайном направлении, и поэтому возвращаются на более низкие энергетические уровни. Таким образом, атомы ведут себя как фильтр, который формирует серию темных полос поглощения на выходе энергии. (Наблюдатель, рассматривающий атомы с точки зрения, которая не включает непрерывный спектр на заднем плане, вместо этого видит серию линий излучения фотонов, испускаемых атомами.) Спектроскопические измерения силы и ширины атомных спектральных линий позволяют составить состав и физические свойства вещества, подлежащие определению. [89]
Внимательное изучение спектральных линий показывает, что некоторые из них демонстрируют тонкое расщепление структуры . Это происходит из-за спин-орбитальной связи , которая представляет собой взаимодействие между спином и движением самого внешнего электрона. [90] Когда атом находится во внешнем магнитном поле, спектральные линии расщепляются на три или более компонентов; явление, называемое эффектом Зеемана . Это вызвано взаимодействием магнитного поля с магнитным моментом атома и его электронов. Некоторые атомы могут иметь несколько электронных конфигураций с одним и тем же энергетическим уровнем, которые, таким образом, выглядят как одна спектральная линия. Взаимодействие магнитного поля с атомом сдвигает эти электронные конфигурации на несколько разные энергетические уровни, что приводит к появлению множества спектральных линий. [91] Наличие внешнего электрического поля может вызвать аналогичное расщепление и смещение спектральных линий за счет изменения энергетических уровней электронов — явление, называемое эффектом Штарка . [92]
Если связанный электрон находится в возбужденном состоянии, взаимодействующий фотон с соответствующей энергией может вызвать вынужденное излучение фотона с соответствующим уровнем энергии. Чтобы это произошло, электрон должен перейти в состояние с более низкой энергией, разница в энергии которого соответствует энергии взаимодействующего фотона. Испущенный фотон и взаимодействующий фотон затем удаляются параллельно и с совпадающими фазами. То есть волновые структуры двух фотонов синхронизированы. Это физическое свойство используется для создания лазеров , которые могут излучать когерентный луч световой энергии в узком диапазоне частот. [93]
Валентность – это объединяющая сила элемента. Это определяется количеством связей, которые он может образовать с другими атомами или группами. [94] Внешняя электронная оболочка атома в несвязанном состоянии известна как валентная оболочка , а электроны в этой оболочке называются валентными электронами . Количество валентных электронов определяет поведение связи с другими атомами. Атомы имеют тенденцию химически реагировать друг с другом таким образом, что заполняют (или опустошают) их внешние валентные оболочки. [95] Например, перенос одного электрона между атомами является полезным приближением для связей, которые образуются между атомами, у которых на один электрон больше, чем в заполненной оболочке, и других связей, которым не хватает одного электрона до полной оболочки, например, в соединении хлорида натрия и других химических ионных солей. Многие элементы обладают множественной валентностью или склонностью к разделению разного количества электронов в разных соединениях. Таким образом, химическая связь между этими элементами принимает множество форм совместного использования электронов, которые представляют собой нечто большее, чем простой перенос электронов. Примеры включают элемент углерод и органические соединения . [96]
Химические элементы часто отображаются в таблице Менделеева , которая составлена так, чтобы отображать повторяющиеся химические свойства, а элементы с одинаковым количеством валентных электронов образуют группу, выровненную в одном столбце таблицы. (Горизонтальные строки соответствуют заполнению квантовой оболочки электронов.) Внешняя оболочка элементов в правой части таблицы полностью заполнена электронами, в результате чего образуются химически инертные элементы, известные как благородные газы . [97] [98]

Количества атомов находятся в разных состояниях материи, которые зависят от физических условий, таких как температура и давление . Изменяя условия, материалы могут переходить между твердыми телами , жидкостями , газами и плазмой . [99] Внутри состояния материал также может существовать в различных аллотропах . Примером этого является твердый углерод, который может существовать в виде графита или алмаза . [100] Также существуют газообразные аллотропы, такие как дикислород и озон .
При температурах, близких к абсолютному нулю , атомы могут образовывать конденсат Бозе-Эйнштейна , в этот момент квантово-механические эффекты, которые обычно наблюдаются только на атомном уровне, становятся очевидными на макроскопическом уровне. [101] [102] Эта переохлажденная совокупность атомов затем ведет себя как один суператом , что может позволить провести фундаментальную проверку квантово-механического поведения. [103]

Хотя атомы слишком малы, чтобы их можно было увидеть, такие устройства, как сканирующий туннельный микроскоп (СТМ), позволяют их визуализировать на поверхности твердых тел. Микроскоп использует явление квантового туннелирования , которое позволяет частицам проходить через барьер, который с классической точки зрения был бы непреодолим. Электроны туннелируют через вакуум между двумя смещенными электродами, создавая туннельный ток, который экспоненциально зависит от их разделения. Один электрод представляет собой острый кончик, в идеале заканчивающийся одним атомом. В каждой точке сканирования поверхности высота иглы регулируется таким образом, чтобы поддерживать туннельный ток на заданном значении. Насколько кончик перемещается к поверхности и от нее, интерпретируется как профиль высоты. При малом смещении микроскоп отображает усредненные электронные орбитали на плотно упакованных энергетических уровнях — локальную плотность электронных состояний вблизи уровня Ферми . [104] [105] Из-за больших расстояний оба электрода должны быть чрезвычайно стабильными; только тогда можно наблюдать периодичности, соответствующие отдельным атомам. Сам по себе метод не является химически специфичным и не может идентифицировать виды атомов, присутствующие на поверхности.
Атомы можно легко идентифицировать по их массе. Если атом ионизируется путем удаления одного из его электронов, его траектория при прохождении через магнитное поле искривится. Радиус, на который траектория движущегося иона поворачивается магнитным полем, определяется массой атома. Масс -спектрометр использует этот принцип для измерения отношения массы к заряду ионов. Если образец содержит несколько изотопов, масс-спектрометр может определить долю каждого изотопа в образце, измеряя интенсивность различных пучков ионов. Методы испарения атомов включают атомно-эмиссионную спектроскопию с индуктивно связанной плазмой и масс-спектрометрию с индуктивно связанной плазмой , оба из которых используют плазму для испарения образцов для анализа. [106]
Томограф с атомным зондом имеет субнанометровое разрешение в 3D и может химически идентифицировать отдельные атомы с помощью времяпролетной масс-спектрометрии . [107]
Методы электронной эмиссии, такие как рентгеновская фотоэлектронная спектроскопия (XPS) и электронная оже-спектроскопия (AES), которые измеряют энергии связи основных электронов , используются для идентификации видов атомов, присутствующих в образце, неразрушающим способом. При правильной фокусировке оба можно сделать специфичными для конкретной области. Другим таким методом является спектроскопия потерь энергии электронов (EELS), которая измеряет потери энергии электронного луча в просвечивающем электронном микроскопе при его взаимодействии с частью образца.
Спектры возбужденных состояний можно использовать для анализа атомного состава далеких звезд . Определенные длины волн света , содержащиеся в наблюдаемом свете звезд, можно выделить и связать с квантованными переходами в атомах свободного газа. Эти цвета можно воспроизвести с помощью газоразрядной лампы , содержащей тот же элемент. [108] Гелий был открыт таким образом в спектре Солнца за 23 года до того, как он был обнаружен на Земле. [109]
Барионная материя составляет около 4% от общей плотности энергии наблюдаемой Вселенной со средней плотностью около 0,25 частиц/м 3 (в основном протонов и электронов). [110] Внутри такой галактики, как Млечный Путь , частицы имеют гораздо более высокую концентрацию: плотность вещества в межзвездной среде (МЗС) варьируется от 10 5 до 10 9 атомов/м 3 . [111] Считается, что Солнце находится внутри Местного Пузыря , поэтому плотность в окрестностях Солнца составляет всего лишь около 10 3 атомов/м 3 . [112] Звезды формируются из плотных облаков в МЗС, и эволюционные процессы звезд приводят к постоянному обогащению МЗС элементами, более массивными, чем водород и гелий.
До 95% барионной материи Млечного Пути сосредоточено внутри звезд, где условия неблагоприятны для атомной материи. Полная барионная масса составляет около 10% массы галактики; [113] остальная часть массы представляет собой неизвестную темную материю . [114] Высокая температура внутри звезд делает большинство «атомов» полностью ионизированными, то есть отделяет все электроны от ядер. В остатках звезд , за исключением их поверхностных слоев, огромное давление делает образование электронных оболочек невозможным.
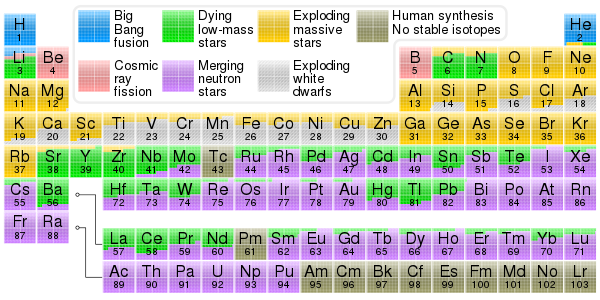
Считается, что электроны существуют во Вселенной с ранних стадий Большого взрыва . Атомные ядра образуются в реакциях нуклеосинтеза . Примерно за три минуты в результате нуклеосинтеза Большого Взрыва была произведена большая часть гелия , лития и дейтерия во Вселенной, а также, возможно, некоторое количество бериллия и бора . [115] [116] [117]
Вездесущность и стабильность атомов зависит от их энергии связи , а это означает, что атом имеет более низкую энергию, чем несвязанная система ядра и электронов. Там, где температура значительно превышает потенциал ионизации , вещество существует в виде плазмы — газа положительно заряженных ионов (возможно, голых ядер) и электронов. Когда температура падает ниже потенциала ионизации, атомы становятся статистически выгодными. Атомы (полные со связанными электронами) стали доминировать над заряженными частицами через 380 000 лет после Большого взрыва — эпохи, называемой рекомбинацией , когда расширяющаяся Вселенная остыла достаточно, чтобы позволить электронам прикрепиться к ядрам. [118]
Со времени Большого взрыва, в ходе которого не было произведено ни углерода , ни более тяжелых элементов , атомные ядра объединялись в звездах посредством процесса ядерного синтеза с образованием большего количества элемента гелия и (посредством тройного альфа-процесса ) последовательности элементов от углерода до железо ; [119] подробнее см. звездный нуклеосинтез .
Изотопы, такие как литий-6, а также некоторые бериллий и бор, генерируются в космосе в результате расщепления космических лучей . [120] Это происходит, когда протон высокой энергии ударяется о атомное ядро, вызывая выброс большого количества нуклонов.
Элементы тяжелее железа были произведены в сверхновых и сталкивающихся нейтронных звездах посредством r-процесса , а также в звездах AGB посредством s-процесса , оба из которых включают захват нейтронов атомными ядрами. [121] Такие элементы, как свинец, образовались в основном в результате радиоактивного распада более тяжелых элементов. [122]
Большинство атомов, составляющих Землю и ее обитателей, в своей нынешней форме присутствовали в туманности , которая выпала из молекулярного облака и образовала Солнечную систему . Остальные являются результатом радиоактивного распада, и их относительную долю можно использовать для определения возраста Земли посредством радиометрического датирования . [123] [124] Большая часть гелия в земной коре (около 99% гелия из газовых скважин, о чем свидетельствует более низкое содержание гелия-3 ) является продуктом альфа-распада . [125]
На Земле есть несколько следов атомов, которых не было вначале (т. е. они не были «первоначальными»), а также они не являются результатами радиоактивного распада. Углерод-14 постоянно генерируется космическими лучами в атмосфере. [126] Некоторые атомы на Земле были созданы искусственно либо преднамеренно, либо как побочные продукты ядерных реакторов или взрывов. [127] [128] Из трансурановых элементов — с атомным номером больше 92 — на Земле в природе встречаются только плутоний и нептуний . [129] [130] Трансурановые элементы имеют радиоактивное время жизни меньше нынешнего возраста Земли [131] и, таким образом, идентифицируемые количества этих элементов уже давно распались, за исключением следов плутония-244, возможно, отложенного космической пылью. [123] Природные месторождения плутония и нептуния производятся путем захвата нейтронов в урановой руде. [132]
На Земле содержится примерно1,33 × 10 50 атомов. [133] Хотя существует небольшое количество независимых атомов благородных газов , таких как аргон , неон и гелий , 99% атмосферы связано в форме молекул, включая углекислый газ , двухатомный кислород и азот . На поверхности Земли подавляющее большинство атомов объединяются с образованием различных соединений, включая воду , соли , силикаты и оксиды . Атомы также могут объединяться для создания материалов, которые не состоят из отдельных молекул, включая кристаллы и жидкие или твердые металлы . [134] [135] Эта атомная материя образует сетевые структуры, в которых отсутствует особый тип мелкомасштабного прерывистого порядка, связанный с молекулярной материей. [136]
Известно, что все нуклиды с атомным номером выше 82 ( свинец ) радиоактивны. Ни один нуклид с атомным номером, превышающим 92 ( уран ), не существует на Земле в качестве первичного нуклида , а более тяжелые элементы обычно имеют более короткий период полураспада. Тем не менее, « остров стабильности », охватывающий относительно долгоживущие изотопы сверхтяжелых элементов [137] с атомными номерами от 110 до 114 , может существовать. [138] Прогнозы периода полураспада самого стабильного нуклида на острове варьируются от нескольких минут до миллионов лет. [139] В любом случае сверхтяжелые элементы (с Z > 104) не существовали бы из-за увеличения кулоновского отталкивания (что приводит к спонтанному делению со все более короткими периодами полураспада) в отсутствие каких-либо стабилизирующих эффектов. [140]
Каждой частице материи соответствует частица антиматерии с противоположным электрическим зарядом. Таким образом, позитрон — это положительно заряженный антиэлектрон , а антипротон — отрицательно заряженный эквивалент протона . Когда материя и соответствующая ей частица антиматерии встречаются, они аннигилируют друг друга. Из-за этого, а также из-за дисбаланса между количеством частиц материи и антивещества, последние во Вселенной встречаются редко. Первые причины этого дисбаланса еще полностью не изучены, хотя теории бариогенеза могут предложить объяснение. В результате в природе не было обнаружено атомов антивещества. [141] [142] В 1996 году в лаборатории ЦЕРН в Женеве был синтезирован аналог антивещества атома водорода ( антиводород ) . [143] [144]
Другие экзотические атомы были созданы путем замены одного из протонов, нейтронов или электронов другими частицами с таким же зарядом. Например, электрон может быть заменен более массивным мюоном , образуя мюонный атом . Эти типы атомов можно использовать для проверки фундаментальных предсказаний физики. [145] [146] [147]
В одной капле воды содержится 2 000 000 000 000 000 000 000 (это 2 секстиллиона) атомов кислорода — и в два раза больше атомов водорода.
Ошибка цитирования: определенная в списке ссылка с именем «npc1921» не используется в содержимом (см. страницу справки ).
Ошибка цитирования: определенная в списке ссылка с именем «prsA_89_1_1913» не используется в содержимом (см. страницу справки ).
Ошибка цитирования: определенная в списке ссылка с именем «pm39_6_449» не используется в содержимом (см. страницу справки ).
Ошибка цитирования: определенная в списке ссылка с именем «chadwick1935» не используется в содержимом (см. страницу справки ).
Ошибка цитирования: определенная в списке ссылка с именем «CHF» не используется в содержимом (см. страницу справки ).
Ошибка цитирования: определенная в списке ссылка с именем «Боуден» не используется в содержимом (см. страницу справки ).
Ошибка цитирования: определенная в списке ссылка с именем «nature143_3615_239» не используется в содержимом (см. страницу справки ).
Ошибка цитирования: определенная в списке ссылка с именем «schroeder» не используется в содержимом (см. страницу справки ).
Ошибка цитирования: определенная в списке ссылка с именем «pt50_9_26» не используется в содержимом (см. страницу справки ).
Ошибка цитирования: определенная в списке ссылка с именем «kullander2001» не используется в содержимом (см. страницу справки ).