Клетки нервного гребня представляют собой временную группу клеток, которые возникают из зародышевого листка эмбриональной эктодермы и, в свою очередь, дают начало разнообразному клеточному клону, включая меланоциты , черепно-лицевой хрящ и кости, гладкие мышцы , периферические и кишечные нейроны и глию . [1] [2]
После гаструляции на границе нервной пластинки и ненейральной эктодермы определяются клетки нервного гребня . Во время нейруляции границы нервной пластинки, также известные как нервные складки , сходятся на дорсальной срединной линии, образуя нервную трубку . [3] Впоследствии клетки нервного гребня из пластинки крыши нервной трубки подвергаются эпителиально-мезенхимальному переходу , отслаиваясь от нейроэпителия и мигрируя через периферию, где они дифференцируются в различные типы клеток. [1] Появление нервного гребня сыграло важную роль в эволюции позвоночных , поскольку многие из его структурных производных являются определяющими особенностями клады позвоночных . [4]
В основе развития нервного гребня лежит регуляторная сеть генов , описываемая как набор взаимодействующих сигналов, факторов транскрипции и нижестоящих эффекторных генов, которые придают клеткам такие характеристики, как мультипотентность и миграционные способности. [5] Понимание молекулярных механизмов формирования нервного гребня важно для наших знаний о болезнях человека из-за его вклада в множественные клеточные линии . Аномалии развития нервного гребня вызывают нейрокристопатии , которые включают такие состояния, как лобно-носовая дисплазия , синдром Ваарденбурга-Шаха и синдром ДиДжорджа . [1]
Следовательно, определение механизмов развития нервного гребня может раскрыть ключевую информацию об эволюции позвоночных и нейрокристопатиях.
Нервный гребень был впервые описан у куриного эмбриона Вильгельмом Хисом-старшим в 1868 году как «промежуточный шнур» (Zwischenstrang) из-за его происхождения между нервной пластинкой и ненейральной эктодермой. [1] Он назвал тканевой ганглиозный гребень, поскольку его конечным пунктом назначения была каждая боковая сторона нервной трубки, где он дифференцировался в спинальные ганглии. [6] В первой половине 20-го века большинство исследований нервного гребня проводилось с использованием эмбрионов амфибий, обзор которых был сделан Хёрстадиусом (1950) в хорошо известной монографии. [7]
Методы маркировки клеток продвинули область исследования нервного гребня, поскольку позволили исследователям визуализировать миграцию ткани по развивающимся эмбрионам. В 1960-х годах Уэстон и Чибон использовали радиоизотопное мечение ядра тритиевым тимидином у эмбрионов кур и амфибий соответственно. Однако этот метод страдает недостатками стабильности, поскольку каждый раз, когда меченая клетка делится, сигнал ослабляется. Современные методы мечения клеток, такие как декстран, лизированный родамином, и витальный краситель diI также были разработаны для временной маркировки линий нервного гребня. [6]
Система маркировки перепелок-цыплят, разработанная Николь Ле Дуарен в 1969 году, была еще одним инструментальным методом, используемым для отслеживания клеток нервного гребня. [8] [9] Химеры , полученные в результате трансплантации, позволили исследователям отличить клетки нервного гребня одного вида от окружающей ткани другого вида. С помощью этого метода поколения ученых смогли надежно отметить и изучить онтогенез клеток нервного гребня.
Молекулярный каскад событий участвует в установлении миграционных и мультипотентных характеристик клеток нервного гребня. Эту сеть регуляции генов можно разделить на следующие четыре подсети, описанные ниже.
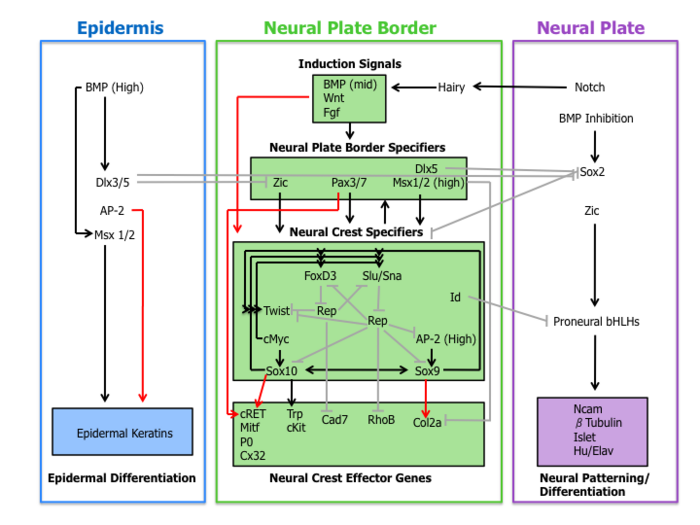
Во-первых, внеклеточные сигнальные молекулы, секретируемые из прилежащего эпидермиса и подлежащей мезодермы , такие как Wnts , BMPs и Fgfs , отделяют ненейральную эктодерму (эпидермис) от нервной пластинки во время нервной индукции . [1] [4]
Передача сигналов Wnt была продемонстрирована при индукции нервного гребня у нескольких видов посредством экспериментов по приобретению и потере функции. В соответствии с этим наблюдением, промоторная область слизняка (ген, специфичный для нервного гребня) содержит сайт связывания для транскрипционных факторов , участвующих в активации Wnt-зависимых генов-мишеней, что указывает на прямую роль передачи сигналов Wnt в спецификации нервного гребня. [10]
Современная роль BMP в формировании нервного гребня связана с индукцией нервной пластинки. Антагонисты BMP, диффундирующие из эктодермы, создают градиент активности BMP. Таким образом, линия нервного гребня формируется из промежуточных уровней передачи сигналов BMP, необходимых для развития нервной пластинки (низкий BMP) и эпидермиса (высокий BMP). [1]
Fgf из параксиальной мезодермы был предложен в качестве источника индуктивного сигнала нервного гребня. Исследователи продемонстрировали, что экспрессия доминантно-негативного рецептора Fgf в эксплантатах эктодермы блокирует индукцию нервного гребня при рекомбинации с параксиальной мезодермой. [11] Понимание роли путей BMP, Wnt и Fgf в экспрессии спецификаторов нервного гребня остается неполным.
Сигнальные события, которые устанавливают границу нервной пластинки, приводят к экспрессии набора транскрипционных факторов, описанных здесь как спецификаторы границы нервной пластинки. Эти молекулы включают факторы Zic, Pax3/7, Dlx5, Msx1/2, которые могут опосредовать влияние Wnts, BMP и Fgfs. Эти гены широко экспрессируются в пограничной области нервной пластинки и предшествуют экспрессии достоверных маркеров нервного гребня. [4]
Экспериментальные данные помещают эти транскрипционные факторы выше спецификаторов нервного гребня. Например, у Xenopus Msx1 необходим и достаточен для экспрессии Slug, Snail и FoxD3. [12] Более того, Pax3 необходим для экспрессии FoxD3 в эмбрионах мышей. [13]
За экспрессией спецификаторов границ нервной пластинки следует набор генов, включая Slug/Snail, FoxD3, Sox10, Sox9, AP-2 и c-Myc. Этот набор генов, обозначенный здесь как спецификаторы нервного гребня, активируется в возникающих клетках нервного гребня. По крайней мере, у Xenopus каждый спецификатор нервного гребня необходим и/или достаточен для экспрессии всех других спецификаторов, демонстрируя существование обширной перекрестной регуляции. [4] Более того, этот модельный организм сыграл важную роль в выяснении роли сигнального пути Hedgehog в спецификации нервного гребня, при этом транскрипционный фактор Gli2 играет ключевую роль. [14]
За пределами жестко регулируемой сети спецификаторов нервного гребня находятся два других фактора транскрипции Twist и Id. Twist, транскрипционный фактор bHLH , необходим для мезенхимной дифференцировки структур глоточной дуги . [15] Id является непосредственной мишенью c-Myc и, как известно, важен для поддержания стволовых клеток нервного гребня. [16]
Наконец, спецификаторы нервного гребня включают экспрессию эффекторных генов, которые придают определенные свойства, такие как миграция и мультипотентность. Два эффектора нервного гребня, Rho GTPases и кадгерины , действуют при расслаивании, регулируя морфологию клеток и адгезивные свойства. Sox9 и Sox10 регулируют дифференцировку нервного гребня путем активации многих эффекторов, специфичных для типа клеток, включая Mitf, P0, Cx32, Trp и cKit. [4]

Миграция клеток нервного гребня включает высокоскоординированный каскад событий, который начинается с закрытия дорсальной нервной трубки .
После слияния нервных складок с образованием нервной трубки клетки , первоначально расположенные на границе нервной пластинки, становятся клетками нервного гребня . [17] Чтобы миграция началась, клетки нервного гребня должны пройти процесс, называемый расслаиванием, который включает полный или частичный эпителиально-мезенхимальный переход (ЕМТ) . [18] Расслоение определяется как разделение ткани на различные популяции, в данном случае клетки нервного гребня отделяются от окружающей ткани. [19] И наоборот, ЕМТ представляет собой серию событий, координирующих изменение эпителиального фенотипа на мезенхимальный . [18] Например, деламинация у куриных эмбрионов запускается каскадом BMP / Wnt , который индуцирует экспрессию ЕМТ, способствующих транскрипционным факторам , таким как SNAI2 и FoxD3 . [19] Хотя все клетки нервного гребня подвергаются ЭМП, время расслаивания происходит на разных стадиях у разных организмов: у эмбрионов Xenopus laevis наблюдается массивное расслоение, которое происходит, когда нервная пластинка не полностью слита, тогда как у куриного эмбриона происходит расслаивание. при сращении нервной складки . [19]
Перед расслоением презумптивные клетки нервного гребня первоначально закрепляются с соседними клетками с помощью белков плотного соединения, таких как окклюдин , и молекул клеточной адгезии , таких как NCAM и N - кадгерин . [20] Дорсально экспрессированные BMP инициируют расслоение, индуцируя экспрессию факторов транскрипции белка цинкового пальца улитки , слизняка и твиста . [17] Эти факторы играют непосредственную роль в индукции эпителиально-мезенхимального перехода за счет снижения экспрессии окклюдина и N-кадгерина , а также способствуют модификации NCAM остатками полисиаловой кислоты для уменьшения адгезивности. [17] [21] Клетки нервного гребня также начинают экспрессировать протеазы , способные расщеплять кадгерины , такие как ADAM10 [22] и секретировать матриксные металлопротеиназы (ММП) , которые разрушают вышележащую базальную пластинку нервной трубки, позволяя клеткам нервного гребня выйти наружу. [20] Кроме того, клетки нервного гребня во время миграции начинают экспрессировать интегрины , которые связываются с белками внеклеточного матрикса , включая коллаген , фибронектин и ламинин . [23] Как только базальная пластинка становится проницаемой, клетки нервного гребня могут начать мигрировать по всему эмбриону.
.jpg/440px-Migration_of_Neural_Crest_Cells_(v2).jpg)
Миграция клеток нервного гребня происходит в ростральном направлении к каудальному без необходимости использования нейронного каркаса , например, вдоль радиальных глиальных клеток . По этой причине процесс миграции клеток гребня называется «свободной миграцией». Вместо каркаса на клетках-предшественниках миграция нервного гребня является результатом отталкивающего направления через EphB / EphrinB и передачу сигналов семафорина / нейропилина , взаимодействия с внеклеточным матриксом и контактного ингибирования друг с другом. [17] Хотя белки эфрин и Eph обладают способностью передавать двунаправленный сигнал, отталкивание клеток нервного гребня использует преимущественно прямую передачу сигналов, чтобы инициировать ответ внутри рецептора , несущего клетку нервного гребня. [23] Растущие клетки нервного гребня экспрессируют EphB, рецепторную тирозинкиназу , которая связывает трансмембранный лиганд EphrinB , экспрессируемый в каудальной половине каждого сомита . Когда эти два домена взаимодействуют, это вызывает фосфорилирование тирозина рецептора, активацию rhoGTPase и возможные цитоскелетные перестройки внутри клеток гребня, вызывающие их отталкивание. Это явление позволяет клеткам нервного гребня проходить через ростральную часть каждого сомита. [17]
Передача отталкивающих сигналов семафорин-нейропилин работает синергетически с передачей сигналов EphB, направляя клетки нервного гребня вниз по ростральной половине сомитов у мышей. У куриных эмбрионов семафорин действует в головной области, направляя клетки нервного гребня через глоточные дуги . Помимо отталкивающей передачи сигналов, клетки нервного гребня экспрессируют интегрины β1 и α4 , которые обеспечивают связывание и управляемое взаимодействие с коллагеном , ламинином и фибронектином внеклеточного матрикса во время их перемещения. Кроме того, клетки гребня обладают внутренним торможением контакта друг с другом, свободно проникая в ткани различного происхождения, такие как мезодерма . [17] Клетки нервного гребня, мигрирующие через ростральную половину сомитов, дифференцируются в сенсорные и симпатические нейроны периферической нервной системы . Другой основной путь, по которому идут клетки нервного гребня, — дорсолатеральный между эпидермисом и дермамиотомом . Клетки, мигрирующие по этому пути , дифференцируются в пигментные клетки дермы . Дальнейшая дифференцировка клеток нервного гребня и спецификация их окончательного типа клеток смещены в зависимости от их пространственно-временной подчиненности морфогенным сигналам, таким как BMP, Wnt, FGF, Hox и Notch . [20]
Нейрокристопатии возникают в результате аномальной спецификации, миграции, дифференцировки или гибели клеток нервного гребня на протяжении эмбрионального развития. [24] [25] Эта группа заболеваний включает широкий спектр врожденных пороков развития, поражающих многих новорожденных. Кроме того, они возникают из-за генетических дефектов, влияющих на формирование нервного гребня, и из-за действия тератогенов [26].
Синдром Ваарденбурга — нейрокристопатия , возникающая в результате нарушения миграции клеток нервного гребня. Основные характеристики этого заболевания включают пегие глаза и врожденную глухоту . В случае пегости бесцветные участки кожи вызваны полным отсутствием меланоцитов , вырабатывающих пигмент нервного гребня . [27] Существует четыре различных типа синдрома Ваарденбурга, каждый из которых имеет различные генетические и физиологические особенности. Типы I и II различают в зависимости от того, страдают ли члены семьи больного человека антиутопией канторум . [28] Тип III приводит к аномалиям верхних конечностей. Наконец, тип IV также известен как синдром Ваарденбурга-Шаха, и у больных с ним наблюдаются как синдром Ваарденбурга, так и болезнь Гиршпрунга . [29] Типы I и III наследуются по аутосомно -доминантному типу, [27] тогда как II и IV демонстрируют аутосомно-рецессивный тип наследования. В целом синдром Ваарденбурга встречается редко, его частота в США составляет ~ 2/100 000 человек. Все расы и полы страдают в равной степени. [27] В настоящее время не существует лекарства или лечения синдрома Ваарденбурга.
К дефектам, связанным с развитием и миграцией клеток нервного гребня, также причастна болезнь Гиршпрунга (HD или HSCR), характеризующаяся отсутствием иннервации в участках кишечника . Отсутствие иннервации может привести к дальнейшим физиологическим отклонениям, таким как увеличение толстой кишки ( мегаколон ), непроходимость кишечника или даже замедление роста. При здоровом развитии клетки нервного гребня мигрируют в кишечник и образуют кишечные ганглии . Гены, играющие роль в здоровой миграции этих клеток нервного гребня в кишечник, включают RET , GDNF , GFRα , EDN3 и EDNRB . RET , рецепторная тирозинкиназа (RTK), образует комплекс с GDNF и GFRα . EDN3 и EDNRB тогда участвуют в одной и той же сигнальной сети. Когда эта передача сигналов нарушается у мышей, возникает аганглионоз или отсутствие этих кишечных ганглиев. [30]
Пренатальное воздействие алкоголя (ПАЭ) является одной из наиболее частых причин пороков развития . [31] В зависимости от степени воздействия и тяжести возникших в результате нарушений у пациентов диагностируется ряд расстройств, получивших широкое название «расстройство фетального алкогольного спектра» (ФАСН). Тяжелая форма ФАСН может нарушать миграцию нервного гребня , о чем свидетельствуют характерные черепно-лицевые аномалии , включая короткие глазные щели , удлиненную верхнюю губу и сглаженный желобок . Однако из-за беспорядочного характера связывания этанола механизмы возникновения этих нарушений до сих пор неясны. Эксплантаты клеточной культуры клеток нервного гребня, а также развивающиеся in vivo эмбрионы рыбок данио , подвергнутые воздействию этанола, демонстрируют уменьшенное количество мигрирующих клеток и уменьшение расстояний, которые проходят мигрирующие клетки нервного гребня. Механизмы этих изменений не совсем понятны, но данные свидетельствуют о том, что ПАЭ может усиливать апоптоз из-за повышения уровня цитозольного кальция , вызванного IP3 -опосредованным высвобождением кальция из внутриклеточных депо. Также было высказано предположение, что снижение жизнеспособности клеток нервного гребня, подвергшихся воздействию этанола, вызвано повышенным окислительным стрессом . Несмотря на эти и другие достижения, еще многое предстоит выяснить о том, как этанол влияет на развитие нервного гребня. Например, оказывается, что этанол по-разному влияет на одни клетки нервного гребня по сравнению с другими; то есть, хотя черепно-лицевые аномалии часто встречаются при ПАЭ, пигментные клетки нервного гребня поражаются минимально. [32]
Синдром ДиДжорджа связан с делециями или транслокациями небольшого сегмента хромосомы человека 22 . Эта делеция может нарушить миграцию или развитие ростральных клеток нервного гребня . Некоторые наблюдаемые дефекты связаны с системой глоточного мешка , которая получает вклад от клеток рострального мигрирующего гребня. Симптомы синдрома ДиДжорджа включают врожденные пороки сердца , дефекты лица , а также некоторые неврологические нарушения и нарушения обучаемости . Сообщалось также, что у пациентов с делецией 22q11 чаще встречается шизофрения и биполярное расстройство . [33]
Синдром Тричера-Коллинза (TCS) возникает в результате нарушения развития первой и второй глоточных дуг на ранней эмбриональной стадии, что в конечном итоге приводит к аномалиям средней и нижней части лица. TCS вызван миссенс-мутацией гена TCOF1 , которая заставляет клетки нервного гребня подвергаться апоптозу во время эмбриогенеза . Хотя мутации гена TCOF1 являются одними из наиболее изученных по своей роли при СТО, мутации в генах POLR1C и POLR1D также связаны с патогенезом СТО. [34]
Клетки нервного гребня, возникающие из разных положений по передне -задней оси, развиваются в различные ткани. Эти области нервного гребня можно разделить на четыре основных функциональных домена, которые включают краниальный нервный гребень, туловищный нервный гребень, блуждающий и крестцовый нервный гребень и сердечный нервный гребень.
Краниальный нервный гребень мигрирует дорсолатерально, образуя черепно-лицевую мезенхиму, которая дифференцируется в различные черепные ганглии, черепно-лицевые хрящи и кости. [21] Эти клетки попадают в глоточные мешочки и дуги, где вносят вклад в вилочковую железу , кости среднего уха и челюсти, а также одонтобласты зачатков зубов. [35]
Ствол нервного гребня дает начало двум популяциям клеток. [36] Одна группа клеток, которым суждено стать меланоцитами , мигрирует дорсолатерально в эктодерму по направлению к вентральной срединной линии. Вторая группа клеток мигрирует вентролатерально через переднюю часть каждого склеротома . Клетки, которые остаются в склеротоме, образуют ганглии дорсальных корешков , тогда как те, которые продолжаются вентрально, образуют симпатические ганглии, мозговое вещество надпочечников и нервы, окружающие аорту. [35]
Клетки блуждающего и сакрального нервного гребня развиваются в ганглии кишечной нервной системы и парасимпатические ганглии. [35]
Сердечный нервный гребень развивается в меланоциты, хрящи, соединительную ткань и нейроны некоторых глоточных дуг. Кроме того, этот домен дает начало таким областям сердца, как мышечно-соединительная ткань крупных артерий и части перегородки , которая отделяет малое кровообращение от аорты. [35] Согласно новому исследованию, полулунные клапаны сердца связаны с клетками нервного гребня. [37]
Ряд структур, отличающих позвоночных от других хордовых, образован из производных клеток нервного гребня. В своей теории «новой головы» Ганс и Норткат утверждают, что наличие нервного гребня было основой специфических особенностей позвоночных, таких как сенсорные ганглии и черепной скелет. Более того, появление этих особенностей сыграло решающую роль в эволюции позвоночных, поскольку позволило им вести хищнический образ жизни. [38] [39]
Однако признание нервного гребня инновацией позвоночных не означает, что он возник de novo . Вместо этого новые структуры часто возникают в результате модификации существующих программ регулирования развития. Например, программы регулирования могут быть изменены за счет привлечения новых вышестоящих регуляторов или за счет использования новых нижестоящих генов-мишеней, помещая таким образом существующие сети в новый контекст. [40] [41] Эта идея подтверждается данными гибридизации in situ , которые показывают сохранение спецификаторов границ нервной пластинки у протохордовых , что позволяет предположить, что часть сети предшественников нервного гребня присутствовала у общего предка хордовых. [5] У некоторых беспозвоночных хордовых, таких как оболочники, была идентифицирована линия клеток (меланоцитов), которые похожи на клетки нервного гребня у позвоночных. Это означает, что рудиментарный нервный гребень существовал у общего предка позвоночных и оболочников. [42]
Эктомезенхима (также известная как мезэктодерма ): [43] одонтобласты , зубные сосочки , хондрокраниум (носовая капсула, меккелевы хрящи , склеральные косточки, квадратные кости, суставы, подъязычная кость и колумелла), трахеальный и гортанный хрящи, дерматокраниум (перепончатые кости), дорсальная часть. плавники и пластрон черепахи (низшие позвоночные животные), перициты и гладкие мышцы жаберных артерий и вен, сухожилия глазных и жевательных мышц, соединительная ткань желез головы и шеи (гипофиз, слюнные, слезные, тимус, щитовидная железа), дерма и жировая ткань свод черепа, вентральная часть шеи и лицо
Эндокринные клетки : хромаффинные клетки мозгового вещества надпочечников, гломусные клетки I/II типа.
Периферическая нервная система : сенсорные нейроны и глия ганглиев дорсальных корешков , головные ганглии (VII и частично V, IX и X), клетки Рохона-Борода , некоторые клетки Меркеля в усах, [44] [45] Сателлитная глия. клетки всех вегетативных и сенсорных ганглиев, шванновские клетки всех периферических нервов.
Кишечные клетки : Энтерохромаффинные клетки . [46]
Меланоциты , мышечные и пигментные клетки радужной оболочки и даже ассоциированы с некоторыми опухолями (например, меланотической нейроэктодермальной опухолью младенчества ).