
Кокколитофориды , или кокколитофориды , — одноклеточные организмы , входящие в состав фитопланктона , автотрофного (самопитающегося) компонента планктонного сообщества . Они образуют группу, насчитывающую около 200 видов, и принадлежат либо к королевству Protista , согласно системе пяти королевств Роберта Уиттакера , либо к кладе Hacrobia , согласно более новой системе биологической классификации. В пределах Hacrobia кокколитофоры относятся к типу или разделу Haptophyta , классу Prymnesiophyceae (или Coccolithophyceae ). Кокколитофоры почти исключительно морские , фотосинтезирующие и существуют в больших количествах по всей солнечной зоне океана .
Кокколитофоры — самые продуктивные кальцинирующие организмы на планете, покрытые оболочкой из карбоната кальция, называемой коккосферой . Однако причины их кальцификации остаются неясными. Одной из ключевых функций может быть то, что коккосфера обеспечивает защиту от хищничества микрозоопланктона , который является одной из основных причин гибели фитопланктона в океане. [1]
Кокколитофоры экологически важны и биогеохимически играют важную роль в морском биологическом насосе и углеродном цикле . [2] [1] В зависимости от среды обитания они могут производить до 40 процентов местной первичной морской продукции . [3] Они представляют особый интерес для тех, кто изучает глобальное изменение климата , поскольку по мере повышения кислотности океана их кокколиты могут стать еще более важными поглотителями углерода . [4] Стратегии управления используются для предотвращения цветения кокколитофоров, связанного с эвтрофикацией , поскольку это цветение приводит к уменьшению потока питательных веществ в нижние уровни океана. [5]
Самый распространенный вид кокколитофоры, Emiliania huxleyi , принадлежит к порядку Isochrysidales и семейству Noëlaerhabdaceae . [6] Встречается в умеренных , субтропических и тропических океанах. [7] Это делает E. huxleyi важной частью планктонной основы значительной части морских пищевых сетей . Это также самый быстрорастущий кокколитофор в лабораторных культурах. [8] Его изучают на предмет обширного цветения , которое он образует в водах, обедненных питательными веществами, после реформирования летнего термоклина . [9] [10] и для производства молекул, известных как алкеноны , которые обычно используются учеными-землеведами в качестве средства для оценки прошлых температур поверхности моря . [11]
Кокколитофориды (или кокколитофориды, от прилагательного [12] ) образуют группу, насчитывающую около 200 видов фитопланктона. [13] Они принадлежат либо к королевству Протиста , согласно классификации Пяти королевств Роберта Уиттакера , либо к кладе Хакробия , согласно новой биологической системе классификации. В составе Hacrobia кокколитофоры относятся к типу или разделу Haptophyta , классу Prymnesiophyceae (или Coccolithophyceae ). [6] Кокколитофоры отличаются особыми пластинками (или чешуйками) карбоната кальция неопределенной функции, называемыми кокколитами , которые также являются важными микроокаменелостями . Однако существуют виды Prymnesiophyceae, лишенные кокколитов (например, в роде Prymnesium ), поэтому не каждый представитель Prymnesiophyceae является кокколитофором. [14]
Кокколитофоры — одноклеточный фитопланктон , образующий мелкие чешуйки карбоната кальция (CaCO 3 ) ( кокколиты ), которые покрывают поверхность клеток в виде сферического покрытия, называемого коккосферой . Они были неотъемлемой частью морских планктонных сообществ начиная с юрского периода . [15] [16] Сегодня кокколитофоры способствуют ~1–10% фиксации неорганического углерода (кальцификации) от общей фиксации углерода (кальцификации плюс фотосинтеза) в поверхностном океане [17] и ~50% пелагических отложений CaCO 3 . [18] Их известковая оболочка увеличивает скорость погружения фотосинтетически зафиксированного CO 2 в глубокие глубины океана за счет балластирования органического вещества. [19] [20] В то же время биогенное осаждение карбоната кальция во время образования кокколита снижает общую щелочность морской воды и выделяет CO 2 . [21] [22] Таким образом, кокколитофоры играют важную роль в морском углеродном цикле , влияя на эффективность биологического углеродного насоса и поглощение океаном атмосферного CO 2 . [1]
По состоянию на 2021 год неизвестно, почему кокколитофоры кальцифицируются и как их способность производить кокколиты связана с их экологическим успехом. [23] [24] [25] [26] [27] Наиболее вероятным преимуществом наличия коккосферы является защита от хищников и вирусов. [28] [26] Вирусная инфекция является важной причиной гибели фитопланктона в океанах, [29] и недавно было показано, что кальцификация может влиять на взаимодействие между кокколитофором и его вирусом. [30] [31] Основными хищниками морского фитопланктона являются микрозоопланктон, такой как инфузории и динофлагелляты . По оценкам, они потребляют около двух третей первичной продукции океана [32], а микрозоопланктон может оказывать сильное пастбищное давление на популяции кокколитофороф. [33] Хотя кальцификация не предотвращает хищничество, утверждается, что коккосфера снижает эффективность выпаса, затрудняя хищнику использование органического содержимого кокколитофоров. [34] Гетеротрофные протисты способны выборочно выбирать добычу на основе ее размера или формы, а также с помощью химических сигналов [35] [36] и, таким образом, могут отдавать предпочтение другой добыче, которая доступна и не защищена кокколитами. [1]

Кокколитофоры представляют собой сферические клетки диаметром около 5–100 микрометров, окруженные известковыми пластинками, называемыми кокколитами , диаметром около 2–25 микрометров. Каждая клетка содержит два коричневых хлоропласта , окружающих ядро . [39]
В каждой коккосфере заключена одна клетка с мембраносвязанными органеллами . Два крупных хлоропласта с коричневым пигментом расположены по обе стороны клетки и окружают ядро , митохондрии , аппарат Гольджи , эндоплазматическую сеть и другие органеллы. Каждая клетка также имеет две жгутиковые структуры, которые участвуют не только в подвижности, но и в митозе и формировании цитоскелета . [40] У некоторых видов также присутствует функциональная или рудиментарная гаптонема . [41] Эта структура, уникальная для гаптофитов , скручивается и раскручивается в ответ на раздражители окружающей среды. Хотя это плохо изучено, было предложено участвовать в захвате добычи. [40]
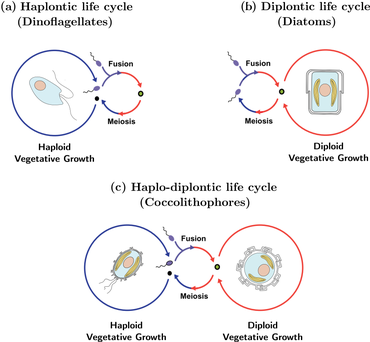
Сложный жизненный цикл кокколитофоров известен как гаплодиплонтный жизненный цикл и характеризуется чередованием как бесполых, так и половых фаз. Бесполая фаза известна как гаплоидная фаза, а половая фаза известна как диплоидная фаза. Во время гаплоидной фазы кокколитофороры производят гаплоидные клетки посредством митоза . Эти гаплоидные клетки затем могут делиться дальше посредством митоза или подвергаться половому размножению с другими гаплоидными клетками. Полученная диплоидная клетка проходит мейоз и снова производит гаплоидные клетки, начиная цикл заново. У кокколитофоров бесполое размножение путем митоза возможно на обеих фазах жизненного цикла, что контрастирует с большинством других организмов, имеющих чередующиеся жизненные циклы. [42] Как абиотические , так и биотические факторы могут влиять на частоту возникновения каждой фазы. [43]
Кокколитофоры размножаются бесполым путем путем бинарного деления. В этом процессе кокколиты родительской клетки делятся между двумя дочерними клетками. Были предположения о возможном наличии процесса полового размножения за счет диплоидных стадий кокколитофоров, но этот процесс никогда не наблюдался. [44]
K или r-выбранные стратегии кокколитофоров зависят от стадии их жизненного цикла. Когда кокколитофороры диплоидны, они подвергаются r-отбору. На этом этапе они переносят более широкий диапазон питательных составов. Когда они гаплоидны, они подвергаются K-отбору и часто более конкурентоспособны в стабильной среде с низким содержанием питательных веществ. [44] Большинство кокколитофоров являются стратегами K и обычно встречаются в бедных питательными веществами поверхностных водах. Они являются плохими конкурентами по сравнению с другим фитопланктоном и процветают в средах обитания, где другой фитопланктон не выжил бы. [45] Эти две стадии жизненного цикла кокколитофоров происходят сезонно, когда больше питательных веществ доступно в более теплые сезоны и меньше — в более прохладные. Этот тип жизненного цикла известен как сложный гетероморфный жизненный цикл. [44]

Кокколитофоры встречаются во всем Мировом океане. Их распределение варьируется по вертикали в зависимости от стратифицированных слоев океана и географически в зависимости от временных зон. [46] Хотя большинство современных кокколитофоров могут быть расположены в связанных с ними стратифицированных олиготрофных условиях, наиболее обильные районы кокколитофоров, где наблюдается наибольшее видовое разнообразие, расположены в субтропических зонах с умеренным климатом. [47] Хотя температура воды и интенсивность света, попадающего на поверхность воды, являются более влиятельными факторами в определении местонахождения видов, океанские течения также могут определять местонахождения определенных видов кокколитофоров. [48]
Хотя подвижность и образование колоний варьируются в зависимости от жизненного цикла различных видов кокколитофоров, часто происходит чередование подвижной, гаплоидной фазы и неподвижной диплоидной фазы. На обеих фазах распространение организма во многом происходит за счет океанских течений и особенностей циркуляции. [49]
В Тихом океане было идентифицировано около 90 видов в шести отдельных зонах, относящихся к различным тихоокеанским течениям, которые содержат уникальные группы разных видов кокколитофоров. [50] Самое большое разнообразие кокколитофоров в Тихом океане наблюдалось в районе океана, который считается центральной северной зоной, которая представляет собой область между 30 ° и 5 ° северной широты, состоящую из Северного экваториального течения и экваториального противотечения. Эти два течения движутся в противоположных направлениях, на восток и запад, что приводит к сильному смешиванию вод и позволяет заселить территорию большому разнообразию видов. [50]
В Атлантическом океане наиболее многочисленными видами являются E. huxleyi и Florisphaera profunda с меньшими концентрациями видов Umbellosphaera ignores , Umbellosphaera tenuis и различных видов Gephyrocapsa . [50] На численность глубоководных видов кокколитофоров сильно влияет глубина нутриклина и термоклина . Численность этих кокколитофоров увеличивается, когда нутриклин и термоклин глубоки, и уменьшается, когда они неглубоки. [51]

Полное распространение кокколитофоров в настоящее время неизвестно, а некоторые регионы, такие как Индийский океан, изучены не так хорошо, как другие места в Тихом и Атлантическом океанах. Также очень сложно объяснить распределение из-за множества постоянно меняющихся факторов, влияющих на свойства океана, таких как прибрежный и экваториальный апвеллинг , фронтальные системы, донная среда, уникальная топография океана и очаги изолированных высоких или низких температур воды. [53]
Верхняя фототическая зона имеет низкую концентрацию питательных веществ, высокую интенсивность и проникновение света и обычно более высокую температуру. Нижняя фотозона отличается высокой концентрацией питательных веществ, низкой интенсивностью и проникновением света и относительно прохладной. Средняя фотозона — это область, которая содержит одинаковые значения между нижней и верхней фотозоной. [47]
Большой кальцитовый пояс Южного океана представляет собой область повышенной концентрации кальцита в верхних слоях океана в летнее время, полученную из кокколитофоров, несмотря на то, что этот регион известен преобладанием диатомовых водорослей. Перекрытие двух основных групп фитопланктона, кокколитофоров и диатомей, в динамических фронтальных системах, характерных для этого региона, обеспечивает идеальные условия для изучения влияния окружающей среды на распределение различных видов внутри этих таксономических групп. [56]
Большой кальцитовый пояс, определяемый как повышенное содержание неорганического углерода в виде частиц (PIC), встречающийся наряду с сезонно повышенным содержанием хлорофилла а южной весной и летом в Южном океане, [57] играет важную роль в колебаниях климата, [58] [59] на более чем 60% площади Южного океана (30–60° ю.ш.). [60] Регион между 30° и 50° ю.ш. имеет самое высокое поглощение антропогенного углекислого газа (CO 2 ) наряду с Северной Атлантикой и северной частью Тихого океана. [61]
Недавние исследования показывают, что изменение климата оказывает прямое и косвенное влияние на распространение и продуктивность кокколитофор. На них неизбежно повлияют повышение температуры и термическая стратификация верхнего слоя океана, поскольку они являются основными средствами контроля их экологии, хотя неясно, приведет ли глобальное потепление к чистому увеличению или уменьшению численности кокколитофоров. Поскольку они являются кальцифицирующими организмами, было высказано предположение, что закисление океана из-за увеличения количества углекислого газа может серьезно повлиять на кокколитофоры. [51] Недавнее увеличение выбросов CO 2 привело к резкому увеличению популяции кокколитофоров. [62]


Кокколитофоры — одни из наиболее распространенных первичных производителей в океане. Как таковые, они вносят большой вклад в первичную продуктивность тропических и субтропических океанов, однако какой именно объем еще предстоит зарегистрировать. [66]
Соотношение концентраций азота , фосфора и силикатов в отдельных районах океана диктует конкурентное доминирование внутри фитопланктонных сообществ. Каждое соотношение по существу склоняет шансы в пользу либо диатомовых водорослей , либо других групп фитопланктона, таких как кокколитофоры. Низкое соотношение силикатов к азоту и фосфору позволяет кокколитофорам вытеснять другие виды фитопланктона; однако, когда соотношение силикатов, фосфора и азота высокое, кокколитофоры вытесняются диатомовыми водорослями. Увеличение сельскохозяйственных процессов приводит к эвтрофикации вод и, таким образом, к цветению кокколитофоров в этих средах с высоким содержанием азота и фосфора и низким содержанием силиката. [5]
Кальцит в карбонате кальция позволяет кокколитам рассеивать больше света , чем поглощать. Это имеет два важных последствия: 1) поверхностные воды становятся ярче, что означает, что у них более высокое альбедо , и 2) происходит фотоингибирование , то есть производство фотосинтеза уменьшается из-за избытка света. В случае 1) высокая концентрация кокколитов приводит к одновременному повышению температуры поверхностных вод и снижению температуры более глубоких вод. Это приводит к большей стратификации толщи воды и уменьшению вертикального перемешивания питательных веществ. Однако исследование 2012 года показало, что общее влияние кокколитофоров на увеличение радиационного воздействия на океан меньше, чем влияние антропогенных факторов. [67] Таким образом, общим результатом большого цветения кокколитофоров является снижение продуктивности водной толщи, а не вклад в глобальное потепление.
Их хищники включают обычных хищников всего фитопланктона, включая мелкую рыбу, зоопланктон и личинки моллюсков. [45] [68] Вирусы, специфичные для этого вида, были выделены из нескольких мест по всему миру и, по-видимому, играют важную роль в динамике весеннего цветения.
Никаких свидетельств токсичности кокколитофоров из окружающей среды не поступало, но они принадлежат к классу Prymnesiophyceae, который включает отряды с токсичными видами. Токсичные виды обнаружены у родов Prymnesium Massart и Chrysochromulina Lackey. Было обнаружено , что представители рода Prymnesium продуцируют гемолитические соединения - агент, ответственный за токсичность. Некоторые из этих токсичных видов являются причиной гибели крупных рыб и могут накапливаться в таких организмах, как моллюски; перенося его по пищевой цепи. Лабораторные испытания на токсичность показали, что представители океанических кокколитофор родов Emiliania, Gephyrocapsa, Calcidiscus и Coccolithus нетоксичны, как и виды прибрежного рода Hymenomonas , однако несколько видов Pleurochrysis и Jomonlithus (оба прибрежных рода) были токсичны для артемии . [68]
Кокколитофориды преимущественно встречаются в виде одиночных свободно плавающих гаплоидных или диплоидных клеток. [46]
Большинству фитопланктона для выживания необходим солнечный свет и питательные вещества из океана, поэтому они процветают в районах с большим количеством богатой питательными веществами воды, поднимающейся с нижних уровней океана. Большинству кокколитофоров требуется солнечный свет только для производства энергии, и у них более высокий коэффициент поглощения нитратов по сравнению с поглощением аммония (азот необходим для роста и может использоваться непосредственно из нитрата, но не из аммония). Из-за этого они процветают в тихой, бедной питательными веществами среде, где другой фитопланктон голодает. [69] Компромиссы , связанные с такими более высокими темпами роста, включают меньший радиус клеток и меньший объем клеток, чем у других типов фитопланктона.
Известно, что гигантские ДНК-содержащие вирусы литически заражают кокколитофоры, особенно E. huxleyi . Эти вирусы, известные как вирусы E. huxleyi (EhV), по-видимому, почти исключительно заражают покрытую коккосферой диплоидную фазу жизненного цикла. Было высказано предположение, что, поскольку гаплоидный организм не инфицирован и, следовательно, не затронут вирусом, коэволюционная « гонка вооружений » между кокколитофорами и этими вирусами не следует классической эволюционной схеме Красной Королевы , а вместо этого следует «Чеширскому коту». экологическая динамика. [70] Более поздние работы показали, что вирусный синтез сфинголипидов и индукция запрограммированной гибели клеток обеспечивает более прямую связь для изучения коэволюционной гонки вооружений, подобной Красной Королеве, по крайней мере, между кокколитовирусами и диплоидным организмом. [43]
Кокколитофоры являются членами клады Haptophyta , которая является сестринской кладой Centrohelida , которые оба находятся в Haptista . [71] Самые старые известные кокколитофоры известны из позднего триаса, вокруг границы Нория и Ретии . [72] Разнообразие неуклонно увеличивалось в течение мезозоя, достигнув своего апогея в позднем меловом периоде . Однако во время мел-палеогенового вымирания произошло резкое падение , когда вымерло более 90% видов кокколитофоров. Кокколиты достигли другого, более низкого пика разнообразия во время палеоцен-эоценового термического максимума , но впоследствии их численность сократилась с олигоцена из-за снижения глобальных температур, при этом наиболее сильно пострадали виды, производившие крупные и сильно кальцинированные кокколиты. [26]


Каждый кокколитофор заключен в защитную оболочку из кокколитов , кальцинированных чешуек, которые составляют его экзоскелет или коккосферу . [73] Кокколиты создаются внутри клетки кокколитофора, и хотя некоторые виды поддерживают один слой на протяжении всей жизни, производя только новые кокколиты по мере роста клетки, другие постоянно производят и сбрасывают кокколиты.
Основным компонентом кокколитов является карбонат кальция или мел . Карбонат кальция прозрачен, поэтому фотосинтетическая активность организмов не снижается из-за инкапсуляции в коккосферу. [45]
Кокколиты образуются в результате процесса биоминерализации , известного как кокколитогенез. [39] Как правило, кальцификация кокколитов происходит в присутствии света, и эти чешуйки образуются гораздо чаще во время экспоненциальной фазы роста, чем в стационарной фазе. [74] Хотя процесс биоминерализации еще не до конца понятен, он жестко регулируется передачей сигналов кальция . Образование кальцита начинается в комплексе Гольджи , где белковые матрицы способствуют образованию кристаллов CaCO 3 , а сложные кислые полисахариды контролируют форму и рост этих кристаллов. [49] По мере образования каждой чешуи она экспортируется в везикулу , полученную из аппарата Гольджи , и добавляется на внутреннюю поверхность коккосферы. Это означает, что кокколиты, образовавшиеся совсем недавно, могут лежать под более старыми кокколитами. [42] В зависимости от стадии жизненного цикла фитопланктона могут образовываться два разных типа кокколитов. Голококколиты образуются только в гаплоидной фазе, лишены радиальной симметрии и состоят из сотен или тысяч одинаковых мельчайших (около 0,1 мкм) ромбических кристаллов кальцита . Считается, что эти кристаллы формируются, по крайней мере частично, вне клетки. Гетерококколиты встречаются только в диплоидной фазе, имеют радиальную симметрию и состоят из относительно небольшого числа сложных кристаллических единиц (менее 100). Хотя они и редки, в планктоне наблюдались комбинированные коккосферы, содержащие как голококколиты, так и гетерококколиты, регистрирующие переходы жизненного цикла кокколитофоров. Наконец, коккосферы некоторых видов сильно модифицированы различными придатками, состоящими из специализированных кокколитов. [53]
Хотя точная функция коккосферы неясна, было предложено множество потенциальных функций. Наиболее очевидно, что кокколиты могут защищать фитопланктон от хищников. Похоже также, что это помогает им создать более стабильный уровень pH . В ходе фотосинтеза из воды удаляется углекислый газ, что делает ее более щелочной. Кальцификация также удаляет углекислый газ, но химические процессы, стоящие за ней, приводят к противоположной реакции pH; это делает воду более кислой. Таким образом, сочетание фотосинтеза и кальцификации уравновешивает друг друга в отношении изменений pH. [75] Кроме того, эти экзоскелеты могут дать преимущество в производстве энергии, поскольку кокколитогенез, по-видимому, тесно связан с фотосинтезом. Органическое осаждение карбоната кальция из раствора бикарбоната приводит к образованию свободного углекислого газа непосредственно внутри клеточного тела водоросли, этот дополнительный источник газа затем доступен кокколитофору для фотосинтеза. Было высказано предположение, что они могут обеспечивать барьер, подобный клеточной стенке, для изоляции внутриклеточных химических веществ от морской среды. [76] Более специфические защитные свойства кокколитов могут включать защиту от осмотических изменений, химического или механического шока и коротковолнового света. [41] Также было высказано предположение, что добавленный вес нескольких слоев кокколитов позволяет организму погружаться в более низкие, более богатые питательными веществами слои воды и, наоборот, что кокколиты добавляют плавучесть, не давая клетке опускаться на опасные глубины. [77] Предполагается, что придатки кокколита выполняют несколько функций, например, препятствуют выпасу зоопланктона. [53]
Кокколиты являются основным компонентом Мела , позднемелового горного образования, которое широко выходит на поверхность на юге Англии и образует Белые скалы Дувра , а также других подобных пород во многих других частях мира. [10] В настоящее время осадочные кокколиты являются основным компонентом известковых илов , которые покрывают до 35% дна океана и местами имеют толщину в несколько километров. [49] Из-за своего обилия и широкого географического распространения кокколиты, составляющие слои этого ила, и меловые осадки, образующиеся при его уплотнении, служат ценными микроископаемыми .

Кальцификация , биологическое производство карбоната кальция (CaCO 3 ), является ключевым процессом в морском углеродном цикле . Кокколитофоры являются основной планктонной группой, ответственной за пелагическое производство CaCO 3 . [78] [79] На диаграмме справа показаны энергетические затраты на кальцификацию кокколитофора:

На диаграмме слева показаны преимущества кальцификации кокколитофоров. (A) Ускоренный фотосинтез включает CCM (1) и повышенное поглощение света за счет рассеяния редких фотонов для глубоко обитающих видов (2). (B) Защита от фотоповреждений включает защиту солнцезащитного козырька от ультрафиолетового (УФ) света и фотосинтетического активного излучения (ФАР) (1), а также рассеивание энергии в условиях яркого освещения (2). (C) Броневая защита включает защиту от вирусных/бактериальных инфекций (1) и выпаса селективными (2) и неселективными (3) травоядными. [26]
Степень, в которой кальцификация может адаптироваться к закислению океана , в настоящее время неизвестна. Физиологические исследования клеток показали, что существенный отток H + (вытекающий из использования HCO 3 − для внутриклеточной кальцификации) становится более дорогостоящим при продолжающемся закислении океана, поскольку электрохимический градиент H + внутрь наружу снижается и пассивный отток протонов затрудняется. [80] Адаптированным клеткам придется чаще активировать протонные каналы , регулировать свой мембранный потенциал и/или снижать внутренний pH . [81] Снижение внутриклеточного pH серьезно повлияет на весь клеточный механизм и потребует совместной адаптации других процессов (например, фотосинтеза ), чтобы поддерживать отток H + . [82] [83] Обязательный отток H + , связанный с кальцификацией, поэтому может представлять собой фундаментальное ограничение на адаптацию, что потенциально может объяснить, почему «кризис кальцификации» был возможен во время длительных (тысячи лет) событий возмущения CO 2 [84] [ 85] , хотя эволюционная адаптация к изменяющимся условиям карбонатного химии возможна в течение одного года. [84] [85] Распутывание этих фундаментальных ограничений и пределов адаптации должно быть в центре внимания будущих исследований кокколитофоров, поскольку их знание является ключевой информацией, необходимой для понимания того, в какой степени реакция кальцификации на химические возмущения карбонатов может быть компенсирована эволюцией. [86]
Функциональные группы, защищенные силикатом или целлюлозой, такие как диатомовые водоросли и динофлагелляты , не нуждаются в поддержании связанного с кальцификацией оттока H + . Таким образом, им, вероятно, не нужно адаптироваться, чтобы сохранить низкие затраты на производство конструктивных элементов. Напротив, динофлагелляты (за исключением кальцифицирующих видов; [87] с обычно неэффективными ферментами RuBisCO , фиксирующими CO 2 [88] могут даже извлечь выгоду из химических изменений, поскольку фотосинтетическая фиксация углерода как источника структурных элементов в форме целлюлозы должна быть облегчена. в результате подкисления океана, связанного с удобрением CO 2. [89] [90] Если предположить, что любая форма панциря/экзоскелета защищает фитопланктон от хищников [28], неизвестковая броня может быть предпочтительным решением для реализации защиты в будущем океане. [86]
Диаграмма справа показывает, как действуют сравнительные энергетические усилия для построения панциря у диатомей, динофлагеллят и кокколитофоров. Панцирь (панцирь диатомовой водоросли) кажется самым недорогим панцирем при любых обстоятельствах, поскольку диатомовые водоросли обычно вытесняют все другие группы, когда доступен силикат . Коккосфера относительно недорога при достаточном [CO 2 ], высоком [HCO 3 - ] и низком [H + ], поскольку субстрат насыщает и протоны легко высвобождаются в морскую воду. [80] Напротив, строительству текальных элементов, которые представляют собой органические ( целлюлозные ) пластинки, составляющие оболочку динофлагеллят, скорее следует отдавать предпочтение при высоких концентрациях H + , поскольку они обычно совпадают с высокими [CO 2 ]. В этих условиях динофлагелляты могут подавлять энергозатратную работу механизмов концентрации углерода, необходимых для производства органического исходного материала для их панциря. Следовательно, сдвиг условий карбонатной химии в сторону высоких значений [CO 2 ] может повысить их конкурентоспособность по сравнению с кокколитофорами. Однако такое гипотетическое повышение конкурентоспособности за счет изменения условий карбонатного химического состава не приведет автоматически к доминированию динофлагеллят, поскольку на видовой состав также влияет огромное количество факторов, помимо химического состава карбонатов . [86] [91]
В настоящее время данные, подтверждающие или опровергающие защитную функцию коккосферы от хищников, ограничены. Некоторые исследователи обнаружили, что общие показатели хищничества микрозоопланктона снижались во время цветения кокколитофоры Emiliania huxleyi , [92] [93] , в то время как другие обнаружили высокие показатели выедания микрозоопланктона в естественных сообществах кокколитофоров. [94] В 2020 году исследователи обнаружили, что скорость поступления микрозоопланктона in situ на E. huxleyi существенно не отличается от таковой на некальцифицирующемся фитопланктоне аналогичного размера. [95] В лабораторных экспериментах гетеротрофная динофлагеллята Oxyrris marina предпочитала кальцинированные, а не некальцинированные клетки E. huxleyi , что, как предполагалось, было связано с селективным пищевым поведением по размеру, поскольку кальцинированные клетки крупнее, чем некальцинированные E. huxleyi . [96] В 2015 году Харви и др. исследовали хищничество динофлагелляты O. marina на разных генотипах некальцифицирующегося E. huxleyi , а также на кальцинированных штаммах, различающихся по степени кальцификации. [97] Они обнаружили, что частота употребления O. marina зависела от предложенного генотипа E. huxleyi , а не от степени их кальцификации. Однако в том же исследовании авторы обнаружили, что хищники, которые охотились на некальцифицирующиеся генотипы, росли быстрее, чем те, которых кормили кальцинированными клетками. [97] В 2018 году Стром и др. сравнили уровень хищничества динофлагелляты Amphidinium longum на кальцинированной добыче по сравнению с голой добычей E. huxleyi и не обнаружили доказательств того, что коккосфера предотвращает проглатывание травоядным. [98] Вместо этого уровень потребления зависел от предложенного генотипа E. huxleyi. [98] В целом, эти два исследования показывают, что генотип оказывает сильное влияние на поедание видами микрозоопланктона, но не может быть полностью выяснено, защищает ли кальцификация кокколитофоры от хищничества микрозоопланктона и каким образом. [1]
Кокколитофоры оказывают как долгосрочное, так и краткосрочное воздействие на углеродный цикл . Для образования кокколитов необходимо поглощение растворенного неорганического углерода и кальция. Карбонат кальция и диоксид углерода получают из кальция и бикарбоната посредством следующей химической реакции: [99]
Поскольку кокколитофоры являются фотосинтезирующими организмами, они способны использовать часть CO2, выделяющегося в реакции кальцификации, для фотосинтеза . [100]
Однако производство карбоната кальция снижает щелочность поверхности, и в условиях низкой щелочности CO 2 вместо этого выбрасывается обратно в атмосферу. [101] В результате этого исследователи предположили, что массовое цветение кокколитофоров может способствовать глобальному потеплению в краткосрочной перспективе. [102] Однако более широко распространенная идея заключается в том, что в долгосрочной перспективе кокколитофоры способствуют общему снижению концентрации CO 2 в атмосфере . Во время кальцификации поглощаются два атома углерода, а один из них захватывается в виде карбоната кальция. Этот карбонат кальция опускается на дно океана в виде кокколитов и становится частью осадка; таким образом, кокколитофоры служат поглотителем выбрасываемого углерода, смягчая последствия выбросов парниковых газов. [102]
Исследования также показывают, что закисление океана из-за увеличения концентрации CO 2 в атмосфере может повлиять на механизм кальцификации кокколитофоров. Это может не только повлиять на непосредственные события, такие как увеличение популяции или производства кокколитов, но также может вызвать эволюционную адаптацию видов кокколитофоров в течение более длительных периодов времени. Например, кокколитофоры используют ионные каналы H + для постоянной выкачки ионов H + из клетки во время производства кокколита. Это позволяет им избежать ацидоза , поскольку в противном случае образование кокколита привело бы к токсичному избытку ионов H + . Когда функция этих ионных каналов нарушается, кокколитофороры останавливают процесс кальцификации, чтобы избежать ацидоза, образуя таким образом петлю обратной связи . [103] Низкая щелочность океана ухудшает функцию ионных каналов и, следовательно, оказывает эволюционное селективное давление на кокколитофоры и делает их (и другие кальцификаторы океана) уязвимыми для закисления океана. [104] В 2008 году полевые данные, указывающие на увеличение кальцификации вновь образовавшихся океанских отложений, содержащих кокколитофоры, подтвердили первые в истории экспериментальные данные, показывающие, что увеличение концентрации CO 2 в океане приводит к увеличению кальцификации этих организмов. Уменьшение массы кокколита связано как с увеличением концентрации CO 2 , так и с уменьшением концентрации CO.2-3в мировом океане. Предполагается, что такая более низкая кальцификация ставит кокколитофоры в невыгодное экологическое положение. Однако некоторые виды, такие как Calcidiscus leptoporus , не подвергаются такому воздействию, в то время как наиболее распространенный вид кокколитофоров, E. huxleyi , может пострадать (результаты исследования неоднозначны). [103] [105] Кроме того, вопреки прогнозам, в условиях низкого насыщения CaCO 3 были обнаружены сильно кальцинированные кокколитофориды . [4] Понимание воздействия растущего закисления океана на виды кокколитофоров абсолютно необходимо для прогнозирования будущего химического состава океана, особенно его карбонатного состава. Жизнеспособные меры по сохранению и управлению станут результатом будущих исследований в этой области. Такие группы, как европейская CALMARO [106], отслеживают реакцию популяций кокколитофоров на изменение pH и работают над определением экологически обоснованных мер контроля.
Окаменелости кокколита представляют собой известные и ценные известковые микроокаменелости . Они являются крупнейшим глобальным источником биогенного карбоната кальция и вносят значительный вклад в глобальный углеродный цикл . [107] Они являются основной составляющей меловых отложений, таких как белые скалы Дувра .
Особый интерес представляют окаменелости, датируемые палеоцен -эоценовым термальным максимумом 55 миллионов лет назад. Считается, что этот период наиболее точно соответствует нынешнему уровню CO 2 в океане. [108] Наконец, полевые данные о окаменелостях кокколитофоров в горных породах были использованы, чтобы показать, что глубоководная летопись окаменелостей несет в себе предвзятость в летописи горных пород , аналогичную той, которая широко распространена в отношении наземной летописи окаменелостей . [109]
Кокколитофориды помогают регулировать температуру океанов. Они процветают в теплых морях и выделяют в воздух диметилсульфид (ДМС), ядра которого помогают создавать более толстые облака, закрывающие солнце. [110] Когда океаны остывают, количество кокколитофорид уменьшается, а количество облаков также уменьшается. Когда меньше облаков, закрывающих солнце, температура также повышается. Таким образом, это поддерживает баланс и равновесие природы. [111] [112]
Источники подробной информации
Знакомство с кокколитофорами