В химии константа диссоциации кислоты (также известная как константа кислотности или константа ионизации кислоты ; обозначается ) является количественной мерой силы кислоты в растворе . Это константа равновесия химической реакции.
известный как диссоциация в контексте кислотно-основных реакций . Химическая разновидность HA представляет собой кислоту , которая диссоциирует на A− , сопряженное основание кислоты и ион водорода H + . [а] Говорят, что система находится в равновесии , если концентрации ее компонентов не меняются с течением времени, поскольку как прямая, так и обратная реакции протекают с одинаковой скоростью. [1]
Константа диссоциации определяется выражением [b]
где количества в квадратных скобках представляют собой концентрации веществ в равновесии. [c] [2] В качестве простого примера для слабой кислоты с K a = 10 −5 , log K a представляет собой показатель степени, равный -5, так что p K a = 5. А для уксусной кислоты с K a = 1,8 x 10 -5 , p K a близка к 5. Более высокая K a соответствует более сильной кислоте, которая более диссоциирует в равновесии. В более удобной логарифмической шкале более низкое значение pKa означает более сильную кислоту.
Константа диссоциации кислоты является прямым следствием основной термодинамики реакции диссоциации; значение p K a прямо пропорционально стандартному изменению свободной энергии Гиббса для реакции. Значение p K a меняется с температурой и качественно может быть понято на основе принципа Ле Шателье : когда реакция эндотермическая , K a увеличивается, а p K a уменьшается с увеличением температуры; обратное верно для экзотермических реакций.
Величина p K a также во многом зависит от молекулярной структуры кислоты. Например, Полинг предложил два правила: одно для последовательных p K a полипротонных кислот (см. Полипротонные кислоты ниже), и одно для оценки p K a оксикислот на основе количества групп = O и -OH (см. Факторы, влияющие на значения pKa ниже). Другие структурные факторы, влияющие на величину константы диссоциации кислоты, включают индуктивные эффекты , мезомерные эффекты и водородную связь . Уравнения типа Хэммета часто применялись для оценки p K a . [3] [4]
Количественное поведение кислот и оснований в растворах можно понять, только если известны значения их рКа . В частности, pH раствора можно предсказать, если известны аналитическая концентрация и значения p K a всех кислот и оснований ; и наоборот, если известен pH, можно рассчитать равновесную концентрацию кислот и оснований в растворе. Эти расчеты находят применение во многих различных областях химии, биологии, медицины и геологии. Например, многие соединения, используемые в лекарствах, представляют собой слабые кислоты или основания, и знание значений p K a вместе с коэффициентом распределения октанол-вода может быть использовано для оценки степени, в которой соединение попадает в кровоток. Константы диссоциации кислоты также важны в водной химии и химической океанографии , где кислотность воды играет фундаментальную роль. В живых организмах кислотно-основной гомеостаз и кинетика ферментов зависят от значений p K a многих кислот и оснований, присутствующих в клетке и организме. В химии знание значений рКа необходимо для приготовления буферных растворов , а также является предпосылкой для количественного понимания взаимодействия кислот или оснований с ионами металлов с образованием комплексов . Экспериментально значения p K a могут быть определены потенциометрическим (pH) титрованием , но для значений p K a менее примерно 2 или более примерно 11 могут потребоваться спектрофотометрические измерения или измерения ЯМР из-за практических трудностей с измерениями pH.
Согласно оригинальному молекулярному определению Аррениуса , кислота — это вещество, которое диссоциирует в водном растворе, выделяя ион водорода H + (протон): [5]
Константа равновесия этой реакции диссоциации известна как константа диссоциации . Освободившийся протон соединяется с молекулой воды с образованием иона гидроксония (или оксония) H 3 O + (голые протоны в растворе не существуют), поэтому позже Аррениус предложил записать диссоциацию как кислотно-основную реакцию :
Брёнстед и Лоури обобщили это на реакцию протонного обмена: [6] [7] [8]
Кислота теряет протон, оставляя сопряженное основание; протон переносится на основание, образуя сопряженную кислоту. Для водных растворов кислой ГК основанием является вода; сопряженное основание представляет собой A - , а сопряженная кислота представляет собой ион гидроксония. Определение Бренстеда-Лоури применимо и к другим растворителям, таким как диметилсульфоксид : растворитель S действует как основание, принимая протон и образуя сопряженную кислоту SH + .
В химии растворов принято использовать H + как сокращение для сольватированного иона водорода, независимо от растворителя. В водном растворе H + обозначает сольватированный ион гидроксония , а не протон. [9] [10]
Обозначение кислоты или основания как «конъюгата» зависит от контекста. Сопряженная кислота BH + основания B диссоциирует по закону
что является противоположностью равновесия
Гидроксид -ион OH - , хорошо известное основание, действует здесь как сопряженное основание кислой воды. Таким образом, кислоты и основания рассматриваются просто как доноры и акцепторы протонов соответственно.
Более широкое определение диссоциации кислоты включает гидролиз , при котором протоны образуются в результате расщепления молекул воды. Например, борная кислота ( B(OH) 3 ) производит H 3 O + как если бы она была донором протона, [11] но методом рамановской спектроскопии было подтверждено , что это происходит из-за гидролизного равновесия: [12]
Аналогичным образом, гидролиз ионов металлов приводит к тому, что ионы, такие как [Al(H 2 O) 6 ] 3+, ведут себя как слабые кислоты: [13]
Согласно первоначальному определению Льюиса , кислота — это вещество, которое принимает электронную пару с образованием координатной ковалентной связи . [14]
Константа диссоциации кислоты является частным примером константы равновесия . Диссоциацию монопротонной кислоты ГК в разбавленном растворе можно записать как
Константу термодинамического равновесия можно определить по формуле [15]
где {X} представляет собой активность химического соединения X в состоянии равновесия. Оно безразмерно , поскольку активность безразмерна. В числителе стоят активности продуктов диссоциации, в знаменателе – активности реагирующих веществ. См. коэффициент активности для получения этого выражения.

Поскольку активность является продуктом концентрации и коэффициента активности ( γ ), определение также можно записать как
где представляет собой концентрацию ГК и представляет собой частное коэффициентов активности.
Во избежание осложнений, связанных с использованием активностей, константы диссоциации определяют , где это возможно, в среде высокой ионной силы , т. е. в условиях, в которых можно считать всегда постоянными. [15] Например, среда может представлять собой раствор 0,1 молярного (М) нитрата натрия или 3 М перхлората калия . При этом предположении,
получается. Однако обратите внимание, что все опубликованные значения констант диссоциации относятся к конкретной ионной среде, используемой при их определении, и что разные значения получаются в разных условиях, как показано для уксусной кислоты на иллюстрации выше. Когда опубликованные константы относятся к ионной силе, отличной от той, которая требуется для конкретного применения, они могут быть скорректированы с помощью специфической теории ионов (SIT) и других теорий. [16]
Кумулятивная константа равновесия, обозначаемая как, связана с произведением ступенчатых констант, обозначаемых как Для двухосновной кислоты соотношение между ступенчатыми и общими константами следующее:
Обратите внимание, что в контексте образования комплексов металл-лиганд константы равновесия для образования металлокомплексов обычно определяются как константы ассоциации . В этом случае константы равновесия протонирования лиганда также определяются как константы ассоциации. Нумерация констант ассоциации обратна нумерации констант диссоциации; в этом примере
При обсуждении свойств кислот константы равновесия обычно определяют как константы диссоциации кислот, обозначаемые K a , с числовыми значениями, обозначаемыми символом p K a .
С другой стороны, для оснований используются константы ассоциации.
Однако компьютерные программы общего назначения , которые используются для получения значений констант равновесия на основе экспериментальных данных, используют константы ассоциации как для кислот, так и для оснований. Поскольку константы стабильности комплекса металл-лиганд всегда указываются как константы ассоциации, протонирование лиганда также необходимо указывать как реакцию ассоциации. [15] Определения показывают, что значение константы диссоциации кислоты обратно пропорционально значению соответствующей константы ассоциации.
Примечания
Все константы равновесия изменяются с температурой согласно уравнению Ван 'т-Гоффа [17]
– газовая постоянная , – абсолютная температура . Таким образом, для экзотермических реакций стандартное изменение энтальпии отрицательно, а K уменьшается с температурой. Для эндотермических реакций положительно, и K увеличивается с температурой.
Стандартное изменение энтальпии реакции само по себе является функцией температуры в соответствии с законом термохимии Кирхгофа :
где - изменение теплоемкости при постоянном давлении. На практике ее можно считать постоянной в небольшом диапазоне температур.
В уравнении
K a, по-видимому, имеет размерность концентрации. Однако, поскольку , константа равновесия , не может иметь физического измерения. Этот кажущийся парадокс можно разрешить разными способами.
Процедуры (1) и (2) дают одинаковые численные значения константы равновесия. Более того, поскольку концентрация просто пропорциональна мольной доле и плотности :
и поскольку молярная масса является константой в разбавленных растворах, значение константы равновесия, определенное с помощью (3), будет просто пропорционально значениям, полученным с помощью (1) и (2).
В биохимии принято указывать значение с размером, например, « K a = 30 мМ», чтобы указать масштаб, миллимолярный (мМ) или микромолярный (мкМ) значений концентрации, используемых для его расчета.
Кислота классифицируется как «сильная», если концентрация ее недиссоциированных частиц слишком мала для измерения. [6] Любая водная кислота со значением ap K меньше 0 почти полностью депротонирована и считается сильной кислотой . [19] Все такие кислоты переносят свои протоны в воду и образуют катионы растворителя (H 3 O + в водном растворе), так что все они имеют по существу одинаковую кислотность, явление, известное как выравнивание растворителя . [20] [21] Говорят, что они полностью диссоциированы в водном растворе, поскольку количество недиссоциировавшей кислоты, находящейся в равновесии с продуктами диссоциации, находится ниже предела обнаружения . Аналогичным образом, любое водное основание с константой ассоциации p K b менее примерно 0, что соответствует p K a более примерно 14, выравнивается до OH - и считается сильным основанием . [21]
Азотная кислота со значением ap K около -1,7 ведет себя как сильная кислота в водных растворах с pH выше 1. [22] При более низких значениях pH она ведет себя как слабая кислота.
Значения p K a для сильных кислот были оценены теоретическим путем. [23] Например, значение p K a водного раствора HCl оценивается как -9,3.
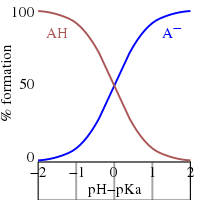
Переставив выражение, определяющее K a , и положив pH = −log 10 [H + ] , получим [24]
Это уравнение Хендерсона–Хассельбаха , из которого можно сделать следующие выводы.
В воде измеримые значения p K a варьируются от примерно -2 для сильной кислоты до примерно 12 для очень слабой кислоты (или сильного основания).
Буферный раствор с желаемым pH можно приготовить как смесь слабой кислоты и сопряженного с ней основания. На практике смесь можно создать, растворив кислоту в воде и добавив необходимое количество сильной кислоты или основания. Когда известны p K a и аналитическая концентрация кислоты, степень диссоциации и pH раствора монопротонной кислоты можно легко рассчитать с помощью таблицы ICE .

Полипротонная кислота — это соединение, которое может потерять более 1 протона. Каждая константа ступенчатой диссоциации определяется для потери одного протона. Константу диссоциации первого протона можно обозначить как K a1 , а константы диссоциации последующих протонов - как K a2 и т. д. Фосфорная кислота H 3 PO 4 является примером полипротонной кислоты, поскольку она может потерять три протона .
Когда разница между последовательными значениями p K составляет около четырех или более, как в этом примере, каждый вид можно рассматривать как кислоту сам по себе; [26] Фактически соли H
2ПО−
4можно кристаллизовать из раствора путем доведения pH примерно до 5,5 и солей HPO .2-4может быть кристаллизован из раствора путем доведения pH примерно до 10. Диаграмма распределения видов показывает, что концентрации двух ионов максимальны при pH 5,5 и 10.
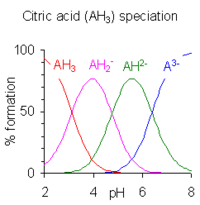
Когда разница между последовательными значениями p K меньше примерно четырех, происходит перекрытие диапазонов pH существования видов в равновесии. Чем меньше разница, тем больше совпадение. Случай лимонной кислоты показан справа; растворы лимонной кислоты забуферены во всем диапазоне pH от 2,5 до 7,5.
Согласно первому правилу Полинга, последовательные значения p K данной кислоты увеличиваются (p K a2 > p K a1 ) . [27] Для оксикислот с более чем одним ионизируемым водородом на одном и том же атоме значения p K a часто увеличиваются примерно на 5 единиц для каждого удаленного протона, [28] [29], как в приведенном выше примере с фосфорной кислотой.
Из таблицы выше видно, что второй протон удаляется из отрицательно заряженной частицы. Поскольку протон несет положительный заряд, для его удаления необходима дополнительная работа, поэтому p K a2 больше, чем p K a1 . p K a3 больше, чем p K a2 , поскольку происходит дальнейшее разделение зарядов. Когда обнаруживается исключение из правила Полинга, это указывает на то, что также происходят серьезные изменения в структуре. В случае с ВО+2(водный раствор), ванадий октаэдрический , 6-координатный, тогда как ванадиевая кислота тетраэдрический , 4-координатный. Это означает, что при первой диссоциации высвобождаются четыре «частицы», но при других диссоциациях высвобождаются только две «частицы», что приводит к гораздо большему вкладу энтропии в стандартное изменение свободной энергии Гиббса для первой реакции, чем для остальных.
Для веществ в растворе изоэлектрическая точка (p I ) определяется как pH, при котором взвешенная по величине заряда сумма концентраций положительно заряженных частиц равна взвешенной сумме концентраций отрицательно заряженных частиц. В случае, если имеется по одному виду каждого типа, изоэлектрическую точку можно получить непосредственно из значений p K. Возьмем, к примеру, глицин , определяемый как AH. Следует рассмотреть два равновесия диссоциации.
Подставим выражение для [AH] из второго уравнения в первое уравнение.
В изоэлектрической точке концентрация положительно заряженных частиц AH+2, равен концентрации отрицательно заряженных частиц A − , поэтому
Следовательно, если принять кологарифмы , pH определяется выражением
Значения p I для аминокислот указаны для протеиногенных аминокислот . Когда более двух заряженных видов находятся в равновесии друг с другом, может потребоваться полный расчет видообразования.
Константу равновесия K b для основания обычно определяют как константу ассоциации протонирования основания B с образованием сопряженной кислоты HB + .
Используя рассуждения, аналогичные использованным ранее
K b связан с K a для сопряженной кислоты. В воде концентрация гидроксид- иона [OH - ] связана с концентрацией ионов водорода соотношением K w = [H + ][OH - ] , поэтому
Подстановка выражения для [OH − ] в выражение для K b дает
Когда K a , K b и K w определяются при одинаковых условиях температуры и ионной силы, то, принимая кологарифмы , следует , что p K b = p K w − p K a . В водных растворах при 25 °C p K w составляет 13,9965, [30] , поэтому
с достаточной точностью для большинства практических целей. Фактически нет необходимости определять p K b отдельно от p K a , [31] но это делается здесь, поскольку часто в более старой литературе можно найти только значения p K b .
Для гидролизованного иона металла K b также можно определить как константу ступенчатой диссоциации .
Это обратная константа ассоциации для образования комплекса.
Поскольку соотношение p K b = p K w - p K a справедливо только в водных растворах (хотя аналогичные соотношения применимы и для других амфотерных растворителей), в таких разделах химии, как органическая химия , которые обычно имеют дело с неводными растворами, обычно не используется p K b в качестве мера основности. Вместо этого, p K a сопряженной кислоты, обозначаемой p K aH , указывается, когда необходимо количественно определить основность. Для основания B и сопряженной с ним кислоты BH + , находящихся в равновесии, это определяется как
Более высокое значение p K aH соответствует более сильному основанию. Например, значения p K aH (C 5 H 5 N) = 5,25 и p K aH ((CH 3 CH 2 ) 3 N) = 10,75 указывают на то, что (CH 3 CH 2 ) 3 N (триэтиламин) является более сильным основанием. чем C 5 H 5 N (пиридин).
Амфотерное вещество – это вещество, которое в зависимости от pH может действовать как кислота или как основание. Вода (внизу) амфотерна. Другим примером амфотерной молекулы является ион бикарбоната HCO.−3то есть сопряженное основание молекулы угольной кислоты H2CO3 в равновесии
но также кислота, сопряженная с карбонат- ионом CO2-3в (обратном) равновесии
Равновесие углекислоты важно для кислотно-основного гомеостаза в организме человека.
Аминокислота также является амфотерной , однако нейтральная молекула находится в состоянии внутреннего кислотно-щелочного равновесия, при котором основная аминогруппа притягивает и связывает протон кислой карбоксильной группы, образуя цвиттер- ион .
При pH менее примерно 5 протонируются как карбоксилатная группа, так и аминогруппа. По мере увеличения pH кислота диссоциирует по
При высоком pH может иметь место вторая диссоциация.
Таким образом, молекула аминокислоты является амфотерной, поскольку она может быть как протонирована, так и депротонирована.
Молекула воды может как приобрести, так и потерять протон. Говорят, что он амфипротный . Ионизационное равновесие можно записать
где в водном растворе Н + обозначает сольватированный протон. Часто это записывают как ион гидроксония H 3 O + , но эта формула не точна, поскольку на самом деле происходит сольватация более чем одной молекулой воды и такими частицами, как H 5 O.+2, Н 7 О+3, и H 9 O+4также присутствуют. [32]
Константа равновесия определяется выражением
В растворах, в которых концентрации растворенных веществ не очень высоки, концентрацию [H 2 O] можно считать постоянной, независимо от растворенного вещества(й); это выражение затем можно заменить на
Таким образом , константа самоионизации воды Kw является частным случаем константы диссоциации кислоты. Логарифмическая форма, аналогичная p K a, также может быть определена
Эти данные можно смоделировать параболой с
Из этого уравнения p K w = 14 при 24,87 °C. При этой температуре концентрация ионов водорода и гидроксида составляет 10 -7 М.
Растворитель с большей вероятностью будет способствовать ионизации растворенной молекулы кислоты в следующих обстоятельствах: [34]
Значения p K a органических соединений часто получают с использованием апротонных растворителей диметилсульфоксида (ДМСО) [34] и ацетонитрила (ACN). [35]
ДМСО широко используется в качестве альтернативы воде, поскольку он имеет более низкую диэлектрическую проницаемость, чем вода, менее полярен и поэтому легче растворяет неполярные гидрофобные вещества. Он имеет измеримый диапазон pK от 1 до 30. Ацетонитрил менее щелочной, чем ДМСО, поэтому в этом растворителе обычно кислоты слабее, а основания сильнее. Некоторые значения p K a при 25 °C для ацетонитрила (ACN) [36] [37] [38] и диметилсульфоксида (ДМСО). [39] показаны в следующих таблицах. Значения для воды включены для сравнения.
Ионизация кислот в кислом растворителе меньше, чем в воде. Например, хлористый водород является слабой кислотой при растворении в уксусной кислоте . Это связано с тем, что уксусная кислота является гораздо более слабым основанием, чем вода.
Сравните эту реакцию с тем, что происходит при растворении уксусной кислоты в более кислом растворителе, чистой серной кислоте: [40]

Маловероятная разновидность геминального диола CH 3 C(OH)+2стабилен в этих средах. Для водных растворов наиболее удобной функцией кислотности является шкала pH . [41] Другие функции кислотности были предложены для неводных сред, наиболее примечательной из которых является функция кислотности Гаммета , H 0 , для сверхкислотных сред и ее модифицированная версия H - для сверхосновных сред. [42]
В апротонных растворителях олигомеры , такие как хорошо известный димер уксусной кислоты , могут образовываться за счет водородных связей. Кислота также может образовывать водородные связи со своим сопряженным основанием. Этот процесс, известный как гомоконъюгация , приводит к повышению кислотности кислот, снижению их эффективных значений p K a за счет стабилизации основания конъюгата. Гомоконъюгация увеличивает протондонорную способность толуолсульфокислоты в растворе ацетонитрила почти в 800 раз. [43]
В водных растворах гомоконъюгация не происходит, поскольку вода образует более прочные водородные связи с сопряженным основанием, чем кислота.
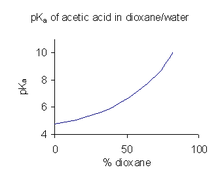
Когда соединение имеет ограниченную растворимость в воде, обычной практикой (например, в фармацевтической промышленности) является определение значений p K a в смеси растворителей, такой как вода/ диоксан или вода/ метанол , в которой соединение более растворимо. [45] В примере, показанном справа, значение p K a резко возрастает с увеличением процентного содержания диоксана, поскольку диэлектрическая проницаемость смеси уменьшается.
Значение A p K a , полученное в смешанном растворителе, нельзя использовать непосредственно для водных растворов. Причина этого в том, что когда растворитель находится в стандартном состоянии, его активность определяется как единица. Например, стандартное состояние смеси воды и диоксана с соотношением смешивания 9:1 представляет собой именно смесь растворителей без добавления растворенных веществ. Чтобы получить значение p K a для использования с водными растворами, его необходимо экстраполировать до нулевой концентрации сорастворителя из значений, полученных для различных смесей сорастворителей.
Эти факты затенены отсутствием растворителя в выражении, которое обычно используется для определения pKa , но значения pKa , полученные в данном смешанном растворителе, можно сравнивать друг с другом, получая относительную силу кислоты. То же самое справедливо и для значений p K a , полученных в конкретном неводном растворителе, таком как ДМСО.
Универсальная, независимая от растворителя шкала констант диссоциации кислот не разработана, поскольку не известно способа сравнения стандартных состояний двух разных растворителей.
Второе правило Полинга состоит в том, что значение первого p K a для кислот формулы XO m (OH) n зависит прежде всего от числа оксогрупп m и примерно не зависит от количества гидроксильных групп n , а также от количества центральный атом X. Приблизительные значения p K a составляют 8 для m = 0, 2 для m = 1, -3 для m = 2 и < -10 для m = 3. [27] В качестве альтернативы были предложены различные числовые формулы, включая p K a = 8 - 5 м (известное как правило Белла ), [28] [46] p K a = 7 - 5 м , [29] [47] или p K a = 9 - 7 м . [28] Зависимость от m коррелирует со степенью окисления центрального атома X: чем выше степень окисления, тем сильнее оксикислота.
Например, p K a для HClO равно 7,2, для HClO 2 равно 2,0, для HClO 3 равно -1 и HClO 4 является сильной кислотой ( p K a ≪ 0 ). [7] Повышенная кислотность при добавлении оксогруппы обусловлена стабилизацией сопряженного основания за счет делокализации его отрицательного заряда по дополнительному атому кислорода. [46] Это правило может помочь определить молекулярную структуру: например, фосфористая кислота , имеющая молекулярную формулу H 3 PO 3 , имеет ap K a около 2, что позволяет предположить, что структура представляет собой HPO(OH) 2 , что позднее было подтверждено методом ЯМР-спектроскопии. , а не P(OH) 3 , для которого можно было бы ожидать, что ap K a будет около 8. [47]

Индуктивные эффекты и мезомерные эффекты влияют на значения p K a . Простой пример — эффект замены атомов водорода в уксусной кислоте более электроотрицательным атомом хлора. Электроноакцепторный эффект заместителя облегчает ионизацию, поэтому последовательные значения p K a уменьшаются в ряду 4,7, 2,8, 1,4 и 0,7 при наличии 0, 1, 2 или 3 атомов хлора. [48] Уравнение Гаммета дает общее выражение влияния заместителей. [49]
K a – константа диссоциации замещенного соединения, K0
а— константа диссоциации, когда заместителем является водород, ρ — свойство незамещенного соединения, а σ имеет особое значение для каждого заместителя. График зависимости log( K a ) от σ представляет собой прямую линию с пересечением log( K0
а) и наклон ρ. Это пример линейной зависимости свободной энергии , поскольку log( Ka ) пропорционален стандартному изменению свободной энергии. Первоначально Хэммет [50] сформулировал связь с данными по бензойной кислоте с различными заместителями в орто- и пара - положениях : некоторые числовые значения находятся в уравнении Гаммета . Это и другие исследования позволили упорядочить заместители в зависимости от их электроноакцепторной или электроноотдающей способности, а также различить индуктивные и мезомерные эффекты. [51] [52]
Спирты обычно не ведут себя в воде как кислоты, но наличие двойной связи, примыкающей к ОН-группе, может существенно уменьшить p K a по механизму кето-енольной таутомерии . Аскорбиновая кислота является примером такого эффекта. Дикетон 2,4-пентандион ( ацетилацетон ) также является слабой кислотой из-за кето-енольного равновесия. В ароматических соединениях, например феноле , имеющих ОН-заместитель, сопряжение с ароматическим кольцом в целом значительно повышает стабильность депротонированной формы.
Структурные эффекты также могут иметь важное значение. Разница между фумаровой кислотой и малеиновой кислотой является классическим примером. Фумаровая кислота представляет собой (E)-1,4-бут-2-эндиовую кислоту, транс- изомер , тогда как малеиновая кислота является соответствующим цис- изомером, т.е. (Z)-1,4-бут-2-эндиовой кислотой (см. цис-изомер ). транс-изомерия ). Фумаровая кислота имеет значения p K a примерно 3,0 и 4,5. Напротив, малеиновая кислота имеет значения p K a приблизительно 1,5 и 6,5. Причина такой большой разницы заключается в том, что при удалении одного протона от цис- изомера (малеиновой кислоты) образуется прочная внутримолекулярная водородная связь с оставшейся поблизости карбоксильной группой. Это способствует образованию малеата H + и препятствует удалению второго протона из этого вида. В транс- изомере две карбоксильные группы всегда расположены далеко друг от друга, поэтому водородная связь не наблюдается. [53]
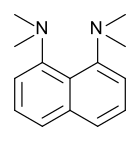
Протонная губка , 1,8-бис(диметиламино)нафталин, имеет значение ap K 12,1 . Это одно из самых сильных известных аминных оснований. Высокая основность объясняется снятием напряжения при протонировании и сильной внутренней водородной связью. [54] [55]
В этом разделе также следует упомянуть влияние растворителя и сольватации. Оказывается, эти влияния более тонкие, чем у упомянутой выше диэлектрической среды. Например, ожидаемый (по электронным эффектам метильных заместителей) и наблюдаемый в газовой фазе порядок основности метиламинов Me 3 N > Me 2 NH > MeNH 2 > NH 3 под действием воды меняется на Me 2 NH > MeNH 2 > Me 3 N > NH 3 . Молекулы нейтрального метиламина связаны водородной связью с молекулами воды преимущественно за счет одного акцепторного взаимодействия N–HOH и лишь изредка еще одной донорной связи NH–OH 2 . Следовательно, метиламины стабилизируются гидратацией примерно в одинаковой степени независимо от числа метильных групп. Напротив, соответствующие катионы метиламмония всегда используют все доступные протоны для донорной связи NH–OH 2 . Таким образом, относительная стабилизация ионов метиламмония уменьшается с увеличением числа метильных групп, что объясняет порядок основности воды в метиламинах. [4]
Константа равновесия связана со стандартным изменением энергии Гиббса для реакции, поэтому для константы диссоциации кислоты
R — газовая постоянная , а T — абсолютная температура . Обратите внимание, что p K a = −log( K a ) и 2,303 ≈ ln (10) . При 25 °C Δ G ⊖ в кДж·моль -1 ≈ 5,708 п K a (1 кДж·моль -1 = 1000 джоулей на моль ). Свободная энергия состоит из энтальпийного и энтропийного членов. [11]
Стандартное изменение энтальпии можно определить калориметрически или с помощью уравнения Ван-т-Гоффа , хотя калориметрический метод предпочтительнее. Когда определены как стандартное изменение энтальпии, так и константа диссоциации кислоты, стандартное изменение энтропии легко рассчитать по приведенному выше уравнению. В следующей таблице энтропийные члены рассчитаны на основе экспериментальных значений p K a и Δ H ⊖ . Данные были тщательно отобраны и относятся к температуре 25 °C и нулевой ионной силе в воде. [11]
Первое, что следует отметить, это то, что когда p K a положительно, стандартное изменение свободной энергии реакции диссоциации также является положительным. Во-вторых, некоторые реакции являются экзотермическими , а некоторые — эндотермическими , но когда Δ H ⊖ отрицательно , T ΔS ⊖ является доминирующим фактором, который определяет, что Δ G ⊖ является положительным. Наконец, вклад энтропии в этих реакциях всегда неблагоприятный ( Δ S ⊖ < 0 ). Ионы в водном растворе стремятся ориентировать окружающие молекулы воды, что упорядочивает раствор и уменьшает энтропию. Вклад иона в энтропию представляет собой частичную молярную энтропию, которая часто бывает отрицательной, особенно для небольших или сильно заряженных ионов. [56] Ионизация нейтральной кислоты включает образование двух ионов, так что энтропия уменьшается ( Δ S ⊖ < 0 ). При второй ионизации той же кислоты ионов теперь уже три, и анион имеет заряд, поэтому энтропия снова уменьшается.
Обратите внимание, что стандартное изменение свободной энергии реакции относится к изменениям реагентов в их стандартных состояниях к продуктам в их стандартных состояниях. Изменение свободной энергии в состоянии равновесия равно нулю, поскольку химические потенциалы реагентов и продуктов в состоянии равновесия равны.

Экспериментальное определение значений pKa обычно проводят методом титрования в среде с высокой ионной силой и при постоянной температуре. [57] Типичная процедура выглядит следующим образом. Раствор соединения в среде подкисляют сильной кислотой до полного протонирования соединения. Затем раствор титруют сильным основанием до удаления всех протонов. В каждой точке титрования pH измеряют с помощью стеклянного электрода и pH-метра . Константы равновесия находятся путем подгонки рассчитанных значений pH к наблюдаемым значениям с использованием метода наименьших квадратов . [58]
Общий объем добавляемого сильного основания должен быть небольшим по сравнению с исходным объемом раствора титранда, чтобы ионная сила оставалась практически постоянной. Это гарантирует, что p K a останется неизменным во время титрования.
Расчетная кривая титрования щавелевой кислоты показана справа. Щавелевая кислота имеет значения p K a 1,27 и 4,27. Следовательно, буферные области будут сосредоточены примерно при pH 1,3 и pH 4,3. Буферные области несут информацию, необходимую для получения значений p K a , поскольку концентрации кислоты и сопряженного основания изменяются вдоль буферной области.
Между двумя буферными областями есть конечная точка, или точка эквивалентности , примерно при pH 3. Эта конечная точка не является резкой и типична для дипротонной кислоты, буферные области которой перекрываются на небольшую величину: p K a2 − p K. В этом примере a1 составляет около трех. (Если бы разница в значениях p K составляла около двух или меньше, конечная точка не была бы заметна.) Вторая конечная точка начинается примерно при pH 6,3 и является резкой. Это указывает на то, что все протоны были удалены. В этом случае раствор не является буферным, и pH резко возрастает при добавлении небольшого количества сильного основания. Однако уровень pH не может продолжать расти бесконечно. Новая буферная область начинается примерно при pH 11 (p K w - 3), где самоионизация воды становится важной.
Очень трудно измерить значения pH менее двух в водном растворе с помощью стеклянного электрода , поскольку уравнение Нернста не выполняется при таких низких значениях pH. Для определения значений p K менее примерно 2 или более примерно 11 спектрофотометрических [59] [60] или ЯМР [61] [62] измерений можно использовать вместо измерений pH или в сочетании с ними.
Когда стеклянный электрод невозможно использовать, как в случае с неводными растворами, часто применяют спектрофотометрические методы. [37] Они могут включать измерения оптической плотности или флуоресценции . В обоих случаях предполагается, что измеряемая величина пропорциональна сумме вкладов каждого фотоактивного вида; Предполагается , что при измерении поглощения применяется закон Бера-Ламберта .
Изотермическую титровальную калориметрию (ITC) можно использовать для определения как значения ap K , так и соответствующей стандартной энтальпии диссоциации кислоты. [63] Программное обеспечение для выполнения расчетов поставляется производителями приборов для простых систем.
Водные растворы с обычной водой нельзя использовать для измерений 1 H ЯМР, вместо них необходимо использовать тяжелую воду D 2 O. Однако данные 13 C ЯМР можно использовать с обычной водой, а спектры 1 H ЯМР можно использовать с неводными средами. Величины, измеренные с помощью ЯМР, представляют собой усредненные по времени химические сдвиги , поскольку протонный обмен происходит быстро в шкале времени ЯМР. Можно измерить и другие химические сдвиги, например, сдвиги 31 P.

Для некоторых полипротонных кислот диссоциация (или ассоциация) происходит более чем в одном неэквивалентном сайте [4] , а наблюдаемая макроскопическая константа равновесия или макроконстанта представляет собой комбинацию микроконстант , включающих различные виды. Когда один реагент образует два продукта параллельно, макроконстанта представляет собой сумму двух микроконстант. Это справедливо, например, для депротонирования аминокислоты цистеина , которая существует в растворе в виде нейтрального цвиттер-иона HS-CH 2 -CH(NH +3)-COO - . Две микроконстанты представляют собой депротонирование либо по сере, либо по азоту, а сумма макроконстант здесь представляет собой константу диссоциации кислоты [64]

Точно так же такое основание, как спермин, имеет более одного места, где может происходить протонирование. Например, монопротонирование может происходить по концевой группе -NH 2 или по внутренним группам -NH- . Значения K b для диссоциации спермина, протонированного в том или ином из сайтов, являются примерами микроконстант . Их нельзя определить напрямую с помощью измерений pH, поглощения, флуоресценции или ЯМР; Измеренное значение K b представляет собой сумму значений K для микрореакций.
Тем не менее, место протонирования очень важно для биологической функции, поэтому были разработаны математические методы определения микроконстант. [65]
Когда два реагента параллельно образуют один продукт, макроконстанта [64] Например, вышеупомянутое равновесие для спермина можно рассматривать с точки зрения значений K a двух таутомерных сопряженных кислот с макроконстантой. В этом случае это эквивалентно предыдущему выражению поскольку пропорционально
Когда реагент подвергается двум последовательным реакциям, макроконстанта объединенной реакции представляет собой произведение микроконстанты двух стадий. Например, упомянутый выше цвиттер-ион цистеина может потерять два протона: один от серы и один от азота, а общая макроконстанта потери двух протонов является произведением двух констант диссоциации [64] . Это также можно записать через логарифмические константы как
Знание значений p K a важно для количественной оценки систем, имеющих кислотно-основное равновесие в растворе. В биохимии существует множество приложений ; например, значения pKa белков и боковых цепей аминокислот имеют большое значение для активности ферментов и стабильности белков. [66] Значения белка p K a не всегда могут быть измерены напрямую, но могут быть рассчитаны с использованием теоретических методов. Буферные растворы широко используются для получения растворов с физиологическим pH или близким к нему для изучения биохимических реакций; [67] разработка этих решений зависит от знания значений p K a их компонентов. Важные буферные растворы включают MOPS , который обеспечивает раствор с pH 7,2, и трицин , который используется в гель-электрофорезе . [68] [69] Буферизация является важной частью кислотно-щелочной физиологии , включая кислотно-основной гомеостаз , [70] и является ключом к пониманию таких расстройств, как кислотно-основное расстройство . [71] [72] [73] Изоэлектрическая точка данной молекулы является функцией ее значений p K , поэтому разные молекулы имеют разные изоэлектрические точки. Это позволяет использовать метод, называемый изоэлектрическим фокусированием [74] , который используется для разделения белков с помощью 2-D электрофореза в полиакриламидном геле .
Буферные растворы также играют ключевую роль в аналитической химии . Их используют всякий раз, когда возникает необходимость зафиксировать pH раствора на определенном значении. По сравнению с водным раствором pH буферного раствора относительно нечувствителен к добавлению небольшого количества сильной кислоты или сильного основания. Буферная емкость [ 75] простого буферного раствора максимальна при pH = pKa . При кислотно-основной экстракции эффективность экстракции соединения в органическую фазу, например эфир , можно оптимизировать путем регулирования pH водной фазы с использованием соответствующего буфера. При оптимальном pH концентрация электрически нейтральных веществ максимальна; такой вид более растворим в органических растворителях с низкой диэлектрической постоянной , чем в воде. Этот метод используется для очистки слабых кислот и оснований. [76]
Индикатор pH представляет собой слабую кислоту или слабое основание, меняющую цвет в переходном диапазоне pH, который составляет примерно p K a ± 1. Для создания универсального индикатора требуется смесь индикаторов, соседние значения p K a которых отличаются примерно на два, так что их переходные диапазоны pH просто перекрываются.
В фармакологии ионизация соединения изменяет его физическое поведение и макросвойства, такие как растворимость и липофильность , log p ). Например, ионизация любого соединения увеличит растворимость в воде, но уменьшит липофильность. Это используется при разработке лекарств для увеличения концентрации соединения в крови путем регулирования pKa ионизируемой группы . [77]
Знание значений p K a важно для понимания координационных комплексов , которые образуются при взаимодействии иона металла M m+ , действующего как кислота Льюиса , с лигандом L, действующим как основание Льюиса . Однако лиганд может вступать и в реакции протонирования, поэтому образование комплекса в водном растворе можно символически представить реакцией
Чтобы определить константу равновесия для этой реакции, в которой лиганд теряет протон, необходимо знать p K a протонированного лиганда. На практике лиганд может быть полипротическим; например, ЭДТА 4- может принять четыре протона; в этом случае должны быть известны все значения p K a . Кроме того, ион металла подвержен гидролизу , то есть ведет себя как слабая кислота, поэтому необходимо также знать значения p K для реакций гидролиза. [78]
Оценка опасности , связанной с кислотой или основанием, может потребовать знания значений pKa . [79] Например, цианистый водород является очень токсичным газом, поскольку ион цианида ингибирует железосодержащий фермент цитохром с-оксидазу . Цианистый водород представляет собой слабую кислоту в водном растворе с ap K a около 9. В сильнощелочных растворах, скажем, с pH выше 11, из этого следует, что цианид натрия «полностью диссоциирован», поэтому опасность, связанная с газообразным цианистым водородом, значительно снижается. . С другой стороны, кислый раствор очень опасен, поскольку весь цианид находится в кислотной форме. Проглатывание цианида через рот потенциально смертельно, независимо от pH, из-за реакции с цитохром-с-оксидазой.
В науке об окружающей среде кислотно-щелочное равновесие важно для озер [80] и рек; [81] [82] Например, гуминовые кислоты являются важными компонентами природных вод. Другой пример встречается в химической океанографии : [83] для количественной оценки растворимости железа(III) в морской воде при различной солености используются значения p K a для образования продуктов гидролиза железа(III) Fe(OH) 2+ , Fe(ОН)+2и Fe(OH) 3 определяли вместе с продуктом растворимости гидроксида железа . [84]
Существует несколько методов определения p K a химического вещества, что приводит к некоторым расхождениям между различными источниками. Хорошо измеренные значения обычно находятся в пределах 0,1 единицы друг от друга. Представленные здесь данные были получены при температуре 25 °C в воде. [7] [85] Дополнительные значения можно найти в разделе «Термодинамика» выше. Таблицу р Ка углеродных кислот, измеренную в ДМСО, можно найти на странице карбанионов .
Вам интересно... Как использование активностей делает константу равновесия безразмерной?