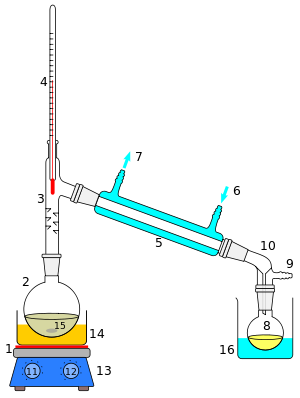
Дистилляция , также классическая дистилляция , представляет собой процесс разделения компонентов жидкой смеси двух или более химически дискретных веществ; процесс разделения осуществляется путём избирательного кипения смеси и конденсации паров в перегонном кубе .
Сухая перегонка ( термолиз и пиролиз ) — это нагревание твердых материалов для получения газов, которые конденсируются либо в жидкие продукты, либо в твердые продукты. Термин «сухая перегонка» включает в себя процессы разделения деструктивной перегонки и химического крекинга , разбивающие большие молекулы углеводородов на более мелкие молекулы углеводородов. Более того, частичная перегонка приводит к частичному разделению компонентов смеси, что дает почти чистые компоненты; частичная перегонка также реализует частичное разделение смеси для увеличения концентрации выбранных компонентов. В любом из методов процесс разделения перегонки использует различия в относительной летучести компонентов веществ нагретой смеси.
В промышленных применениях классической дистилляции термин « дистилляция» используется как единица операции , которая определяет и обозначает процесс физического разделения, а не химическую реакцию ; таким образом, промышленная установка, которая производит дистиллированные напитки , является дистилляцией спирта . Вот некоторые применения процесса химического разделения, который называется дистилляцией:
Ранние свидетельства дистилляции были найдены на аккадских табличках, датированных ок. 1200 г. до н. э., описывающих парфюмерные операции. Таблички предоставили текстовые доказательства того, что ранняя, примитивная форма дистилляции была известна вавилонянам древней Месопотамии . [ 5]
По словам британского химика Т. Фэрли, ни у греков, ни у римлян не было термина для современной концепции дистилляции. Такие слова, как «дистилляция», могли бы относиться к чему-то другому, в большинстве случаев к части какого-то процесса, не связанного с тем, что сейчас известно как дистилляция. По словам Фэрли и немецкого инженера-химика Норберта Кокмана соответственно:
Латинское «distillo», от de-stillo, от stilla, капля, относилось к каплепадению жидкости человеческими или искусственными средствами и применялось к любому процессу, в котором жидкость разделялась на капли. Перегонять в современном смысле можно было только окольным путем. [6]
В древности и средневековье дистилляция имела более широкое значение, поскольку под термином « дистилляция» понимались почти все операции по очистке и разделению , такие как фильтрация, кристаллизация, экстракция, сублимация или механическое прессование масла. [7]
По словам голландского историка химии Роберта Дж. Форбса , слово distillare (капать), когда его использовали римляне, например, Сенека и Плиний Старший , «никогда не использовалось в нашем смысле». [8]
Аристотель знал, что вода, конденсирующаяся при испарении морской воды, является пресной: [9]
Я доказал экспериментально, что соленая вода, испаряясь, образует пресную, и пар, конденсируясь, не конденсируется снова в морскую воду.
Испарение морской воды и ее конденсация в пресную воду не может называться «дистилляцией», поскольку дистилляция подразумевает кипение, но эксперимент мог стать важным шагом на пути к дистилляции. [10]

Ранние свидетельства дистилляции были обнаружены в связи с работой алхимиков в Александрии в Римском Египте в I веке н. э. [14] : 57, 89
Дистиллированная вода используется по крайней мере с 200 г. н. э. , когда Александр Афродисийский описал этот процесс. [15] [16] Работа по дистилляции других жидкостей продолжалась в раннем византийском Египте под руководством Зосимы из Панополиса в III веке.
Дистилляция практиковалась на древнем индийском субконтиненте , что очевидно из реторт и приемников из обожженной глины, найденных в Таксиле , Шайхан Дхери и Чарсадде в Пакистане и Ранг Махале в Индии , датируемых первыми веками нашей эры . [17] [18] [19] Фрэнк Рэймонд Оллчин говорит, что эти терракотовые дистилляционные трубки были «сделаны для имитации бамбука». [20] Эти « перегонные кубы Гандхары » были способны производить только очень слабый напиток , поскольку не было эффективных средств сбора паров при низком нагреве. [21]
Дистилляция в Китае, возможно, началась самое раннее во времена династии Восточная Хань (I–II вв. н. э.) [22] .
Средневековые мусульманские химики , такие как Джабир ибн Хайян (лат. Geber, девятый век) и Абу Бакр ар-Рази (лат. Rhazes, ок. 865–925 ), много экспериментировали с перегонкой различных веществ. Фракционная перегонка органических веществ играет важную роль в работах, приписываемых Джабиру, таких как Kitāb al-Sabʿīn («Книга семидесяти»), переведенная на латынь Герардом Кремонским ( ок. 1114–1187 ) под названием Liber de septuaginta . [23] Джабирские эксперименты с фракционной перегонкой животных и растительных веществ, а также в меньшей степени минеральных веществ, являются главной темой De anima in arte alkimiae , изначально арабского труда, ошибочно приписываемого Авицене , который был переведен на латынь и впоследствии стал важнейшим алхимическим источником для Роджера Бэкона ( ок. 1220–1292 ). [24]
Перегонка вина засвидетельствована в арабских трудах, приписываемых аль-Кинди ( ок. 801–873 гг. н. э. ) и аль-Фараби ( ок. 872–950 гг .), а также в 28-й книге Kitāb al-Taṣrīf аз-Захрави (лат. Abulcasis, 936–1013 гг.) (позднее переведенной на латынь как Liber servatoris ). [25] В двенадцатом веке рецепты производства aqua ardens («горящей воды», т. е. этанола) путем перегонки вина с солью начали появляться в ряде латинских трудов, и к концу тринадцатого века он стал широко известным веществом среди западноевропейских химиков. [26] В работах Таддео Альдеротти (1223–1296) описывается метод концентрирования спирта, включающий повторную перегонку через охлаждаемый водой перегонный куб, с помощью которого можно было получить чистоту спирта 90%. [27]
Согласно археологическим данным, дистилляция напитков началась в эпоху династий Южная Сун (10–13 века) и Цзинь (12–13 века). [22] На археологических раскопках в Цинлуне, провинция Хэбэй , Китай, был найден перегонный аппарат, датируемый 12 веком. Дистиллированные напитки были распространены во времена династии Юань (13–14 века). [22]
В 1500 году немецкий алхимик Иероним Бруншвиг опубликовал Liber de arte distillandi de simplicibus ( Книгу об искусстве перегонки из простых ингредиентов ) [28] , первую книгу, посвященную исключительно теме перегонки, за которой в 1512 году последовала значительно расширенная версия. Сразу после этого, в 1518 году, была основана старейшая в Европе винокурня The Green Tree Distillery . [29]
В 1651 году Джон Френч опубликовал «Искусство дистилляции » [30], первый крупный английский сборник по этой практике, но утверждалось [31] , что большая его часть происходит из работы Брауншвейга. Это включает диаграммы с людьми на них, показывающие промышленный, а не лабораторный масштаб операции.


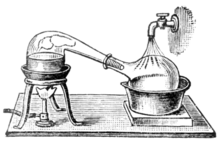


По мере того, как алхимия развивалась в науку химии , сосуды, называемые ретортами, стали использоваться для дистилляции. И алембики , и реторты представляют собой формы стеклянной посуды с длинными горлышками, направленными в сторону под углом вниз, чтобы действовать как конденсаторы с воздушным охлаждением для конденсации дистиллята и его стекания вниз для сбора. Позже были изобретены медные алембики. Заклепочные соединения часто сохраняли герметичность с помощью различных смесей, например, теста из ржаной муки. [32] Эти алембики часто имели систему охлаждения вокруг клюва, например, с использованием холодной воды, что делало конденсацию алкоголя более эффективной. Их называли перегонными кубами . Сегодня реторты и перегонные кубы в значительной степени вытеснены более эффективными методами дистилляции в большинстве промышленных процессов. Тем не менее, перегонный куб по-прежнему широко используется для производства некоторых изысканных спиртов, таких как коньяк , шотландский виски , ирландский виски , текила , ром , кашаса и некоторые водки . Перегонные кубы из различных материалов (дерево, глина, нержавеющая сталь) также используются бутлегерами в разных странах. Небольшие перегонные кубы также продаются для использования в домашнем производстве [33] цветочной воды или эфирных масел .
Ранние формы дистилляции включали пакетные процессы с использованием одного испарения и одной конденсации. Чистота была улучшена путем дальнейшей дистилляции конденсата. Большие объемы обрабатывались путем простого повторения дистилляции. Сообщается, что химики проводили от 500 до 600 дистилляций, чтобы получить чистое соединение. [34]
В начале 19 века были разработаны основы современных технологий, включая предварительный нагрев и орошение . [34] В 1822 году Энтони Перье разработал один из первых непрерывных дистилляторов, а затем, в 1826 году, Роберт Штайн усовершенствовал эту конструкцию, чтобы создать свой патентный дистиллятор . В 1830 году Эней Коффи получил патент на дальнейшее улучшение конструкции. [35] Непрерывный дистиллятор Коффи можно считать архетипом современных нефтехимических установок. Французский инженер Арман Саваль разработал свой паровой регулятор около 1846 года. [14] : 323 В 1877 году Эрнест Сольвей получил патент США на тарельчатую колонну для перегонки аммиака , [36] и в те же и последующие годы наблюдались разработки в этой области для масел и спиртов.
С появлением химической инженерии как дисциплины в конце 19-го века можно было применять научные, а не эмпирические методы. Развивающаяся нефтяная промышленность в начале 20-го века дала толчок к разработке точных методов проектирования, таких как метод МакКейба-Тиле Эрнеста Тиле и уравнение Фенске . Первый промышленный завод в Соединенных Штатах, использующий дистилляцию в качестве средства опреснения океана, открылся в Фрипорте, штат Техас, в 1961 году с надеждой на обеспечение водной безопасности в регионе. [37] Наличие мощных компьютеров позволило проводить прямое компьютерное моделирование дистилляционных колонн.
Применение дистилляции можно условно разделить на четыре группы: лабораторная, промышленная, дистилляция трав для парфюмерии и лекарственных средств ( травяной дистиллят ) и переработка пищевых продуктов. Последние два существенно отличаются от первых двух тем, что дистилляция не используется как истинный метод очистки, а скорее для переноса всех летучих веществ из исходных материалов в дистиллят при обработке напитков и трав.
Основное различие между лабораторной и промышленной дистилляцией заключается в том, что лабораторная дистилляция часто выполняется партиями, тогда как промышленная дистилляция часто происходит непрерывно. При периодической дистилляции состав исходного материала, паров дистиллируемых соединений и дистиллята изменяются во время дистилляции. При периодической дистилляции в перегонный куб загружается (подается) партия исходной смеси, которая затем разделяется на составляющие ее фракции, которые последовательно собираются от наиболее летучих к менее летучим, с остатками — оставшейся наименее или нелетучей фракцией — удаляются в конце. Затем перегонный куб можно перезагрузить, и процесс повторить.
При непрерывной дистилляции исходные материалы, пары и дистиллят поддерживаются в постоянном составе путем тщательного пополнения исходного материала и удаления фракций как из пара, так и из жидкости в системе. Это приводит к более детальному контролю процесса разделения.
Температура кипения жидкости — это температура, при которой давление паров жидкости равно давлению вокруг жидкости, что позволяет пузырькам образовываться, не разрушаясь. Особым случаем является нормальная температура кипения , при которой давление паров жидкости равно давлению окружающей атмосферы .
Ошибочно полагать, что в жидкой смеси при заданном давлении каждый компонент кипит при температуре кипения, соответствующей заданному давлению, что позволяет парам каждого компонента собираться отдельно и в чистом виде. Однако этого не происходит даже в идеализированной системе. Идеализированные модели дистилляции по сути подчиняются закону Рауля и закону Дальтона и предполагают, что достигается равновесие пар-жидкость .
Закон Рауля гласит, что давление пара раствора зависит от 1) давления пара каждого химического компонента в растворе и 2) доли раствора, которую составляет каждый компонент, также известной как мольная доля . Этот закон применим к идеальным растворам или растворам, которые имеют разные компоненты, но чьи молекулярные взаимодействия такие же или очень похожи на чистые растворы.
Закон Дальтона гласит, что общее давление является суммой парциальных давлений каждого отдельного компонента в смеси. При нагревании многокомпонентной жидкости давление пара каждого компонента будет расти, тем самым вызывая рост общего давления пара. Когда общее давление пара достигает давления, окружающего жидкость, происходит кипение , и жидкость превращается в газ по всему объему жидкости. Смесь с заданным составом имеет одну точку кипения при заданном давлении, когда компоненты взаимно растворимы. Смесь постоянного состава не имеет нескольких точек кипения.
Следствием одной точки кипения является то, что более легкие компоненты никогда не «кипят первыми». В точке кипения все летучие компоненты кипят, но для компонента его процент в паре такой же, как его процент от общего давления пара. Более легкие компоненты имеют более высокое парциальное давление и, таким образом, концентрируются в паре, но более тяжелые летучие компоненты также имеют (меньшее) парциальное давление и обязательно также испаряются, хотя и при более низкой концентрации в паре. Действительно, периодическая перегонка и фракционирование достигаются путем изменения состава смеси. При периодической перегонке партия испаряется, что меняет ее состав; при фракционировании жидкость выше в ректификационной колонне содержит больше легких компонентов и кипит при более низких температурах. Поэтому, начиная с данной смеси, она, по-видимому, имеет интервал кипения вместо точки кипения, хотя это происходит из-за изменения ее состава: каждая промежуточная смесь имеет свою собственную, единственную точку кипения.
Идеализированная модель точна в случае химически подобных жидкостей, таких как бензол и толуол . В других случаях наблюдаются серьезные отклонения от закона Рауля и закона Дальтона, наиболее известные из которых наблюдаются в смеси этанола и воды. Эти соединения при совместном нагревании образуют азеотроп , когда паровая фаза и жидкая фаза содержат одинаковый состав. Хотя существуют вычислительные методы , которые можно использовать для оценки поведения смеси произвольных компонентов, единственный способ получить точные данные о равновесии пар-жидкость — это измерение.
Невозможно полностью очистить смесь компонентов путем перегонки, так как для этого потребуется, чтобы каждый компонент в смеси имел нулевое парциальное давление . Если целью являются сверхчистые продукты, то необходимо применять дальнейшее химическое разделение . Когда бинарная смесь испаряется, а другой компонент, например соль, имеет нулевое парциальное давление для практических целей, процесс упрощается.
Нагревание идеальной смеси двух летучих веществ, A и B, где A имеет более высокую летучесть или более низкую температуру кипения, в установке для периодической перегонки (например, в аппарате, изображенном на начальном рисунке) до тех пор, пока смесь не закипит, приводит к образованию пара над жидкостью, содержащего смесь A и B. Соотношение между A и B в паре будет отличаться от соотношения в жидкости. Соотношение в жидкости будет определяться тем, как была приготовлена исходная смесь, в то время как соотношение в паре будет обогащено более летучим соединением A (из-за закона Рауля, см. выше). Пар проходит через конденсатор и удаляется из системы. Это, в свою очередь, означает, что соотношение соединений в оставшейся жидкости теперь отличается от начального соотношения (т. е. более обогащено B, чем в исходной жидкости).
В результате соотношение в жидкой смеси меняется, становясь богаче компонентом B. Это приводит к повышению температуры кипения смеси, что приводит к повышению температуры в паре, что приводит к изменению соотношения A : B в газовой фазе (по мере продолжения дистилляции увеличивается доля B в газовой фазе). Это приводит к медленному изменению соотношения A : B в дистилляте.
Если разница в давлении паров между двумя компонентами А и В велика (обычно выражаемая разницей в температурах кипения), то в начале перегонки смесь сильно обогащена компонентом А, а после отгонки компонента А кипящая жидкость обогащается компонентом В.
Непрерывная дистилляция — это непрерывная дистилляция, при которой жидкая смесь непрерывно (без перерыва) подается в процесс, а разделенные фракции непрерывно удаляются по мере того, как выходные потоки возникают с течением времени в ходе операции. Непрерывная дистилляция производит минимум две выходные фракции, включая по крайней мере одну летучую фракцию дистиллята, которая выкипела и была отдельно захвачена в виде пара, а затем сконденсирована в жидкость. Всегда есть фракция кубового остатка (или остатка), которая является наименее летучим остатком, который не был отдельно захвачен в виде конденсированного пара.
Непрерывная перегонка отличается от периодической тем, что концентрации не должны меняться с течением времени. Непрерывная перегонка может проводиться в устойчивом состоянии в течение произвольного периода времени. Для любого исходного материала определенного состава основными переменными, которые влияют на чистоту продуктов при непрерывной перегонке, являются флегмовое число и число теоретических равновесных стадий, на практике определяемых числом тарелок или высотой насадки. Флегмовое число — это поток из конденсатора обратно в колонну, который создает рециркуляцию, которая обеспечивает лучшее разделение при заданном числе тарелок. Равновесные стадии — это идеальные стадии, на которых составы достигают равновесия пар-жидкость, повторяя процесс разделения и обеспечивая лучшее разделение при заданном флегмовом числе. Колонна с высоким флегмовым числом может иметь меньше стадий, но она возвращает большое количество жидкости, что дает широкую колонну с большой задержкой. Наоборот, колонна с низким флегмовым числом должна иметь большое количество стадий, поэтому требуется более высокая колонна.
Как периодическая, так и непрерывная дистилляция может быть улучшена путем использования фракционирующей колонны наверху дистилляционной колбы. Колонна улучшает разделение, предоставляя большую площадь поверхности для контакта пара и конденсата. Это помогает ему оставаться в равновесии как можно дольше. Колонна может даже состоять из небольших подсистем («тарелок» или «тарелок»), которые все содержат обогащенную, кипящую жидкую смесь, все со своим собственным равновесием пара и жидкости.
Между лабораторными и промышленными ректификационными колоннами есть различия, но принципы одинаковы. Примеры лабораторных ректификационных колонн (по повышению эффективности) включают:
Лабораторные дистилляции почти всегда проводятся как периодические дистилляции. Устройство, используемое при дистилляции, иногда называемое перегонным кубом , состоит как минимум из ребойлера или горшка , в котором нагревается исходный материал, конденсатора, в котором нагретый пар охлаждается до жидкого состояния , и приемника, в котором собирается концентрированная или очищенная жидкость, называемая дистиллятом. Существует несколько методов лабораторной дистилляции (см. также типы дистилляции ).
Полностью герметичный дистилляционный аппарат может испытывать экстремальное и быстро меняющееся внутреннее давление, что может привести к его разрыву в местах соединения. Поэтому обычно оставляют открытым некоторый путь (например, в приемной колбе), чтобы внутреннее давление могло уравняться с атмосферным давлением. В качестве альтернативы можно использовать вакуумный насос , чтобы поддерживать давление в аппарате ниже атмосферного. Если вовлеченные вещества чувствительны к воздуху или влаге, соединение с атмосферой можно осуществить через одну или несколько осушительных трубок, заполненных материалами, которые удаляют нежелательные компоненты воздуха, или через барботеры , которые обеспечивают подвижный барьер для жидкости. Наконец, попадание нежелательных компонентов воздуха можно предотвратить, закачивая в аппарат слабый, но постоянный поток подходящего инертного газа, например азота .

При простой перегонке пар сразу направляется в конденсатор. Следовательно, дистиллят не является чистым, но его состав идентичен составу паров при данной температуре и давлении. Эта концентрация следует закону Рауля .
В результате простая перегонка эффективна только тогда, когда температуры кипения жидкостей сильно различаются (правило 25 °C) [38] или при отделении жидкостей от нелетучих твердых веществ или масел. В этих случаях давления паров компонентов обычно достаточно различны, чтобы дистиллят мог быть достаточно чистым для своего предполагаемого использования.
Справа показана схема в разрезе простой операции дистилляции. Исходная жидкость 15 в кипящей колбе 2 нагревается комбинированной плиткой и магнитной мешалкой 13 через силиконовую масляную баню (оранжевая, 14). Пар протекает через короткую колонну Вигре 3, затем через холодильник Либиха 5, охлаждается водой (синяя), которая циркулирует через порты 6 и 7. Конденсированная жидкость капает в приемную колбу 8, находящуюся в охлаждающей бане (синяя, 16). Адаптер 10 имеет соединение 9, которое может быть установлено на вакуумный насос. Компоненты соединены шлифованными соединениями .
Во многих случаях точки кипения компонентов в смеси будут достаточно близки, поэтому необходимо учитывать закон Рауля . Поэтому для разделения компонентов путем повторных циклов испарения-конденсации в насадочной ректификационной колонне необходимо использовать фракционную перегонку. Это разделение путем последовательных перегонок также называется ректификацией. [39]
По мере нагревания очищаемого раствора его пары поднимаются в ректификационную колонну . Поднимаясь, он охлаждается, конденсируясь на стенках конденсатора и поверхностях насадочного материала. Здесь конденсат продолжает нагреваться поднимающимися горячими парами; он снова испаряется. Однако состав свежих паров снова определяется законом Рауля. Каждый цикл испарения-конденсации (называемый теоретической тарелкой ) даст более чистый раствор более летучего компонента. [40] В действительности каждый цикл при данной температуре не происходит в точно таком же положении в ректификационной колонне; теоретическая тарелка, таким образом, является концепцией, а не точным описанием.
Больше теоретических тарелок приводит к лучшему разделению. Система дистилляции с вращающейся лентой использует вращающуюся ленту из тефлона или металла, чтобы заставить восходящие пары вступить в тесный контакт с нисходящим конденсатом, увеличивая количество теоретических тарелок. [41]
Как и вакуумная перегонка , паровая перегонка является методом перегонки соединений, чувствительных к теплу. [1] : 151–153 Температуру пара легче контролировать, чем поверхность нагревательного элемента , и она обеспечивает высокую скорость теплопередачи без нагрева при очень высокой температуре. Этот процесс включает барботирование пара через нагретую смесь сырья. По закону Рауля часть целевого соединения испаряется (в соответствии с его парциальным давлением). Паровая смесь охлаждается и конденсируется, обычно давая слой масла и слой воды.
Паровая дистилляция различных ароматических трав и цветов может привести к двум продуктам: эфирному маслу , а также водному травяному дистилляту . Эфирные масла часто используются в парфюмерии и ароматерапии, в то время как водные дистилляты имеют множество применений в ароматерапии , пищевой промышленности и уходе за кожей .


Некоторые соединения имеют очень высокие температуры кипения. Чтобы закипятить такие соединения, часто лучше понизить давление, при котором они кипят, вместо того, чтобы повышать температуру. Как только давление понижается до давления паров соединения (при данной температуре), можно начинать кипение и оставшуюся часть процесса дистилляции. Этот метод называется вакуумной дистилляцией и обычно встречается в лаборатории в виде роторного испарителя .
Этот метод также очень полезен для соединений, которые кипят выше температуры разложения при атмосферном давлении и которые, следовательно, разложились бы при любой попытке вскипятить их при атмосферном давлении.
Молекулярная дистилляция — это вакуумная дистилляция ниже давления 0,01 торр . 0,01 торр на порядок выше высокого вакуума , где жидкости находятся в режиме свободного молекулярного течения , т. е. длина свободного пробега молекул сопоставима с размером оборудования. Газообразная фаза больше не оказывает значительного давления на испаряемое вещество, и, следовательно, скорость испарения больше не зависит от давления. То есть, поскольку предположения о непрерывности динамики жидкости больше не применяются, массоперенос регулируется молекулярной динамикой, а не динамикой жидкости. Таким образом, необходим короткий путь между горячей поверхностью и холодной поверхностью, обычно путем подвешивания горячей пластины, покрытой пленкой сырья, рядом с холодной пластиной с прямой видимостью между ними. Молекулярная дистилляция используется в промышленности для очистки масел.
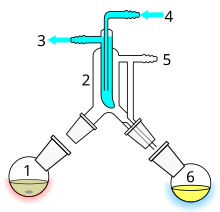
Короткая дистилляция — это метод дистилляции, при котором дистиллят проходит короткое расстояние, часто всего несколько сантиметров, и обычно выполняется при пониженном давлении. [1] : 150 Классическим примером может служить дистилляция, при которой дистиллят проходит из одной стеклянной колбы в другую, без необходимости в конденсаторе, разделяющем две камеры. Этот метод часто используется для соединений, которые нестабильны при высоких температурах, или для очистки небольших количеств соединения. Преимущество заключается в том, что температура нагрева может быть значительно ниже (при пониженном давлении), чем точка кипения жидкости при стандартном давлении, и дистилляту нужно пройти только короткое расстояние перед конденсацией. Короткий путь гарантирует, что мало соединения будет потеряно на стенках аппарата. Аппарат Кугельрора — это своего рода метод короткой дистилляции, который часто содержит несколько камер для сбора фракций дистиллята.
Некоторые соединения имеют высокие температуры кипения, а также чувствительны к воздуху . Можно использовать простую систему вакуумной дистилляции, как показано выше, в которой вакуум заменяется инертным газом после завершения дистилляции. Однако это менее удовлетворительная система, если требуется собирать фракции при пониженном давлении. Для этого можно добавить адаптер «корова» или «свинья» к концу конденсатора, или для лучших результатов или для очень чувствительных к воздуху соединений можно использовать аппарат треугольника Перкина .
Треугольник Перкина имеет средства с помощью ряда стеклянных или тефлоновых кранов, которые позволяют изолировать фракции от остальной части дистиллята , без удаления основного тела дистилляции из вакуума или источника тепла, и, таким образом, может оставаться в состоянии рефлюкса . Для этого образец сначала изолируется от вакуума с помощью кранов, затем вакуум над образцом заменяется инертным газом (таким как азот или аргон ), а затем может быть закупорен и удален. Затем в систему можно добавить новый сосуд для сбора, вакуумировать и снова подключить к системе дистилляции через краны для сбора второй фракции, и так далее, пока все фракции не будут собраны.
Zone distillation is a distillation process in a long container with partial melting of refined matter in moving liquid zone and condensation of vapor in the solid phase at condensate pulling in cold area. The process is worked in theory. When zone heater is moving from the top to the bottom of the container then solid condensate with irregular impurity distribution is forming. Then most pure part of the condensate may be extracted as product. The process may be iterated many times by moving (without turnover) the received condensate to the bottom part of the container on the place of refined matter. The irregular impurity distribution in the condensate (that is efficiency of purification) increases with the number of iterations. Zone distillation is the distillation analog of zone recrystallization. Impurity distribution in the condensate is described by known equations of zone recrystallization – with the replacement of the distribution co-efficient k of crystallization - for the separation factor α of distillation.[42][43][44]
Non-condensable gas can be expelled from the apparatus by the vapor of relatively volatile co-solvent, which spontaneously evaporates during initial pumping, and this can be achieved with regular oil or diaphragm pump.[45][46]
The unit process of evaporation may also be called "distillation":
Other uses:
Interactions between the components of the solution create properties unique to the solution, as most processes entail non-ideal mixtures, where Raoult's law does not hold. Such interactions can result in a constant-boiling azeotrope which behaves as if it were a pure compound (i.e., boils at a single temperature instead of a range). At an azeotrope, the solution contains the given component in the same proportion as the vapor, so that evaporation does not change the purity, and distillation does not result in separation. For example, 95.6% ethanol (by mass) in water forms an azeotrope at 78.1 °C.
If the azeotrope is not considered sufficiently pure for use, there exist some techniques to break the azeotrope to give a more pure distillate. These techniques are known as azeotropic distillation. Some techniques achieve this by "jumping" over the azeotropic composition (by adding another component to create a new azeotrope, or by varying the pressure). Others work by chemically or physically removing or sequestering the impurity. For example, to purify ethanol beyond 95%, a drying agent (or desiccant, such as potassium carbonate) can be added to convert the soluble water into insoluble water of crystallization. Molecular sieves are often used for this purpose as well.
Immiscible liquids, such as water and toluene, easily form azeotropes. Commonly, these azeotropes are referred to as a low boiling azeotrope because the boiling point of the azeotrope is lower than the boiling point of either pure component. The temperature and composition of the azeotrope is easily predicted from the vapor pressure of the pure components, without use of Raoult's law. The azeotrope is easily broken in a distillation set-up by using a liquid–liquid separator (a decanter) to separate the two liquid layers that are condensed overhead. Only one of the two liquid layers is refluxed to the distillation set-up.
High boiling azeotropes, such as a 20 percent by weight mixture of hydrochloric acid in water, also exist. As implied by the name, the boiling point of the azeotrope is greater than the boiling point of either pure component.
The boiling points of components in an azeotrope overlap to form a band. By exposing an azeotrope to a vacuum or positive pressure, it is possible to bias the boiling point of one component away from the other by exploiting the differing vapor pressure curves of each; the curves may overlap at the azeotropic point, but are unlikely to remain identical further along the pressure axis to either side of the azeotropic point. When the bias is great enough, the two boiling points no longer overlap and so the azeotropic band disappears.
This method can remove the need to add other chemicals to a distillation, but it has two potential drawbacks.
Under negative pressure, power for a vacuum source is needed and the reduced boiling points of the distillates requires that the condenser be run cooler to prevent distillate vapors being lost to the vacuum source. Increased cooling demands will often require additional energy and possibly new equipment or a change of coolant.
Alternatively, if positive pressures are required, standard glassware can not be used, energy must be used for pressurization and there is a higher chance of side reactions occurring in the distillation, such as decomposition, due to the higher temperatures required to effect boiling.
A unidirectional distillation will rely on a pressure change in one direction, either positive or negative.
Pressure-swing distillation is essentially the same as the unidirectional distillation used to break azeotropic mixtures, but here both positive and negative pressures may be employed.
This improves the selectivity of the distillation and allows a chemist to optimize distillation by avoiding extremes of pressure and temperature that waste energy. This is particularly important in commercial applications.
One example of the application of pressure-swing distillation is during the industrial purification of ethyl acetate after its catalytic synthesis from ethanol.

Large scale industrial distillation applications include both batch and continuous fractional, vacuum, azeotropic, extractive, and steam distillation. The most widely used industrial applications of continuous, steady-state fractional distillation are in petroleum refineries, petrochemical and chemical plants and natural gas processing plants.
To control and optimize such industrial distillation, a standardized laboratory method, ASTM D86, is established. This test method extends to the atmospheric distillation of petroleum products using a laboratory batch distillation unit to quantitatively determine the boiling range characteristics of petroleum products.
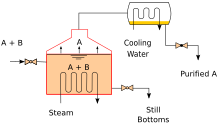
Industrial distillation[39][47] is typically performed in large, vertical cylindrical columns known as distillation towers or distillation columns with diameters ranging from about 0.65 to 16 metres (2 ft 2 in to 52 ft 6 in) and heights ranging from about 6 to 90 metres (20 to 295 ft) or more. When the process feed has a diverse composition, as in distilling crude oil, liquid outlets at intervals up the column allow for the withdrawal of different fractions or products having different boiling points or boiling ranges. The "lightest" products (those with the lowest boiling point) exit from the top of the columns and the "heaviest" products (those with the highest boiling point) exit from the bottom of the column and are often called the bottoms.
Industrial towers use reflux to achieve a more complete separation of products. Reflux refers to the portion of the condensed overhead liquid product from a distillation or fractionation tower that is returned to the upper part of the tower as shown in the schematic diagram of a typical, large-scale industrial distillation tower. Inside the tower, the downflowing reflux liquid provides cooling and condensation of the upflowing vapors thereby increasing the efficiency of the distillation tower. The more reflux that is provided for a given number of theoretical plates, the better the tower's separation of lower boiling materials from higher boiling materials. Alternatively, the more reflux that is provided for a given desired separation, the fewer the number of theoretical plates required. Chemical engineers must choose what combination of reflux rate and number of plates is both economically and physically feasible for the products purified in the distillation column.
Such industrial fractionating towers are also used in cryogenic air separation, producing liquid oxygen, liquid nitrogen, and high purity argon. Distillation of chlorosilanes also enables the production of high-purity silicon for use as a semiconductor.
Design and operation of a distillation tower depends on the feed and desired products. Given a simple, binary component feed, analytical methods such as the McCabe–Thiele method[39][48] or the Fenske equation[39] can be used. For a multi-component feed, simulation models are used both for design and operation. Moreover, the efficiencies of the vapor–liquid contact devices (referred to as "plates" or "trays") used in distillation towers are typically lower than that of a theoretical 100% efficient equilibrium stage. Hence, a distillation tower needs more trays than the number of theoretical vapor–liquid equilibrium stages. A variety of models have been postulated to estimate tray efficiencies.
In modern industrial uses, a packing material is used in the column instead of trays when low pressure drops across the column are required. Other factors that favor packing are: vacuum systems, smaller diameter columns, corrosive systems, systems prone to foaming, systems requiring low liquid holdup, and batch distillation. Conversely, factors that favor plate columns are: presence of solids in feed, high liquid rates, large column diameters, complex columns, columns with wide feed composition variation, columns with a chemical reaction, absorption columns, columns limited by foundation weight tolerance, low liquid rate, large turn-down ratio and those processes subject to process surges.
This packing material can either be random or dumped packing (25–76 millimetres (1–3 in) wide) such as Raschig rings or structured sheet metal. Liquids tend to wet the surface of the packing and the vapors pass across this wetted surface, where mass transfer takes place. Unlike conventional tray distillation in which every tray represents a separate point of vapor–liquid equilibrium, the vapor–liquid equilibrium curve in a packed column is continuous. However, when modeling packed columns, it is useful to compute a number of "theoretical stages" to denote the separation efficiency of the packed column with respect to more traditional trays. Differently shaped packings have different surface areas and void space between packings. Both these factors affect packing performance.
Another factor in addition to the packing shape and surface area that affects the performance of random or structured packing is the liquid and vapor distribution entering the packed bed. The number of theoretical stages required to make a given separation is calculated using a specific vapor to liquid ratio. If the liquid and vapor are not evenly distributed across the superficial tower area as it enters the packed bed, the liquid to vapor ratio will not be correct in the packed bed and the required separation will not be achieved. The packing will appear to not be working properly. The height equivalent to a theoretical plate (HETP) will be greater than expected. The problem is not the packing itself but the mal-distribution of the fluids entering the packed bed. Liquid mal-distribution is more frequently the problem than vapor. The design of the liquid distributors used to introduce the feed and reflux to a packed bed is critical to making the packing perform to it maximum efficiency. Methods of evaluating the effectiveness of a liquid distributor to evenly distribute the liquid entering a packed bed can be found in references.[50][51] Considerable work has been done on this topic by Fractionation Research, Inc. (commonly known as FRI).[52]
The goal of multi-effect distillation is to increase the energy efficiency of the process, for use in desalination, or in some cases one stage in the production of ultrapure water. The number of effects is inversely proportional to the kW·h/m3 of water recovered figure and refers to the volume of water recovered per unit of energy compared with single-effect distillation. One effect is roughly 636 kW·h/m3:
There are many other types of multi-effect distillation processes, including one referred to as simply multi-effect distillation (MED), in which multiple chambers, with intervening heat exchangers, are employed.
Carbohydrate-containing plant materials are allowed to ferment, producing a dilute solution of ethanol in the process. Spirits such as whiskey and rum are prepared by distilling these dilute solutions of ethanol. Components other than ethanol, including water, esters, and other alcohols, are collected in the condensate, which account for the flavor of the beverage. Some of these beverages are then stored in barrels or other containers to acquire more flavor compounds and characteristic flavors.
As already mentioned, the textual evidence for Sumero-Babylonian distillation is disclosed in a group of Akkadian tablets describing perfumery operations, dated ca. 1200 B.C.
The earliest possible period seems to be the Eastern Han dynasty ... the most likely period for the beginning of true distillation of spirits for drinking in China is during the Jin and Southern Song dynasties