
Микротрубочки представляют собой полимеры тубулина , которые составляют часть цитоскелета и обеспечивают структуру и форму эукариотических клеток. Микротрубочки могут достигать длины 50 микрометров , ширины от 23 до 27 нм [2] и внутреннего диаметра от 11 до 15 нм. [3] Они образуются в результате полимеризации димера двух глобулярных белков , альфа- и бета-тубулина, в протофиламенты, которые затем могут соединяться латерально, образуя полую трубку, микротрубочку. [4] Наиболее распространенная форма микротрубочек состоит из 13 протофиламентов в трубчатом расположении.

Микротрубочки играют важную роль в ряде клеточных процессов . Они участвуют в поддержании структуры клетки и вместе с микрофиламентами и промежуточными нитями образуют цитоскелет. Они также составляют внутреннюю структуру ресничек и жгутиков . Они обеспечивают платформу для внутриклеточного транспорта и участвуют во множестве клеточных процессов, включая движение секреторных везикул , органелл и внутриклеточных макромолекулярных ансамблей. [5] Они также участвуют в делении клеток (путем митоза и мейоза ) и являются основными компонентами митотических веретен , которые используются для разделения эукариотических хромосом .
Микротрубочки зарождаются и организуются центрами организации микротрубочек , такими как центросома , обнаруженная в центре многих животных клеток, или базальные тельца ресничек и жгутиков, или тельца полюсов веретена, обнаруженные у большинства грибов.
Существует множество белков, которые связываются с микротрубочками, включая моторные белки динеин и кинезин , белки, разрывающие микротрубочки, такие как катанин , и другие белки, важные для регуляции динамики микротрубочек. [6] Недавно в грамположительной бактерии Bacillus thuringiensis был обнаружен актиноподобный белок , который образует структуру, подобную микротрубочкам, называемую нанотрубочкой, участвующую в сегрегации плазмид . [7] Другие бактериальные микротрубочки имеют кольцо из пяти протофиламентов.
Тубулин и процессы, опосредованные микротрубочками, такие как передвижение клеток, были замечены ранними микроскопистами, такими как Левенгук (1677). Однако волокнистая природа жгутиков и других структур была открыта два столетия спустя с помощью усовершенствованных световых микроскопов и подтверждена в 20 веке с помощью электронного микроскопа и биохимических исследований. [8]
Анализы in vitro на моторные белки микротрубочек , такие как динеин и кинезин , исследуются путем флуоресцентной маркировки микротрубочек и фиксации микротрубочек или моторных белков на предметном стекле микроскопа, а затем визуализации предметного стекла с помощью видеоусиленной микроскопии для записи движения моторных белков. Это обеспечивает перемещение моторных белков вдоль микротрубочек или микротрубочек, перемещающихся поперек моторных белков. [9] Следовательно, некоторые процессы в микротрубочках можно определить с помощью кимографа . [10]

У эукариот микротрубочки представляют собой длинные полые цилиндры, состоящие из полимеризованных димеров α- и β-тубулина . [12] Внутреннее пространство полых цилиндров микротрубочек называется просветом. Субъединицы α- и β-тубулина примерно на 50% идентичны на уровне аминокислот, и обе имеют молекулярную массу примерно 50 кДа. [13] [14]
Эти димеры α/β-тубулина полимеризуются конец в конец в линейные протофиламенты , которые соединяются латерально с образованием одной микротрубочки, которая затем может быть расширена за счет добавления большего количества димеров α/β-тубулина. Обычно микротрубочки образуются путем параллельной ассоциации тринадцати протофиламентов, хотя микротрубочки, состоящие из меньшего или большего количества протофиламентов, наблюдались у различных видов [15] , а также in vitro . [16]
Микротрубочки имеют четкую полярность, которая имеет решающее значение для их биологической функции. Тубулин полимеризуется конец к концу, при этом β-субъединицы одного димера тубулина контактируют с α-субъединицами следующего димера. Следовательно, в протофиламенте на одном конце будут обнажены α-субъединицы, а на другом конце — обнажены β-субъединицы. Эти концы обозначены концами (-) и (+) соответственно. Протофиламенты пучатся параллельно друг другу с одинаковой полярностью, поэтому в микротрубочке есть один конец, (+) конец, на котором обнажены только β-субъединицы, в то время как другой конец, (-) конец, имеет только α -субъединицы обнажены. Хотя удлинение микротрубочек может происходить как на (+), так и на (-) концах, оно происходит значительно быстрее на (+) конце. [17]
Латеральная ассоциация протофиламентов образует псевдоспиральную структуру, в которой один виток спирали содержит 13 димеров тубулина, каждый из разных протофиламентов. В наиболее распространенной архитектуре «13-3» 13-й димер тубулина взаимодействует со следующим димером тубулина со смещением по вертикали 3 мономеров тубулина из-за спиральности поворота. Существуют и другие альтернативные архитектуры, такие как 11-3, 12-3, 14-3, 15-4 или 16-4, которые обнаруживаются гораздо реже. [18] Микротрубочки также могут трансформироваться в другие формы, такие как спиральные нити, которые наблюдаются у протистских организмов, таких как фораминиферы . [19] Существует два различных типа взаимодействий, которые могут происходить между субъединицами боковых протофиламентов внутри микротрубочек, называемых решетками А-типа и В-типа. В решетке А-типа латеральные ассоциации протофиламентов происходят между соседними субъединицами α- и β-тубулина (т.е. субъединица α-тубулина из одного протофиламента взаимодействует с субъединицей β-тубулина из соседнего протофиламента). В решетке B-типа субъединицы α и β-тубулина одного протофиламента взаимодействуют с субъединицами α и β-тубулина соседнего протофиламента соответственно. Экспериментальные исследования показали, что решетка B-типа является основным расположением внутри микротрубочек. Однако в большинстве микротрубочек имеется шов, в котором субъединицы тубулина взаимодействуют α-β. [20]
Таким образом, последовательность и точный состав молекул при образовании микротрубочек можно резюмировать следующим образом: β-тубулин соединяется несуществующей ковалентной связью с α-тубулином, которые в связанной форме являются гетеродимерами, поскольку состоят из два разных полипептида (β-тубулин и α-тубулин). Поэтому после образования гетеродимеров они соединяются вместе, образуя длинные цепочки, которые образно поднимаются в одном направлении (например, вверх). Эти гетеродимеры, соединенные в определенном направлении, образуют протофиламенты. Эти длинные цепочки (протофиламенты) теперь постепенно скапливаются рядом друг с другом, так что образуется трубчатая структура, имеющая типичный для трубки просвет. Соответственно, внешнюю стенку микротрубочек образуют преимущественно 13 протофиламентов. Гетеродимеры состоят из положительного и отрицательного концов, причем альфа-тубулин образует отрицательный конец, а бета-тубулин - положительный конец. Благодаря тому, что гетеродимеры наложены друг на друга, всегда есть отрицательный и положительный конец. Микротрубочки растут за счет добавления гетеродимеров на плюс-конце.
Некоторые виды Prosthecobacter также содержат микротрубочки. Структура этих бактериальных микротрубочек аналогична структуре эукариотических микротрубочек, состоящих из полой трубки протофиламентов, собранных из гетеродимеров бактериального тубулина А (BtubA) и бактериального тубулина B (BtubB). И BtubA, и BtubB имеют общие черты как α-, так и β- тубулина . В отличие от эукариотических микротрубочек, бактериальные микротрубочки не требуют для сворачивания шаперонов. [21] В отличие от 13 протофиламентов эукариотических микротрубочек, бактериальные микротрубочки состоят только из пяти. [22]
Микротрубочки являются частью цитоскелета , структурной сети внутри цитоплазмы клетки . Роли цитоскелета микротрубочек включают механическую поддержку, организацию цитоплазмы, транспорт, подвижность и сегрегацию хромосом. В развивающихся нейронах микротрубочки известны как нейротрубочки [ 23] и могут модулировать динамику актина , другого компонента цитоскелета. [24] Микротрубочка способна расти и сжиматься, чтобы генерировать силу, и существуют моторные белки, которые позволяют органеллам и другим клеточным компонентам переноситься по микротрубочкам. Такое сочетание ролей делает микротрубочки важными для организации и перемещения внутриклеточных компонентов.
Организация микротрубочек в клетке зависит от типа клетки. В эпителии минус-концы полимера микротрубочек закреплены вблизи места межклеточного контакта и организованы вдоль апикально-базальной оси. После нуклеации минус-концы высвобождаются и затем повторно закрепляются на периферии с помощью таких факторов, как ninein и PLEKHA7 . [25] Таким образом, они могут облегчить транспорт белков, везикул и органелл вдоль апикально-базальной оси клетки. В фибробластах и других типах мезенхимальных клеток микротрубочки закреплены на центросоме и расходятся своими плюсовыми концами наружу к периферии клетки (как показано на первом рисунке). В этих клетках микротрубочки играют важную роль в миграции клеток. Более того, на полярность микротрубочек влияют моторные белки, которые организуют многие компоненты клетки, включая эндоплазматический ретикулум и аппарат Гольджи .

Нуклеация — это событие, которое инициирует образование микротрубочек из димера тубулина. Микротрубочки обычно зарождаются и организуются органеллами, называемыми центрами организации микротрубочек (MTOC). В MTOC содержится другой тип тубулина, γ-тубулин, который отличается от α- и β-субъединиц самих микротрубочек. γ-тубулин соединяется с несколькими другими связанными белками, образуя структуру, похожую на стопорную шайбу, известную как «кольцевой комплекс γ-тубулина» (γ-TuRC). Этот комплекс действует как матрица для димеров α/β-тубулина, на которой начинается полимеризация; он действует как колпачок на (-) конце, в то время как рост микротрубочек продолжается от MTOC в направлении (+). [26]
Центросома является основным MTOC большинства типов клеток . Однако микротрубочки могут образовываться и из других мест. Например, реснички и жгутики имеют в основании MTOC, называемые базальными тельцами . Кроме того, работа группы Каверина из Вандербильта и других предполагает, что аппарат Гольджи может служить важной платформой для зарождения микротрубочек. [27] Поскольку нуклеация из центросомы по своей сути симметрична, ассоциированная с Гольджи нуклеация микротрубочек может позволить клетке устанавливать асимметрию в сети микротрубочек. В недавних исследованиях группа Вейла из UCSF определила белковый комплекс augmin как критический фактор для зависимой от центросомы генерации микротрубочек на основе веретена. Было показано, что он взаимодействует с γ-TuRC и увеличивает плотность микротрубочек вокруг начала митотического веретена. [28]
Некоторые типы клеток, такие как растительные клетки, не содержат четко определенных MTOC. В этих клетках микротрубочки зарождаются из отдельных участков цитоплазмы. Другие типы клеток, такие как паразиты -трипаносоматиды , имеют MTOC, но он постоянно обнаруживается в основании жгутика. Здесь зарождение микротрубочек для структурных ролей и для генерации митотического веретена происходит не из канонического центриоль-подобного MTOC.
После начального события нуклеации к растущему полимеру необходимо добавить мономеры тубулина. Процесс добавления или удаления мономеров зависит от концентрации димеров αβ-тубулина в растворе по отношению к критической концентрации, которая представляет собой устойчивую концентрацию димеров, при которой больше не происходит чистой сборки или разборки на конце микротрубочки. . Если концентрация димера превышает критическую концентрацию, микротрубочка будет полимеризоваться и расти. Если концентрация меньше критической, длина микротрубочки уменьшится. [29]
Динамическая нестабильность относится к сосуществованию сборки и разборки на концах микротрубочки. Микротрубочка может динамически переключаться между фазами роста и сокращения в этой области. [30] Димеры тубулина могут связывать две молекулы GTP, одна из которых может быть гидролизована после сборки. Во время полимеризации димеры тубулина находятся в ГТФ -связанном состоянии. [12] GTP, связанный с α-тубулином, стабилен и в этом связанном состоянии выполняет структурную функцию. Однако GTP, связанный с β-тубулином, может гидролизоваться до GDP вскоре после сборки. Свойства сборки GDP-тубулина отличаются от свойств GTP-тубулина, поскольку GDP-тубулин более склонен к деполимеризации. [31] Субъединица тубулина, связанная с GDP, на кончике микротрубочки будет иметь тенденцию отпадать, хотя тубулин, связанный с GDP, в середине микротрубочки не может спонтанно выскочить из полимера. Поскольку тубулин присоединяется к концу микротрубочки в ГТФ-связанном состоянии, предполагается, что на кончике микротрубочки существует колпачок ГТФ-связанного тубулина, защищающий ее от разборки. Когда гидролиз достигает кончика микротрубочки, начинается быстрая деполимеризация и сжатие. Этот переход от роста к сокращению называется катастрофой. ГТФ-связанный тубулин может снова начать добавляться к кончику микротрубочки, образуя новую крышку и защищая микротрубочку от сжатия. Это называется «спасением». [32]
В 1986 году Марк Киршнер и Тим Митчисон предположили, что микротрубочки используют свои динамические свойства роста и сжатия на своих плюсовых концах для исследования трехмерного пространства клетки. Плюсовые концы, которые сталкиваются с кинетохорами или участками полярности, захватываются и больше не демонстрируют роста или сжатия. В отличие от нормальных динамических микротрубочек, период полураспада которых составляет 5–10 минут, захваченные микротрубочки могут существовать часами. Эта идея широко известна как модель «поиска и захвата». [33] Действительно, работа, проведенная с тех пор, во многом подтвердила эту идею. Было показано, что в кинетохоре различные комплексы захватывают (+)-концы микротрубочек. [34] Кроме того, также была описана активность кэпирования (+)-конца интерфазных микротрубочек. [35] Эта более поздняя активность опосредована форминами , [36] белком аденоматозного полипоза coli , и EB1 , [37] белком, который отслеживает растущие плюс-концы микротрубочек.

Хотя период полураспада большинства микротрубочек составляет 5–10 минут, некоторые микротрубочки могут оставаться стабильными в течение нескольких часов. [35] Эти стабилизированные микротрубочки накапливают посттрансляционные модификации субъединиц тубулина под действием ферментов, связанных с микротрубочками. [38] [39] Однако, как только микротрубочки деполимеризуются, большинство этих модификаций быстро обращаются растворимыми ферментами. Поскольку большинство реакций модификации протекают медленно, а их обратные реакции — быстро, модифицированный тубулин обнаруживается только на долгоживущих стабильных микротрубочках. Большинство этих модификаций происходит в С-концевой области альфа-тубулина. Эта область, богатая отрицательно заряженным глутаматом, образует относительно неструктурированные хвосты, которые выступают из микротрубочек и образуют контакты с моторами. Таким образом, полагают, что модификации тубулина регулируют взаимодействие моторов с микротрубочками. Поскольку эти стабильные модифицированные микротрубочки обычно ориентированы к месту клеточной полярности в интерфазных клетках, это подмножество модифицированных микротрубочек обеспечивает специализированный путь, который помогает доставлять пузырьки в эти поляризованные зоны. Эти модификации включают в себя:
Тубулин также известен как фосфорилированный , убиквитинированный , сумойилированный и пальмитоилированный . [38]
Широкий спектр лекарств способен связываться с тубулином и изменять его свойства сборки. Эти препараты могут оказывать эффект при внутриклеточных концентрациях, значительно меньших, чем у тубулина. Это вмешательство в динамику микротрубочек может привести к остановке клеточного цикла клетки и привести к запрограммированной гибели клеток или апоптозу . Однако есть данные, позволяющие предположить, что вмешательства в динамику микротрубочек недостаточно, чтобы блокировать клетки, подвергающиеся митозу. [46] Эти исследования показали, что подавление динамики происходит при концентрациях ниже тех, которые необходимы для блокирования митоза. Было показано, что подавление динамики микротрубочек мутациями тубулина или медикаментозным лечением ингибирует миграцию клеток. [47] Как стабилизаторы, так и дестабилизаторы микротрубочек могут подавлять динамику микротрубочек.
К препаратам, которые могут изменить динамику микротрубочек, относятся:
Таксаны (отдельно или в сочетании с производными платины (карбоплатином) или гемцитабином) применяются при злокачественных новообразованиях молочной железы и гинекологии, плоскоклеточном раке (рак головы и шеи, некоторые виды рака легких) и др.
Сообщалось, что экспрессия β3-тубулина изменяет клеточные ответы на вызванное лекарственными средствами подавление динамики микротрубочек. В целом динамика обычно подавляется низкими субтоксичными концентрациями препаратов микротрубочек, которые также ингибируют миграцию клеток. Однако включение β3-тубулина в микротрубочки увеличивает концентрацию препарата, необходимую для подавления динамики и ингибирования миграции клеток. Таким образом, опухоли, экспрессирующие β3-тубулин, устойчивы не только к цитотоксическому действию препаратов, нацеленных на микротрубочки, но и к их способности подавлять метастазирование опухоли. [48] Более того, экспрессия β3-тубулина также противодействует способности этих препаратов ингибировать ангиогенез, что обычно является еще одним важным аспектом их действия. [49]
Полимеры микротрубочек чрезвычайно чувствительны к различным воздействиям окружающей среды. Очень низкие уровни свободного кальция могут дестабилизировать микротрубочки, и это помешало ранним исследователям изучить полимер in vitro. [12] Низкие температуры также вызывают быструю деполимеризацию микротрубочек. Напротив, тяжелая вода способствует стабильности полимера микротрубочек. [50]
Было показано, что MAP играют решающую роль в регуляции динамики микротрубочек in vivo . Скорость полимеризации, деполимеризации и катастрофы микротрубочек варьируется в зависимости от того, какие белки, ассоциированные с микротрубочками (MAP), присутствуют. Первоначально идентифицированные MAP из ткани головного мозга можно разделить на две группы в зависимости от их молекулярной массы. Этот первый класс включает MAP с молекулярной массой ниже 55-62 кДа и называется τ (тау) белками . In vitro было показано, что тау-белки напрямую связывают микротрубочки, способствуют нуклеации и предотвращают разборку, а также индуцируют образование параллельных массивов. [51] Кроме того, было показано, что тау-белки стабилизируют микротрубочки в аксонах и участвуют в болезни Альцгеймера. [52] Второй класс составляют MAP с молекулярной массой 200-1000 кДа, из которых известны четыре типа: MAP-1, MAP-2 , MAP-3 и MAP-4 . Белки MAP-1 состоят из набора трех различных белков: A , B и C. Белок C играет важную роль в ретроградном транспорте везикул и известен также как цитоплазматический динеин . Белки MAP-2 расположены в дендритах и в теле нейронов, где они связываются с другими филаментами цитоскелета. Белки MAP-4 обнаружены в большинстве клеток и стабилизируют микротрубочки. Помимо MAP, оказывающих стабилизирующее действие на структуру микротрубочек, другие MAP могут оказывать дестабилизирующее действие либо за счет расщепления, либо за счет индукции деполимеризации микротрубочек. Было обнаружено, что три белка, называемые катанин , спастин и фиджетин, регулируют количество и длину микротрубочек посредством своей дестабилизирующей активности. Более того, предполагается , что CRACD-подобный белок локализуется в микротрубочках. [53]
MAP являются детерминантами различных цитоскелетных форм аксонов и дендритов , при этом микротрубочки в дендритах расположены дальше друг от друга [54]
Белки отслеживания концов плюс представляют собой белки MAP, которые связываются с кончиками растущих микротрубочек и играют важную роль в регуляции динамики микротрубочек. Например, было обнаружено, что +TIPs участвуют во взаимодействиях микротрубочек с хромосомами во время митоза. Первым MAP, который был идентифицирован как +TIP, был CLIP1 70 (цитоплазматический линкерный белок), который, как было показано, играет роль в спасательных операциях при деполимеризации микротрубочек. Дополнительные примеры +TIP включают EB1 , EB2 , EB3 , p150Glued , Dynamitin , Lis1 , CLIP115 , CLASP1 и CLASP2 . [ нужна цитата ]
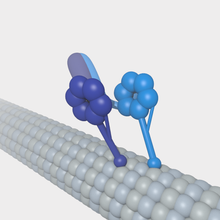

Микротрубочки могут выступать в качестве субстратов для моторных белков, которые участвуют в важных клеточных функциях, таких как транспорт везикул и деление клеток. В отличие от других белков, связанных с микротрубочками, моторные белки используют энергию гидролиза АТФ для создания механической работы, которая перемещает белок вдоль субстрата. Основными моторными белками, которые взаимодействуют с микротрубочками, являются кинезин , который обычно движется к (+) концу микротрубочки, и динеин , который движется к (-) концу.
Некоторые вирусы (включая ретровирусы , герпесвирусы , парвовирусы и аденовирусы ), которым требуется доступ к ядру для репликации своих геномов, прикрепляются к моторным белкам.

Центросома является основным MTOC ( центром организации микротрубочек ) клетки во время митоза. Каждая центросома состоит из двух цилиндров, называемых центриолями , ориентированных под прямым углом друг к другу. Центриоль образована из 9 основных микротрубочек, к каждой из которых прикреплены две частичные микротрубочки. Каждая центриоль имеет длину примерно 400 нм и окружность около 200 нм. [56]
Центросома имеет решающее значение для митоза, поскольку большинство микротрубочек, участвующих в этом процессе, происходят из центросомы. Минусовые концы каждой микротрубочки начинаются у центросомы, а плюсовые концы расходятся во всех направлениях. Таким образом, центросома также важна для поддержания полярности микротрубочек во время митоза. [57]
Большинство клеток имеют только одну центросому на протяжении большей части клеточного цикла, однако непосредственно перед митозом центросома удваивается, и клетка содержит две центросомы. [58] Некоторые микротрубочки, отходящие от центросомы, растут непосредственно от сестринской центросомы. Эти микротрубочки называются астральными микротрубочками. С помощью этих астральных микротрубочек центросомы удаляются друг от друга к противоположным сторонам клетки. Оказавшись там, могут начать формироваться другие типы микротрубочек, необходимые для митоза, включая межполярные микротрубочки и К-волокна. [59]
Последнее важное замечание о центросомах и микротрубочках во время митоза: хотя центросома является MTOC для микротрубочек, необходимых для митоза, исследования показали, что как только сами микротрубочки сформированы и находятся в правильном месте, сами центросомы не нужны для митоза. происходить. [60]
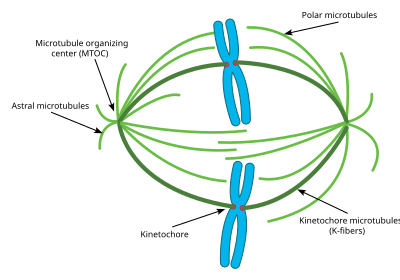
Астральные микротрубочки представляют собой подкласс микротрубочек, которые существуют только во время и вокруг митоза. Они происходят из центросомы, но не взаимодействуют с хромосомами, кинетохорами или с микротрубочками, исходящими из другой центросомы. [61] Вместо этого их микротрубочки расходятся к клеточной мембране. Оказавшись там, они взаимодействуют со специфическими моторными белками, которые создают силу, которая притягивает микротрубочки и, следовательно, всю центросому к клеточной мембране. Как указано выше, это помогает центросомам ориентироваться друг от друга в клетке. Однако эти астральные микротрубочки не взаимодействуют с самим митотическим веретеном. Эксперименты показали, что без этих астральных микротрубочек митотическое веретено может сформироваться, однако его ориентация в клетке не всегда правильная, и поэтому митоз происходит не так эффективно. [62] Другая ключевая функция астральных микротрубочек — участие в цитокинезе. Астральные микротрубочки взаимодействуют с моторными белками на клеточной мембране, разделяя веретено и всю клетку после репликации хромосом.
Межполярные/полярные микротрубочки представляют собой класс микротрубочек, которые также отходят от центросомы во время митоза. Эти микротрубочки расходятся к митотическому веретену, в отличие от астральных микротрубочек. Межполярные микротрубочки являются наиболее многочисленным и динамичным подклассом микротрубочек во время митоза. Около 95 процентов микротрубочек митотического веретена можно охарактеризовать как интерполярные. Кроме того, период полураспада этих микротрубочек чрезвычайно короток и составляет менее одной минуты. [63] Межполярные микротрубочки, которые не прикрепляются к кинетохорам, могут способствовать скоплению хромосом посредством латерального взаимодействия с кинетохорами. [64]
K-волокна/микротрубочки кинетохора представляют собой третий важный подкласс митотических микротрубочек. Эти микротрубочки образуют прямые связи с кинетохорами митотического веретена. Каждое К-волокно состоит из 20–40 параллельных микротрубочек, образующих прочную трубку, прикрепленную одним концом к центросоме, а другим — к кинетохору, расположенному в центре каждой хромосомы. Поскольку каждая центросома имеет K-волокно, соединяющееся с каждой парой хромосом, хромосомы связываются в середине митотического веретена K-волокнами. К-волокна имеют гораздо более длительный период полураспада, чем межполярные микротрубочки, от 4 до 8 минут. [65] В конце митозов микротрубочки, образующие каждое K-волокно, начинают диссоциировать, тем самым укорачивая K-волокна. Поскольку K-волокна укорачиваются, парные хромосомы разрываются прямо перед цитокинезом. Ранее некоторые исследователи полагали, что К-волокна образуются на их минус-конце, исходящем из центросомы, как и другие микротрубочки, однако новые исследования указали на другой механизм. В этом новом механизме K-волокна первоначально стабилизируются на своем плюсовом конце кинетохорами и растут оттуда. Минусовый конец этих K-волокон в конечном итоге соединяется с существующей межполярной микротрубочкой и в конечном итоге таким образом соединяется с центросомой. [66]
Большинство микротрубочек, образующих митотическое веретено, происходят из центросомы. Первоначально считалось, что все эти микротрубочки произошли из центросомы с помощью метода, называемого поиском и захватом, более подробно описанного в разделе выше, однако новые исследования показали, что существуют дополнительные способы зарождения микротрубочек во время митоза. Одним из наиболее важных из этих дополнительных способов нуклеации микротрубочек является путь RAN-GTP. RAN-GTP связывается с хроматином во время митоза, создавая градиент, который обеспечивает локальное зарождение микротрубочек рядом с хромосомами. Более того, второй путь, известный как комплекс augmin/HAUS (некоторые организмы используют более изученный комплекс augmin, в то время как другие, например люди, используют аналогичный комплекс, называемый HAUS), действует как дополнительное средство зарождения микротрубочек в митотическом веретене. [66]
Плюс-концы микротрубочек часто локализуются в определенных структурах. В поляризованных интерфазных клетках микротрубочки непропорционально ориентированы от MTOC к месту полярности, например, к переднему краю мигрирующих фибробластов . Считается, что эта конфигурация помогает доставлять связанные с микротрубочками везикулы из аппарата Гольджи к месту полярности.
Динамическая нестабильность микротрубочек также необходима для миграции большинства ползающих клеток млекопитающих. [67] Динамические микротрубочки регулируют уровни ключевых G-белков , таких как RhoA [68] и Rac1 , [69] , которые регулируют сократимость клеток и их распространение. Динамические микротрубочки также необходимы для запуска разборки фокальной адгезии , которая необходима для миграции. [70] Было обнаружено, что микротрубочки действуют как «стойки», которые противодействуют сократительным силам, которые необходимы для ретракции заднего края во время движения клеток. Когда микротрубочки на заднем крае клетки динамичны, они способны ремоделироваться, обеспечивая втягивание. Когда динамика подавлена, микротрубочки не могут реконструироваться и, следовательно, противодействовать сократительным силам. [47] Морфология клеток с подавленной динамикой микротрубочек указывает на то, что клетки могут расширять передний край (поляризованно в направлении движения), но испытывают трудности с втягиванием заднего края. [71] С другой стороны, высокие концентрации лекарства или мутации микротрубочек, которые деполимеризуют микротрубочки, могут восстановить миграцию клеток, но при этом происходит потеря направленности. Можно заключить, что микротрубочки действуют как для ограничения движения клеток, так и для установления направленности.
Микротрубочки играют важную структурную роль в ресничках и жгутиках эукариот . Реснички и жгутики всегда отходят непосредственно от MTOC, в данном случае называемого базальным тельцем. Действие моторных белков динеина на различные нити микротрубочек, которые проходят вдоль ресничек или жгутиков, позволяет органелле сгибаться и генерировать силу для плавания, перемещения внеклеточного материала и других функций. Прокариоты обладают тубулиноподобными белками, включая FtsZ . Однако жгутики прокариот совершенно отличаются по строению от жгутиков эукариот и не содержат структур на основе микротрубочек.
Цитоскелет, образованный микротрубочками, важен для морфогенетического процесса развития организма . Например, сеть поляризованных микротрубочек необходима внутри ооцита Drosophila melanogaster во время его эмбриогенеза , чтобы установить ось яйцеклетки. Сигналы, посылаемые между фолликулярными клетками и ооцитом (например, факторы, подобные эпидермальному фактору роста ), вызывают реорганизацию микротрубочек так, что их (-) концы располагаются в нижней части ооцита, поляризуя структуру и приводя к появлению передне-задней оси. [72] Такое участие в архитектуре тела наблюдается и у млекопитающих . [73]
Другой областью, где микротрубочки играют важную роль, является развитие нервной системы у высших позвоночных , где динамика тубулина и динамика связанных с ним белков (таких как белки, связанные с микротрубочками) тонко контролируются во время развития нервной системы . [74]
Клеточный цитоскелет представляет собой динамическую систему, которая функционирует на многих различных уровнях: помимо придания клетке определенной формы и поддержки транспорта везикул и органелл, он также может влиять на экспрессию генов . Механизмы передачи сигналов , участвующие в этой коммуникации, мало изучены. Однако была описана связь между лекарственной деполимеризацией микротрубочек и специфической экспрессией факторов транскрипции , что дало информацию о дифференциальной экспрессии генов в зависимости от присутствия этих факторов. [75] Эта связь между цитоскелетом и регуляцией клеточного ответа также связана с действием факторов роста : например, такая связь существует для фактора роста соединительной ткани . [76]