
Никотиновые рецепторы ацетилхолина , или nAChR , представляют собой рецепторные полипептиды , которые реагируют на нейромедиатор ацетилхолин . Никотиновые рецепторы также реагируют на такие лекарства, как агонист никотин . Они обнаружены в центральной и периферической нервной системе, мышцах и многих других тканях многих организмов. В нервно-мышечном соединении они являются первичными рецепторами в мышцах, обеспечивающими двигательную нервно-мышечную связь, которая контролирует сокращение мышц. В периферической нервной системе : (1) они передают исходящие сигналы от пресинаптических к постсинаптическим клеткам симпатической и парасимпатической нервной системы и (2) являются рецепторами скелетных мышц, которые получают ацетилхолин, высвобождаемый для подачи сигнала о мышечном сокращении. В иммунной системе нАХР регулируют воспалительные процессы и передают сигналы через отдельные внутриклеточные пути. [1] У насекомых холинергическая система ограничена центральной нервной системой . [2]
Никотиновые рецепторы считаются холинергическими рецепторами , поскольку они реагируют на ацетилхолин. Никотиновые рецепторы получили свое название от никотина , который не стимулирует мускариновые рецепторы ацетилхолина , а вместо этого избирательно связывается с никотиновыми рецепторами. [3] [4] [5] Мускариновый рецептор ацетилхолина также получил свое название от химического вещества, которое избирательно присоединяется к этому рецептору — мускарина . [6] Сам ацетилхолин связывается как с мускариновыми, так и с никотиновыми рецепторами ацетилхолина. [7]
Являясь ионотропными рецепторами, нАХР напрямую связаны с ионными каналами. Новые данные свидетельствуют о том, что эти рецепторы в некоторых случаях могут также использовать вторичные мессенджеры (как это делают метаботропные рецепторы ). [8] Никотиновые рецепторы ацетилхолина являются наиболее изученными из ионотропных рецепторов. [3]
Поскольку никотиновые рецепторы помогают передавать исходящие сигналы для симпатической и парасимпатической систем, антагонисты никотиновых рецепторов, такие как гексаметоний , препятствуют передаче этих сигналов. Так, например, антагонисты никотиновых рецепторов влияют на барорефлекс [ 9] , который в норме корректирует изменения артериального давления путем симпатической и парасимпатической стимуляции сердца.
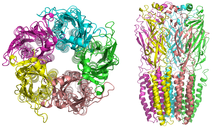
Никотиновые рецепторы с молекулярной массой 290 кДа [ 10] состоят из пяти субъединиц, расположенных симметрично вокруг центральной поры . [3] Каждая субъединица состоит из четырех трансмембранных доменов, N- и C-концы которых расположены внеклеточно. Они обладают сходством с рецепторами ГАМК А , рецепторами глицина и рецепторами серотонина 3 типа (которые все являются ионотропными рецепторами) или характерными белками Cys-петли . [11]
У позвоночных никотиновые рецепторы подразделяются на два подтипа в зависимости от их основных мест экспрессии: никотиновые рецепторы мышечного типа и никотиновые рецепторы нейронального типа . В рецепторах мышечного типа, обнаруженных в нервно-мышечном соединении, рецепторы представляют собой либо эмбриональную форму, состоящую из субъединиц α 1 , β 1 , γ и δ в соотношении 2:1:1:1 ((α 1 ) 2 β 1 γδ), или взрослая форма, состоящая из субъединиц α 1 , β 1 , δ и ε в соотношении 2:1:1:1 ((α 1 ) 2 β 1 δε). [3] [4] [5] [12] Подтипы нейронов представляют собой различные гомомерные (все один тип субъединицы) или гетеромерные (по крайней мере, один α и один β) комбинации двенадцати различных субъединиц никотиновых рецепторов: α 2 -α 10 и β 2 -β 4 . Примеры подтипов нейронов включают: (α 4 ) 3 (β 2 ) 2 , (α 4 ) 2 (β 2 ) 3 , (α 3 ) 2 (β 4 ) 3 , α 4 α 6 β 3 (β 2 ) 2 , (α 7 ) 5 и многие другие. В рецепторах как мышечного, так и нейронального типа субъединицы очень похожи друг на друга, особенно в гидрофобных областях. [13]
Ряд исследований электронной микроскопии и рентгеновской кристаллографии предоставили структурную информацию с очень высоким разрешением для мышечных и нейрональных нАХР и их связывающих доменов. [10] [14] [15] [16]
Как и во всех лиганд-управляемых ионных каналах, открытие поры канала нАХР требует связывания химического мессенджера. Для обозначения молекул, связывающих рецепторы, используются несколько разных терминов, таких как лиганд , агонист или передатчик. Помимо эндогенного агониста ацетилхолина , агонисты нАХР включают никотин , эпибатидин и холин . Никотиновые антагонисты, блокирующие рецептор, включают мекамиламин, дигидро-β-эритроидин и гексаметоний . [13]
В нАХР мышечного типа сайты связывания ацетилхолина расположены на границе раздела субъединиц α и ε или δ. В нейрональных нАХР сайт связывания расположен на границе раздела субъединиц α и β или между двумя субъединицами α в случае α7- рецепторов . Сайт связывания расположен во внеклеточном домене рядом с N-концом . [4] [17] Когда агонист связывается с сайтом, все присутствующие субъединицы претерпевают конформационные изменения, и канал открывается [18] и открывается пора диаметром около 0,65 нм. [4]
Никотиновые АХР могут существовать в различных взаимопревращаемых конформационных состояниях. Связывание агониста стабилизирует открытое и десенсибилизированное состояния. В нормальных физиологических условиях для открытия рецептору необходимо ровно две молекулы АХ. [19] Открытие канала позволяет положительно заряженным ионам перемещаться по нему; в частности, натрий поступает в клетку, а калий выходит. Чистый поток положительно заряженных ионов направлен внутрь.
НАХР представляет собой неселективный катионный канал, а это означает, что через него могут проходить несколько различных положительно заряженных ионов. [3] Он проницаем для Na + и K + , а некоторые комбинации субъединиц также проницаемы для Ca 2+ . [4] [20] [21] Количество натрия и калия, которые каналы пропускают через свои поры (их проводимость ), варьируется от 50 до 110 пСм , причем проводимость зависит от конкретного состава субъединиц, а также от проникающего иона. [22]
Многие нейрональные нАХР могут влиять на высвобождение других нейротрансмиттеров. [5] Канал обычно открывается быстро и имеет тенденцию оставаться открытым до тех пор, пока агонист не диффундирует , что обычно занимает около 1 миллисекунды . [4] AChR могут спонтанно открываться без связанных лигандов или могут спонтанно закрываться со связанными лигандами, а мутации в канале могут изменить вероятность любого события. [23] [18] Таким образом, связывание ACh изменяет вероятность открытия пор, которая увеличивается по мере связывания большего количества ACh.
nAChR не способен связывать ACh при связывании с любым из α-нейротоксинов змеиного яда . Эти α- нейротоксины прочно и нековалентно связываются с нАХР скелетных мышц и нейронов, блокируя тем самым действие АХ на постсинаптическую мембрану, ингибируя поток ионов и приводя к параличу и смерти. nAChR содержит два сайта связывания нейротоксинов змеиного яда. Прогресс в обнаружении динамики связывающего действия этих сайтов оказался трудным, хотя недавние исследования с использованием динамики нормального режима [24] помогли предсказать природу как механизмов связывания змеиных токсинов, так и ACh с nAChR. Эти исследования показали, что закручивающееся движение, вызванное связыванием ACh, вероятно, ответственно за открытие пор, и что одной или двух молекул α-бунгаротоксина (или другого длинноцепочечного α-нейротоксина) достаточно, чтобы остановить это движение. Токсины, по-видимому, сцепляют соседние субъединицы рецептора, подавляя поворот и, следовательно, открывающее движение. [25]
Активация рецепторов никотином изменяет состояние нейронов посредством двух основных механизмов. С одной стороны, движение катионов вызывает деполяризацию плазматической мембраны (что приводит к возникновению возбуждающего постсинаптического потенциала в нейронах ), что приводит к активации потенциалзависимых ионных каналов . С другой стороны, поступление кальция прямо или косвенно воздействует на различные внутриклеточные каскады . Это приводит, например, к регуляции активности некоторых генов или высвобождению нейротрансмиттеров . [ нужна цитата ]
Лиганд-связанная десенсибилизация рецепторов была впервые охарактеризована Кацем и Теслеффом в никотиновом рецепторе ацетилхолина. [26]
Длительное или неоднократное воздействие раздражителя часто приводит к снижению реакции этого рецептора на раздражитель, что называется десенсибилизацией. Функция нАХР может модулироваться фосфорилированием [27] за счет активации вторичных мессенджер-зависимых протеинкиназ. Было показано, что PKA [26] и PKC [28] , а также тирозинкиназы [29] фосфорилируют nAChR, что приводит к его десенсибилизации. Сообщалось, что после длительного воздействия агониста на рецептор сам агонист вызывает вызванное агонистом конформационное изменение рецептора, что приводит к десенсибилизации рецептора. [30]
Десенсибилизированные рецепторы могут вернуться в пролонгированное открытое состояние, когда агонист связывается в присутствии положительного аллостерического модулятора, например PNU-120,596 . [31] Кроме того, есть данные, указывающие на то, что определенные молекулы-шапероны оказывают регуляторное воздействие на эти рецепторы. [32]
Субъединицы никотиновых рецепторов принадлежат к мультигенному семейству (16 членов у человека), и сборка комбинаций субъединиц приводит к образованию большого количества различных рецепторов (более подробную информацию см. в базе данных Ligand-Gated Ion Channel). Эти рецепторы с сильно варьирующими кинетическими , электрофизиологическими и фармакологическими свойствами по-разному реагируют на никотин при очень разных эффективных концентрациях. Это функциональное разнообразие позволяет им принимать участие в двух основных типах нейротрансмиссии. Классическая синаптическая передача (проводная передача) предполагает высвобождение высоких концентраций нейромедиатора, действующего на непосредственно соседние рецепторы. Напротив, паракринная передача (объемная передача) включает нейротрансмиттеры, высвобождаемые окончаниями аксонов , которые затем диффундируют через внеклеточную среду, пока не достигнут своих рецепторов, которые могут находиться на расстоянии. [33] Никотиновые рецепторы также можно обнаружить в разных синаптических местах; например, мышечный никотиновый рецептор всегда функционирует постсинаптически. Нейрональные формы рецептора могут быть обнаружены как постсинаптически (участвуют в классической нейротрансмиссии), так и пресинаптически [34] , где они могут влиять на высвобождение множества нейротрансмиттеров.
Идентифицировано 17 субъединиц нАХР позвоночных, которые разделены на субъединицы мышечного и нейронального типа. Хотя субъединица/ген α8 присутствует у видов птиц, таких как курица, она не присутствует у человека или млекопитающих. [35]
Субъединицы nAChR были разделены на 4 подсемейства (I–IV) на основании сходства белковых последовательностей. [36] Кроме того, подсемейство III было разделено на 3 типа.
Нейрональные nAChR представляют собой трансмембранные белки , которые образуют пентамерные структуры , собранные из семейства субъединиц, состоящих из α 2 –α 10 и β 2 –β 4 . [37] Эти субъединицы были обнаружены с середины 1980-х по начало 1990-х годов, когда кДНК для нескольких субъединиц nAChR были клонированы из мозга крыс и кур, что привело к идентификации одиннадцати различных генов (двенадцать у кур), которые кодируют нейрональные субъединицы nAChR. ; Идентифицированные гены-субъединицы были названы α 2 –α 10 (α 8 обнаружен только у кур) и β 2 –β 4 . [38] Также было обнаружено, что различные комбинации субъединиц могут образовывать функциональные нАХР, которые могут активироваться ацетилхолином и никотином , а различные комбинации субъединиц создают подтипы нАХР с разнообразными функциональными и фармакологическими свойствами. [39] При экспрессии по отдельности α 7 , α 8 , α 9 и α 10 способны образовывать функциональные рецепторы, но другие субъединицы α требуют присутствия субъединиц β для формирования функциональных рецепторов. [37] Было обнаружено, что у млекопитающих субъединицы nAchR кодируются 17 генами, из них девять генов, кодирующих α-субъединицы, и три, кодирующие β-субъединицы, экспрессируются в мозге. nAChR, содержащие субъединицу β 2 (β 2 nAChR) и α 7 nAChR, широко экспрессируются в головном мозге, тогда как другие субъединицы nAChR имеют более ограниченную экспрессию. [40] Пентамерная сборка nAChR подвергается воздействию субъединиц, которые продуцируются в различных типах клеток, например, в легких человека, где эпителиальные и мышечные пентамеры существенно различаются. [41]
Важный кластер генов nAchR (CHRNA5/A3/B4) содержит гены, кодирующие субъединицы α 5 , α3 и β 4 . Генетические исследования выявили однонуклеотидные полиморфизмы (SNP) в хромосомном локусе, кодирующем эти три гена nAChR, как факторы риска никотиновой зависимости , рака легких , хронической обструктивной болезни легких , алкоголизма и заболеваний периферических артерий . [37] [42] Гены субъединицы nAChR CHRNA5/A3/B4 обнаружены в плотном кластере в хромосомной области 15q24–25. Субъединицы nAChR, кодируемые этим локусом, образуют преобладающие подтипы никотиновых рецепторов, экспрессируемые в периферической нервной системе (ПНС) и других ключевых участках центральной нервной системы (ЦНС) , таких как медиальная хабенула , структура между лимбической частью переднего мозга и средним мозгом, участвующая в основных процессах. пути холинергической системы. [37] Дальнейшие исследования генов CHRNA5/A3/B4 показали, что «нейрональные» гены nAChR также экспрессируются в ненейрональных клетках, где они участвуют в различных фундаментальных процессах, таких как воспаление. [43] Гены CHRNA5/A3/B4 совместно экспрессируются во многих типах клеток, а транскрипционная активность промоторных областей трех генов регулируется многими из одних и тех же факторов транскрипции, демонстрируя, что их кластеризация может отражать контроль экспрессии генов. . [37]
CHRNB3 и CHRNA6 также сгруппированы в кластер генов, расположенный на 8p11. [42] Многочисленные исследования показали, что SNPS в CHRNB3–CHRNA6 связаны с никотиновой зависимостью и курением, например, два SNP в CHRNB3, rs6474413 и rs10958726. [42] Генетические вариации в этом регионе также влияют на предрасположенность к употреблению наркотиков, включая кокаин и употребление алкоголя. [44] Никотиновые рецепторы, содержащие субъединицы α6 или β3 , экспрессируемые в областях мозга, особенно в вентральной области покрышки и черной субстанции , важны для поведения, связанного с употреблением наркотиков, из-за их роли в высвобождении дофамина . [45] Генетические вариации в этих генах могут изменять чувствительность к наркотикам различными способами, включая изменение аминокислотной структуры белка или вызывать изменения в регуляции транскрипции и трансляции. [44]
Другие хорошо изученные гены nAChR включают CHRNA4 и CHRNB2, которые ассоциированы с генами аутосомно-доминантной ночной лобной эпилепсии (ADNFLE) . [42] [46] Обе эти субъединицы nAChR присутствуют в головном мозге, и возникновение мутаций в этих двух субъединицах вызывает генерализованный тип эпилепсии. Примеры включают инсерционную мутацию CHRNA4 776ins3, которая связана с ночными судорогами и психическими расстройствами, а также мутацию CHRNB2 I312M, которая, по-видимому, вызывает не только эпилепсию, но и очень специфические когнитивные нарушения, такие как дефицит обучения и памяти. [46] [47] Между этими двумя генами существуют естественные генетические вариации, и анализ однонуклеотидных полиморфизмов (SNP) и других модификаций генов показывает более высокую изменчивость в гене CHRNA4, чем в гене CHRNB2, подразумевая, что nAChR β 2 , Белок, кодируемый CHRNB2, связан с большим количеством субъединиц, чем α 4 . Сообщалось также, что CHRNA2 является третьим кандидатом на ночные судороги в лобных долях. [42] [46]
В нескольких исследованиях сообщалось о связи между CHRNA7 и эндофенотипами психических расстройств и никотиновой зависимостью, что способствует значительной клинической значимости α7 и проводимым по нему исследованиям. [46] CHRNA7 был одним из первых генов, которые, как считалось, связаны с шизофренией . Исследования выявили несколько полиморфизмов промотора CHRNA7, которые снижают транскрипционную активность генов, что связано с шизофренией, что согласуется с обнаружением сниженных уровней a7 nAChR в мозге пациентов с шизофренией. [46] Было обнаружено , что оба подтипа nAChRs, α 4 β 2 и α 7 , значительно снижены в посмертных исследованиях людей с шизофренией. [48] Кроме того, уровень курения значительно выше среди больных шизофренией, а это означает, что курение никотина может быть формой самолечения. [49]
Никотиновые рецепторы представляют собой пентамеры этих субъединиц; т.е. каждый рецептор содержит пять субъединиц. Таким образом, существует огромный потенциал вариаций этих субъединиц, некоторые из которых встречаются чаще, чем другие. Наиболее широко выраженные подтипы включают (α 1 ) 2 β 1 δε (взрослый мышечный тип), (α 3 ) 2 (β 4 ) 3 (ганглиозный тип), (α 4 ) 2 (β 2 ) 3 (ЦНС-тип ). тип) и (α 7 ) 5 (другой тип ЦНС). [50] Далее следует сравнение:
K
заключается
в следующем; α
2
β
4
=9900 нМ [5], α
3
β
2
=14 нМ [1], α
3
β
4
=187 нМ [1], α
4
β
2
=1 нМ [4,6]. Из-за гетерогенности каналов nACh мы не отметили первичную мишень препарата для никотина, хотя сообщается, что α
4
β
2
является преобладающим подтипом с высоким сродством в мозге, который опосредует никотиновую зависимость [2-3].