Фенол (также известный как карболовая кислота , фенольная кислота или бензол ) представляет собой ароматическое органическое соединение с молекулярной формулой C 6 H 5 OH . [5] Это белое кристаллическое вещество , летучее . Молекула состоит из фенильной группы ( -C 6 H 5 ), связанной с гидроксильной группой ( -OH ). Умеренно кислый , он требует осторожного обращения, поскольку может вызвать химические ожоги . [5]
Фенол впервые был извлечен из каменноугольной смолы , но сегодня производится в больших масштабах (около 7 миллионов тонн в год) из нефтяного сырья. Это важный промышленный товар как предшественник многих материалов и полезных соединений. [8] В основном он используется для синтеза пластмасс и родственных материалов. Фенол и его химические производные необходимы для производства поликарбонатов , эпоксидных смол , взрывчатых веществ , бакелита , нейлона , моющих средств , гербицидов , таких как феноксигербициды , и многочисленных фармацевтических препаратов . [9]
Фенол представляет собой органическое соединение, хорошо растворимое в воде, около 84,2 г которого растворяется в 1000 мл (0,895 М ). Возможны гомогенные смеси фенола и воды при массовом соотношении фенола и воды ~2,6 и выше. Натриевая соль фенола, феноксид натрия , гораздо лучше растворима в воде. Это горючее твердое вещество (рейтинг NFPA = 2). При нагревании фенол выделяет легковоспламеняющиеся пары, взрывоопасные при концентрации в воздухе от 3 до 10%. Для тушения фенольных пожаров следует использовать углекислотные или сухие химические огнетушители. [5]
Фенол – слабая кислота (рН 6,6). В водном растворе в диапазоне pH ок. 8 - 12 находится в равновесии с фенолят- анионом C 6 H 5 O - (также называемым феноксидом или карболатом ): [10]

Фенол более кислый, чем алифатические спирты. Его повышенная кислотность объясняется резонансной стабилизацией фенолят - аниона. Таким образом, отрицательный заряд кислорода делокализуется на орто- и параатомах углерода через пи-систему. [11] Альтернативное объяснение включает в себя сигма-структуру, постулирующую, что доминирующим эффектом является индукция от более электроотрицательных sp 2- гибридизированных атомов углерода ; сравнительно более мощный индуктивный отвод электронной плотности, обеспечиваемый системой sp 2 по сравнению с системой sp 3 , позволяет добиться большей стабилизации оксианиона. В подтверждение второго объяснения p K a енола ацетона в воде составляет 10,9, что делает его лишь немного менее кислым, чем фенол (p K a 10,0 ). [5] Таким образом, большее количество резонансных структур, доступных для феноксида по сравнению с енолятом ацетона, по-видимому, мало способствует его стабилизации. Однако ситуация меняется при исключении эффектов сольватации.
В четыреххлористом углероде и в алкановых растворителях фенол образует водородные связи с широким спектром оснований Льюиса, таких как пиридин , диэтиловый эфир и диэтилсульфид . Сопоставлены энтальпии образования аддукта и ИК-сдвиги частоты −OH , сопровождающие образование аддукта. [12] Фенол классифицируется как жесткая кислота . [13] [14]

Фенол демонстрирует кето-еноловую таутомерию с его нестабильным кето-таутомером циклогексадиеноном, но эффект практически незначителен. Константа равновесия енолизации составляет примерно 10–13 , что означает, что только одна из каждых десяти триллионов молекул в любой момент находится в кето-форме. [15] Небольшая степень стабилизации, полученная при замене связи C=C на связь C=O, более чем компенсируется значительной дестабилизацией, возникающей в результате потери ароматичности. Таким образом, фенол существует по существу исключительно в енольной форме. [16] 4,4'-замещенный циклогексадиенон может подвергаться диенон-фенольной перегруппировке в кислых условиях и образовывать стабильный 3,4-дизамещенный фенол. [17]
Для замещенных фенолов несколько факторов могут способствовать образованию кетотаутомера: (а) дополнительные гидроксильные группы (см. резорцин ) (б) аннелирование, как при образовании нафтолов , и (в) депротонирование с образованием фенолята. [18]
Феноксиды представляют собой еноляты , стабилизированные по ароматичности . В нормальных условиях феноксид более реакционноспособен в положении кислорода, но положение кислорода является «жестким» нуклеофилом, тогда как положения альфа-углерода имеют тенденцию быть «мягкими». [19]
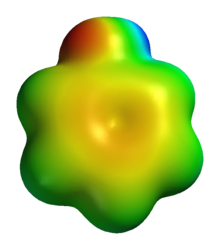
Фенол очень активен в отношении электрофильного ароматического замещения . Повышенная нуклеофильность объясняется передачей pi-электронной плотности из O в кольцо. Многие группы могут быть присоединены к кольцу посредством галогенирования , ацилирования , сульфирования и родственных процессов.
Фенол настолько сильно активируется, что бромирование и хлорирование легко приводят к полизамещению. [20] В результате реакции образуются 2- и 4-замещенные производные. Региохимия галогенирования меняется в сильнокислых растворах, где преобладает PhOH 2 ] + . Фенол реагирует с разбавленной азотной кислотой при комнатной температуре с образованием смеси 2-нитрофенола и 4-нитрофенола, тогда как с концентрированной азотной кислотой вводятся дополнительные нитрогруппы, например, с образованием 2,4,6-тринитрофенола . Алкилирование фенола и его производных по Фриделю Крафту часто протекает без катализаторов. Алкилирующие агенты включают алкилгалогениды, алкены и кетоны. Так, адамантил-1-бромид , дициклопентадиен ) и циклогексаноны дают соответственно 4-адамантилфенол, бис(2-гидроксифенил)производное и 4-циклогексилфенолы. Спирты и гидропероксиды алкилируют фенолы в присутствии твердых кислотных катализаторов (например, некоторых цеолитов ). Таким способом можно получать крезолы и кумилфенолы. [21]
Водные растворы фенола слабокислые и слегка окрашивают лакмус из синего в красный. Фенол нейтрализуется гидроксидом натрия с образованием фената или фенолята натрия, но, будучи более слабым, чем угольная кислота , он не может быть нейтрализован бикарбонатом натрия или карбонатом натрия с выделением углекислого газа .
При встряхивании смеси фенола и бензоилхлорида в присутствии разбавленного раствора гидроксида натрия образуется фенилбензоат. Это пример реакции Шоттена-Баумана :
Фенол восстанавливается до бензола при перегонке его с цинковой пылью или при пропускании его паров над гранулами цинка при 400 °С: [22]
При обработке фенола диазометаном в присутствии трифторида бора ( BF 3 ) получается анизол в качестве основного продукта и газообразный азот в качестве побочного продукта.
Фенол и его производные реагируют с хлоридом железа(III) с образованием интенсивно окрашенных растворов, содержащих феноксидные комплексы.
Из-за коммерческой важности фенола было разработано множество методов его производства, но доминирующей технологией является кумоловый процесс.

На долю 95% производства (2003 г.) приходится кумоловый процесс , также называемый процессом Хока . Он включает частичное окисление кумола (изопропилбензола) посредством перегруппировки Хока : [ 8] По сравнению с большинством других процессов, в кумоловом процессе используются мягкие условия и недорогое сырье. Чтобы процесс был экономичным, как фенол, так и побочный продукт ацетон должны быть востребованы. [23] [24] В 2010 году мировой спрос на ацетон составил около 6,7 миллионов тонн, 83 процента из которых было удовлетворено ацетоном, полученным кумоловым процессом.
Путь, аналогичный кумоловому процессу, начинается с циклогексилбензола . Он окисляется до гидропероксида , аналогично производству гидропероксида кумола . В результате перегруппировки Хока гидропероксид циклогексилбензола расщепляется с образованием фенола и циклогексанона . Циклогексанон является важным предшественником некоторых нейлонов . [25]
Прямое окисление бензола ( C 6 H 6 ) до фенола теоретически возможно и представляет большой интерес, но не получило коммерческого применения:
Закись азота является потенциально «зеленым» окислителем, который является более сильным окислителем, чем O 2 . Однако маршруты производства закиси азота остаются неконкурентоспособными. [26] [23] [25]
Электросинтез с использованием переменного тока дает фенол из бензола. [27]
Окисление толуола , разработанное Dow Chemical , включает катализируемую медью реакцию расплавленного бензоата натрия с воздухом:
Предполагается, что реакция протекает через образование бензиоилсалицилата. [8]
Автоокисление циклогексилбензола дает гидропероксид . Разложение этого гидропероксида дает циклогексанон и фенол. [8]
Ранние методы основывались на экстракции фенола из производных угля или гидролизе производных бензола.
Оригинальный коммерческий маршрут был разработан компаниями Bayer и Monsanto в начале 1900-х годов на основе открытий Вюрца и Кекуле. Метод включает реакцию сильного основания с бензолсульфоновой кислотой , протекающую по реакции гидроксида с бензолсульфонатом натрия с образованием феноксида натрия. Подкисление последнего дает фенол. Чистая конверсия равна: [28]
Хлорбензол можно гидролизовать до фенола с использованием основания ( процесс Доу ) или пара ( процесс Рашига-Хукера ): [24] [25] [29]
Недостатком этих методов является стоимость хлорбензола и необходимость утилизации побочного хлорида.
Фенол также является извлекаемым побочным продуктом пиролиза угля . [29] В процессе Ламмуса окисление толуола до бензойной кислоты проводится отдельно.

Соли фенилдиазония гидролизуются до фенола. Коммерческого интереса метод не представляет, поскольку прекурсор дорог. [30]
Салициловая кислота декарбоксилируется до фенола. [31]
Основное применение фенола, на которое приходится две трети его производства, связано с его переработкой в прекурсоры для производства пластмасс. Конденсация с ацетоном дает бисфенол-А , ключевой предшественник поликарбонатов и эпоксидных смол. Конденсация фенола, алкилфенолов или дифенолов с формальдегидом дает фенольные смолы , известным примером которых является бакелит . Частичное гидрирование фенола дает циклогексанон , [32] предшественник нейлона . Неионогенные моющие средства производятся путем алкилирования фенола с образованием алкилфенолов , например нонилфенола , которые затем подвергаются этоксилированию . [8]
Фенол также является универсальным предшественником большого количества лекарств, в первую очередь аспирина , а также многих гербицидов и фармацевтических препаратов .
Фенол является компонентом метода жидкостно-жидкостной фенол-хлороформной экстракции, используемого в молекулярной биологии для получения нуклеиновых кислот из тканей или образцов клеточных культур. В зависимости от pH раствора можно экстрагировать ДНК или РНК .
Фенол широко использовался как антисептик . Впервые его использование было предложено Джозефом Листером (см. § Раздел «История»).
С начала 1900-х по 1970-е годы его использовали при производстве карболового мыла . Концентрированные фенольные жидкости используются для постоянного лечения вросших ногтей на ногах и руках — процедура, известная как химическая матриксэктомия . Процедура была впервые описана Отто Боллом в 1945 году. С тех пор фенол стал предпочтительным химикатом для химической матричноэктомии, выполняемой ортопедами.
Концентрированный жидкий фенол можно использовать местно в качестве местного анестетика при отологических процедурах, таких как миринготомия и установка тимпанотомической трубки, в качестве альтернативы общей анестезии или другим местным анестетикам. Он также обладает кровоостанавливающими и антисептическими свойствами, что делает его идеальным для такого применения.
Феноловый спрей, обычно содержащий 1,4% фенола в качестве активного ингредиента, используется в медицине для лечения боли в горле. [33] Это активный ингредиент некоторых пероральных анальгетиков, таких как хлорасептический спрей, TCP и Carmex . [34]
Фенол настолько недорог, что его также привлекают многие мелкие применения. Входит в состав промышленных средств для снятия краски , используемых в авиационной промышленности для удаления эпоксидных, полиуретановых и других химически стойких покрытий. [35]
Из соображений безопасности фенол запрещен к использованию в косметической продукции в Европейском Союзе [36] [37] и Канаде . [38] [39]
Фенол был открыт в 1834 году Фридлибом Фердинандом Рунге , который извлек его (в нечистом виде) из каменноугольной смолы . [40] Рунге назвал фенол «Karbolsäure» (угольно-масляная кислота, карболовая кислота). Каменноугольная смола оставалась основным источником до развития нефтехимической промышленности . В 1841 году французский химик Огюст Лоран выделил фенол в чистом виде как производное бензола. [41]
В 1836 году Огюст Лоран придумал название бензола «фен»; [42] это корень слов «фенол» и « фенил ». В 1843 году французский химик Шарль Герхардт придумал название «фенол». [43]
Антисептические свойства фенола были использованы сэром Джозефом Листером (1827–1912) в его новаторской технике антисептической хирургии. Листер решил, что необходимо тщательно промыть сами раны. Затем он прикрыл раны куском тряпки или ворса [44] , покрытого карболовой кислотой (фенолом). Раздражение кожи, вызванное постоянным воздействием фенола, в конечном итоге привело к внедрению асептических (безмикробных) методов в хирургии. Работа Листера была вдохновлена работами и экспериментами его современника Луи Пастера по стерилизации различных биологических сред. Он предположил, что если микробы можно будет убить или предотвратить, заражения не произойдет. Листер предположил, что химическое вещество можно использовать для уничтожения микроорганизмов, вызывающих инфекцию. [45]
Тем временем в Карлайле, Англия, чиновники экспериментировали с очисткой сточных вод с использованием карболовой кислоты, чтобы уменьшить запах выгребных ям. Услышав об этих разработках и сам ранее без особого успеха экспериментируя с другими химическими веществами в антисептических целях, Листер решил попробовать карболовую кислоту в качестве антисептика для ран. Первый шанс у него появился 12 августа 1865 года, когда он принял пациента: одиннадцатилетнего мальчика с переломом большеберцовой кости, пронзившим кожу голени. Обычно ампутация была бы единственным решением. Однако Листер решил попробовать карболовую кислоту. Вправив кость и закрепив ногу шинами, он пропитал чистые хлопчатобумажные полотенца неразбавленной карболовой кислотой и приложил их к ране, накрыв слоем оловянной фольги, оставив на четыре дня. Осмотрев рану, Листер был приятно удивлен, не обнаружив никаких признаков инфекции, только покраснение по краям раны от легкого жжения карболовой кислотой. Повторно наложив свежие повязки с разбавленной карболовой кислотой, мальчик смог вернуться домой примерно через шесть недель лечения. [46]
К 16 марта 1867 года, когда первые результаты работы Листера были опубликованы в журнале «Ланцет», он вылечил в общей сложности одиннадцать пациентов, используя свой новый антисептический метод. Из них только один умер, и то из-за осложнения, не связанного с техникой перевязки ран Листера. Теперь впервые пациенты со сложными переломами могли покинуть больницу с целыми конечностями.
- - Ричард Холлингем, Кровь и кишки: история хирургии , с. 62 [46]
До того, как в больнице начали проводить антисептические операции, в тридцати пяти хирургических случаях было зарегистрировано шестнадцать смертей. Почти каждый второй пациент умер. После того, как летом 1865 года была введена антисептическая хирургия, в сорока случаях было всего шесть смертей. Уровень смертности снизился с почти 50 процентов до примерно 15 процентов. Это было выдающееся достижение
- - Ричард Холлингем, Кровь и кишки: история хирургии , с. 63 [47]
Фенол был основным ингредиентом Carbolic Smoke Ball , неэффективного устройства, продававшегося в Лондоне в 19 веке для защиты от гриппа и других заболеваний, а также предметом известного судебного дела « Карлилл против Carbolic Smoke Ball Company ».
Токсическое воздействие фенола на центральную нервную систему, обсуждаемое ниже, вызывает внезапный коллапс и потерю сознания как у людей, так и у животных; Этим симптомам предшествует состояние судорог из-за двигательной активности, контролируемой центральной нервной системой. [48] Инъекции фенола использовались в качестве средства индивидуальной казни в нацистской Германии во время Второй мировой войны . [49] Первоначально он использовался нацистами в 1939 году в рамках массового убийства нежелательных лиц в рамках Акции Т4 . [50] Немцы узнали, что уничтожение небольших групп было более экономичным путем инъекции каждой жертве фенола. Инъекции фенола были сделаны тысячам людей. Максимилиан Кольбе также был убит инъекцией фенола после того, как пережил две недели обезвоживания и голодания в Освенциме , когда он вызвался умереть вместо незнакомца . Примерно одного грамма достаточно, чтобы вызвать смерть. [51]
Фенол является нормальным продуктом обмена веществ, выводится в количестве до 40 мг/л с мочой человека. [48]
Секреция височных желез слонов -самцов показала присутствие фенола и 4-метилфенола во время сусла . [52] [53]
Это также одно из химических соединений, содержащихся в кастореуме . Это соединение попадает в организм из растений, которые едят бобр. [54]
Фенол является измеримым компонентом аромата и вкуса характерного шотландского виски с острова Айла , [55] обычно ~30 частей на миллион , но в солодовом ячмене, используемом для производства виски , его концентрация может превышать 160 частей на миллион . [56] Это количество отличается от количества в дистилляте и предположительно превышает его. [55]
Cryptanaerobacterphenolicus — это вид бактерий, который производит бензоат из фенола через 4-гидроксибензоат . [57] Rhodococcus Phoenix – это вид бактерий, способный разлагать фенол как единственный источник углерода. [58]
Фенол и его пары разъедают глаза, кожу и дыхательные пути. [59] Его разъедающее воздействие на кожу и слизистые оболочки обусловлено дегенеративным действием на белки. [48] Повторный или длительный контакт кожи с фенолом может вызвать дерматит или даже ожоги второй и третьей степени. [60] Вдыхание паров фенола может вызвать отек легких . [59] Вещество может оказывать вредное воздействие на центральную нервную систему и сердце, приводя к аритмии , судорогам и коме . [ 61] Также могут поражаться почки . Длительное или многократное воздействие вещества может оказать вредное воздействие на печень и почки . [62] Нет никаких доказательств того, что фенол вызывает рак у людей. [63] Помимо гидрофобных эффектов, другим механизмом токсичности фенола может быть образование феноксильных радикалов . [64]
Поскольку фенол относительно быстро всасывается через кожу, помимо местных едких ожогов может возникнуть системное отравление. [48] Резорбтивное отравление большим количеством фенола может произойти даже на небольшом участке кожи, быстро приводя к параличу центральной нервной системы и резкому падению температуры тела. ЛД 50 при пероральной токсичности составляет менее 500 мг/кг для собак, кроликов или мышей; минимальная смертельная доза для человека составляла 140 мг/кг. [48] Агентство по регистрации токсичных веществ и заболеваний (ATSDR) Министерства здравоохранения и социальных служб США утверждает, что смертельная доза при приеме внутрь фенола составляет от 1 до 32 г. [65]
Химические ожоги кожи можно обеззаразить путем промывания полиэтиленгликолем , [66] изопропиловым спиртом , [67] или, возможно, даже обильным количеством воды. [68] Необходимо снять загрязненную одежду, а также немедленно обратиться в больницу в случае крупных брызг. Это особенно важно, если фенол смешан с хлороформом (обычно используемая смесь в молекулярной биологии для очистки ДНК и РНК ). [ нужна ссылка ] Фенол также является репродуктивным токсином, вызывающим повышенный риск выкидыша и низкого веса при рождении, что указывает на задержку развития внутриутробно. [5]
Слово фенол также используется для обозначения любого соединения, которое содержит шестичленное ароматическое кольцо, непосредственно связанное с гидроксильной группой (-ОН). Таким образом, фенолы представляют собой класс органических соединений , простейшим представителем которого является фенол, обсуждаемый в этой статье.
Для C 6
H
5
-OH сохранено только одно название, фенол, как в качестве предпочтительного названия, так и для общей номенклатуры.