Вирус гриппа А подтипа H5N1 (A/H5N1) — подтип вируса гриппа А , вызывающий грипп (грипп), преимущественно у птиц. Он является энзоотическим (сохраняется в популяции) во многих популяциях птиц, а также панзоотическим (поражает животных многих видов на обширной территории). [1] Вирус A/H5N1 может также инфицировать млекопитающих (включая человека), которые контактировали с инфицированными птицами; в этих случаях симптомы часто бывают тяжелыми или фатальными. [2]
Вирус A/H5N1 выделяется со слюной, слизистой и фекалиями инфицированных птиц; другие инфицированные животные могут выделять вирусы птичьего гриппа через дыхательные выделения и другие жидкости организма (например, коровье молоко). [3] Вирус может быстро распространяться среди домашних птиц и среди диких птиц. [3] По оценкам, в попытках сдержать вирус было убито полмиллиарда птиц, выращиваемых на фермах. [2]
Симптомы гриппа A/H5N1 варьируются в зависимости как от штамма вируса, лежащего в основе инфекции, так и от вида пораженных птиц или млекопитающих. [4] [5] Классификация на низкопатогенный птичий грипп (LPAI) или высокопатогенный птичий грипп (HPAI) основана на тяжести симптомов у домашних кур и не позволяет предсказать тяжесть симптомов у других видов. [6] Куры, инфицированные вирусом LPAI A/H5N1, проявляют легкие симптомы или протекают бессимптомно , тогда как HPAI A/H5N1 вызывает серьезные затруднения дыхания, значительное снижение яйценоскости и внезапную смерть. [7]
Люди и другие млекопитающие могут заразиться только после длительного тесного контакта с зараженными птицами. [8] У млекопитающих, включая человека, грипп A/H5N1 (будь то LPAI или HPAI) встречается редко. Симптомы инфекции варьируются от легких до тяжелых, включая лихорадку, диарею и кашель. [5] С 1997 года в 23 странах были зарегистрированы случаи заражения людей вирусом A/H5N1, что привело к тяжелой пневмонии и смерти примерно в 50% случаев. [8] По состоянию на май 2024 года во всем мире было выявлено 889 случаев заболевания людей, из них 463 со смертельным исходом, что соответствует уровню летальности около 50%; [9] однако вполне вероятно, что это завышенная оценка, учитывая, что легкие инфекции могут остаться незамеченными и заниженными. [10]
Вирус гриппа A/H5N1 был впервые идентифицирован у сельскохозяйственных птиц в Южном Китае в 1996 году. [11] В период с 1996 по 2018 год A/H5N1 сосуществовал в популяциях птиц с другими подтипами вируса, но с тех пор высокопатогенный подтип HPAI A(H5N1) стал доминирующим штаммом в популяциях птиц во всем мире. [12] Некоторые штаммы A/H5N1, высокопатогенные для кур, приспособились вызывать легкие симптомы у уток и гусей, [13] [6] и способны быстро распространяться посредством миграции птиц. [14] К видам млекопитающих, у которых была зарегистрирована инфекция H5N1, относятся коровы, тюлени, козы и скунсы. [15]
Из-за высокой летальности и вирулентности вируса HPAI A(H5N1), его присутствия во всем мире, все более разнообразного резервуара -хозяина и значительных продолжающихся мутаций вирус H5N1 считается крупнейшей пандемической угрозой в мире. [16] Домашняя птица потенциально может быть защищена от определенных штаммов вируса путем вакцинации. [17] На случай серьезной вспышки гриппа H5N1 среди людей агентства здравоохранения подготовили вакцины-кандидаты, которые можно использовать для предотвращения заражения и контроля вспышки, однако для наращивания массового производства может потребоваться несколько месяцев. [3] [18] [19]
Клинические признаки H5N1 у птиц варьируются от легких (снижение яйценоскости, выделения из носа, кашель и чихание) до тяжелых, включая потерю координации, энергии и аппетита; яйца с мягкой скорлупой или деформированной формы; пурпурное изменение цвета сережек, головы, век, гребней и скакательных суставов; и диарея. Иногда первым заметным признаком является внезапная смерть. [20]
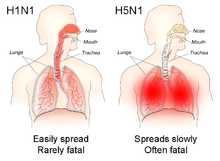
В целом, люди, заразившиеся гуманизированным вирусом гриппа А ( вирус человеческого гриппа типа А), обычно имеют такие симптомы, как лихорадка , кашель , боль в горле , мышечные боли , конъюнктивит и, в тяжелых случаях, проблемы с дыханием и пневмония , которые могут быть фатально. [20] Тяжесть инфекции во многом зависит от состояния иммунной системы инфицированных людей и от того, подвергались ли они воздействию этого штамма ранее (в этом случае они будут частично иммунны). Никто не знает, будут ли те или иные симптомы симптомами гуманизированного гриппа H5N1.
Гемагглютинин птичьего гриппа предпочитает связываться с рецепторами альфа-2,3 сиаловой кислоты , тогда как гемагглютинин гриппа человека предпочитает связываться с рецепторами альфа-2,6 сиаловой кислоты. [22] [23] Это означает, что когда штамм H5N1 заражает людей, он будет реплицироваться в нижних дыхательных путях (где у людей больше рецепторов альфа-2,3-сиаловой кислоты) и, следовательно, вызывать вирусную пневмонию . [24] [25] По состоянию на апрель 2024 года не существует адаптированной к человеку формы гриппа H5N1, поэтому все заразившиеся до сих пор люди заразились птичьим H5N1.
Сообщается о высоком уровне смертности человека от высокопатогенного птичьего гриппа H5N1; По данным ВОЗ , 60% случаев, классифицированных как H5N1, закончились смертью. Однако есть некоторые свидетельства того, что реальный уровень смертности от птичьего гриппа может быть намного ниже, поскольку может быть много людей с более легкими симптомами, которые не обращаются за лечением и не учитываются. [26] [27]
В одном случае у мальчика с H5N1 возникла диарея, за которой быстро последовала кома без развития респираторных или гриппоподобных симптомов. [28] Были проведены исследования уровней цитокинов у людей, инфицированных вирусом гриппа H5N1. Особое беспокойство вызывают повышенные уровни фактора некроза опухоли-альфа , белка, связанного с разрушением тканей в местах инфекции и увеличением продукции других цитокинов. Вызванное вирусом гриппа повышение уровня цитокинов также связано с симптомами гриппа, включая лихорадку, озноб, рвоту и головную боль. Повреждение тканей, связанное с инфекцией патогенного вируса гриппа, в конечном итоге может привести к смерти. [29] Воспалительный каскад , вызванный H5N1, некоторые называют « цитокиновым штормом » из-за того, что, по-видимому, это процесс положительной обратной связи , наносящий ущерб организму в результате стимуляции иммунной системы . H5N1 индуцирует более высокие уровни цитокинов, чем более распространенные типы вируса гриппа. [30]
Первый известный штамм ВПГП A(H5N1) (названный A/chicken/Scotland/59) убил два стада кур в Шотландии в 1959 году, но этот штамм сильно отличался от высокопатогенного штамма H5N1. Доминирующий штамм ВПГП A(H5N1) в 2004 году эволюционировал с 1999 по 2002 год, создав генотип Z. [31] Его также называют «ВПГП А(H5N1) азиатской линии».
Азиатская линия HPAI A(H5N1) разделена на две антигенные клады. «Клада 1 включает в себя изоляты людей и птиц из Вьетнама , Таиланда и Камбоджи , а также изоляты птиц из Лаоса и Малайзии . Вирусы клада 2 были впервые идентифицированы в изолятах птиц из Китая , Индонезии , Японии и Южной Кореи , а затем распространились на запад , на Ближний Восток» . Европа и Африка . По данным ВОЗ, вирусы клада 2 были главным образом ответственны за инфицирование человека вирусом H5N1 в конце 2005 и 2006 годов. Генетический анализ выявил шесть субкладов клада 2, три из которых имеют четко выраженное географическое распространение. был причастен к инфекциям человека: Карта
Исследование 2007 года, посвященное субкладу EMA, пролило дополнительный свет на мутации EMA. «Сообщенные здесь 36 новых изолятов значительно расширяют объем данных по полногеномным последовательностям, доступных для недавних изолятов птичьего гриппа (H5N1). До нашего проекта GenBank содержал только 5 других полных геномов из Европы за период 2004–2006 годов, и он содержал нет целых геномов с Ближнего Востока или Северной Африки. Наш анализ показал несколько новых результатов. Во-первых, все европейские, ближневосточные и африканские образцы попадают в кладу, отличную от других современных азиатских кладов, все из которых имеют общее происхождение. исходный штамм Гонконга 1997 года. Филогенетические деревья, построенные на каждом из 8 сегментов, демонстрируют последовательную картину трех линий, как показано на дереве HA, показанном на рисунке 1. Две клады содержат исключительно вьетнамские изоляты, насчитывающие 5; изоляты мы обозначаем V1; более крупная клада, состоящая из 9 изолятов, - это V2. Остальные 22 изолята попадают в третью, четко обособленную кладу, обозначенную EMA, которая включает образцы из Европы, Ближнего Востока и Африки. Деревья остальных семи сегментов имеют аналогичную топологию, в каждом случае клады V1, V2 и EMA четко разделены. Анализ всех доступных полных геномов гриппа (H5N1) и 589 последовательностей HA позволил отличить кладу EMA от основных клад , циркулирующих в Китайской Народной Республике, Индонезии и Юго-Восточной Азии».
Изоляты H5N1 идентифицируются следующим образом: A/chicken/Nakorn-Patom/Thailand/CU-K2/04(H5N1) :
Другие примеры включают: A/duck/Hong Kong/308/78(H5N3), A/avian/NY/01(H5N2), A/chicken/Mexico/31381-3/94(H5N2) и A/ лопатка /Египет. /03(H5N2). [36]
Как и другие вирусы птичьего гриппа, H5N1 имеет штаммы, называемые «высокопатогенными» (ВП) и «низкопатогенными» (ЛП). Вирусы птичьего гриппа, вызывающие ВПГП, очень вирулентны , а уровень смертности в инфицированных стадах часто приближается к 100%. Вирусы LPAI обладают незначительной вирулентностью, но эти вирусы могут служить предшественниками вирусов HPAI. Штамм H5N1, ответственный за гибель птиц во всем мире, является штаммом HPAI; все остальные штаммы H5N1, включая североамериканский штамм, который вообще не вызывает заболевания ни у одного вида, являются штаммами LPAI. Все штаммы HPAI, идентифицированные на сегодняшний день, относятся к подтипам H5 и H7. Различие касается патогенности у домашней птицы, а не у человека. Обычно высокопатогенный птичий вирус не является высокопатогенным ни для человека, ни для птиц, не являющихся домашними птицами. Это [ какой? ] смертельный штамм H5N1 необычен тем, что он смертелен для столь многих видов, включая некоторых, например домашних кошек, которые ранее никогда не были восприимчивы к какому-либо вирусу гриппа . [37] [ не удалось проверить ]

H5N1 является подтипом видового вируса гриппа А рода Alphainfluenzavirus семейства Orthomyxoviridae . Как и все другие подтипы гриппа А, подтип H5N1 представляет собой РНК-вирус . Он имеет сегментированный геном из восьми одноцепочечных одноцепочечных РНК , сокращенно PB2, PB1, PA, HA, NP, NA, MP и NS. [ нужна цитата ]
HA кодирует гемагглютинин , антигенный гликопротеин , обнаруженный на поверхности вирусов гриппа и отвечающий за связывание вируса с инфицированной клеткой. NA кодирует нейраминидазу , антигенный гликозилированный фермент , обнаруженный на поверхности вирусов гриппа. Это облегчает высвобождение дочерних вирусов из инфицированных клеток. [38] Нити РНК гемагглютинина (HA) и нейраминидазы (NA) определяют структуру белков, которые наиболее важны с медицинской точки зрения в качестве мишеней для противовирусных препаратов и антител . HA и NA также используются в качестве основы для наименования различных подтипов вирусов гриппа А. Вот откуда берутся H и N в H5N1 .
Низкопатогенный птичий грипп H5N1 (LPAI H5N1), также называемый «североамериканским» H5N1, обычно встречается у диких птиц. В большинстве случаев он вызывает у птиц незначительное недомогание или отсутствие заметных признаков заболевания. Неизвестно, как оно вообще влияет на людей. Единственное беспокойство по этому поводу заключается в том, что он может передаться домашней птице и у птицы мутировать в высокопатогенный штамм. [ нужна цитата ]
«Раньше не требовалось сообщать или отслеживать обнаружение LPAI H5 или H7 у диких птиц, поэтому штаты и университеты тестировали образцы диких птиц независимо от Министерства сельского хозяйства США. По этой причине приведенный выше список предыдущих обнаружений не может включать все предыдущие обнаружения. Обнаружения LPAI H5N1 Однако Всемирная организация здравоохранения животных ( МЭБ ) недавно изменила свои требования о сообщении об обнаружении птичьего гриппа. С 2006 года обо всех подтвержденных подтипах AI LPAI H5 и H7 необходимо сообщать в МЭБ из-за их потенциальной мутации. в высокопатогенные штаммы, поэтому Министерство сельского хозяйства США теперь отслеживает эти обнаружения у диких птиц, приусадебных стадах, коммерческих стадах и на рынках живых птиц». [42]
Вирусы гриппа имеют относительно высокую скорость мутаций, характерную для РНК-вирусов . Сегментация его генома облегчает генетическую рекомбинацию путем рекомбинации сегментов у хозяев, инфицированных двумя разными штаммами вирусов гриппа одновременно. [43] [44] Ранее незаразный штамм может затем передаваться между людьми, что является одним из нескольких возможных путей к пандемии. [ нужна цитата ]
Способность различных штаммов гриппа проявлять видовую избирательность во многом обусловлена вариациями генов гемагглютинина . Генетические мутации в гене гемагглютинина, вызывающие замены отдельных аминокислот, могут существенно изменить способность белков вирусного гемагглютинина связываться с рецепторами на поверхности клеток-хозяев. Такие мутации в птичьих вирусах H5N1 могут превратить штаммы вируса из неэффективных для заражения клеток человека в столь же эффективные в вызывании инфекций у человека, как и более распространенные типы вируса человеческого гриппа. [45] Это не означает, что одна аминокислотная замена может вызвать пандемию, но это означает, что одна аминокислотная замена может привести к тому, что вирус птичьего гриппа, который не является патогенным для человека, станет патогенным для человека. [ нужна цитата ]
Вирус гриппа А подтипа H3N2 эндемичен для свиней в Китае и был обнаружен у свиней во Вьетнаме, что усиливает опасения по поводу появления новых вариантов штаммов. Доминирующим штаммом ежегодного вируса гриппа в январе 2006 года был H3N2 , который в настоящее время устойчив к стандартным противовирусным препаратам амантадину и римантадину . Возможность обмена генами H5N1 и H3N2 посредством рекомбинации вызывает серьезную озабоченность. Если произойдет рекомбинация H5N1, он может остаться подтипом H5N1 или может сменить подтип, как это произошло с H2N2 , когда он превратился в штамм гонконгского гриппа H3N2 .
Пандемические штаммы H2N2 и H3N2 содержали сегменты РНК вируса птичьего гриппа . «Хотя пандемические вирусы человеческого гриппа 1957 (H2N2) и 1968 (H3N2) явно возникли в результате реассортации между человеческими и птичьими вирусами, вирус гриппа, вызвавший «испанку» в 1918 году, по-видимому, полностью произошел из птичьего источника». [46]
Существует несколько вакцин против H5N1 для нескольких разновидностей птичьего H5N1, но постоянная мутация H5N1 делает их применение ограниченным на сегодняшний день: хотя вакцины иногда могут обеспечить перекрестную защиту от родственных штаммов гриппа, лучшей защитой будет вакцина, специально произведенная для любого будущего пандемического штамма вируса гриппа. Дэниел Р. Люси , содиректор аспирантуры по биологически опасным угрозам и возникающим заболеваниям в Джорджтаунском университете, отметил: « Пандемия H5N1 не существует , поэтому не может быть никакой пандемической вакцины ». [47] Однако были созданы «предпандемические вакцины»; дорабатываются и тестируются; и у них есть некоторые надежды как на дальнейшее исследование, так и на обеспечение готовности к следующей пандемии. [48] [49] [50] Компаниям-производителям вакцин рекомендуется наращивать мощности, чтобы в случае необходимости пандемической вакцины были доступны мощности для быстрого производства больших количеств вакцины, специфичной для нового пандемического штамма.
« Соединенные Штаты тесно сотрудничают с восемью международными организациями, включая Всемирную организацию здравоохранения (ВОЗ), Продовольственную и сельскохозяйственную организацию Объединенных Наций (ФАО), Всемирную организацию по охране здоровья животных (МЭБ) и 88 иностранных правительств, чтобы решить проблему ситуации посредством планирования, усиления мониторинга и полной прозрачности в отчетности и расследовании случаев птичьего гриппа. Соединенные Штаты и эти международные партнеры возглавили глобальные усилия, направленные на то, чтобы побудить страны усилить эпиднадзор за вспышками среди домашней птицы и значительным количеством смертей среди перелетных птиц. быстро ввести меры сдерживания. Агентство США по международному развитию (USAID) и Государственный департамент США , Министерство здравоохранения и социальных служб США (HHS) и Министерство сельского хозяйства (USDA) координируют будущие международные меры реагирования от имени Белого дома. с департаментами и агентствами федерального правительства». [51]
Совместно предпринимаются шаги для «минимизации риска дальнейшего распространения среди популяций животных», «снижения риска заражения людей» и «дальнейшей поддержки планирования и готовности к пандемии». [51]
Национальный центр здоровья дикой природы Геологической службы США, Центры по контролю и профилактике заболеваний , Всемирная организация здравоохранения , Европейская комиссия и другие проводят постоянный детальный и взаимно скоординированный надзор и анализ вспышек птичьего гриппа H5N1 среди людей и животных, о чем сообщают Национальный центр здоровья дикой природы Геологической службы США . [52]
Высокоэффективного лечения гриппа H5N1 не существует, но осельтамивир (коммерчески продаваемый компанией «Рош» под названием «Тамифлю») иногда может препятствовать распространению вируса гриппа внутри организма пользователя. Этот препарат стал предметом внимания некоторых правительств и организаций, пытающихся подготовиться к возможной пандемии H5N1. [53] 20 апреля 2006 г. компания Roche AG объявила, что в распоряжении Всемирной организации здравоохранения находятся три миллиона курсов лечения Тамифлю для использования в случае пандемии гриппа; Отдельно компания Roche пожертвовала ВОЗ два миллиона курсов лечения для использования в развивающихся странах , которые могут пострадать от такой пандемии, но не имеют возможности закупать большие количества препарата. [54]
Однако эксперт ВОЗ Хасан аль-Бушра сказал:
Исследования на животных и лабораторные исследования показывают, что Реленза ( занамивир ), который относится к тому же классу препаратов, что и Тамифлю, также может быть эффективен против H5N1. В исследовании, проведенном на мышах в 2000 году, «была показана эффективность занамивира при лечении вирусов птичьего гриппа H9N2, H6N1 и H5N1, передающихся млекопитающим». [56] Кроме того, исследования на мышах показывают, что комбинация занамивира, целекоксиба и месалазина выглядит многообещающе, обеспечивая 50% выживаемость по сравнению с отсутствием выживаемости в группе плацебо. [57] Хотя никто не знает, будет ли занамивир полезен или нет при еще существующем пандемическом штамме H5N1, было бы полезно запастись занамивиром, а также осельтамивиром на случай пандемии гриппа H5N1. Ни осельтамивир, ни занамивир не могут производиться в количествах, которые были бы значимы, как только начнется эффективная передача вируса человеку. [58] В сентябре 2006 года ученый ВОЗ объявил, что исследования подтвердили случаи штаммов H5N1, устойчивых к Тамифлю и Амантадину. [59] В ЕС также появились штаммы, устойчивые к Тамифлю , которые остаются чувствительными к Релензе. [60] [61]
Самые ранние случаи заражения людей вирусом H5N1 совпали с эпизоотией (эпидемией среди животных) гриппа H5N1 среди домашней птицы Гонконга в 1997 году. Эта панзоотическая вспышка (болезнь, поражающая животных многих видов, особенно на обширной территории) была остановлена благодаря убой всего поголовья домашней птицы на территории. Однако болезнь продолжала распространяться; вспышки снова были зарегистрированы в Азии в 2003 году. 21 декабря 2009 года ВОЗ объявила в общей сложности о 447 случаях, в результате которых 263 человека умерли. [20] [62]

H5N1 легко передается между птицами, что способствует потенциальному глобальному распространению H5N1 . Хотя H5N1 претерпевает мутации и реассортацию, создавая вариации, которые могут заражать виды, о которых ранее не было известно, что они являются носителями вируса, не все из этих вариантов форм могут заразить человека. H5N1 как птичий вирус преимущественно связывается с типом рецепторов галактозы , которые заселяют дыхательные пути птиц от носа до легких и практически отсутствуют у людей, обнаруживаясь только в альвеолах и вокруг них, структурах глубоко в легких, где кислород передается к кровь. Поэтому вирус нелегко вывести при кашле и чихании — обычных путях передачи. [23] [24] [63]
H5N1 в основном передается домашней птицей как при перемещении зараженных птиц и продуктов птицеводства, так и при использовании зараженного птичьего помета в качестве удобрения или корма. Люди с H5N1 обычно заразились от кур, которые, в свою очередь, были заражены другой домашней или водоплавающей птицей. Мигрирующие водоплавающие птицы (дикие утки , гуси и лебеди ) являются переносчиками H5N1, часто не заболевая. [64] [65] Многие виды птиц и млекопитающих могут быть инфицированы ВПГП A(H5N1), но роль других животных, кроме домашних и водоплавающих птиц, в качестве хозяев-распространителей заболевания неизвестна. [66]
Согласно отчету Всемирной организации здравоохранения , H5N1 может распространяться косвенным путем. В отчете говорится, что вирус иногда может прилипать к поверхностям или подниматься с пылью удобрений и заражать людей. [67]
H5N1 мутировал в множество штаммов с разными патогенными профилями: некоторые патогенны для одного вида, но не для других, некоторые патогенны для нескольких видов. Каждая конкретная известная генетическая вариация связана с изолятом вируса конкретного случая инфекции. В результате антигенного дрейфа H5N1 мутировал в десятки высокопатогенных разновидностей, разделенных на генетические клады, которые известны по конкретным изолятам, но все они принадлежат к генотипу Z вируса птичьего гриппа H5N1, который в настоящее время является доминирующим генотипом. [44] [43] Изоляты H5N1, обнаруженные в Гонконге в 1997 и 2001 годах, не всегда эффективно передавались среди птиц и не вызывали серьезных заболеваний у этих животных. В 2002 году в популяции птиц Гонконга появились новые изоляты H5N1. Эти новые изоляты вызвали острое заболевание, включая тяжелую неврологическую дисфункцию и смерть уток . Это был первый зарегистрированный случай летального заражения вирусом гриппа у диких водоплавающих птиц с 1961 года. [68]
Генотип Z появился в 2002 году в результате рекомбинации более ранних высокопатогенных генотипов H5N1 [69] , которые впервые заразили птиц в Китае в 1996 году и впервые заразили людей в Гонконге в 1997 году. [43] [44] [70] Генотип Z является эндемичным для птиц в Юго-Восточной Азии, создал по крайней мере две клады, которые могут заразить человека, и распространяется по всему миру в популяциях птиц. Мутации, происходящие внутри этого генотипа, повышают их патогенность. [71] Птицы также способны выделять вирус в течение более длительных периодов времени до своей смерти, что увеличивает заразность вируса.

Инфицированные птицы передают H5N1 через слюну , носовые выделения , фекалии и кровь . Другие животные могут заразиться вирусом при прямом контакте с этими биологическими жидкостями или при контакте с зараженными ими поверхностями. H5N1 остается заразным после более чем 30 дней при 0 °C (32 °F) (более одного месяца при минусовой температуре) или 6 дней при 37 °C (99 °F) (одна неделя при температуре человеческого тела); при обычных температурах он сохраняется в окружающей среде неделями. При арктических температурах он вообще не разлагается.
Поскольку перелетные птицы относятся к числу переносчиков высокопатогенного вируса H5N1, он распространяется во всех частях света. H5N1 отличается от всех ранее известных высокопатогенных вирусов птичьего гриппа способностью передаваться животными, кроме домашней птицы.
В октябре 2004 года исследователи обнаружили, что H5N1 гораздо более опасен, чем считалось ранее. Было обнаружено, что водоплавающие птицы непосредственно передают этот высокопатогенный штамм курам , воронам , голубям и другим птицам, а также способность вируса увеличивать свою способность заражать млекопитающих. С этого момента эксперты по птичьему гриппу все чаще стали называть сдерживание стратегией, которая может отсрочить, но не предотвратить в конечном итоге будущую пандемию птичьего гриппа.
«Начиная с 1997 года исследования гриппа А (H5N1) показывают, что эти вирусы продолжают развиваться, с изменениями антигенности и внутренних генных констелляций; расширением круга хозяев среди видов птиц и способностью заражать кошачьих; повышением патогенности у экспериментально инфицированных мышей и хорьков. , при которых они вызывают системные инфекции и повышают экологическую стабильность». [72]
Газета New York Times в статье о передаче H5N1 через контрабандных птиц сообщает Уэйду Хагемейеру из Wetlands International, заявляя: «Мы считаем, что вирус распространяется как в результате миграции птиц, так и в результате торговли, но эта торговля, особенно незаконная, более важна». [73]
29 сентября 2007 г. исследователи сообщили, что вирус птичьего гриппа H5N1 также может проходить через плаценту беременной женщины и заражать плод. Они также нашли доказательства того, о чем давно подозревали врачи: вирус не только поражает легкие, но и проникает по всему организму в желудочно-кишечный тракт, мозг, печень и клетки крови. [74]
В мае 2013 года Северная Корея подтвердила вспышку птичьего гриппа H5N1, которая вынудила власти убить более 160 000 уток в Пхеньяне . [75]
Крупная вспышка нового штамма H5N1 среди диких птиц и домашней птицы возникла в России в августе 2020 года и к октябрю быстро распространилась на другие части Европы. [77]
Зимой 2021 и 2022 годов птичий грипп распространился среди популяции белощеких казарок в Солуэй-Ферт, Великобритания, при этом, по оценкам, погибло до трети популяции Шпицбергена; [78] [79] Там также пострадали розовоногие гуси, и, похоже, вирус перенесся в новые места на севере Шотландии. Болезнь была подтверждена у сэндвич-крачек в Южной Африке в апреле 2022 года. [80] В конце весны 2022 года вспышки птичьего гриппа затронули многие виды диких птиц в Соединенном Королевстве, при этом были зарегистрированы тяжелые потери среди морских птиц, возвращающихся для размножения в колониях на Северных островах. и Внешние Гебриды, [81] включая больших поморников (бонкси), вспышки которых первоначально были зарегистрированы в 2021 году [82] (в Шотландии проживает около 60% мировой гнездящейся популяции) – перепись 2022 года на Сент-Килде показала снижение на 64%. в 2019 году зарегистрировано 106 погибших птиц (по состоянию на 6 июня), [83] олуши (более 1000 птиц зарегистрированы как погибшие только в колонии Херманесс на Шетландских островах , [81] где насчитывается около 26 000 гнездящихся пар), и гораздо больше олуш сообщалось о погибших в других колониях ( Труп-Хед , Басс-Рок и Сент-Килда ); [84] Ассортимент видов также, по-видимому, расширяется: сообщается о многих видах диких, морских птиц (гагарки, крачки и чайки) и видах-падальщиках (врановые и хищные птицы). [85] [86]
В других странах Европы вирус убил сотни (574+) кудрявых пеликанов в Греции, [87] [88] , а в Израиле около 6000 обыкновенных журавлей были найдены мертвыми в Хуле в декабре 2021 года. [89] Отчет Научной целевой группы по птичьим птицам. Грипп и дикие птицы: «Высокопатогенный птичий грипп H5N1 у домашних и диких птиц: зима 2021/2022 г. с акцентом на массовую смертность диких птиц в Великобритании и Израиле» подводит итог ситуации по состоянию на 24 января 2022 г. и упоминает, что «H5N8 HPAI по-прежнему является причиной случаев заболевания домашней птицы и диких птиц, главным образом в Азии, H5N1 в настоящее время фактически заменил этот подтип в Африке и Евразии как у домашних, так и у диких птиц». [90]
Сезон 2022–2023 годов также стал самой сильной зарегистрированной вспышкой в Соединенном Королевстве: британское правительство потребовало так называемого «изоляции домашней птицы», которая требовала, чтобы фермеры держали своих птиц в помещении. [91] Между тем, вспышка H5N1 на испанской норковой ферме заставила исследователей поверить в то, что они наблюдали первый случай передачи H5N1 от млекопитающего к млекопитающим. [92] Случаи заболевания людей были зарегистрированы в Испании в ноябре 2022 г. и в Великобритании в мае 2023 г. [77]
К ноябрю 2020 года крупные вспышки нового штамма H5N1 начали распространяться среди диких и сельскохозяйственных птиц по всей Азии. В феврале 2023 года случаи заболевания людей были зарегистрированы в Камбодже. [77]
Крупные потери домашней и дикой птицы из-за вируса H5N1 начались в Африке в ноябре 2021 года и продолжались до 2022 года. [77]
Как и в отчетах 2021 года, вспышки были отмечены в колониях олушей в Канаде: в июне 2022 года погибли тысячи птиц [93] , а также обыкновенные гаги и большие чайки . [94] До этого поступали сообщения о распространении среди диких птиц в более чем 30 штатах США, в том числе о большой смертности в колонии двугребневых бакланов в Баррингтоне, штат Иллинойс , [95] [96] вирус также распространялся среди падальщиков, в том числе три белоголовых орлана в Грузии. [97] Массовая гибель как птиц, так и млекопитающих была отмечена в Перу в сезоне 2022–2023 гг. [98] В частности, правительство Перу сообщило о гибели примерно 63 000 птиц, а также 716 морских львов , при этом ВОЗ отметила, что за распространением инфекции среди млекопитающих необходимо «пристально следить». [91] [99] В Соединенных Штатах птичья вспышка в 2022–2023 годах была самой серьезной с момента первого обнаружения вируса H5N1. [91]
Эквадор ввел трехмесячную «чрезвычайную ситуацию в области здоровья животных» 29 ноября 2022 года, всего через несколько дней после того, как был зарегистрирован первый случай заболевания, тогда как Аргентина и Уругвай объявили «национальную санитарную чрезвычайную ситуацию» 15 февраля 2023 года, после того как у них были обнаружены первые случаи заболевания. . [100] 22 мая 2023 года Бразилия, крупнейший в мире экспортер куриного мяса, объявила 180-дневную чрезвычайную ситуацию после нескольких случаев, выявленных у диких птиц, и создала центр экстренных операций для планирования и смягчения потенциального дальнейшего распространения H5N1. [101] Случаи заболевания людей были зарегистрированы в Эквадоре и Чили. [77]
В марте 2024 года инфекция H5N1 впервые была зафиксирована у павшего и больного скота, находящегося на территории США. Козы и коровы в трех штатах заболели после контакта с дикими птицами и убитой домашней птицей. [102] В начале апреля сообщалось, что вирус H5N1 распространился среди стад молочных коров во многих штатах США, что указывает на передачу вируса от коровы к корове. Работник молочной фермы в Техасе также заразился, основным симптомом которого был конъюнктивит . [103]
H5N1 впервые был обнаружен у погибших птиц на материковой части Антарктики в феврале 2024 г. [104]
В декабре 2023 года представители охраны природы подтвердили, что белый медведь умер от H5N1 недалеко от самого северного города Аляски, Уткиагвика . [105]
В мае 2024 года вирус H5N1 был впервые обнаружен в Австралии после того, как у ребенка, вернувшегося в страну из Индии, был обнаружен положительный результат. Ребенок перенес тяжелую инфекцию, но выздоровел. [106]
Новые заразные штаммы H5N1 были созданы Роном Фушье из Медицинского центра Эразмус в Роттердаме, Нидерланды, который впервые представил свою работу публике на конференции по гриппу на Мальте в сентябре 2011 года. В геном вируса H5N1 были внесены три мутации: Затем вирус передавался из носов инфицированных хорьков в носы неинфицированных, что повторялось 10 раз. [107] После этих 10 пассажей вирус H5N1 приобрел способность передаваться между хорьками аэрозольным или воздушно-капельным путем.
После того, как Фушье предложил статью с описанием этой работы ведущему академическому журналу Science , Национальный научный консультативный совет США по биобезопасности (NSABB) рекомендовал не публиковать полные подробности исследования, а также статью, представленную в журнал Nature Ёсихиро Каваока из Университета Висконсин, описывающий соответствующую работу. Однако после дополнительных консультаций во Всемирной организации здравоохранения и NSABB NSABB изменил свою позицию и рекомендовал опубликовать исправленные версии двух документов. [108] Однако затем правительство Нидерландов заявило, что этот тип рукописей требует от Фушье подачи заявления на получение разрешения на экспорт в свете директивы ЕС 428/2009 о товарах двойного назначения. [примечание 1] После долгих разногласий вокруг публикации своего исследования Фушье подчинился (под официальным протестом) требованиям правительства Нидерландов о получении специального разрешения [109] на подачу своей рукописи, и его исследование появилось в специальном выпуске журнала Science. посвященный H5N1. [110] [111] [112] В статьях Фушье и Каваока делается вывод о том, что вполне возможно, что естественная цепочка мутаций может привести к тому, что вирус H5N1 приобретет способность передаваться воздушно-капельным путем между млекопитающими, и что пандемия гриппа H5N1 не произойдет. быть невозможным. [113]
В мае 2013 года сообщалось, что ученые из Харбинского ветеринарного научно-исследовательского института в Харбине , Китай, создали штаммы H5N1, которые передавались между морскими свинками . [114]
В ответ на работу Фушье и Каваоки ряд ученых выразили обеспокоенность по поводу рисков создания новых потенциальных пандемических патогенов, кульминацией чего стало создание Кембриджской рабочей группы - консенсусного заявления, призывающего к оценке рисков и преимуществ таких исследований. [115] [116]
Хотя в прошлом млекопитающие, включая людей, заражались штаммами птичьего гриппа H5N1, эти случаи якобы были вызваны прямым контактом с инфицированными птицами, например, в результате потребления птиц дикими животными или контакта с инфицированной домашней птицей фермерами. Напротив, вспышка H5N1 среди млекопитающих в октябре 2022 года на испанской норковой ферме стала первым зарегистрированным случаем передачи инфекции от млекопитающего к млекопитающим: 4 процента популяции норок на ферме умерли от геморрагической пневмонии, связанной с H5N1. [92] [117] Дыхательные пути норки особенно хорошо подходят в качестве пути передачи вируса человеку, что обеспокоило специалистов общественного здравоохранения в связи с тем, что для производства всех одобренных вакцин для человека, кроме одной, требуются куриные яйца, которые H5N1 убивает с вероятностью 90–100 процентов смертности. [118] Также было обнаружено, что у инфицированных норок в Испании наблюдалась вирусная мутация «PB2», обнаруженная при попадании вируса H5N1 к свиньям более десяти лет назад, что усиливает опасения, что фермы могут действовать как инкубаторы и/или резервуары вируса, подобно роль норок в SARS-CoV-2 . [92]
По состоянию на январь 2023 года пятнадцать видов диких и содержащихся в неволе млекопитающих заразились H5N1 на всей территории Соединенных Штатов. [119] Массовая гибель каспийского тюленя в декабре 2022 года, когда 700 зараженных тюленей были обнаружены мертвыми вдоль побережья Каспийского моря в российской республике Дагестан , обеспокоила исследователей возможностью начала распространения инфекции от диких млекопитающих к млекопитающим. [120] Аналогичная массовая гибель 95% детенышей южного морского слона в 2023 году также вызвала обеспокоенность по поводу распространения заболевания от млекопитающих к млекопитающим, поскольку кормящие детеныши меньше подвергались воздействию птиц. [121]
В апреле 2024 года распространение вируса H5N1 среди стад молочных коров в девяти штатах США убедительно свидетельствовало о наличии передачи вируса от коровы к корове. [122] Хотя смертность крупного рогатого скота, инфицированного H5N1, редка, обильное выделение вируса в молоко очевидно. Около 50% кошек, которые жили на пострадавших молочных фермах и кормились непастеризованным молоком от коров с симптомами заболевания, умерли в течение нескольких дней от тяжелой системной инфекции гриппа, что вызывает серьезную обеспокоенность по поводу межвидовой передачи вируса от млекопитающих к млекопитающим. [123]
По состоянию на апрель 2024 года ВОЗ сообщила в общей сложности о 889 подтвержденных случаях заболевания людей, в результате которых с 2003 года умерло 463 человека. [124]
После смерти от H5N1 в феврале 2023 года 11-летней девочки из камбоджийской провинции Прейвэнг у ее отца был подтвержден положительный результат на вирус, и у нескольких близких контактов также начали проявляться признаки инфекции. 24 февраля 2023 года ВОЗ выразила обеспокоенность тем, что вирус потенциально начал распространяться среди людей, и распорядилась о производстве новой человеческой вакцины против H5N1. [125] После подтвержденных случаев заражения ВОЗ начала работать с правительством Камбоджи, чтобы определить, заразились ли оба человека вирусом непосредственно от зараженной домашней птицы или это действительно был случай передачи вируса от человека к человеку. [126] Дальнейшее секвенирование показало, что по крайней мере один из двух случаев был из более старой клады H5N1, 2.3.2.1c, которая циркулировала как обычный штамм H5N1 в Камбодже в течение многих лет, а не из более поздней клады 2.3.4.4b. , что стало причиной массовой гибели домашней птицы с 2020 года. Эта старая клада в прошлом перешла к людям, но ранее не приводила к какой-либо известной передаче вируса от человека к человеку. [127]
1 марта 2023 года, когда Тайвань объявил предупреждение о поездках в Камбоджу, ВОЗ и Центр по контролю и профилактике заболеваний США совместно с властями Камбоджи установили, что оба человека заразились в результате прямого контакта с домашней птицей. [128] [129]
H5N1 оказал значительное влияние на человеческое общество , особенно на финансовую , политическую , социальную и личную реакцию как на фактическую, так и на прогнозируемую смертность птиц , людей и других животных . Миллиарды долларов собираются и тратятся на исследование H5N1 и подготовку к потенциальной пандемии птичьего гриппа . В попытках сдержать H5N1 было потрачено более 10 миллиардов долларов и убито более 200 миллионов птиц. [130] [131] [132] [133] [134] [135] [136] [137] [138]
Люди отреагировали на это тем, что стали покупать меньше курицы, что привело к падению продаж и цен на птицу. [139] Многие люди накопили запасы на случай возможной пандемии гриппа. Международные представители здравоохранения и другие эксперты отмечают, что вокруг этой болезни все еще остается много неясных вопросов. [140]
Доктор Дэвид Набарро , главный координатор ООН по птичьему гриппу и бывший руководитель отдела кризисного реагирования Всемирной организации здравоохранения, описал себя как «весьма напуганного» потенциальным воздействием H5N1 на людей. Набарро и раньше обвиняли в паникёрстве, и в свой первый день в должности в ООН он заявил, что птичий грипп может убить 150 миллионов человек. В интервью International Herald Tribune Набарро сравнил птичий грипп со СПИДом в Африке, предупредив, что недооценка привела к неправильному сосредоточению внимания на исследованиях и вмешательствах. [141]
HA вируса гриппа связывается с альфа-2–3-связанными (птичьи вирусы) или альфа-2-6-связанными (человеческие вирусы) сиаловыми кислотами, представленными белками или липидами на поверхности клетки-хозяина.
Патофизиология птичьего гриппа отличается от патофизиологии обычного гриппа. Птичий грипп по-прежнему является преимущественно респираторной инфекцией, но поражает больше нижних дыхательных путей, чем обычно человеческий грипп. Вероятно, это связано с различиями в белке гемагглютинина и типах остатков сиаловой кислоты, с которыми этот белок связывается. Птичьи вирусы, как правило, предпочитают сиаловую кислоту альфа(2-3)галактозу, которая у человека обнаруживается в терминальных бронхах и альвеолах. И наоборот, человеческие вирусы предпочитают сиаловую кислоту альфа(2-6)галактозу, которая обнаруживается на эпителиальных клетках верхних дыхательных путей.
{{cite journal}}: CS1 maint: unfit URL (link)Научно-исследовательский институт проблем биологической безопасности (НИИБББ), Жамбылская область, Республика Казахстан