Neisseria gonorrhoeae , также известный как гонококк (единственное число) или гонококки (множественное число), представляет собой разновидность грамотрицательных бактерий диплококков , выделенных Альбертом Нейссером в 1879 году. [3] Он вызывает гонорею , передаваемую половым путем, мочеполовую инфекцию [4] , а также другие формы гонококковой инфекции, включая диссеминированную гонококцемию, септический артрит и гонококковую офтальмию новорожденных.
Он оксидазоположителен и аэробен, выживает при фагоцитозе и растет внутри нейтрофилов . [4] Для его культивирования требуется добавление углекислого газа и обогащенный агар ( шоколадный агар ) различными антибиотиками ( Тэйер-Мартин ). Он демонстрирует антигенные вариации за счет генетической рекомбинации пилей и поверхностных белков, которые взаимодействуют с иммунной системой . [3]
Половой путь передачи – вагинальный, анальный или оральный секс. [5] Передачу половым путем можно предотвратить с помощью барьерной защиты. [6] Перинатальная передача инфекции может произойти во время родов и может быть предотвращена лечением матери антибиотиками до рождения и нанесением глазного геля с антибиотиком на глаза новорожденного. [6] После эпизода гонококковой инфекции у инфицированных людей не развивается иммунитет к будущим инфекциям. Повторное заражение возможно из-за способности N. gonorrhoeae уклоняться от иммунной системы путем изменения ее поверхностных белков. [7]
N. gonorrhoeae может вызывать инфекцию половых органов, горла и глаз. [8] Бессимптомное течение инфекции часто встречается у мужчин и женщин. [6] [9] При отсутствии лечения инфекция может распространиться на остальные части тела (диссеминированная гонорейная инфекция), особенно на суставы (септический артрит). Невылеченная инфекция у женщин может вызвать воспалительные заболевания органов малого таза и возможное бесплодие из-за образующихся рубцов. [8] Диагноз ставится с помощью посева , окраски по Граму или тестов на нуклеиновые кислоты , таких как полимеразная цепная реакция , образца мочи, мазка из уретры или мазка из шейки матки. [10] [11] Совместное тестирование на хламидиоз и другие ИППП рекомендуется из-за высоких показателей коинфекции. [12]
Устойчивость N. gonorrhoeae к антибиотикам является растущей проблемой общественного здравоохранения, особенно с учетом склонности к легкому развитию резистентности. [13]

Виды Neisseria — это требовательные грамотрицательные кокки, которым для роста в лабораторных культурах требуются добавки питательных веществ. Они факультативно внутриклеточные и обычно появляются парами (диплококки), напоминающие по форме кофейные зерна. Представители этого рода не образуют спор, способны передвигаться с помощью подергивающейся моторики и являются облигатными аэробами (для роста необходим кислород). Из этих 11 видов, населяющих человека, только два являются патогенами. N. gonorrhoeae является возбудителем гонореи , а N. meningitidis является одной из причин бактериального менингита. [14]
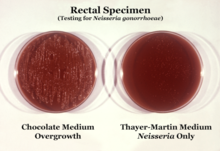

N. gonorrhoeae обычно выделяют на агаре Тайера-Мартина (или VPN) в атмосфере, обогащенной 3-7% углекислого газа. [10] Агар Тайера-Мартина представляет собой пластинку с шоколадным агаром (нагретый кровяной агар), содержащую питательные вещества и противомикробные препараты ( ванкомицин , колистин , нистатин и триметоприм ). Этот препарат агара способствует росту видов Neisseria , одновременно подавляя рост загрязняющих бактерий и грибов. Агар Мартина Льюиса и агар Нью-Йорка — это другие типы селективного шоколадного агара, обычно используемые для роста нейссерий . [10] N. gonorrhoeae является оксидазо- положительным (обладает цитохром-с-оксидазой) и каталазо -положительным (способен превращать перекись водорода в кислород). [10] При инкубации с углеводами лактозой, мальтозой , сахарозой и глюкозой N. gonorrhoeae окисляет только глюкозу. [10]
На своей поверхности N. gonorrhoeae несет волосоподобные пили , поверхностные белки с различными функциями и сахара, называемые липоолигосахаридами . Пили опосредуют прикрепление, движение и обмен ДНК. Белки Opa взаимодействуют с иммунной системой, как и порины . Липоолигосахарид (ЛОС) представляет собой эндотоксин , вызывающий иммунный ответ. Все они антигенны и все демонстрируют антигенные вариации (см. ниже). Пили демонстрируют наибольшее разнообразие. Пили, белки Opa, порины и даже LOS обладают механизмами ингибирования иммунного ответа, что делает возможным бессимптомное течение инфекции. [15]
Динамические полимерные белковые нити, называемые пилями IV типа, позволяют N. gonorrhoeae прикрепляться к поверхностям и перемещаться по ним. Для проникновения в хозяина бактерии используют пили, чтобы прикрепиться к поверхности слизистой оболочки и проникнуть в нее. [4] Пили являются необходимым фактором вирулентности для N. gonorrhoeae ; без них бактерия не способна вызвать инфекцию. [8] Для перемещения отдельные бактерии используют свои пили как крюк: сначала они отрываются от поверхности клетки и прикрепляются к субстрату . Последующая ретракция пилуса тянет клетку вперед. Возникающее в результате движение называется подергиванием моторики. [16] N. gonorrhoeae способен тянуть вес, в 100 000 раз превышающий его собственный, а пили, используемые для этого, являются одними из самых сильных биологических двигателей, известных на сегодняшний день, с усилием в один наноньютон . [17] Белки АТФазы PilF и PilT отвечают за выдвижение и втягивание пилуса IV типа соответственно. [18] [19] Адгезивные функции гонококковых ворсинок играют роль в агрегации микроколоний и образовании биопленок . [20] Поверхностные белки, называемые белками Opa, могут использоваться для связывания с рецепторами иммунных клеток и предотвращения иммунного ответа. Известно по меньшей мере 12 белков Opa, а многочисленные перестановки поверхностных белков затрудняют распознавание N. gonorrhoeae и обеспечение защиты иммунных клеток. [21]
Липоолигосахарид (LOS) представляет собой облегченную версию липополисахарида, присутствующую на поверхности большинства других грамотрицательных бактерий. Это боковая цепь сахара (сахарида), прикрепленная к липиду А (таким образом, «липо-») во внешней мембране, покрывающей клеточную стенку бактерий. Корень «олиго» относится к тому факту, что он на несколько сахаров короче типичного липополисахарида. [4] Как эндотоксин, ЛОС провоцирует воспаление. Выделение LOS бактериями ответственно за местные повреждения, например, при воспалительных заболеваниях органов малого таза. [4] Хотя его основной функцией является эндотоксин, ЛОС может маскироваться под сиаловую кислоту хозяина и блокировать инициацию каскада комплемента . [4]
N. gonorrhoeae уклоняется от иммунной системы посредством процесса, называемого антигенной изменчивостью . [22] Этот процесс позволяет N. gonorrhoeae рекомбинировать свои гены и изменять антигенные детерминанты (сайты, где связываются антитела), такие как пили типа IV, [23] , которые украшают его поверхность. [4] Проще говоря, химический состав молекул изменяется вследствие изменений на генетическом уровне. [7] N. gonorrhoeae способна изменять состав своих пилей и ЛОС; из них пили демонстрируют наиболее антигенные вариации из-за хромосомной перестройки. [8] [4] Ген PilS является примером такой способности к перестройке, поскольку, по оценкам, его комбинация с геном PilE приводит к образованию более 100 вариантов белка PilE. [7] Эти изменения позволяют адаптироваться к различиям местной среды в месте заражения, уклоняться от распознавания таргетными антителами и способствуют отсутствию эффективной вакцины. [7]
Помимо способности реаранжировать уже имеющиеся у него гены, он также естественным образом способен приобретать новую ДНК (через плазмиды ) через свои пилусы типа IV, в частности белки Pil Q и Pil T. [24] Эти процессы позволяют N. gonorrhoeae приобретать/распространять новые гены, маскироваться под различные поверхностные белки и предотвращать развитие иммунологической памяти – способности, которая привела к устойчивости к антибиотикам, а также препятствовала разработке вакцин. [25]
Фазовые вариации аналогичны антигенным вариациям, но вместо изменений на генетическом уровне, изменяющих состав молекул, эти генетические изменения приводят к включению или выключению гена. [7] Фазовые вариации чаще всего возникают из-за сдвига рамки экспрессируемого гена. [7] Белки Opacity, или Opa, N. gonorrhoeae зависят исключительно от фазовых изменений. [7] Каждый раз, когда бактерии размножаются, они могут включать или выключать несколько белков Opa из-за неправильного спаривания . То есть бактерии вносят мутации со сдвигом рамки считывания, которые приводят гены в рамку или из нее. В результате каждый раз транслируются разные гены Opa. [4] Пили различаются не только антигенными вариациями, но и фазовыми вариациями. [7] Сдвиг рамки происходит как в генах pilE , так и в pilC , эффективно отключая экспрессию пилей в ситуациях, когда они не нужны, например, после колонизации, когда N. gonorrhoeae выживает внутри клеток, а не на их поверхности. [7]
После того как гонококки проникают в эпителиальные клетки хозяина и трансцитируют их , они попадают в подслизистую оболочку, где нейтрофилы быстро их поглощают. [4] Белки пилей и Opa на поверхности могут мешать фагоцитозу, [8] но большинство гонококков попадают в нейтрофилы. В экссудате инфицированных лиц содержится много нейтрофилов с попавшими в организм гонококками. Нейтрофилы высвобождают окислительный выброс активных форм кислорода в своих фагосомах, чтобы убить гонококки. [26] Однако значительная часть гонококков может противостоять уничтожению за счет действия их каталазы [4] , которая расщепляет активные формы кислорода и способна размножаться в фагосомах нейтрофилов. [27]
Столь и Зейферт показали, что бактериальный белок RecA, который опосредует восстановление повреждений ДНК, играет важную роль в выживании гонококков. [28] Мишо и др. предположили, что N. gonorrhoeae может заменять ДНК, поврежденную в фагосомах нейтрофилов, ДНК соседних гонококков. [29] Процесс, при котором гонококки-реципиенты интегрируют ДНК соседних гонококков в свой геном, называется трансформацией. [30]
Геномы нескольких штаммов N . gonorrhoeae секвенированы. Большинство из них имеют размер около 2,1 МБ и кодируют от 2100 до 2600 белков (хотя большинство, похоже, находятся в нижнем диапазоне). [31] Например, штамм NCCP11945 состоит из одной кольцевой хромосомы (2 232 025 п.н.), кодирующей 2662 предсказанные открытые рамки считывания (ORF), и одной плазмиды (4153 п.н.), кодирующей 12 предсказанных ORF. Предполагаемая плотность кодирования по всему геному составляет 87%, а среднее содержание G+C составляет 52,4%, значения аналогичны значениям для штамма FA1090. Геном NCCP11945 кодирует 54 тРНК и четыре копии оперонов 16S-23S-5S рРНК. [32]
В 2011 году исследователи из Северо-Западного университета обнаружили доказательства наличия фрагмента ДНК человека в геноме N. gonorrhoeae , что стало первым примером горизонтального переноса генов от человека к бактериальному патогену. [33] [34]
Симптомы заражения N. gonorrhoeae различаются в зависимости от места заражения, и многие инфекции протекают бессимптомно независимо от пола. [35] [15] [5] Важно отметить, что в зависимости от пути передачи N. gonorrhoeae может вызвать инфекцию горла ( фарингит ) или инфекцию ануса/прямой кишки ( проктит ). [36] [8]
Диссеминированная гонококковая инфекция может возникнуть при попадании N. gonorrhoeae в кровоток, часто распространяясь на суставы и вызывая сыпь (синдром дерматита-артрита). [36] Синдром дерматита-артрита приводит к боли в суставах ( артрит ), воспалению сухожилий ( тендосиновит ) и безболезненному незудному ( незудящему) дерматиту . [8] Диссеминированная инфекция и воспалительные заболевания органов малого таза у женщин, как правило, начинаются после менструации из-за рефлюкса во время менструации, что способствует распространению инфекции. [36] В редких случаях диссеминированная инфекция может вызвать инфицирование оболочек головного и спинного мозга ( менингит ) или инфицирование сердечных клапанов ( эндокардит ). [36] [37]
У мужчин с симптомами основным симптомом мочеполовой инфекции является уретрит – жжение при мочеиспускании ( дизурия ), усиление позывов к мочеиспусканию и гнойные (гнойные) выделения из полового члена. Выделения могут иметь неприятный запах. [36] При отсутствии лечения рубцевание уретры может привести к затруднению мочеиспускания. Инфекция может распространиться из уретры полового члена на близлежащие структуры, включая яички ( эпидидимит / орхит ) или на простату ( простатит ). [36] [8] [38] Мужчины, перенесшие гонорею , имеют значительно повышенный риск развития рака простаты. [39]
У женщин с симптомами первичными симптомами мочеполовой инфекции являются увеличение выделений из влагалища, жжение при мочеиспускании ( дизурия ), усиление позывов к мочеиспусканию, боль при половом акте или нарушения менструального цикла. Воспалительные заболевания органов малого таза возникают, если N. gonorrhoeae поднимается в тазовую брюшину (через шейку матки , эндометрий и фаллопиевы трубы ). Возникающее в результате воспаление и рубцевание маточных труб может привести к бесплодию и повышенному риску внематочной беременности. [36] Воспалительные заболевания органов малого таза развиваются у 10–20% женщин, инфицированных N. gonorrhoeae . [36]
При перинатальной инфекции первичным проявлением является инфекция глаз (неонатальный конъюнктивит или офтальмия новорожденных ), когда новорожденный подвергается воздействию N. gonorrhoeae в родовых путях. Глазная инфекция может привести к рубцеванию или перфорации роговицы, что в конечном итоге приводит к слепоте. Если новорожденный подвергся воздействию во время рождения, конъюнктивит возникает в течение 2–5 дней после рождения и имеет тяжелую форму. [36] [37] Гонококковую офтальмию новорожденных, которая когда-то часто встречалась у новорожденных, можно предотвратить путем нанесения геля эритромицина (антибиотика) на глаза младенцев при рождении в качестве меры общественного здравоохранения. Нитрат серебра больше не используется в США. [37] [36]
N. gonorrhoeae передается при вагинальном, оральном или анальном сексе; неполовая передача маловероятна при заражении взрослых. [5] Он также может передаваться новорожденному во время прохождения через родовые пути, если у матери имеется невылеченная мочеполовая инфекция. Учитывая высокий уровень бессимптомной инфекции, все беременные женщины должны пройти тестирование на инфекцию гонореи. [5] Тем не менее, общие ванны, полотенца или ткань, ректальные термометры и руки лиц, осуществляющих уход, были признаны средствами передачи инфекции в педиатрической практике. [40] Согласно новейшим исследованиям, поцелуи также считаются теоретическим средством передачи инфекции среди мужчин-геев. [41] [42] [43]
Традиционно считалось, что бактерия перемещается, прикрепившись к сперматозоидам, но эта гипотеза не объясняет передачу заболевания от женщины к мужчине. Недавнее исследование показывает, что вместо того, чтобы «плавать» на шевелящихся сперматозоидах , бактерии N. gonorrhoeae используют пили для закрепления на белках спермы и перемещения через коитальную жидкость. [44]
Для N. gonorrhoeae первым шагом после успешной передачи является прикрепление к эпителиальным клеткам , обнаруженным на инфицированном участке слизистой оболочки. [45] Бактерия опирается на пили типа IV , которые прикрепляются и втягиваются, притягивая N. gonorrhoeae к эпителиальной мембране, где ее поверхностные белки, такие как белки непрозрачности, могут напрямую взаимодействовать. [45] После присоединения N. gonorrhoeae размножается и образует микроколонии . [46] Во время колонизации N. gonorrhoeae может трансцитозировать через эпителиальный барьер и проникать в кровоток. [13] Во время роста и колонизации N. gonorrhoeae стимулирует высвобождение цитокинов и хемокинов из иммунных клеток хозяина, которые являются провоспалительными . [13] Эти провоспалительные молекулы приводят к привлечению макрофагов и нейтрофилов . [7] Эти фагоцитирующие клетки обычно поглощают чужеродные патогены и уничтожают их, но N. gonorrhoeae развила множество механизмов, которые позволяют ей выживать внутри этих иммунных клеток и препятствовать попыткам элиминации. [7]
Передача инфекции снижается за счет использования латексных барьеров (например, презервативов или коффердамов ) во время секса и ограничения сексуальных партнеров. [6] Презервативы и коффердам следует использовать также во время орального и анального секса. Спермициды, вагинальные пены и спринцевания не эффективны для предотвращения передачи инфекции. [4]
В настоящее время лечение, рекомендованное Центрами по контролю и профилактике заболеваний (CDC), представляет собой однократное введение цефтриаксона ( цефалоспорина третьего поколения ). [47] Сексуальных партнеров (определяемых CDC как сексуальный контакт в течение последних 60 дней) [11] также следует уведомить, пройти тестирование и пройти лечение. [6] [47] Важно, чтобы, если симптомы сохраняются после лечения инфекции N. gonorrhoeae , следует провести повторную оценку. [47]
Устойчивость гонореи к антибиотикам отмечалась начиная с 1940-х годов. Гонорею лечили пенициллином, но для сохранения эффективности дозы приходилось постепенно увеличивать. К 1970-м годам в Тихоокеанском бассейне появилась гонорея, устойчивая к пенициллину и тетрациклину. Эти устойчивые штаммы затем распространились на Гавайи, Калифорнию, остальную часть США, Австралию и Европу. Следующей линией защиты были фторхинолоны, но вскоре возникла устойчивость и к этому антибиотику. С 2007 года стандартным лечением являются цефалоспорины третьего поколения, такие как цефтриаксон, которые считаются нашей «последней линией защиты». [48] [49] Недавно в Японии был обнаружен штамм гонореи с высоким уровнем устойчивости к цефтриаксону под названием H041. Лабораторные тесты показали, что он устойчив к высоким концентрациям цефтриаксона, а также к большинству других протестированных антибиотиков. В N. gonorrhoeae существуют гены, которые придают устойчивость к каждому антибиотику, используемому для лечения гонореи, но до сих пор они не сосуществуют в одном гонококке. Однако из-за высокой склонности N. gonorrhoeae к горизонтальному переносу генов устойчивая к антибиотикам гонорея рассматривается как новая угроза общественному здравоохранению. [49]
Как грамотрицательная бактерия, N. gonorrhoeae нуждается в защитных механизмах для защиты от системы комплемента (или каскада комплемента), компоненты которого обнаруживаются в сыворотке человека . [15] Существует три различных пути активации этой системы, однако все они приводят к активации белка комплемента 3 (C3). [50] Расщепленная часть этого белка, C3b , откладывается на патогенных поверхностях и приводит к опсонизации , а также к последующей активации мембраноатакующего комплекса . [50] N. gonorrhoeae имеет несколько механизмов, позволяющих избежать этого действия. [13] В целом эти механизмы называются сывороточной резистентностью. [13]
Neisseria gonorrhoeae названа в честь Альберта Нейссера, который выделил ее как возбудителя гонореи в 1878 году. [13] [3] Гален (130 г. н.э.) ввел термин «гонорея» от греческого gonos , что означает «семя» и икра . что означает «поток». [51] [7] Таким образом, гонорея означает «поток семян», описание, относящееся к белым выделениям из полового члена, предположительно сперме, наблюдаемым при мужской инфекции. [13]
В 1878 году Альберт Нейссер выделил и визуализировал диплококки N. gonorrhoeae в образцах гноя 35 мужчин и женщин с классическими симптомами мочеполовой инфекции, вызванной гонореей, двое из которых также имели инфекции глаз. [7] В 1882 году Лейстиков и Леффлер смогли вырастить этот организм в культуре. [13] Затем, в 1883 году, Макс Бокхарт убедительно доказал, что бактерия, выделенная Альбертом Нейссером, была возбудителем заболевания, известного как гонорея, путем прививки пениса здорового мужчины бактериями. [7] Через несколько дней у мужчины появились классические симптомы гонореи, что соответствует последнему постулату Коха . До этого момента исследователи спорили, являются ли сифилис и гонорея проявлениями одного и того же заболевания или двумя разными заболеваниями. [52] [7] Один из таких исследователей 18-го века, Джон Хантер, попытался урегулировать спор в 1767 году [7] , привив мужчине гной, взятый у пациента с гонореей. Он ошибочно пришел к выводу, что и сифилис, и гонорея на самом деле были одним и тем же заболеванием, когда у мужчины появилась сыпь медного цвета, классическая для сифилиса. [50] [52] Хотя многие источники повторяют, что Хантер сделал прививку себе, [50] [13] другие утверждают, что на самом деле это был другой человек. [53] После эксперимента Хантера другие учёные попытались опровергнуть его выводы, привив другим мужчинам-врачам, студентам-медикам, [13] и заключенным мужчинам гонорейный гной, у всех которых развилось жжение и выделения гонореи. Один исследователь, Рикорд, выступил с инициативой провести 667 прививок гонорейного гноя пациентам психиатрической больницы без случаев сифилиса. [7] [13] Примечательно, что появление пенициллина в 1940-х годах сделало доступным эффективное лечение гонореи. [ нужна цитата ]