Фермент фенилаланинаммиаклиаза (EC 4.3.1.24) катализирует превращение L - фенилаланина в аммиак и транс -коричную кислоту .: [1]
Фенилаланиновая аммиачная лиаза (PAL) является первым и обязательным этапом в фенилпропаноидном пути и, следовательно, участвует в биосинтезе полифенольных соединений , таких как флавоноиды , фенилпропаноиды и лигнин в растениях . [2] [3] Фенилаланиновая аммиачная лиаза широко встречается в растениях, а также в некоторых бактериях , дрожжах и грибах , при этом изоферменты существуют во многих различных видах. Она имеет молекулярную массу в диапазоне 270–330 кДа . [1] [4] Активность PAL резко индуцируется в ответ на различные стимулы, такие как ранение тканей, патогенная атака, свет, низкие температуры и гормоны . [1] [5] Недавно PAL изучалась на предмет возможных терапевтических преимуществ у людей, страдающих фенилкетонурией . [6] Он также использовался при получении L -фенилаланина в качестве предшественника подсластителя аспартама . [7]
Фермент является членом семейства аммиачных лиаз , которые расщепляют связи углерод-азот. Как и другие лиазы, PAL требует только один субстрат для прямой реакции, но два для обратной. Считается, что он механистически похож на родственный фермент гистидинаммиачную лиазу (EC:4.3.1.3, HAL). [8] Систематическое название этого класса ферментов - L -фенилаланинаммиачную лиазу ( транс -циннаматобразующую) . Ранее он был обозначен как EC 4.3.1.5, но этот класс был переименован в EC 4.3.1.24 (фенилаланинаммиачные лиазы), EC 4.3.1.25 (тирозинаммиачные лиазы) и EC 4.3.1.26 (фенилаланин/тирозинаммиачные лиазы). Другие общеупотребительные названия включают тиразу , фенилаланиндезаминазу , тирозинаммиаклиазу , L -тирозинаммиаклиазу , фенилаланинаммонийлиазу , PAL и L- фенилаланинаммиаклиазу .
Фенилаланиновая аммиачная лиаза специфична для L -фенилаланина и, в меньшей степени, для L - тирозина . [9] [10] Реакция, катализируемая PAL, представляет собой спонтанную реакцию элиминирования , а не окислительное дезаминирование . [11]
Кофактор 3,5-дигидро - 5-метилдиен-4H-имидазол-4-он (MIO) участвует в реакции и находится на положительном полюсе трех полярных спиралей в активном центре, что помогает увеличить его электрофильность . [12] MIO подвергается атаке ароматического кольца L - phe , которое активирует связь CH на β-углероде для депротонирования основным остатком. [13] [14] Промежуточный карбанион этой реакции элиминирования E1cB , который стабилизируется частичными положительными областями в активном центре, затем вытесняет аммиак с образованием циннаматного алкена. Механизм реакции PAL , как полагают, аналогичен механизму родственного фермента гистидин-аммиачной лиазы. [13]

Остаток дегидроаланина долгое время считался ключевым электрофильным каталитическим остатком в PAL и HAL, но позже было обнаружено, что активным остатком является MIO, который еще более электрофилен. [16] [17] Он образуется путем циклизации и дегидратации консервативного трипептидного сегмента Ala-Ser-Gly. Первым шагом образования MIO является циклизация-элиминирование путем внутримолекулярной нуклеофильной атаки азота Gly204 на карбонильную группу Ala202. Последующее удаление воды из боковой цепи Ser203 завершает систему перекрестно сопряженных двойных связей. [15] Номера приведены для фенилаланиновой аммиачной лиазы из Petroselinum crispum ( PDB 1W27). Хотя MIO является модификацией полипептида, было предложено назвать ее простетической группой, поскольку она имеет качество добавленного органического соединения. [8]
PAL ингибируется транс-коричной кислотой, а у некоторых видов может ингибироваться производными транс- коричной кислоты. [1] [18] Неприродные аминокислоты D -Phe и D -Tyr, энантиомерные формы нормального субстрата, являются конкурентными ингибиторами . [9]
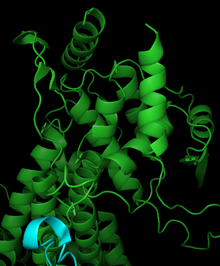
Фенилаланиновая аммиачная лиаза состоит из четырех идентичных субъединиц, состоящих в основном из альфа-спиралей , с парами мономеров , образующих один активный центр . [17] Катализ в PAL может регулироваться дипольными моментами семи различных альфа-спиралей, связанных с активным центром. [19] Активный центр содержит электрофильную группу MIO, нековалентно связанную с тремя спиралями. Leu266, Asn270, Val269, Leu215, Lys486 и Ile472 расположены на спиралях активного центра, в то время как Phe413, Glu496 и Gln500 способствуют стабилизации кофактора MIO. Ориентация дипольных моментов, генерируемых спиралями в активном центре, создает электроположительную область для идеальной реакционной способности с MIO. Частично положительные области в активном центре также могут помочь стабилизировать заряд промежуточного карбаниона. PAL структурно похож на механически связанную гистидинаммиачную лиазу, хотя PAL имеет приблизительно 215 дополнительных остатков. [17]
Фенилаланиновая аммиачная лиаза может выполнять различные функции у разных видов. Она встречается в основном в некоторых растениях и грибах (например, дрожжах). В клетках грибов и дрожжей PAL играет важную катаболическую роль, генерируя углерод и азот . [2] В растениях это ключевой биосинтетический фермент, который катализирует первый этап синтеза различных полифенильных соединений [2] [3] и в основном участвует в защитных механизмах. PAL участвует в 5 метаболических путях : метаболизм тирозина , метаболизм фенилаланина , метаболизм азота , биосинтез фенилпропаноидов и биосинтез алкалоидов .
Изучается заместительная ферментная терапия с использованием PAL для лечения фенилкетонурии (ФКУ), аутосомно-рецессивного генетического заболевания у людей, при котором мутации в гене фенилаланингидроксилазы (PAH, EC 1.14.16.1) инактивируют фермент. [6] Это приводит к неспособности пациента метаболизировать фенилаланин, вызывая повышенный уровень Phe в кровотоке ( гиперфенилаланинемия ) и умственную отсталость, если терапия не начата с рождения. [6]
В мае 2018 года FDA одобрило пегвалиазу , рекомбинантную пегилированную фенилаланинаммиачную лиазу для лечения фенилкетонурии, разработанную компанией Biomarin. [20] [21]
Lactuca sativa была исследована Васкесом и др. в 2017 году. Они обнаружили, что обработка ультрафиолетом увеличила активность фермента PAL. Это увеличение приводит к снижению восприимчивости к Botrytis cinerea . [22]
Обратная реакция, катализируемая PAL, была исследована для использования в преобразовании транс -коричной кислоты в L -фенилаланин, который является предшественником подсластителя аспартама. Этот процесс был разработан Genex Corporation, но никогда не был коммерчески принят. [23]
Аналогично тому, как синтезируется аспартам, PAL также используется для синтеза неприродных аминокислот из различных замещенных коричных кислот в исследовательских целях. [24] Однако стерические препятствия от замены арена ограничивают полезность PAL для этой цели. [25] Например, когда Rhodotorula glutinis использовался для воздействия на эту биотрансформацию, было обнаружено, что фермент не переносит все пара- заместители, кроме фтора , предположительно из-за малого атомного радиуса элемента . Было обнаружено, что мета- и орто- позиции более терпимы, но все еще ограничены более крупными заместителями. Например, активный центр фермента допускает замену орто -метокси, но запрещает мета -этокси . Другие организмы с другими версиями фермента могут быть менее ограничены в этом отношении. [26] [27]
По состоянию на конец 2007 года для этого класса ферментов было решено 5 структур с кодами доступа PDB 1T6J, 1T6P, 1W27, 1Y2M и 2NYF.