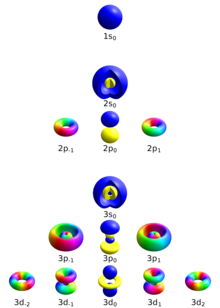
В квантовой физике и химии квантовые числа описывают значения сохраняющихся величин в динамике квантовой системы . Квантовые числа соответствуют собственным значениям операторов , коммутирующих с гамильтонианом .
Важным аспектом квантовой механики является квантование многих наблюдаемых величин, представляющих интерес. Это отличает квантовую механику от классической механики , где значения, характеризующие систему, такие как масса, заряд или импульс, постоянно изменяются. Квантовые числа часто конкретно описывают энергетические уровни электронов в атомах, но другие возможности включают угловой момент , спин и ароматические квантовые числа .
Квантовые числа соответствуют собственным значениям операторов , которые коммутируют с гамильтонианом , величинам, которые могут быть известны с точностью одновременно с энергией системы. В частности, наблюдаемые , которые коммутируют с гамильтонианом, одновременно диагонализуемы с ним, и поэтому собственные значения и энергия (собственные значения гамильтониана) не ограничены соотношением неопределенности , возникающим из-за некоммутативности. Вместе спецификация всех квантовых чисел квантовой системы полностью характеризует базовое состояние системы и в принципе может быть измерена вместе. Многие наблюдаемые в квантовой механике имеют дискретные спектры (наборы собственных значений) , поэтому величины можно измерять только в дискретных (часто целых) значениях. В частности, это приводит к квантовым числам, которые принимают значения в дискретных наборах целых или полуцелых чисел ; хотя в некоторых случаях они могут приближаться к бесконечности .
Подсчет квантовых чисел варьируется от системы к системе и не имеет универсального ответа. Следовательно, эти параметры необходимо найти для каждой анализируемой системы. Квантованная система требует хотя бы одного квантового числа. Динамика ( т.е. эволюция во времени) любой квантовой системы описывается квантовым оператором в форме гамильтониана H . Существует одно квантовое число системы, соответствующее энергии системы; т. е. одно из собственных значений гамильтониана. Также существует одно квантовое число для каждого линейно независимого оператора O , коммутирующего с гамильтонианом. Полный набор коммутирующих наблюдаемых (CSCO), коммутирующих с гамильтонианом, характеризует систему со всеми ее квантовыми числами. Между квантовыми числами и операторами CSCO существует связь один к одному, при этом каждое квантовое число принимает одно из собственных значений соответствующего оператора. В результате разного базиса , который может быть произвольно выбран для формирования полного набора коммутирующих операторов, разные наборы квантовых чисел могут использоваться для описания одной и той же системы в разных ситуациях.
Четыре квантовых числа могут полностью описать электрон в атоме:
Однако спин-орбитальное взаимодействие связывает эти числа . Таким образом, полное описание системы может быть дано с меньшим количеством квантовых чисел, если для этих базисных векторов будет сделан ортогональный выбор.
Разные электроны в системе будут иметь разные квантовые числа. Например, электрон с наивысшей занятой орбитой, фактический дифференцирующий электрон (т.е. электрон, который отличает элемент от предыдущего) или дифференцирующий электрон в соответствии с приближением Ауфбау . В лантане , например, участвующие электроны находятся в положении 6; 5д; и 4f-орбитали соответственно. В этом случае главные квантовые числа равны 6, 5 и 4.
Используемая здесь модель описывает электроны с использованием четырех квантовых чисел n , ℓ , m ℓ , m s , приведенных ниже. Это также общепринятая номенклатура в классическом описании состояний ядерных частиц (например, протонов и нейтронов). Квантовое описание молекулярных орбиталей требует других квантовых чисел, поскольку гамильтониан и его симметрия различны.
Главное квантовое число описывает электронную оболочку или энергетический уровень электрона. Значение n варьируется от 1 до оболочки, содержащей самый внешний электрон этого атома, то есть [1]
Например, в цезии (Cs) самый внешний валентный электрон находится в оболочке с энергетическим уровнем 6, поэтому электрон в цезии может иметь значение n от 1 до 6.
Для частиц в независимом от времени потенциале (см. уравнение Шредингера ) оно также помечает n-е собственное значение гамильтониана ( H ), то есть энергию E , при этом вклад, обусловленный угловым моментом (член, включающий J 2 ), не учитывается. . Так что это число зависит только от расстояния между электроном и ядром (то есть радиальной координаты r ). Среднее расстояние увеличивается с увеличением n . Следовательно, говорят, что квантовые состояния с разными главными квантовыми числами принадлежат разным оболочкам.
Азимутальное квантовое число, также известное как квантовое число углового момента или орбитальное квантовое число , описывает подоболочку и дает величину орбитального углового момента через соотношение.
В химии и спектроскопии ℓ = 0 называется s-орбиталью, ℓ = 1 — p-орбиталью, ℓ = 2 — d-орбиталью и ℓ = 3 — f-орбиталью.
Значение ℓ варьируется от 0 до n - 1 , поэтому первая p-орбиталь ( ℓ = 1 ) появляется во второй электронной оболочке ( n = 2 ), первая d-орбиталь ( ℓ = 2 ) появляется в третьей оболочке ( n = 3 ) и так далее: [2]
Квантовое число, начинающееся с n = 3, ℓ = 0, описывает электрон на s-орбитали третьей электронной оболочки атома. В химии это квантовое число очень важно, поскольку оно определяет форму атомной орбитали и сильно влияет на химические связи и валентные углы . Азимутальное квантовое число также может обозначать количество угловых узлов, присутствующих на орбитали. Например, для p-орбиталей ℓ = 1 , и, следовательно, количество угловых узлов на p-орбитали равно 1.
Форма орбитали также задается азимутальным квантовым числом.
Магнитное квантовое число описывает конкретную орбиталь (или «облако») внутри этой подоболочки и дает проекцию орбитального углового момента вдоль указанной оси :
Значения m ℓ варьируются от − ℓ до ℓ с целыми интервалами. [3] [ нужна страница ]
Подоболочка s ( ℓ = 0 ) содержит только одну орбиталь, и поэтому m ℓ электрона на s-орбитали всегда будет равна 0. Подоболочка p ( ℓ = 1 ) содержит три орбитали (в некоторых системах изображаются как три " облака в форме гантели), поэтому m ℓ электрона на ap-орбитали будет равно -1, 0 или 1. Подоболочка d ( ℓ = 2 ) содержит пять орбиталей со значениями m ℓ -2, -1, 0, 1 и 2.
Спиновое квантовое число описывает собственный спиновый угловой момент электрона внутри каждой орбитали и дает проекцию спинового углового момента S вдоль указанной оси:
В общем, значения m s варьируются от − s до s , где s — спиновое квантовое число , связанное с собственным спиновым угловым моментом частицы: [4]
Электрон имеет спиновое число s =1/2, следовательно, m s будет равно ±1/2, имея в виду состояния «вверх» и «вниз». Каждый электрон на любой отдельной орбитали должен иметь разные квантовые числа из-за принципа Паули , поэтому орбиталь никогда не содержит более двух электронов.
Не существует универсальных фиксированных значений для m ℓ и m s . Скорее, значения m ℓ и m s являются произвольными . Единственное ограничение на выбор этих констант заключается в том, что схема именования, используемая в конкретном наборе вычислений или описаний, должна быть последовательной (например, орбиталь, занимаемая первым электроном на ап-орбитали, может быть описана как m ℓ = −1 или m ℓ = 0 или m ℓ = 1 , но значение m ℓ следующего неспаренного электрона на этой орбитали должно быть другим; тем не менее, m ℓ , присвоенное электронам на других орбиталях, снова может быть m ℓ = -1 или m ℓ = 0 или м ℓ знак равно 1 ).
Эти правила резюмируются следующим образом:
Пример: квантовые числа, используемые для обозначения крайних валентных электронов атома углерода (C) , которые расположены на атомной орбитали 2p , составляют; n = 2 (2-я электронная оболочка), ℓ = 1 (p-орбитальная подоболочка ), m ℓ = 1, 0, −1 , м s =1/2(параллельные вращения).
Результаты спектроскопии показали, что до двух электронов могут занимать одну орбиталь. Однако два электрона никогда не могут иметь одинаковое квантовое состояние или одинаковый набор квантовых чисел в соответствии с правилами Хунда , которые касаются принципа исключения Паули . Четвертое квантовое число, которое представляло спин с двумя возможными значениями, было добавлено в качестве специального предположения для разрешения конфликта; это предположение позже будет подробно объяснено с помощью релятивистской квантовой механики и результатов известного эксперимента Штерна-Герлаха .
На протяжении всей истории квантовой механики было предложено множество различных моделей , но наиболее известная система номенклатуры возникла из теории молекулярных орбиталей Хунда-Малликена Фридриха Хунда , Роберта С. Малликена и вкладов Шредингера , Слейтера и Джона Леннарда-Джонса . Эта система номенклатуры включала уровни энергии Бора , орбитальную теорию Хунда-Малликена и наблюдения за спином электронов, основанные на спектроскопии и правилах Хунда . [5]
Если принять во внимание спин-орбитальное взаимодействие , операторы L и S больше не коммутируют с гамильтонианом , и поэтому их собственные значения изменяются со временем. Таким образом, следует использовать другой набор квантовых чисел. В этот набор входят [6] [7]
что дает полный угловой момент через соотношение
аналогично предыдущему и удовлетворяет
Это отражаемое собственное значение : положительное (+1) для состояний, пришедших из четного ℓ, и отрицательное (-1) для состояний, пришедших из нечетного ℓ . Первый также известен как четная четность , а второй как нечетная четность и определяется выражением
Например, рассмотрим следующие 8 состояний, определяемых их квантовыми числами:
Квантовые состояния в системе можно описать как линейную комбинацию этих восьми состояний. Однако при наличии спин-орбитального взаимодействия , если мы хотим описать одну и ту же систему 8 состояниями, которые являются собственными векторами гамильтониана ( т.е. каждое представляет собой состояние, которое не смешивается с другими с течением времени), нам следует рассмотреть следующие 8 состояния:
В ядрах вся совокупность протонов и нейтронов ( нуклонов ) имеет результирующий угловой момент , обусловленный угловыми моментами каждого нуклона, обычно обозначаемый I. Если полный угловой момент нейтрона j n = ℓ + s , а для протона j p = ℓ + s (где s для протонов и нейтронов равен1/2снова ( см. примечание )), тогда квантовые числа ядерного углового момента I определяются выражением:
Примечание. Все орбитальные угловые моменты ядерных (и атомных) состояний кратны ħ, а собственные угловые моменты нейтрона и протона кратны полуцелому числу. Должно быть сразу очевидно, что комбинация собственных спинов нуклонов с их орбитальным движением всегда будет давать полуцелые значения полного спина I любого ядра с нечетным А и целые значения для любого ядра с четным А.
Четность с числом I используется для обозначения состояний ядерного углового момента, примерами некоторых изотопов водорода (H), углерода (C) и натрия (Na); [8]
Причина необычных флуктуаций I , даже разницей всего в один нуклон, связана с нечетным и четным числом протонов и нейтронов – пары нуклонов имеют нулевой суммарный угловой момент (так же, как электроны на орбиталях), оставляя нечетное или четное число неспаренных нуклонов. Свойство ядерного спина является важным фактором для работы ЯМР- спектроскопии в органической химии [7] и МРТ в ядерной медицине [8] из -за ядерного магнитного момента , взаимодействующего с внешним магнитным полем .
Элементарные частицы содержат множество квантовых чисел, которые обычно считаются присущими им. Однако следует понимать, что элементарные частицы представляют собой квантовые состояния стандартной модели физики элементарных частиц , и, следовательно, квантовые числа этих частиц имеют такое же отношение к гамильтониану этой модели, как квантовые числа атома Бора к его Гамильтониан . Другими словами, каждое квантовое число обозначает симметрию задачи. В квантовой теории поля полезнее различать пространство-время и внутреннюю симметрию.
Типичными квантовыми числами, связанными с симметрией пространства-времени , являются спин (связанный с вращательной симметрией), четность , C-четность и T-четность (связанный с симметрией Пуанкаре пространства - времени ). Типичными внутренними симметриями [ необходимы пояснения ] являются лептонное число и барионное число или электрический заряд . (Полный список таких квантовых чисел см. в статье о вкусе .)
Большинство консервативных квантовых чисел аддитивны, поэтому в реакции элементарных частиц сумма квантовых чисел должна быть одинаковой до и после реакции. Однако некоторые из них, обычно называемые четностью , являются мультипликативными; т. е. их продукт сохраняется. Все мультипликативные квантовые числа принадлежат к симметрии (например, к четности), при которой применение преобразования симметрии дважды эквивалентно бездействию ( инволюция ).