
Т -хелперные клетки ( Т - клетки ), также известные как клетки CD4 + или CD4-позитивные клетки , представляют собой тип Т-клеток , которые играют важную роль в адаптивной иммунной системе . Они способствуют активности других иммунных клеток, высвобождая цитокины . Они считаются необходимыми для переключения класса антител В-клеток , нарушения перекрестной толерантности в дендритных клетках, активации и роста цитотоксических Т-клеток и максимизации бактерицидной активности фагоцитов , таких как макрофаги и нейтрофилы . Клетки CD4 + представляют собой зрелые Т - клетки, которые экспрессируют поверхностный белок CD4. Генетическая изменчивость регуляторных элементов, экспрессируемых клетками CD4 + , определяет восприимчивость к широкому классу аутоиммунных заболеваний . [1]
T h клетки содержат и выделяют цитокины для помощи другим иммунным клеткам. Цитокины — это небольшие белковые медиаторы, которые изменяют поведение целевых клеток, экспрессирующих рецепторы для этих цитокинов. Эти клетки помогают поляризовать иммунный ответ в зависимости от природы иммунологического оскорбления (например, вирус против внеклеточной бактерии против внутриклеточной бактерии против гельминта против грибка против простейшего). [ необходима цитата ]
Зрелые T h клетки экспрессируют поверхностный белок CD4 и называются CD4 + T клетками . CD4 + T клетки обычно рассматриваются как имеющие предопределенную роль в качестве вспомогательных T клеток в иммунной системе . Например, когда антиген-презентирующая клетка демонстрирует пептидный антиген на белках MHC класса II , CD4 + клетка будет помогать этим клеткам посредством комбинации межклеточных взаимодействий (например, CD40 (белок) и CD40L ) и через цитокины .
T h - клетки не являются монолитной иммунологической сущностью, поскольку они разнообразны с точки зрения функций и их взаимодействия с клетками-партнерами. В целом, зрелые наивные T-клетки стимулируются профессиональными антигенпрезентирующими клетками для приобретения эффекторного модуля. Они определяются наличием фактора транскрипции, определяющего линию (или специфичного для линии) (также называемого главным регулятором , хотя этот термин подвергался критике за его излишнюю редуктивность). [2] Потеря функции в факторе транскрипции, специфичном для линии, приводит к отсутствию соответствующего класса вспомогательных T-клеток, что может иметь разрушительные последствия для здоровья хозяина.

После развития в тимусе эти клетки (называемые недавними эмигрантами тимуса (RTE)) выходят из тимуса и направляются во вторичные лимфоидные органы (SLO; селезенка и лимфатические узлы ). Следует отметить, что только очень небольшое меньшинство Т-клеток выходит из тимуса (оценки обычно варьируются от 1 до 5%, но некоторые эксперты считают даже это щедрым). [3] Созревание RTE в SLO приводит к образованию зрелых наивных Т-клеток (наивных, что означает, что они никогда не подвергались воздействию антигена , на который они запрограммированы реагировать), но наивные Т-клетки теперь лишены или имеют пониженную (сниженную) экспрессию поверхностных маркеров, связанных с RTE, таких как CD31 , PTK7 , рецептор комплемента 1 и 2 ( CR1 , CR2 ) и выработку интерлейкина 8 (IL-8) . [4] [5] Как и все Т-клетки, они экспрессируют комплекс рецептор Т-клеток - CD3 . Рецептор Т-клеток (TCR) состоит из константных и вариабельных областей. Вариабельная область определяет, на какой антиген может реагировать Т-клетка. CD4 + T-клетки имеют TCR со сродством к MHC класса II , а CD4 участвует в определении сродства MHC во время созревания в тимусе . Белки MHC класса II обычно обнаруживаются только на поверхности профессиональных антигенпрезентирующих клеток (APC). Профессиональные антигенпрезентирующие клетки — это в первую очередь дендритные клетки , макрофаги и В-клетки , хотя дендритные клетки являются единственной группой клеток, которая конститутивно (всегда) экспрессирует MHC класса II . Некоторые АПК также связывают нативные (или необработанные) антигены со своей поверхностью, например, фолликулярные дендритные клетки (это не тот же тип клеток, что и дендритные клетки иммунной системы, а скорее негематопоэтического происхождения, и в целом не имеют MHC класса II, что означает, что они не являются истинными профессиональными антигенпрезентирующими клетками; однако фолликулярные дендритные клетки могут приобретать белки MHC класса II через экзосомы, которые прикрепляются к ним [6] ). Т-клетки требуют, чтобы антигены были обработаны в короткие фрагменты, которые образуют линейные эпитопы на MHC класса II (в случае хелперных Т-клеток, потому что они экспрессируют CD4) или MHC класса I (в случае цитотоксических Т-клеток , которые экспрессируют CD8)). Карманы связывания MHC класса II являются гибкими в отношении длины пептидов, которые они удерживают. Обычно существует 9 основных аминокислотных остатков с несколькими фланкирующими аминокислотами, которые образуют длину около 12–16 аминокислот в общей сложности [7], но известно, что они удерживают до 25 аминокислот. [8] Для сравнения, белки MHC класса I обычно имеют длину 9–10 пептидов. [9] Активация наивных Т-клеток обычно объясняется в терминах 3-сигнальной модели, подробно описанной ниже. [10]
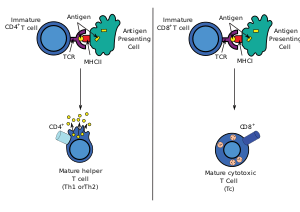
Во время иммунного ответа профессиональные антигенпрезентирующие клетки (АПК) эндоцитируют антигены (обычно бактерии или вирусы), которые подвергаются обработке , а затем перемещаются из места инфекции в лимфатические узлы . Обычно ответственной АПК является дендритная клетка. Если антиген экспрессирует соответствующие молекулярные паттерны (иногда называемые сигналом 0), он может вызвать созревание дендритной клетки, что приводит к усилению экспрессии костимулирующих молекул, необходимых для активации Т-клеток (см. сигнал 2) [11] и MHC класса II. [12] Попав в лимфатические узлы, АПК начинают представлять антигенные пептиды, которые связаны с MHC класса II, что позволяет активировать CD4 + T-клетки, которые экспрессируют специфические TCR против комплекса пептид/MHC. [ необходима цитата ]
Когда Т h- клетка сталкивается с антигеном на АПК и распознает его, комплекс TCR - CD3 прочно связывается с комплексом пептид-MHC, присутствующим на поверхности профессиональных АПК. CD4 , корецептор комплекса TCR, также связывается с другим участком молекулы MHC. Подсчитано, что приблизительно 50 из этих взаимодействий необходимы для активации хелперной Т-клетки, и наблюдалось образование агрегатов, известных как микрокластеры, между комплексами TCR-CD3-CD4 Т-клетки и белками MHC класса II дендритной клетки в зоне контакта. Когда все это объединяется, CD4 способен рекрутировать киназу, называемую Lck , которая фосфорилирует иммунорецепторные мотивы активации на основе тирозина (ITAM), присутствующие на гамма-, дельта-, эпсилон- и дзета-цепях CD3. Белок ZAP-70 может связывать эти фосфорилированные ITAM через свой домен SH2 , а затем сам становится фосфорилированным, при этом он организует нисходящий сигнал, необходимый для активации Т-клеток. Активация Lck контролируется противоположными действиями CD45 и Csk . [13] CD45 активирует Lck, дефосфорилируя тирозин в его C-концевом хвосте, в то время как Csk фосфорилирует Lck в этом месте. Потеря CD45 приводит к форме SCID, поскольку неспособность активировать Lck препятствует надлежащей сигнализации Т-клеток. Клетки памяти T также используют этот путь и имеют более высокие уровни экспрессии Lck, а функция Csk ингибируется в этих клетках. [14]
Связывание антиген-MHC с комплексом TCR и CD4 также может помочь APC и T h -клеткам прилипать во время активации T h -клеток, но интегриновый белок LFA-1 на T-клетке и ICAM на APC являются основными молекулами адгезии в этом клеточном взаимодействии. [ необходима цитата ]
Неизвестно, какую роль играет относительно объемная внеклеточная область CD45 во время клеточных взаимодействий, но CD45 имеет различные изоформы, которые изменяются по размеру в зависимости от активации и состояния созревания Т - клетки. Например, CD45 укорачивается в длину после активации Т -клетки (CD45RA + до CD45RO + ), но неизвестно, влияет ли это изменение длины на активацию. Было высказано предположение, что более крупный CD45RA может снижать доступность рецептора Т-клетки для молекулы антиген-MHC, тем самым требуя увеличения сродства (и специфичности) Т-клетки для активации. Однако после того, как активация произошла, CD45 укорачивается, что облегчает взаимодействия и активацию в качестве эффекторной Т-хелперной клетки. [ необходима цитата ]
Получив первый сигнал TCR/CD3, наивная Т-клетка должна активировать второй независимый биохимический путь, известный как Сигнал 2. Этот шаг проверки является защитной мерой, гарантирующей, что Т-клетка реагирует на чужеродный антиген. Если этот второй сигнал отсутствует во время первоначального воздействия антигена, Т-клетка предполагает, что она аутореактивна. Это приводит к тому, что клетка становится анергической (анергия генерируется из незащищенных биохимических изменений Сигнала 1). Анергические клетки не будут реагировать ни на один антиген в будущем, даже если оба сигнала присутствуют позже. Обычно считается, что эти клетки циркулируют по всему телу без какой-либо ценности, пока не подвергнутся апоптозу . [15]
Второй сигнал включает взаимодействие между CD28 на CD4 + T-клетке и белками CD80 (B7.1) или CD86 (B7.2) на профессиональных АПК. Оба CD80 и CD86 активируют рецептор CD28. Эти белки также известны как костимулирующие молекулы . [ необходима цитата ]
Хотя стадия проверки необходима для активации наивных хелперных Т-клеток, важность этой стадии лучше всего демонстрируется во время аналогичного механизма активации цитотоксических Т-клеток CD8 + . Поскольку наивные Т-клетки CD8 + не имеют истинной предвзятости по отношению к чужеродным источникам, эти Т-клетки должны полагаться на активацию CD28 для подтверждения того, что они распознают чужеродный антиген (поскольку CD80/CD86 экспрессируется только активными АПК). CD28 играет важную роль в снижении риска аутоиммунитета Т-клеток против антигенов хозяина. [ необходима цитата ]
Как только наивная Т-клетка активирует оба пути, биохимические изменения, вызванные Сигналом 1, изменяются, позволяя клетке активироваться вместо того, чтобы подвергаться анергии. Второй сигнал затем устаревает; только первый сигнал необходим для будущей активации. Это также верно для Т-клеток памяти, что является одним из примеров приобретенного иммунитета . Более быстрые ответы возникают при повторном инфицировании, поскольку Т-клетки памяти уже прошли подтверждение и могут производить эффекторные клетки гораздо раньше. [ необходима цитата ]
После завершения двухсигнальной активации Т-хелперная клетка (Т h ) позволяет себе размножаться . Она достигает этого, высвобождая мощный фактор роста Т-клеток, называемый интерлейкином 2 (ИЛ-2), который действует на себя аутокринным образом. Активированные Т-клетки также продуцируют альфа-субъединицу рецептора ИЛ-2 ( CD25 или ИЛ-2R), что позволяет полностью функциональному рецептору связываться с ИЛ-2, что, в свою очередь, активирует пути пролиферации Т-клеток. [ необходима цитата ]
Аутокринная или паракринная секреция IL-2 может связываться с той же T h клеткой или соседними T h через IL-2R, тем самым управляя пролиферацией и клональной экспансией. T h клетки , получающие как сигналы активации, так и пролиферации, затем станут T h 0 клетками (T helper 0), которые секретируют IL-2, IL-4 и интерферон гамма (IFN-γ). Затем T h 0 клетки будут дифференцироваться в T h 1 или T h 2 клетки в зависимости от цитокинового окружения. IFN-γ управляет продукцией T h 1 клеток, в то время как IL-10 и IL-4 ингибируют продукцию T h 1 клеток. И наоборот, IL-4 управляет продукцией T h 2 клеток, а IFN-γ ингибирует T h 2 клетки. Эти цитокины являются плейотропными и выполняют множество других функций иммунного ответа. [ необходима цитата ]
В 1991 году три группы сообщили об открытии CD154, который является молекулярной основой функции Т-хелперов. Сет Ледерман из Колумбийского университета создал мышиное моноклональное антитело 5c8, которое ингибировало контактно-зависимую функцию Т-хелперов в клетках человека, что характеризовало поверхностный белок массой 32 кДа, временно экспрессируемый на Т-клетках CD4 + . [16] Ричард Армитидж из Immunex клонировал кДНК, кодирующую CD154, путем скрининга библиотеки экспрессии с помощью CD40-Ig. [17] Рэндольф Ноэль из Дартмутской медицинской школы создал антитело, которое связывало белок массой 39 кДа на Т-клетках мышей и ингибировало функцию хелперов. [18]
Т-хелперы способны влиять на различные иммунные клетки, и генерируемый Т-клеточный ответ (включая внеклеточные сигналы, такие как цитокины ) может быть необходим для успешного исхода инфекции. Чтобы быть эффективными, Т-хелперы должны определить, какие цитокины позволят иммунной системе быть наиболее полезной или выгодной для хозяина. Понимание того, как именно Т-хелперы реагируют на иммунные вызовы, в настоящее время представляет большой интерес в иммунологии , поскольку такие знания могут быть очень полезны при лечении заболеваний и повышении эффективности вакцинации . [ необходима цитата ]
Пролиферирующие Т-хелперные клетки, которые развиваются в эффекторные Т-клетки, дифференцируются в два основных подтипа клеток, известных как клетки Th 1 и Th 2 (также известные как Т-хелперные клетки типа 1 и типа 2 соответственно).
Клетки-помощники T h 1 приводят к усилению клеточно-опосредованного ответа (в первую очередь макрофагами и цитотоксическими Т-клетками ) [19] , как правило, против внутриклеточных бактерий и простейших. Они запускаются поляризующим цитокином IL-12, а их эффекторными цитокинами являются IFN-γ и IL-2. Основными эффекторными клетками иммунитета T h 1 являются макрофаги, а также Т-клетки CD8, В-клетки IgG и Т-клетки IFN-γ CD4. Ключевыми факторами транскрипции T h 1 являются STAT4 и T-bet. IFN-γ, секретируемый Т-клетками CD4, может активировать макрофаги для фагоцитоза и переваривания внутриклеточных бактерий и простейших. Кроме того, IFN-γ может активировать iNOS (индуцируемую синтазу оксида азота) для выработки свободных радикалов оксида азота для непосредственного уничтожения внутриклеточных бактерий и простейших. Сверхактивация T h 1 против аутоантигенов вызовет реакцию гиперчувствительности IV типа или замедленного типа. Туберкулиновая реакция и диабет 1 типа относятся к этой категории аутоиммунитета. [20]
Клетки-помощники T h 2 приводят к гуморальному иммунному ответу , [19] как правило, против внеклеточных паразитов, таких как гельминты . Они запускаются поляризующими цитокинами IL-4 и IL-2, а их эффекторными цитокинами являются IL-4, IL-5, IL-9, IL-10, IL-13 и IL-25. Основными эффекторными клетками являются эозинофилы, базофилы и тучные клетки, а также В-клетки и IL-4/IL-5 CD4 T-клетки. Ключевыми факторами транскрипции T h 2 являются STAT6 и GATA3 . [21] IL-4 является цитокином положительной обратной связи для дифференцировки клеток Th 2 . Кроме того, IL-4 стимулирует В-клетки к выработке антител IgE, которые в свою очередь стимулируют тучные клетки к высвобождению гистамина , серотонина и лейкотриена, что вызывает сужение бронхов, перистальтику кишечника, закисление желудочного сока для изгнания гельминтов. IL-5 из CD4 T-клеток активирует эозинофилы для атаки гельминтов. IL-10 подавляет дифференцировку клеток Th 1 и функцию дендритных клеток. Сверхактивация Th 2 против антигена вызывает гиперчувствительность I типа , которая является аллергической реакцией, опосредованной IgE. Аллергический ринит, атопический дерматит и астма относятся к этой категории сверхактивации. [20] Помимо экспрессии различных цитокинов, клетки Th 2 также отличаются от клеток Th 1 по гликанам клеточной поверхности (олигосахаридам), что делает их менее восприимчивыми к некоторым индукторам клеточной смерти. [22] [23]

Хотя мы знаем о типах паттернов цитокинов, которые Т-хелперные клетки склонны производить, мы меньше понимаем, как определяются сами паттерны. Различные данные свидетельствуют о том, что тип АПК, представляющей антиген Т-клетке, оказывает большое влияние на ее профиль. Другие данные свидетельствуют о том, что концентрация антигена, представленного Т-клетке во время первичной активации, влияет на ее выбор. Наличие некоторых цитокинов (например, упомянутых выше) также будет влиять на ответ, который в конечном итоге будет сгенерирован, но наше понимание далеко не полное.
Клетки-помощники Th 17 являются подгруппой клеток-помощников T, отличающихся по развитию от линий Th 1 и Th 2. Клетки Th 17 вырабатывают интерлейкин 17 (IL-17), провоспалительное вещество, а также интерлейкины 21 и 22. [26] Это означает, что клетки Th 17 особенно хороши в борьбе с внеклеточными патогенами [26] и грибками, особенно во время слизисто-кожного иммунитета против Candida spp. [27]
Хелперные клетки THαβ обеспечивают иммунитет хозяина против вирусов. Их дифференциация запускается IFN α/β или IL-10 . Их ключевым эффекторным цитокином является IL-10. Их основными эффекторными клетками являются NK-клетки , а также T-клетки CD8, B-клетки IgG и T-клетки CD4 IL-10. Ключевыми факторами транскрипции THαβ являются STAT1 и STAT3, а также IRF. IL-10 из T-клеток CD4 активирует ADCC NK-клеток для апоптоза инфицированных вирусом клеток и для индукции фрагментации ДНК хозяина и вируса. IFN альфа/бета может подавлять транскрипцию, чтобы избежать репликации и передачи вируса. Избыточная активация THαβ против аутоантигена вызовет антителозависимую цитотоксическую гиперчувствительность 2-го типа. Миастения гравис или болезнь Грейвса относятся к этой категории. [28]
Взаимодействие между цитокинами из модели T h 1/Th h 2 может быть более сложным у некоторых животных. Например, цитокин T h 2 IL-10 подавляет продукцию цитокинов обоих подтипов T h у людей. Человеческий IL-10 (hIL-10) подавляет пролиферацию и продукцию цитокинов всех Т-клеток и активность макрофагов, но продолжает стимулировать плазматические клетки , гарантируя, что продукция антител все еще происходит. Таким образом, hIL-10, как полагают, не действительно способствует ответу T h 2 у людей, но действует, предотвращая чрезмерную стимуляцию Т-хелперов, при этом все еще максимизируя продукцию антител . [ необходима цитата ]
Существуют также другие типы Т-клеток, которые могут влиять на экспрессию и активацию Т-хелперных клеток, такие как естественные регуляторные Т-клетки , а также менее распространенные профили цитокинов, такие как подмножество Т-хелперных клеток Th 3. Такие термины, как «регуляторный» и «подавление», стали неоднозначными после открытия того, что Т-хелперные клетки CD4 + также способны регулировать (и подавлять) свои собственные реакции за пределами специализированных регуляторных Т-клеток. [ необходима цитата ]
Одно из основных различий между регуляторными Т-клетками и эффекторными Т-клетками заключается в том, что регуляторные Т-клетки обычно служат для модуляции и дезактивации иммунного ответа, в то время как эффекторные Т-клеточные группы обычно начинают с иммуностимулирующих цитокинов, а затем переключаются на ингибирующие цитокины позже в своем жизненном цикле. Последнее является особенностью клеток T h 3, которые трансформируются в регуляторный подвид после своей первоначальной активации и продукции цитокинов. [ необходима цитата ]
Как регуляторные Т-клетки , так и клетки Th3 продуцируют цитокин , трансформирующий фактор роста-бета (TGF-β), и IL-10. Оба цитокина ингибируют хелперные Т-клетки; TGF-β подавляет активность большей части иммунной системы. Есть данные, позволяющие предположить, что TGF-β может не подавлять активированные клетки Th2 так же эффективно, как он подавляет наивные клетки, но его обычно не считают цитокином Th2. [ необходима цитата ]
Новая характеристика другого подтипа Т-хелперов, Т-хелперов 17 (Т h 17) [29] еще больше усомнилась в базовой модели Т h 1/Т h 2. Эти клетки, продуцирующие ИЛ-17, изначально были описаны как патогенная популяция, вовлеченная в аутоиммунитет, но теперь считается, что они имеют свои собственные отличительные эффекторные и регуляторные функции. Следует отметить, что некоторые данные свидетельствуют о том, что функциональная пластичность является внутренней способностью Т-хелперов. Действительно, исследование на мышах продемонстрировало, что клетки Т h 17 трансформируются в клетки Т h 1 in vivo . [30] Последующее исследование также показало, что обширная пластичность Т-хелперов также выражена у людей. [31]
Многие из цитокинов в этой статье также экспрессируются другими иммунными клетками (см. отдельные цитокины для получения подробной информации), и становится ясно, что, хотя исходная модель T h 1/Th h 2 является просветляющей и дает представление о функциях Т-хелперов, она слишком проста, чтобы определить всю ее роль или действия. Некоторые иммунологи полностью подвергают эту модель сомнению, поскольку некоторые исследования in vivo предполагают, что отдельные Т-хелперы обычно не соответствуют определенным профилям цитокинов модели T h , и многие клетки экспрессируют цитокины из обоих профилей. [32] Тем не менее, модель T h по-прежнему играет важную роль в развитии нашего понимания ролей и поведения Т-хелперов и цитокинов, которые они вырабатывают во время иммунного ответа.
Исследования Стокингера и др. показали, что может существовать еще одна подгруппа Т-хелперов. Утверждается, что клетки Th9 являются подгруппой Т-клеток, продуцирующей IL9 ( интерлейкин 9 ), и направленной на защиту от гельминтных инфекций. [33]
Исторически считалось, что Т-клетки памяти принадлежат либо к эффекторному, либо к центральному подтипу памяти, каждый из которых имеет свой собственный отличительный набор маркеров клеточной поверхности. [34] Центральные Т-клетки памяти находятся в лимфатических узлах, в то время как эффекторные Т-клетки памяти не имеют рецепторов хемокинового рецептора CC типа 7 (CCR7) и L-селектина (CD62L), что препятствует их перемещению в лимфатические узлы.
Теперь известно, что существуют дополнительные популяции клеток памяти Т. К ним относятся резидентные клетки памяти Т (Trm) и виртуальные клетки памяти Т. [35] Единственная объединяющая тема для всех подтипов клеток памяти Т заключается в том, что они долгоживущие и могут быстро расширяться до большого количества эффекторных клеток Т при столкновении с их родственным антигеном. Благодаря этому механизму они обеспечивают иммунную систему «памятью» против ранее встреченных патогенов.
Учитывая разнообразную и важную роль, которую Т-хелперные клетки играют в иммунной системе, неудивительно, что эти клетки часто влияют на иммунный ответ против болезни. Иногда они также генерируют неблагоприятные ответы. Очень редко ответ Т-хелперных клеток может привести к смерти хозяина. [ необходима цитата ]
Иммунная система должна достичь баланса чувствительности, чтобы реагировать на чужеродные антигены, не реагируя на антигены самого хозяина. Когда иммунная система реагирует на очень низкие уровни антигена, на которые она обычно не должна реагировать, возникает реакция гиперчувствительности . Считается, что гиперчувствительность является причиной аллергии и некоторых аутоиммунных заболеваний .
Реакции гиперчувствительности можно разделить на четыре типа:
Другие клеточные гиперчувствительности включают аутоиммунное заболевание , опосредованное цитотоксическими Т-клетками , и похожее явление: отторжение трансплантата . Т-хелперные клетки необходимы для подпитки развития этих заболеваний. Для создания достаточного количества аутореактивных Т-клеток-киллеров должен вырабатываться интерлейкин-2 , и он поставляется Т-клетками CD4 + . Т-клетки CD4 + могут также стимулировать клетки, такие как естественные клетки-киллеры и макрофаги, с помощью цитокинов, таких как интерферон-гамма , побуждая эти цитотоксические клетки убивать клетки хозяина при определенных обстоятельствах.
Механизм, который клетки-киллеры Т используют во время аутоиммунитета, почти идентичен их реакции против вирусов , и некоторые вирусы обвиняются в том, что они вызывают аутоиммунные заболевания, такие как сахарный диабет 1 типа . Клеточное аутоиммунное заболевание возникает из-за того, что системы распознавания антигена хозяина выходят из строя, и иммунная система по ошибке считает, что антиген хозяина является чужеродным. В результате клетки CD8 + T воспринимают клетку хозяина, представляющую этот антиген, как инфицированную и продолжают уничтожать все клетки хозяина (или, в случае отторжения трансплантата, трансплантированный орган), которые экспрессируют этот антиген.
Часть этого раздела является упрощением. Многие аутоиммунные заболевания более сложны. Известным примером является ревматоидный артрит , где известно, что и антитела, и иммунные клетки играют роль в патологии. В целом иммунология большинства аутоиммунных заболеваний не до конца понятна.
Возможно, лучшим примером важности Т-клеток CD4 + является инфекция вируса иммунодефицита человека (ВИЧ). ВИЧ в основном поражает лимфоидные Т-клетки CD4 + , но может инфицировать и другие клетки, которые экспрессируют CD4, такие как макрофаги и дендритные клетки (обе группы экспрессируют CD4 на низком уровне). [ необходима цитата ]
Было высказано предположение, что во время бессимптомной фазы ВИЧ-инфекции вирус имеет относительно низкое сродство к Т-клеткам (и имеет более высокое сродство к макрофагам), что приводит к медленной скорости уничтожения CD4 + Т-клеток иммунной системой. [ необходима цитата ] Это первоначально компенсируется за счет выработки новых вспомогательных Т-клеток из тимуса (первоначально из костного мозга ). Однако, как только вирус становится лимфотропным (или Т-тропным), он начинает инфицировать CD4 + Т-клетки гораздо более эффективно (вероятно, из-за изменения корецепторов , с которыми он связывается во время инфекции), и иммунная система перегружается. Исследования показывают, что только ~5% лимфоидных CD4 Т-клеток, на которые нацелен ВИЧ, являются пермиссивными и становятся продуктивно инфицированными вирусом. Более 95% CD4 Т-клеток, которые умирают, находятся в состоянии покоя и неспособны поддерживать продуктивную инфекцию. Эти клетки подвергаются абортивному инфицированию ВИЧ. [36] Смерть клетки запускается, когда клетка-хозяин обнаруживает чужеродные промежуточные продукты ДНК ВИЧ и инициирует суицидальный путь смерти в попытке защитить хозяина, что приводит к активации каспазы-1 в инфламмасомах , тем самым вызывая пироптоз (высоковоспалительная форма запрограммированной смерти клетки). [37] [38] [39]
В этот момент наступает хроническое воспаление, и функциональные уровни CD4 + T-клеток начинают снижаться, в конечном итоге до точки, когда популяция CD4 + T-клеток становится слишком малой, чтобы распознать весь спектр антигенов , которые потенциально могут быть обнаружены. Истощение CD4 T-клеток и развитие хронического воспаления являются характерными процессами в патогенезе ВИЧ, которые способствуют прогрессированию синдрома приобретенного иммунодефицита (СПИД). CD4 T-клетки, истощенные до количества клеток менее 200 клеток/мкл в крови во время СПИДа, позволяют различным патогенам избегать распознавания T-клеток, тем самым позволяя оппортунистическим инфекциям , которые обычно вызывают реакцию T-хелперов, обходить иммунную систему. [40] Хотя эти ситуации полного обхода возникают только тогда, когда реакция T-хелперов абсолютно необходима для устранения инфекции, большинство инфекций увеличиваются по тяжести и/или продолжительности, поскольку T-хелперы иммунной системы обеспечивают менее эффективный иммунный ответ.
При СПИДе особенно страдают два компонента иммунной системы из-за ее зависимости от Т-клеток CD4 + :
Если пациент не реагирует на лечение ВИЧ (или не получает его), он, как правило, погибает от рака или инфекций; иммунная система в конечном итоге достигает точки, когда она больше не координируется и не стимулируется в достаточной степени, чтобы справиться с болезнью.
Ингибирование расширения Т-клеток CD4 во время ВИЧ-инфекции может происходить из-за микробной транслокации в IL-10-зависимом пути. Активация PD-1, экспрессируемого на активированных моноцитах его лигандом PD-L1, вызывает выработку IL-10, который ингибирует функцию Т-клеток CD4. [41]
При коронавирусной болезни 2019 (COVID-19) количество В-клеток , естественных клеток-киллеров и общее количество лимфоцитов снижается, но количество как клеток CD4 + , так и клеток CD8 + снижается в гораздо большей степени. [42] Это указывает на то, что SARS-Cov-2 атакует клетки CD4 + во время инфекции. Низкий уровень CD4 + предсказывал большую вероятность поступления в отделение интенсивной терапии , а количество клеток CD4 + было единственным параметром, который предсказывал продолжительность времени для элиминации вирусной РНК . [42] Несмотря на сниженные уровни CD4 + , у пациентов с COVID-19 с тяжелым заболеванием были более высокие уровни клеток T h 1 CD4 +, чем у пациентов с умеренным заболеванием. [43]