Надпочечники (также известные как надпочечники ) — это железы внутренней секреции , которые производят различные гормоны, включая адреналин и стероиды альдостерон и кортизол . [1] [2] Они располагаются над почками . Каждая железа имеет внешнюю кору , которая вырабатывает стероидные гормоны , и внутреннюю мозговую оболочку . Сама кора надпочечников делится на три основные зоны: клубочковую зону , пучковую зону и сетчатую зону . [3]
Кора надпочечников вырабатывает три основных типа стероидных гормонов : минералокортикоиды , глюкокортикоиды и андрогены . Минералокортикоиды (такие как альдостерон ), вырабатываемые в клубочковой зоне, помогают регулировать кровяное давление и электролитный баланс . Глюкокортикоиды кортизол и кортизон синтезируются в пучковой зоне; в их функции входит регуляция обмена веществ и подавление иммунной системы . Самый внутренний слой коры головного мозга, сетчатая зона, вырабатывает андрогены, которые преобразуются в полнофункциональные половые гормоны в гонадах и других органах-мишенях. [4] Производство стероидных гормонов называется стероидогенезом и включает в себя ряд реакций и процессов, которые происходят в корковых клетках. [5] Мозговой мозг вырабатывает катехоламины , которые обеспечивают быструю реакцию всего организма в стрессовых ситуациях. [4]
Ряд эндокринных заболеваний сопровождается нарушением функции надпочечников. Перепроизводство кортизола приводит к синдрому Кушинга , тогда как недостаточное производство связано с болезнью Аддисона . Врожденная гиперплазия надпочечников — генетическое заболевание, вызванное нарушением регуляции механизмов эндокринного контроля. [4] [6] Различные опухоли могут возникать из ткани надпочечников и обычно обнаруживаются при медицинской визуализации при поиске других заболеваний. [7]

Надпочечники расположены по обе стороны тела в забрюшинном пространстве , выше и несколько медиальнее почек . У человека правый надпочечник имеет пирамидальную форму, тогда как левый имеет полулунную или серповидную форму и несколько крупнее. [8] Надпочечники имеют длину около 5 см, ширину 3 см и толщину до 1 см. [9] Их общий вес у взрослого человека колеблется от 7 до 10 граммов. [10] Железы желтоватого цвета. [8]
Надпочечники окружены жировой капсулой и лежат внутри почечной фасции , которая также окружает почки. Слабая перегородка (стенка) из соединительной ткани отделяет железы от почек. [11] Надпочечники расположены непосредственно под диафрагмой и прикреплены к ножкам диафрагмы почечной фасцией. [11]
Каждый надпочечник состоит из двух отдельных частей, каждая из которых имеет уникальную функцию: внешнюю кору надпочечников и внутреннюю мозговую оболочку , обе из которых производят гормоны. [12]

Кора надпочечников — это внешняя область, а также самая большая часть надпочечника. Она разделена на три отдельные зоны: клубочковую зону, пучковую зону и сетчатую зону. Каждая зона отвечает за выработку определенных гормонов. Кора надпочечников — это самый внешний слой надпочечников. Внутри коры находятся три слоя, называемые «зонами». При рассмотрении под микроскопом каждый слой имеет свой внешний вид и выполняет разные функции. [13] Кора надпочечников отвечает за выработку гормонов , а именно альдостерона , кортизола и андрогенов . [14]
Самая внешняя зона коры надпочечников — клубочковая зона . Он лежит непосредственно под фиброзной капсулой железы. Клетки этого слоя образуют овальные группы, отделенные тонкими тяжами соединительной ткани от фиброзной капсулы железы и несут широкие капилляры . [15]
Этот слой является основным местом производства альдостерона , минералокортикоида , под действием фермента альдостеронсинтазы . [16] [17] Альдостерон играет важную роль в долгосрочной регуляции артериального давления . [18]
Пучковая зона расположена между клубочковой и сетчатой зонами. Клетки этого слоя ответственны за выработку глюкокортикоидов , таких как кортизол . [19] Это самый большой из трех слоев, на его долю приходится почти 80% объема коры. [3] В пучковой зоне клетки располагаются столбиками, радиально ориентированными к продолговатому мозгу. Клетки содержат многочисленные липидные капли, обильное количество митохондрий и сложную гладкую эндоплазматическую сеть . [15]
Самый внутренний кортикальный слой, сетчатая зона , прилегает непосредственно к продолговатому мозгу. В организме человека он вырабатывает андрогены , в основном дегидроэпиандростерон (ДГЭА), сульфат ДГЭА (ДГЭА-С) и андростенидон (предшественник тестостерона ). [19] Его мелкие клетки образуют неравномерные тяжи и скопления, разделенные капиллярами и соединительной тканью. Клетки содержат относительно небольшое количество цитоплазмы и липидных капель, а иногда содержат коричневый пигмент липофусцин . [15]
Мозговое вещество надпочечников находится в центре каждого надпочечника и окружено корой надпочечников. Хромаффинные клетки мозгового вещества являются основным источником в организме катехоламинов , таких как адреналин и норадреналин, выделяемых мозговым веществом. Здесь секретируется примерно 20% норадреналина (норэпинефрина) и 80% адреналина (эпинефрина). [19]
Мозговое вещество надпочечников приводится в движение симпатической нервной системой через преганглионарные волокна , берущие начало в грудном отделе спинного мозга от позвонков Т5–Т11. [20] Поскольку мозговое вещество надпочечников иннервируется преганглионарными нервными волокнами , его можно рассматривать как специализированный симпатический ганглий . [20] Однако, в отличие от других симпатических ганглиев, мозговое вещество надпочечников не имеет четко выраженных синапсов и выделяет свои секреты непосредственно в кровь.
Надпочечники имеют одну из самых больших скоростей кровоснабжения на грамм ткани любого органа: в каждую железу может входить до 60 мелких артерий . [21] Каждый надпочечник обычно кровоснабжается тремя артериями: [8]
Эти кровеносные сосуды снабжают сеть мелких артерий внутри капсулы надпочечников. Тонкие тяжи капсулы входят в железы, неся к ним кровь. [8]
Венозная кровь оттекает от желез по надпочечным венам , обычно по одной на каждую железу: [8]
Центральная адреномедуллярная вена в мозговом веществе надпочечников представляет собой кровеносный сосуд необычного типа. Ее строение отличается от других вен тем, что гладкая мускулатура ее средней оболочки (среднего слоя сосуда) расположена в виде заметных, продольно ориентированных пучков. [3]
Надпочечники могут вообще не развиваться или сливаться по средней линии позади аорты . [12] Они связаны с другими врожденными аномалиями , такими как задержка развития почек или сращение почек. [12] Железа может развиваться с частичным или полным отсутствием коры или может развиваться в необычном месте. [12]

Надпочечники секретируют ряд различных гормонов, которые метаболизируются ферментами либо внутри железы, либо в других частях тела. Эти гормоны участвуют в ряде важных биологических функций. [23]
Кортикостероиды представляют собой группу стероидных гормонов, вырабатываемых корой надпочечников, от которой они и получили свое название. [24]
Надпочечники вырабатывают альдостерон , минералокортикоид , который играет важную роль в регуляции солевого («минерального») баланса и объема крови . В почках альдостерон действует на дистальные извитые канальцы и собирательные трубочки , увеличивая реабсорбцию натрия и выведение ионов калия и водорода. [18] Альдостерон отвечает за реабсорбцию около 2% отфильтрованного клубочкового фильтрата . [27] Задержка натрия также является реакцией дистального отдела толстой кишки и потовых желез на стимуляцию рецепторов альдостерона. Ангиотензин II и внеклеточный калий являются двумя основными регуляторами продукции альдостерона. [19] Количество натрия, присутствующего в организме, влияет на внеклеточный объем, который, в свою очередь, влияет на кровяное давление . Следовательно, влияние альдостерона на задержку натрия важно для регуляции артериального давления. [28]
Кортизол является основным глюкокортикоидом человека. У видов, которые не вырабатывают кортизол, вместо этого эту роль играет кортикостерон . Глюкокортикоиды оказывают множество эффектов на обмен веществ . Как следует из названия, они повышают уровень глюкозы в крови . Это результат увеличения мобилизации аминокислот из белка и стимуляции синтеза глюкозы из этих аминокислот в печени. Кроме того, они повышают уровень свободных жирных кислот , которые клетки могут использовать в качестве альтернативы глюкозе для получения энергии. Глюкокортикоиды также обладают эффектами, не связанными с регуляцией уровня сахара в крови, включая подавление иммунной системы и мощный противовоспалительный эффект. Кортизол снижает способность остеобластов производить новую костную ткань и снижает всасывание кальция в желудочно-кишечном тракте . [28]
Надпочечники секретируют базальный уровень кортизола, но также могут производить всплески этого гормона в ответ на адренокортикотропный гормон (АКТГ) из передней доли гипофиза . Кортизол высвобождается в течение дня неравномерно – его концентрация в крови максимальна ранним утром и минимальна вечером в результате циркадного ритма секреции АКТГ. [28] Кортизон является неактивным продуктом действия фермента 11β-HSD на кортизол. Реакция, катализируемая 11β-HSD, обратима, что означает, что введенный кортизон может превращаться в кортизол, биологически активный гормон. [28]

У всех кортикостероидных гормонов общим предшественником является холестерин . Следовательно, первым шагом в стероидогенезе является поглощение или синтез холестерина. Клетки, вырабатывающие стероидные гормоны, могут приобретать холестерин двумя путями. Основным источником является пищевой холестерин, транспортируемый кровью в виде эфиров холестерина в составе липопротеинов низкой плотности (ЛПНП). ЛПНП проникают в клетки посредством рецептор-опосредованного эндоцитоза . Другим источником холестерина является его синтез в эндоплазматическом ретикулуме клетки . Синтез может компенсировать аномально низкий уровень ЛПНП. [4] В лизосомах эфиры холестерина превращаются в свободный холестерин, который затем используется для стероидогенеза или хранится в клетке. [29]
В начальном этапе превращения холестерина в стероидные гормоны участвует ряд ферментов семейства цитохрома Р450 , расположенных во внутренней мембране митохондрий . Транспорт холестерина от внешней мембраны к внутренней обеспечивается стероидогенным острым регуляторным белком и является лимитирующей стадией синтеза стероидов. [29]
Слои надпочечников различаются по функциям: каждый слой имеет отдельные ферменты, которые производят разные гормоны из общего предшественника. [4] Первым ферментативным шагом в производстве всех стероидных гормонов является расщепление боковой цепи холестерина, реакция, в результате которой в качестве продукта образуется прегненолон и катализируется ферментом P450scc , также известным как холестерин-десмолаза . После выработки прегненолона специфические ферменты каждого коркового слоя дополнительно его модифицируют. Ферменты, участвующие в этом процессе, включают как митохондриальные, так и микросомальные P450 и гидроксистероиддегидрогеназы . Обычно для образования функциональных гормонов требуется ряд промежуточных этапов, на которых прегненолон несколько раз модифицируется. [5] Ферменты, катализирующие реакции этих метаболических путей, участвуют в ряде эндокринных заболеваний. Например, наиболее распространенная форма врожденной гиперплазии надпочечников развивается в результате дефицита 21-гидроксилазы — фермента, участвующего в промежуточной стадии выработки кортизола. [30]
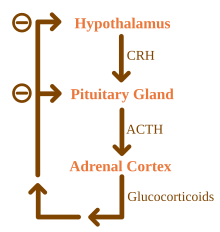
Глюкокортикоиды находятся под регуляторным влиянием оси гипоталамо-гипофиз-надпочечники (ГГН) . Синтез глюкокортикоидов стимулируется адренокортикотропным гормоном (АКТГ), гормоном, выделяемым в кровоток передней долей гипофиза . В свою очередь, выработка АКТГ стимулируется присутствием кортикотропин-рилизинг гормона (CRH), который высвобождается нейронами гипоталамуса . АКТГ действует на клетки надпочечников сначала путем повышения уровня StAR внутри клеток, а затем всех стероидогенных ферментов P450. Ось HPA является примером системы отрицательной обратной связи, в которой кортизол сам по себе действует как прямой ингибитор синтеза как CRH, так и АКТГ. Ось HPA также взаимодействует с иммунной системой посредством увеличения секреции АКТГ в присутствии определенных молекул воспалительного ответа . [4]
Секреция минералокортикоидов регулируется главным образом ренин-ангиотензин-альдостероновой системой (РААС), концентрацией калия и в меньшей степени концентрацией АКТГ. [4] Датчики артериального давления в юкстагломерулярном аппарате почек выделяют в кровь фермент ренин , который запускает каскад реакций, приводящих к образованию ангиотензина II . Рецепторы ангиотензина в клетках клубочковой зоны распознают вещество и при связывании стимулируют высвобождение альдостерона . [31]
Клетки сетчатой зоны надпочечников вырабатывают мужские половые гормоны, или андрогены , наиболее важным из которых является ДГЭА . Как правило, эти гормоны не оказывают общего воздействия на мужской организм и превращаются в более мощные андрогены, такие как тестостерон и ДГТ , или в эстрогены (женские половые гормоны) в половых железах , действуя таким образом как промежуточный продукт метаболизма . [32]
Адреналин и норадреналин , первоначально называемые в Соединенных Штатах адреналином и норадреналином , представляют собой катехоламины , водорастворимые соединения , структура которых состоит из катехоловой группы и аминной группы . Надпочечники отвечают за большую часть адреналина, циркулирующего в организме, но лишь за небольшое количество циркулирующего норадреналина. [23] Эти гормоны выделяются мозговым слоем надпочечников, который содержит густую сеть кровеносных сосудов. Адреналин и норадреналин действуют путем взаимодействия с адренорецепторами по всему телу, что приводит к повышению артериального давления и частоты сердечных сокращений. [23] Действия адреналина и норадреналина отвечают за реакцию «бей или беги» , характеризующуюся учащением дыхания и частоты сердечных сокращений, повышением артериального давления и сужением кровеносных сосудов во многих частях тела. [33]
Катехоламины производятся в хромаффинных клетках мозгового вещества надпочечников из тирозина , заменимой аминокислоты, получаемой с пищей или вырабатываемой из фенилаланина в печени. Фермент тирозингидроксилаза превращает тирозин в L-ДОФА на первом этапе синтеза катехоламинов. L-ДОФА затем преобразуется в дофамин , прежде чем его можно будет превратить в норадреналин. В цитозоле норадреналин превращается в адреналин под действием фермента фенилэтаноламин-N-метилтрансферазы (ПНМТ) и сохраняется в гранулах. Глюкокортикоиды, вырабатываемые в коре надпочечников, стимулируют синтез катехоламинов за счет повышения уровня тирозингидроксилазы и ПНМТ. [4] [13]
Высвобождение катехоламинов стимулируется активацией симпатической нервной системы . Внутренние нервы симпатической нервной системы иннервируют мозговое вещество надпочечников. При активации он вызывает высвобождение катехоламинов из гранул хранения, стимулируя открытие кальциевых каналов в клеточной мембране. [34]
Геном человека включает около 20 000 генов, кодирующих белки, и 70% этих генов экспрессируются в нормальных надпочечниках взрослого человека. [35] [36] Лишь около 250 генов более специфически экспрессируются в надпочечниках по сравнению с другими органами и тканями. Гены, специфичные для надпочечников с самым высоким уровнем экспрессии, включают членов суперсемейства ферментов цитохрома P450 . Соответствующие белки экспрессируются в различных отделах надпочечников, например CYP11A1 , HSD3B2 и FDX1 , участвующие в синтезе стероидных гормонов и экспрессируемые в слоях корковых клеток, а также PNMT и DBH , участвующие в синтезе норадреналина и адреналина и экспрессируемые в мозговом веществе. [37]
Надпочечники состоят из двух гетерогенных типов тканей. В центре находится мозговое вещество надпочечников , которое вырабатывает адреналин и норадреналин и выбрасывает их в кровоток, как часть симпатической нервной системы . Продолговатый мозг окружает кора головного мозга , которая вырабатывает различные стероидные гормоны . Эти ткани происходят от разных эмбриональных предшественников и имеют разные пути внутриутробного развития . Кора надпочечников происходит из мезодермы , тогда как мозговой слой происходит из нервного гребня , имеющего эктодермальное происхождение. [12]
Надпочечники у новорожденного ребенка значительно больше по отношению к размеру тела, чем у взрослого. [38] Например, в возрасте трех месяцев железы в четыре раза превышают размер почек. Размеры желез относительно уменьшаются после рождения, главным образом за счет сморщивания коры. Кора головного мозга, почти полностью исчезающая к 1 году жизни, снова развивается с 4–5 лет. Железы весят около1 грамм при рождении [12] и развиваются до веса взрослого человека околоПо 4 грамма . [28] У плода железы впервые обнаруживаются после шестой недели развития. [12]
Ткань коры надпочечников происходит из промежуточной мезодермы . Впервые он появляется через 33 дня после оплодотворения , демонстрирует способность вырабатывать стероидные гормоны к восьмой неделе и подвергается быстрому росту в течение первого триместра беременности. Кора надпочечников плода отличается от своего взрослого аналога, поскольку она состоит из двух отдельных зон: внутренней «фетальной» зоны, которая несет большую часть гормонпродуцирующей активности, и внешней «дефинитивной» зоны, которая находится в пролиферативном состоянии . фаза. Зона плода вырабатывает большое количество надпочечниковых андрогенов (мужских половых гормонов), которые используются плацентой для биосинтеза эстрогенов . [39] Корковое развитие надпочечников регулируется в основном АКТГ , гормоном, вырабатываемым гипофизом и стимулирующим синтез кортизола . [40] В середине беременности зона плода занимает большую часть коркового объема и производит 100–200 мг/день ДГЭА-С , андрогена и предшественника как андрогенов, так и эстрогенов (женских половых гормонов). [41] Гормоны надпочечников, особенно глюкокортикоиды , такие как кортизол, необходимы для внутриутробного развития органов, особенно для созревания легких . Надпочечники уменьшаются в размерах после рождения из-за быстрого исчезновения плодной зоны с соответствующим снижением секреции андрогенов. [39]
В раннем детстве синтез и секреция андрогенов остаются низкими, но за несколько лет до полового созревания (с 6–8 лет) происходят изменения как в анатомических, так и в функциональных аспектах корковой продукции андрогенов, которые приводят к увеличению секреции стероидов ДГЭА и ДГЭА-С . Эти изменения являются частью процесса, называемого адренархе , который описан только у людей и некоторых других приматов. Адренархе не зависит от АКТГ или гонадотропинов и коррелирует с прогрессирующим утолщением слоя сетчатой оболочки коры. Функционально адренархе обеспечивает источник андрогенов для развития подмышечных и лобковых волос до начала полового созревания. [42] [43]
Мозговое вещество надпочечников происходит из клеток нервного гребня , которые происходят из слоя эктодермы эмбриона . Эти клетки мигрируют из своего исходного положения и агрегируются вблизи дорсальной аорты , примитивного кровеносного сосуда, который активирует дифференцировку этих клеток посредством высвобождения белков, известных как BMP . Эти клетки затем подвергаются второй миграции из дорсальной аорты, образуя мозговое вещество надпочечников и другие органы симпатической нервной системы . [44] Клетки мозгового вещества надпочечников называются хромаффинными клетками , поскольку они содержат гранулы, окрашивающиеся солями хрома , что характерно не для всех симпатических органов. Когда-то считалось, что глюкокортикоиды , вырабатываемые в коре надпочечников, ответственны за дифференцировку хромаффинных клеток. Более поздние исследования показывают, что BMP-4, секретируемый в ткани надпочечников, является основной причиной этого, и что глюкокортикоиды играют роль только в последующем развитии клеток. [45]
Нормальная функция надпочечников может быть нарушена из-за таких заболеваний, как инфекции, опухоли, генетические нарушения и аутоиммунные заболевания , а также в результате побочного эффекта медикаментозной терапии. Эти нарушения поражают железу либо напрямую (как при инфекциях или аутоиммунных заболеваниях), либо в результате нарушения регуляции выработки гормонов (как при некоторых типах синдрома Кушинга ), что приводит к избытку или недостаточности гормонов надпочечников и связанным с ними симптомам.
Синдром Кушинга – проявление избытка глюкокортикоидов. Это может быть результатом длительного лечения глюкокортикоидами или быть вызвано основным заболеванием, которое вызывает изменения в оси HPA или выработку кортизола. Причины можно разделить на АКТГ -зависимые и АКТГ-независимые. Наиболее распространенной причиной эндогенного синдрома Кушинга является аденома гипофиза , вызывающая чрезмерную выработку АКТГ. Заболевание вызывает широкий спектр признаков и симптомов, включая ожирение, диабет, повышенное кровяное давление, чрезмерное оволосение тела ( гирсутизм ), остеопороз , депрессию и, что наиболее характерно, растяжки на коже, вызванные ее прогрессирующим истончением. [4] [6]
Когда клубочковая зона вырабатывает избыток альдостерона , возникает первичный альдостеронизм . Причинами этого состояния являются двусторонняя гиперплазия (чрезмерный рост тканей) желез или аденомы , продуцирующие альдостерон (состояние, называемое синдромом Конна ). Первичный альдостеронизм вызывает гипертонию и электролитный дисбаланс, увеличивая задержку натрия при истощении калия . [6]
Надпочечниковая недостаточность (дефицит глюкокортикоидов ) встречается примерно у 5 из 10 000 населения в целом. [6] Заболевания, классифицируемые как первичная надпочечниковая недостаточность (включая болезнь Аддисона и генетические причины), непосредственно поражают кору надпочечников. Если проблема, затрагивающая ось гипоталамо-гипофиз-надпочечники, возникает за пределами железы, это вторичная недостаточность надпочечников .

Болезнь Аддисона относится к первичному гипоадренализму, который представляет собой дефицит продукции глюкокортикоидов и минералокортикоидов надпочечниками. В западном мире болезнь Аддисона чаще всего является аутоиммунным заболеванием, при котором организм вырабатывает антитела против клеток коры надпочечников. Во всем мире заболевание чаще вызывается инфекцией, особенно туберкулезом . Отличительной особенностью болезни Аддисона является гиперпигментация кожи, которая проявляется другими неспецифическими симптомами, такими как усталость. [4]
Осложнением, наблюдаемым при нелеченой болезни Аддисона и других типах первичной надпочечниковой недостаточности, является надпочечниковый криз , неотложная медицинская помощь , при которой низкие уровни глюкокортикоидов и минералокортикоидов приводят к гиповолемическому шоку и таким симптомам, как рвота и лихорадка. Надпочечниковый криз может постепенно привести к ступору и коме . [4] Лечение кризов надпочечников включает применение инъекций гидрокортизона . [46]
При вторичной надпочечниковой недостаточности дисфункция гипоталамо -гипофизарно-надпочечниковой оси приводит к снижению стимуляции коры надпочечников. Помимо подавления оси глюкокортикоидной терапией, наиболее частой причиной вторичной надпочечниковой недостаточности являются опухоли, влияющие на выработку адренокортикотропного гормона (АКТГ) гипофизом . [6] Этот тип надпочечниковой недостаточности обычно не влияет на выработку минералокортикоидов , которые вместо этого регулируются ренин -ангиотензиновой системой . [4]
Врожденная гиперплазия надпочечников — семейство врожденных заболеваний , при которых мутации ферментов, вырабатывающих стероидные гормоны, приводят к дефициту глюкокортикоидов и нарушению работы петли отрицательной обратной связи оси HPA . В оси HPA кортизол (глюкокортикоид) ингибирует высвобождение CRH и АКТГ , гормонов, которые, в свою очередь, стимулируют синтез кортикостероидов. Поскольку кортизол не может синтезироваться, эти гормоны высвобождаются в больших количествах и вместо этого стимулируют выработку других стероидов надпочечников. Наиболее распространенная форма врожденной гиперплазии надпочечников обусловлена дефицитом 21-гидроксилазы . 21-гидроксилаза необходима для производства как минералокортикоидов, так и глюкокортикоидов, но не андрогенов . Следовательно, стимуляция коры надпочечников АКТГ вызывает выброс избыточного количества надпочечниковых андрогенов , что может привести к развитию неоднозначных гениталий и вторичных половых признаков . [30]

Опухоли надпочечников обычно обнаруживаются как инциденталомы , неожиданные бессимптомные опухоли , обнаруживаемые при медицинской визуализации . Они наблюдаются примерно в 3,4% случаев КТ [7] и в большинстве случаев представляют собой доброкачественные аденомы . [48] Карциномы надпочечников встречаются очень редко, с частотой 1 случай на миллион в год. [4]
Феохромоцитомы — опухоли мозгового слоя надпочечников, развивающиеся из хромаффинных клеток . Они могут вызывать различные неспецифические симптомы, включая головные боли, потливость, беспокойство и сердцебиение . Общие признаки включают гипертонию и тахикардию . Хирургическое вмешательство, особенно лапароскопия надпочечников , является наиболее распространенным методом лечения небольших феохромоцитом. [49]
Бартоломео Эстачи , итальянскому анатому, приписывают первое описание надпочечников в 1563–1564 годах. [50] [51] [52] Однако эти публикации были частью папской библиотеки и не получили общественного внимания, которое впервые было получено с иллюстрациями Каспара Бартолина Старшего в 1611 году . [51]
Надпочечники названы в честь своего расположения относительно почек. Термин «надпочечники» происходит от латинского ad – «около» и ren – «почка». [53] Точно так же слово «супраренальный», как его назвал Жан Риолан Младший в 1629 году, происходит от латинского supra , «над», и ren , «почка». Надпочечная природа желез не была по-настоящему принята до 19 века, когда анатомы выяснили беспротоковую природу желез и их вероятную секреторную роль - до этого велись некоторые споры о том, действительно ли железы являются надпочечными или являются частью надпочечников. почка. [51]
Одна из наиболее известных работ по надпочечникам появилась в 1855 году с публикацией английского врача Томаса Аддисона « О конституциональных и местных эффектах заболевания надпочечниковой капсулы» . В своей монографии Аддисон описал то, что французский врач Жорж Труссо позже назвал болезнью Аддисона , эпонимом, который до сих пор используется для обозначения состояния надпочечниковой недостаточности и связанных с ней клинических проявлений. [54] В 1894 году английские физиологи Джордж Оливер и Эдвард Шафер изучали действие экстрактов надпочечников и наблюдали их прессорные эффекты. В последующие десятилетия несколько врачей экспериментировали с экстрактами коры надпочечников для лечения болезни Аддисона. [50] Эдвард Кэлвин Кендалл , Филип Хенч и Тадеуш Райхштейн были удостоены Нобелевской премии по физиологии и медицине 1950 года за открытия в области структуры и воздействия гормонов надпочечников. [55]
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ){{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка )