

Протеасомы – это белковые комплексы , которые расщепляют ненужные или поврежденные белки путем протеолиза – химической реакции , разрывающей пептидные связи . Ферменты , которые помогают таким реакциям, называются протеазами .
Протеасомы являются частью основного механизма, с помощью которого клетки регулируют концентрацию определенных белков и разрушают неправильно свернутые белки . Белки помечены для деградации небольшим белком, называемым убиквитином . Реакция мечения катализируется ферментами, называемыми убиквитинлигазами . Как только белок помечен одной молекулой убиквитина, это сигнал для других лигаз о присоединении дополнительных молекул убиквитина. В результате образуется полиубиквитиновая цепь , которая связывается с протеасомой, что позволяет ей разрушать меченый белок. [1] В результате процесса деградации образуются пептиды длиной около семи-восьми аминокислот , которые затем можно разложить на более короткие аминокислотные последовательности и использовать при синтезе новых белков. [1]
Протеасомы обнаружены внутри всех эукариот и архей , а также у некоторых бактерий . У эукариот протеасомы расположены как в ядре , так и в цитоплазме . [2]
По структуре протеасома представляет собой цилиндрический комплекс, содержащий «ядро» из четырех уложенных друг на друга колец, образующих центральную пору. Каждое кольцо состоит из семи отдельных белков. Два внутренних кольца состоят из семи β-субъединиц , которые содержат от трех до семи активных центров протеазы . Эти сайты расположены на внутренней поверхности колец, так что целевой белок должен войти в центральную пору, прежде чем он разрушится. Каждое из двух внешних колец содержит по семь α-субъединиц , функция которых заключается в поддержании «ворот», через которые белки попадают в ствол. Эти α-субъединицы контролируются путем связывания с «кэп»-структурами или регуляторными частицами , которые распознают полиубиквитиновые метки, прикрепленные к белковым субстратам, и инициируют процесс деградации. Общая система убиквитинирования и протеасомной деградации известна как система убиквитин-протеасома . [3]
Путь протеасомной деградации важен для многих клеточных процессов, включая клеточный цикл , регуляцию экспрессии генов и реакцию на окислительный стресс . Важность протеолитической деградации внутри клеток и роль убиквитина в протеолитических путях была признана при присуждении Нобелевской премии по химии 2004 года Аарону Чехановеру , Авраму Гершко и Ирвину Роузу . [4]
До открытия системы убиквитин-протеасома считалось, что деградация белков в клетках происходит главным образом за счет лизосом , мембраносвязанных органелл с кислой и заполненной протеазами внутренней частью, которые могут разлагать, а затем перерабатывать экзогенные белки и старые или поврежденные органеллы. [1] Однако работа Джозефа Этлингера и Альфреда Л. Голдберга в 1977 году по АТФ-зависимой деградации белков в ретикулоцитах , у которых отсутствуют лизосомы, предположила наличие второго механизма внутриклеточной деградации. [5] В 1978 году было показано, что он состоит из нескольких отдельных белковых цепей, что было новинкой среди протеаз того времени. [6] Более поздние работы по модификации гистонов привели к идентификации неожиданной ковалентной модификации белка-гистона за счет связи между лизиновой боковой цепью гистона и C-концевым глициновым остатком убиквитина , белка, функция которого неизвестна. . [7] Затем было обнаружено, что ранее идентифицированный белок, связанный с протеолитической деградацией, известный как АТФ-зависимый фактор протеолиза 1 (APF-1), был тем же белком, что и убиквитин. [8] Протеолитическая активность этой системы была выделена в виде мультибелкового комплекса, первоначально названного Шервином Уилком и Мэрион Орловски мультикаталитическим протеиназным комплексом. [9] Позже был открыт АТФ -зависимый протеолитический комплекс, ответственный за убиквитин-зависимую деградацию белков, который получил название 26S протеасома. [10] [11]
Большая часть ранних работ, приведших к открытию протеасомной системы убиквитина, была проведена в конце 1970-х и начале 1980-х годов в Технионе в лаборатории Аврама Гершко , где Аарон Чехановер работал аспирантом. Годовой творческий отпуск Хершко в лаборатории Ирвина Роуза в онкологическом центре Фокс Чейз позволил ему получить ключевые концептуальные идеи, хотя позже Роуз преуменьшил свою роль в этом открытии. [12] Эти трое разделили Нобелевскую премию по химии 2004 года за работу по открытию этой системы. [4]
Хотя данные электронной микроскопии , раскрывающие многоуровневую кольцевую структуру протеасомы, стали доступны в середине 1980-х годов, [13] первая структура коровой частицы протеасомы не была решена с помощью рентгеновской кристаллографии до 1994 года . [14] В 2018 году Первые атомные структуры голофермента 26S протеасомы человека в комплексе с полиубиквитилированным белковым субстратом были решены с помощью криогенной электронной микроскопии , выявив механизмы, с помощью которых субстрат распознается, деубиквитилируется, разворачивается и расщепляется 26S протеасомой человека. [15]
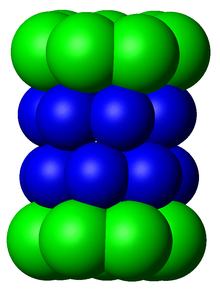
Субкомпоненты протеасом часто обозначаются их коэффициентом седиментации Сведберга (обозначается S ). Протеасома, наиболее часто используемая у млекопитающих, - это цитозольная 26S протеасома, молекулярная масса которой составляет около 2000 килодальтон (кДа), содержащая одну субъединицу белка 20S и две субъединицы регуляторного кэпа 19S. Ядро полое и представляет собой закрытую полость, в которой разлагаются белки; отверстия на двух концах ядра позволяют проникать целевому белку. Каждый конец сердцевинной частицы связан с регуляторной субъединицей 19S, которая содержит несколько активных сайтов АТФазы и сайтов связывания убиквитина; именно эта структура распознает полиубиквитинированные белки и переносит их в каталитическое ядро. [15] Альтернативная форма регуляторной субъединицы, называемая частицей 11S, может связываться с ядром практически таким же образом, как и частица 19S; 11S может играть роль в деградации чужеродных пептидов, например, тех, которые образуются после заражения вирусом . [16]
Количество и разнообразие субъединиц, содержащихся в коровой частице 20S, зависит от организма; число отдельных и специализированных субъединиц больше у многоклеточных, чем у одноклеточных организмов, и больше у эукариот, чем у прокариот. Все частицы 20S состоят из четырех сложенных друг на друга гептамерных кольцевых структур, которые сами состоят из двух разных типов субъединиц; α-субъединицы имеют структурную природу, тогда как β-субъединицы преимущественно каталитические . Субъединицы α представляют собой псевдоферменты , гомологичные субъединицам β. Они собраны так, что их N-концы примыкают к концам β-субъединиц. [17] Два внешних кольца в стопке состоят из семи α-субъединиц каждое, которые служат стыковочными доменами для регуляторных частиц, а N-концы альфа-субъединиц ( Pfam PF10584) образуют ворота, которые блокируют нерегулируемый доступ субстратов во внутреннюю полость. . [18] Каждое из двух внутренних колец состоит из семи β-субъединиц, а на их N-концах содержатся активные центры протеазы, которые выполняют реакции протеолиза. [19] В очищенном комплексе были идентифицированы три различные каталитические активности: химотрипсиноподобная, трипсинподобная и пептидилглутамилпептидная гидролизующая. [20] Размер протеасомы относительно консервативен и составляет около 150 ангстрем (Å) на 115 Å. Ширина внутренней камеры не превышает 53 Å, хотя вход может достигать 13 Å, что позволяет предположить, что для входа белки-субстраты должны быть хотя бы частично развернуты. [21]
У архей , таких как Thermoplasma acidophilum , все α- и все β-субъединицы идентичны, тогда как эукариотические протеасомы, такие как протеасомы дрожжей, содержат семь различных типов каждой субъединицы. У млекопитающих субъединицы β1, β2 и β5 являются каталитическими; хотя они имеют общий механизм, они имеют три различные субстратные специфичности: химотрипсиноподобные , трипсиноподобные и гидролизующие пептидилглутамилпептид (PHGH). [22] Альтернативные β-формы, обозначаемые β1i, β2i и β5i, могут экспрессироваться в гемопоэтических клетках в ответ на воздействие провоспалительных сигналов , таких как цитокины , в частности, гамма-интерферон . Протеасома, собранная с этими альтернативными субъединицами, известна как иммунопротеасома , чья субстратная специфичность изменена по сравнению с нормальной протеасомой. [21] Недавно в клетках человека была обнаружена альтернативная протеасома, в которой отсутствует основная субъединица α3. [23] Эти протеасомы (известные как протеасомы α4-α4) вместо этого образуют коровые частицы 20S, содержащие дополнительную субъединицу α4 вместо отсутствующей субъединицы α3. Ранее было известно, что эти альтернативные протеасомы «α4-α4» существуют у дрожжей. [24] Хотя точная функция этих изоформ протеасом до сих пор в значительной степени неизвестна, клетки, экспрессирующие эти протеасомы, демонстрируют повышенную устойчивость к токсичности, вызванной ионами металлов, таких как кадмий. [23] [25]
Частица 19S у эукариот состоит из 19 отдельных белков и делится на две части: основание из 9 субъединиц, которое непосредственно связывается с α-кольцом коровой частицы 20S, и крышку из 10 субъединиц. Шесть из девяти основных белков представляют собой субъединицы АТФазы из семейства ААА, и у архей существует эволюционный гомолог этих АТФаз, называемый PAN (нуклеотидаза, активирующая протеасомы). [26] Ассоциация частиц 19S и 20S требует связывания АТФ с субъединицами 19S АТФазы, а гидролиз АТФ необходим для собранного комплекса для разрушения свернутых и убиквитинированных белков. Обратите внимание, что только стадия разворачивания субстрата требует энергии гидролиза АТФ, тогда как одно лишь связывание АТФ может поддерживать все остальные этапы, необходимые для деградации белка (например, сборку комплекса, открытие ворот, транслокацию и протеолиз). [27] [28] Фактически, связывание АТФ с АТФазами само по себе поддерживает быструю деградацию развернутых белков. Однако, хотя гидролиз АТФ необходим только для разворачивания, пока неясно, можно ли использовать эту энергию для сопряжения некоторых из этих стадий. [28] [29]

В 2012 году две независимые попытки выяснили молекулярную архитектуру протеасомы 26S с помощью одночастичной электронной микроскопии . [31] [32] В 2016 году три независимых усилия определили первую структуру человеческой 26S протеасомы с почти атомным разрешением в отсутствие субстратов с помощью крио-ЭМ. [33] [34] [35] В 2018 году были предприняты значительные усилия для выяснения детальных механизмов деубиквитилирования, инициации транслокации и процессивного разворачивания субстратов путем одновременного определения семи атомных структур субстрат-задействованной 26S протеасомы. [15] В сердце 19S, непосредственно примыкающем к 20S, находятся ААА-АТФазы ( белки ААА ), которые собираются в гетерогексамерное кольцо порядка Rpt1/Rpt2/Rpt6/Rpt3/Rpt4/Rpt5. Это кольцо представляет собой тример димеров: Rpt1/Rpt2, Rpt6/Rpt3 и Rpt4/Rpt5 димеризуются через свои N-концевые спиральные спирали. Эти спиральные катушки выступают из гексамерного кольца. Самые крупные регуляторные частицы, не относящиеся к АТФазам, Rpn1 и Rpn2, связываются с кончиками Rpt1/2 и Rpt6/3 соответственно. Убиквитиновый рецептор Rpn13 связывается с Rpn2 и завершает базовый подкомплекс. Крышка покрывает половину гексамера ААА-АТФазы (Rpt6/Rpt3/Rpt4) и неожиданно напрямую контактирует с 20S через Rpn6 и в меньшей степени Rpn5. Субъединицы Rpn9, Rpn5, Rpn6, Rpn7, Rpn3 и Rpn12, структурно родственные между собой и субъединицам комплекса COP9 и eIF3 (поэтому называемые субъединицами PCI), собираются в подковообразную структуру, включающую гетеродимер Rpn8/Rpn11. Rpn11, деубиквитинирующий фермент , помещается в устье гексамера ААА-АТФазы и идеально расположен для удаления фрагментов убиквитина непосредственно перед транслокацией субстратов в 20S. Второй идентифицированный на сегодняшний день убиквитиновый рецептор, Rpn10, расположен на периферии века, рядом с субъединицами Rpn8 и Rpn9.
Регуляторная частица 19S в составе голофермента 26S протеасомы наблюдалась в шести сильно различающихся конформационных состояниях в отсутствие субстратов. [36] [37] Отличительной чертой конфигурации ААА-АТФазы в этом преобладающем низкоэнергетическом состоянии является расположение ААА-доменов в виде лестницы или шайбы. [30] [31] В присутствии АТФ , но в отсутствие субстрата, принимаются три альтернативные, менее распространенные конформации 19S, отличающиеся главным образом расположением крышки по отношению к модулю ААА-АТФазы. [33] [37] В присутствии АТФ-γS или субстрата наблюдалось значительно больше конформаций, демонстрирующих резкие структурные изменения модуля ААА-АТФазы. [15] [36] [38] [39] Некоторые из связанных с субстратом конформаций имеют большое сходство с конформациями, не содержащими субстрата, но они не полностью идентичны, особенно в модуле AAA-АТФазы. [15] [36] До сборки 26S регуляторная частица 19S в свободной форме также наблюдалась в семи конформационных состояниях. [40] Примечательно, что все эти конформеры несколько отличаются и имеют различные особенности. Таким образом, регуляторная частица 19S может выбирать по меньшей мере 20 конформационных состояний в различных физиологических условиях.

Регуляторная частица 19S отвечает за стимулирование 20S к расщеплению белков. Основная функция регуляторных АТФаз 19S — открыть ворота в 20S, которые блокируют вход субстратов в камеру разложения. [41] Недавно был выяснен механизм, с помощью которого протеасомальная АТФаза открывает эти ворота. [18] Для открытия ворот 20S и, следовательно, для деградации субстрата необходимы С-концы протеасомальных АТФаз, которые содержат специфический мотив (т.е. мотив HbYX). С-концы АТФазы связываются с карманами в верхней части 20S и привязывают комплекс АТФазы к протеолитическому комплексу 20S, таким образом соединяя оборудование для разворачивания субстрата с механизмом деградации 20S. Связывание этих С-концов с карманами 20S само по себе стимулирует открытие ворот в 20S почти так же, как «ключ в замке» открывает дверь. [18] Точный механизм, с помощью которого функционирует этот механизм «ключ в замке», был структурно выяснен в контексте человеческой 26S протеасомы с почти атомным разрешением, что позволяет предположить, что вставка пяти С-концев субъединиц АТФазы Rpt1 /2/3/5/6 в поверхностные карманы 20S необходимы для полного открытия ворот 20S. [36] [15] [33]
20S протеасомы также могут ассоциироваться со вторым типом регуляторных частиц, 11S регуляторными частицами, гептамерной структурой, которая не содержит АТФаз и может способствовать деградации коротких пептидов , но не полных белков. Предполагается, что это связано с тем, что комплекс не может разворачивать более крупные субстраты. Эта структура также известна как PA28, REG или PA26. [17] Механизмы, с помощью которых он связывается с основной частицей через C-концевые хвосты ее субъединиц и вызывает конформационные изменения α-кольца , открывающие ворота 20S, предполагают аналогичный механизм для частицы 19S. [42] Экспрессия частицы 11S индуцируется гамма-интерфероном и вместе с β-субъединицами иммунопротеасомы отвечает за образование пептидов, которые связываются с главным комплексом гистосовместимости . [16]
Еще одним типом регуляторных частиц, не связанных с АТФазой, является Blm10 (дрожжи) или PA200/ PSME4 (человеческий). Он открывает только одну α-субъединицу в воротах 20S и сам сворачивается в купол с очень маленькой порой над ним. [17]
Сборка протеасомы представляет собой сложный процесс из-за количества субъединиц, которые должны объединиться для образования активного комплекса. Субъединицы β синтезируются с N-концевыми «пропептидами», которые посттрансляционно модифицируются во время сборки частицы 20S, чтобы обнажить протеолитический активный центр. Частица 20S собрана из двух полупротеасом, каждая из которых состоит из семичленного про-β-кольца, присоединенного к семичленному α-кольцу. Объединение β-колец двух полупротеасом запускает треонин -зависимый аутолиз пропептидов с обнажением активного центра. Эти β-взаимодействия опосредуются главным образом солевыми мостиками и гидрофобными взаимодействиями между консервативными альфа-спиралями , разрушение которых в результате мутации повреждает способность протеасомы к сборке. [43] Сборка полупротеасом, в свою очередь, инициируется сборкой α-субъединиц в их гептамерное кольцо, образуя матрицу для ассоциации соответствующего про-β-кольца. Сборка α-субъединиц не охарактеризована. [44]
Лишь недавно процесс сборки регуляторной частицы 19S был в значительной степени выяснен. Регуляторная частица 19S состоит из двух отдельных подкомпонентов: основания и крышки. Сборке базового комплекса способствуют четыре шаперона сборки : Hsm3/S5b, Nas2/p27, Rpn14/PAAF1 и Nas6/ ганкирин (названия дрожжей/млекопитающих). [45] Эти шапероны сборки связываются с субъединицами ААА- АТФазы , и их основная функция, по-видимому, заключается в обеспечении правильной сборки гетерогексамерного кольца ААА- АТФазы . На сегодняшний день все еще обсуждается, собирается ли базовый комплекс отдельно, шаблонируется ли сборка основной частицей 20S или существуют ли альтернативные пути сборки. В дополнение к четырем шаперонам сборки, деубиквитинирующий фермент Ubp6/Usp14 также способствует сборке оснований, но это не является существенным. [46] Крышка собирается отдельно в определенном порядке и не требует сопровождающих для сборки. [47]

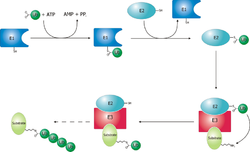
Белки подвергаются деградации протеасомой с ковалентной модификацией остатка лизина, что требует скоординированных реакций трех ферментов . На первом этапе фермент, активирующий убиквитин (известный как E1), гидролизует АТФ и аденилирует молекулу убиквитина . Затем он переносится на остаток цистеина в активном центре E1 одновременно с аденилированием второго убиквитина. [48] Этот аденилированный убиквитин затем переносится на цистеин второго фермента, убиквитин-конъюгирующего фермента (E2). На последнем этапе член весьма разнообразного класса ферментов, известных как убиквитинлигазы (Е3), распознает конкретный белок, подлежащий убиквитинированию, и катализирует перенос убиквитина от Е2 к этому белку-мишени. Целевой белок должен быть помечен как минимум четырьмя мономерами убиквитина (в форме полиубиквитиновой цепи), прежде чем он будет распознан крышкой протеасомы. [49] Таким образом, именно E3 придает субстратную специфичность этой системе. [50] Количество экспрессируемых белков E1, E2 и E3 зависит от организма и типа клеток, но у человека присутствует множество различных ферментов E3, что указывает на огромное количество мишеней для протеасомной системы убиквитина.
Механизм, с помощью которого полиубиквитинированный белок попадает в протеасому, до конца не изучен. Несколько снимков с высоким разрешением протеасомы, связанной с полиубиквитинированным белком, позволяют предположить, что убиквитиновые рецепторы могут координироваться с деубиквитиназой Rpn11 для первоначального нацеливания и взаимодействия с субстратом. [15] Белки убиквитиновых рецепторов имеют N-концевой убиквитин-подобный (UBL) домен и один или несколько убиквитин-ассоциированных (UBA) доменов. Домены UBL распознаются кэпами 19S протеасомы, а домены UBA связывают убиквитин посредством трехспиральных пучков . Эти рецепторные белки могут сопровождать полиубиквитинированные белки к протеасоме, хотя особенности этого взаимодействия и его регуляции неясны. [51]
Сам белок убиквитин имеет длину 76 аминокислот и получил такое название из-за своей повсеместной природы, поскольку он имеет высококонсервативную последовательность и встречается во всех известных эукариотических организмах. [52] Гены, кодирующие убиквитин у эукариот , расположены в виде тандемных повторов , возможно, из-за тяжелых требований транскрипции этих генов для производства достаточного количества убиквитина для клетки. Было высказано предположение, что убиквитин является самым медленно эволюционирующим белком, обнаруженным на сегодняшний день. [53] Убиквитин содержит семь остатков лизина, с которыми может быть связан другой убиквитин, в результате чего образуются различные типы полиубиквитиновых цепей. [54] Цепи, в которых каждый дополнительный убиквитин связан с лизином 48 предыдущего убиквитина, играют роль в нацеливании на протеасомы, в то время как другие типы цепей могут участвовать в других процессах. [55] [56]
Цепи убиквитина, конъюгированные с белком, предназначенным для протеасомной деградации, обычно удаляются с помощью любого из трех ассоциированных с протеасомами деубиквитилирующих ферментов (DUB), а именно Rpn11, Ubp6/USP14 и UCH37. Этот процесс перерабатывает убиквитин и необходим для поддержания резервуара убиквитина в клетках. [56] Rpn11 является внутренней стехиометрической субъединицей регуляторной частицы 19S и необходим для функционирования протеасомы 26S. Активность DUB Rpn11 повышена в протеасоме по сравнению с его мономерной формой. То, как Rpn11 удаляет убиквитиновую цепь целиком из белкового субстрата, было зафиксировано атомной структурой связанной с субстратом человеческой протеасомы в конформации, названной EB . [15] Интересно, что эта структура также показывает, как активность DUB связана с распознаванием субстрата протеасомальной AAA-АТФазой. В отличие от Rpn11, USP14 и UCH37 представляют собой DUB, которые не всегда связаны с протеасомой. Было обнаружено, что в клетках около 10-40% протеасом связаны с USP14. И Ubp6/USP14, и UCH37 в значительной степени активируются протеасомой и сами по себе проявляют очень низкую активность DUB. Было обнаружено, что после активации USP14 подавляет функцию протеасом за счет своей активности DUB и индуцирования параллельных путей конформационных переходов протеасом, один из которых, как оказалось, напрямую запрещает вставку субстрата в AAA-АТФазу, что интуитивно наблюдалось с помощью криогенной электронной микроскопии с временным разрешением. . [57] Похоже, что USP14 регулирует функцию протеасомы во многих контрольных точках, как каталитически конкурируя с Rpn11, так и аллостерически перепрограммируя состояния AAA-АТФазы, что довольно неожиданно для DUB. [57] Эти наблюдения подразумевают, что регуляция протеасомы может зависеть от ее динамических переходов конформационных состояний.
После убиквитинирования белка он распознается регуляторной частицей 19S на этапе АТФ-зависимого связывания. [15] [28] Затем белок-субстрат должен войти внутрь субъединицы 20S, чтобы войти в контакт с протеолитическими активными центрами. Поскольку центральный канал частицы 20S узок и закрыт N-концевыми хвостами субъединиц α-кольца, субстраты должны быть хотя бы частично развернуты, прежде чем они войдут в ядро. [15] Переход развернутого субстрата в ядро называется транслокацией и обязательно происходит после деубиквитинирования. [15] [28] Однако порядок, в котором субстраты деубиквитинируются и разворачиваются, еще не ясен. [58] Какой из этих процессов является лимитирующей стадией в общей реакции протеолиза, зависит от конкретного субстрата; для некоторых белков процесс разворачивания ограничивает скорость, тогда как деубиквитинирование является самым медленным этапом для других белков. [27] Предполагается, что степень, в которой субстраты должны быть развернуты перед транслокацией, составляет около 20 аминокислотных остатков исходя из атомной структуры задействованной в субстрате 26S протеасомы в состоянии, совместимом с деубиквитилированием, [15] , но с существенной третичной структурой , и в особые нелокальные взаимодействия, такие как дисульфидные связи , достаточны для ингибирования деградации. [59] Также предполагается, что наличие внутренне неупорядоченных белковых сегментов достаточного размера, как на конце белка, так и внутри, способствует эффективному инициированию деградации. [60] [61]
Ворота, образованные α-субъединицами, предотвращают проникновение пептидов длиной более четырех остатков внутрь 20S-частицы. Молекулы АТФ, связанные до начальной стадии узнавания, гидролизуются перед транслокацией. Хотя для разворачивания субстрата необходима энергия, для транслокации она не требуется. [27] [28] Собранная 26S протеасома может разрушать развернутые белки в присутствии негидролизуемого аналога АТФ , но не может разрушать свернутые белки, что указывает на то, что энергия гидролиза АТФ используется для разворачивания субстрата. [27] Прохождение развернутого субстрата через открытые ворота происходит посредством облегченной диффузии, если кэп 19S находится в АТФ-связанном состоянии. [62]
Механизм разворачивания глобулярных белков обязательно общий, но в некоторой степени зависит от аминокислотной последовательности . Было показано , что длинные последовательности чередующихся глицина и аланина ингибируют разворачивание субстрата, снижая эффективность протеасомной деградации; это приводит к высвобождению частично разложенных побочных продуктов, возможно, из-за разделения стадий гидролиза АТФ и разворачивания. [63] Такие глицин-аланиновые повторы также встречаются в природе, например, в фиброине шелка ; в частности, некоторые генные продукты вируса Эпштейна-Барр, несущие эту последовательность, могут останавливать протеасому, помогая вирусу размножаться, предотвращая презентацию антигена в главном комплексе гистосовместимости. [64]
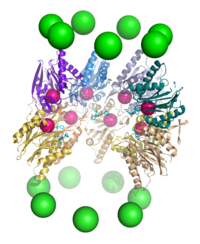
Протеасома функционирует как эндопротеаза . [65] [66] [67] [68] Механизм протеолиза β-субъединиц коровой частицы 20S заключается в треонин-зависимой нуклеофильной атаке . Этот механизм может зависеть от связанной молекулы воды для депротонирования реакционноспособного гидроксила треонина . Деградация происходит внутри центральной камеры, образованной объединением двух β-колец, и обычно не высвобождает частично расщепленные продукты, вместо этого восстанавливая субстрат до коротких полипептидов, обычно длиной 7–9 остатков, хотя их длина может варьироваться от 4 до 25 остатков, в зависимости от организм и субстрат. Биохимический механизм, определяющий длину продукта, полностью не описан. [69] Хотя три каталитические β-субъединицы имеют общий механизм, они имеют несколько разные субстратные специфичности, которые считаются химотрипсиноподобными, трипсиноподобными и пептидил-глутамил-гидролизующими пептидами (PHGH). Эти изменения специфичности являются результатом межатомных контактов с локальными остатками вблизи активных центров каждой субъединицы. Каждая каталитическая β-субъединица также содержит консервативный остаток лизина, необходимый для протеолиза. [22]
Хотя протеасома обычно производит очень короткие пептидные фрагменты, в некоторых случаях эти продукты сами по себе являются биологически активными и функциональными молекулами. Определенные факторы транскрипции, регулирующие экспрессию специфических генов, включая один компонент комплекса NF-κB млекопитающих , синтезируются в виде неактивных предшественников, убиквитинирование которых и последующая протеасомная деградация переводят их в активную форму. Такая активность требует, чтобы протеасома расщепляла белок-субстрат внутри, а не процессивно разрушала его с одного конца. Было высказано предположение, что длинные петли на поверхности этих белков служат субстратами протеасом и входят в центральную полость, тогда как большая часть белка остается снаружи. [70] Подобные эффекты наблюдались в дрожжевых белках; этот механизм избирательной деградации известен как регулируемый убиквитин/протеасомозависимый процессинг (RUP). [71]
Хотя большинство протеосомных субстратов должны быть убиквитинированы перед деградацией, существуют некоторые исключения из этого общего правила, особенно когда протеасома играет нормальную роль в посттрансляционном процессинге белка. Одним из основных примеров является протеасомная активация NF-κB путем процессинга p105 в p50 посредством внутреннего протеолиза. [70] Некоторые белки, которые предположительно нестабильны из-за изначально неструктурированных областей, [72] деградируют убиквитин-независимым способом. Наиболее известным примером убиквитин-независимого протеасомного субстрата является фермент орнитиндекарбоксилаза . [73] Также сообщалось о убиквитин-независимых механизмах, нацеленных на ключевые регуляторы клеточного цикла , такие как р53 , хотя р53 также подвержен убиквитин-зависимой деградации. [74] Наконец, структурно аномальные, неправильно свернутые или сильно окисленные белки также подвергаются убиквитин-независимой и 19S-независимой деградации в условиях клеточного стресса. [75]

Протеасома 20S широко распространена и необходима эукариотам и археям. Бактериальный порядок Actinomycetales также имеет общие гомологи 20S протеасомы, тогда как большинство бактерий обладают генами теплового шока hslV и hslU , чьи генные продукты представляют собой мультимерную протеазу, расположенную в двухслойном кольце, и АТФазу. [76] Было высказано предположение, что белок hslV напоминает вероятного предка 20S протеасомы. [77] В целом, HslV не является существенным для бактерий, и не все бактерии им обладают, тогда как некоторые протисты обладают как 20S, так и системами hslV. [76] Многие бактерии также обладают другими гомологами протеасомы и связанной с ней АТФазы, в первую очередь ClpP и ClpX . Эта избыточность объясняет, почему система HslUV не является необходимой.
Анализ последовательности показывает, что каталитические β-субъединицы разошлись в эволюции раньше, чем преимущественно структурные α-субъединицы. У бактерий, экспрессирующих 20S протеасому, β-субъединицы имеют высокую идентичность последовательности с β-субъединицами архей и эукариот, тогда как идентичность последовательности α значительно ниже. Присутствие 20S протеасом у бактерий может быть результатом латерального переноса генов , тогда как диверсификация субъединиц среди эукариот приписывается множественным событиям дупликации генов . [76]
Развитие клеточного цикла контролируется упорядоченным действием циклин-зависимых киназ (CDK), активируемых специфическими циклинами , которые разграничивают фазы клеточного цикла . Митотические циклины, которые сохраняются в клетке всего несколько минут, имеют один из самых коротких периодов жизни среди всех внутриклеточных белков. [1] После того, как комплекс CDK-циклин выполнил свою функцию, связанный циклин полиубиквитинируется и разрушается протеасомой, что обеспечивает направленность клеточного цикла. В частности, выход из митоза требует протеасомо-зависимой диссоциации регуляторного компонента циклина B от комплекса факторов, способствующих митозу . [78] В клетках позвоночных «проскальзывание» через митотический контрольный пункт, приводящее к преждевременному выходу М-фазы, может произойти, несмотря на задержку этого выхода контрольной точкой веретена . [79]
Более ранние контрольные точки клеточного цикла, такие как проверка точки пострестрикции между фазой G1 и фазой S , аналогичным образом включают протеосомную деградацию циклина А , убиквитинирование которого обеспечивается комплексом , способствующим анафазе (APC), убиквитинлигазой E3 . [80] APC и белковый комплекс Skp1/Cul1/F-box ( комплекс SCF ) являются двумя ключевыми регуляторами деградации циклина и контроля контрольных точек; сам SCF регулируется APC посредством убиквитинирования адаптерного белка Skp2, который предотвращает активность SCF перед переходом G1-S. [81]
Отдельные компоненты частицы 19S выполняют свою регуляторную роль. Ганкирин , недавно идентифицированный онкопротеин , является одним из субкомпонентов 19S, который также прочно связывает циклин-зависимую киназу CDK4 и играет ключевую роль в распознавании убиквитинированного р53 благодаря его сродству к убиквитинлигазе MDM2 . Ганкирин является антиапоптотическим и , как было показано, сверхэкспрессируется в некоторых типах опухолевых клеток, таких как гепатоцеллюлярная карцинома . [82]
Подобно эукариотам, некоторые археи также используют протеасому для контроля клеточного цикла, в частности, путем контроля деления клеток, опосредованного ESCRT -III. [83]
У растений передача сигналов с помощью ауксинов или фитогормонов , которые определяют направление и тропизм роста растений, индуцирует нацеливание на класс репрессоров транскрипционных факторов , известных как белки Aux/IAA, для протеасомной деградации. Эти белки убиквитинируются SCFTIR1 или SCF в комплексе с рецептором ауксина TIR1. Деградация белков Aux/IAA вызывает подавление транскрипционных факторов в семействе факторов ответа на ауксин (ARF) и индуцирует ARF-направленную экспрессию генов. [84] Клеточные последствия активации ARF зависят от типа растения и стадии развития, но они участвуют в управлении ростом корней и жилок листьев. Считается, что специфический ответ на дерепрессию ОПН опосредован специфичностью спаривания отдельных белков АРФ и Aux/IAA. [85]
Как внутренние, так и внешние сигналы могут привести к индукции апоптоза или запрограммированной гибели клеток. Результирующая деконструкция клеточных компонентов в основном осуществляется специализированными протеазами, известными как каспазы , но протеасома также играет важную и разнообразную роль в апоптотическом процессе. Об участии протеасомы в этом процессе свидетельствует как увеличение убиквитинирования белка, так и ферментов Е1, Е2 и Е3, которое наблюдается задолго до апоптоза. [86] [87] [88] Во время апоптоза также наблюдалось перемещение протеасом, локализованных в ядре, на пузыри внешней мембраны , характерные для апоптоза. [89]
Ингибирование протеасом по-разному влияет на индукцию апоптоза в разных типах клеток. В общем, протеасома не требуется для апоптоза, хотя ее ингибирование является проапоптотическим в большинстве изученных типов клеток. Апоптоз опосредован нарушением регулируемой деградации белков клеточного цикла, способствующих росту. [90] Однако некоторые клеточные линии — в частности, первичные культуры покоящихся и дифференцированных клеток , таких как тимоциты и нейроны — не подвергаются апоптозу при воздействии ингибиторов протеасом. Механизм этого эффекта не ясен, но предполагается, что он специфичен для клеток в состоянии покоя или является результатом дифференциальной активности проапоптотической киназы JNK . [91] Способность ингибиторов протеасом индуцировать апоптоз в быстро делящихся клетках была использована в нескольких недавно разработанных химиотерапевтических агентах , таких как бортезомиб и салиноспорамид А.
В ответ на клеточные стрессы, такие как инфекция , тепловой шок или окислительное повреждение , экспрессируются белки теплового шока , которые идентифицируют неправильно свернутые или развернутые белки и нацеливают их на протеосомную деградацию. И Hsp27 , и Hsp90 — белки -шапероны участвуют в повышении активности убиквитин-протеасомной системы, хотя они не являются непосредственными участниками этого процесса. [92] Hsp70 , с другой стороны, связывает открытые гидрофобные участки на поверхности неправильно свернутых белков и привлекает E3 убиквитинлигазы, такие как CHIP, для маркировки белков для протеасомной деградации. [93] Белок CHIP (карбоксильный конец белка, взаимодействующего с Hsp70) сам по себе регулируется посредством ингибирования взаимодействий между ферментом E3 CHIP и его партнером по связыванию E2. [94]
Подобные механизмы существуют, чтобы способствовать деградации окислительно-поврежденных белков через систему протеасом. В частности, протеасомы, локализованные в ядре, регулируются PARP и активно деградируют ненадлежащим образом окисленные гистоны . [95] Окисленные белки, которые часто образуют большие аморфные агрегаты в клетке, могут быть разложены непосредственно под действием коровой частицы 20S без регуляторного колпачка 19S и не требуют гидролиза АТФ или мечения убиквитином. [75] Однако высокий уровень окислительного повреждения увеличивает степень перекрестных связей между фрагментами белка, делая агрегаты устойчивыми к протеолизу. Большие количества и размеры таких сильно окисленных агрегатов связаны со старением . [96]
Нарушение регуляции протеасомной системы убиквитина может способствовать развитию ряда нервных заболеваний. Это может привести к опухолям головного мозга, таким как астроцитомы . [97] При некоторых нейродегенеративных заболеваниях с поздним началом, общим признаком которых является агрегация неправильно свернутых белков, таких как болезнь Паркинсона и болезнь Альцгеймера , могут образовываться большие нерастворимые агрегаты неправильно свернутых белков, которые затем приводят к нейротоксичности посредством механизмов, которые не изучены. но все же хорошо понял. Снижение активности протеасом было предложено как причина агрегации и образования телец Леви при болезни Паркинсона. [98] Эта гипотеза подтверждается наблюдением, что дрожжевые модели болезни Паркинсона более восприимчивы к токсичности α-синуклеина , основного белкового компонента телец Леви, в условиях низкой протеасомной активности. [99] Нарушение протеасомальной активности может лежать в основе когнитивных расстройств, таких как расстройства аутистического спектра , а также заболеваний мышц и нервов, таких как миопатия с включенными тельцами . [97]
Протеасома играет простую, но важную роль в функционировании адаптивной иммунной системы . Пептидные антигены экспонируются белками главного комплекса гистосовместимости класса I (MHC) на поверхности антигенпрезентирующих клеток . Эти пептиды являются продуктами протеасомной деградации белков, образующихся вторгшимся патогеном . Хотя в этом процессе могут участвовать конститутивно экспрессируемые протеасомы, специализированный комплекс, состоящий из белков, экспрессия которых индуцируется гамма-интерфероном , является первичным продуцентом пептидов, оптимальных по размеру и составу для связывания MHC. Эти белки, экспрессия которых увеличивается во время иммунного ответа, включают регуляторную частицу 11S, основная известная биологическая роль которой заключается в регулировании продукции лигандов MHC, а также специализированные β-субъединицы, называемые β1i, β2i и β5i, с измененной субстратной специфичностью. Комплекс, образованный специализированными β-субъединицами, известен как иммунопротеасома . [16] Другая субъединица варианта β5i, β5t, экспрессируется в тимусе, что приводит к образованию специфичной для тимуса « тимопротеасомы », функция которой пока неясна. [100]
Сила связывания лиганда MHC класса I зависит от состава С-конца лиганда , поскольку пептиды связываются за счет водородных связей и тесных контактов с областью, называемой «карманом B» на поверхности MHC. Многие аллели MHC класса I предпочитают гидрофобные С-концевые остатки, а иммунопротеасомный комплекс с большей вероятностью генерирует гидрофобные С-концы. [101]
Благодаря своей роли в генерации активированной формы NF-κB , антиапоптотического и провоспалительного регулятора экспрессии цитокинов , протеасомальная активность связана с воспалительными и аутоиммунными заболеваниями . Повышенные уровни активности протеасом коррелируют с активностью заболевания и связаны с аутоиммунными заболеваниями, включая системную красную волчанку и ревматоидный артрит . [16]
Протеасома также участвует во внутриклеточном антитело-опосредованном протеолизе связанных с антителами вирионов. В этом пути нейтрализации TRIM21 (белок семейства трехчастных мотивов) связывается с иммуноглобулином G , направляя вирион к протеасоме, где он разрушается. [102]
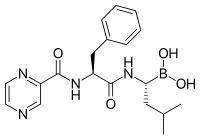
Ингибиторы протеасом обладают эффективной противоопухолевой активностью в культуре клеток , индуцируя апоптоз , нарушая регулируемую деградацию белков клеточного цикла, способствующих росту. [90] Этот подход избирательной индукции апоптоза в опухолевых клетках доказал свою эффективность на животных моделях и в испытаниях на людях.
Лактацистин , природный продукт, синтезируемый бактериями Streptomyces , был первым открытым непептидным ингибитором протеасом [103] и широко используется в качестве исследовательского инструмента в биохимии и клеточной биологии. Лицензия на лактацистин была передана компании Myogenics/Proscript, которая была приобретена компанией Millennium Pharmaceuticals , которая теперь является частью Takeda Pharmaceuticals . Лактацистин ковалентно модифицирует аминоконцевой треонин каталитических β-субъединиц протеасомы, особенно субъединицы β5, ответственной за химотрипсиноподобную активность протеасомы. Это открытие помогло утвердить протеасому как механически новый класс протеаз: аминоконцевую треониновую протеазу .
Бортезомиб (боронатный MG132), молекула, разработанная Millennium Pharmaceuticals и продаваемая под торговой маркой Velcade, является первым ингибитором протеасом, достигшим клинического применения в качестве химиотерапевтического агента. [104] Бортезомиб используется при лечении множественной миеломы . [105] Примечательно, что множественная миелома приводит к повышению уровня пептидов, полученных из протеасом, в сыворотке крови , которые снижаются до нормальных уровней в ответ на успешную химиотерапию. [106] Исследования на животных показали, что бортезомиб также может оказывать клинически значимое воздействие при раке поджелудочной железы . [107] [108] Начаты доклинические и ранние клинические исследования для изучения эффективности бортезомиба в лечении других В-клеточных видов рака, [109] особенно некоторых типов неходжкинской лимфомы . [110] Клинические результаты также, по-видимому, оправдывают использование ингибитора протеасом в сочетании с химиотерапией при остром В-клеточном лимфобластном лейкозе. [111] Ингибиторы протеасом могут убивать некоторые типы культивируемых лейкозных клеток, устойчивых к глюкокортикоидам. [112]
Молекула ритонавир , продаваемая как Норвир, была разработана как ингибитор протеазы и использовалась для борьбы с ВИЧ- инфекцией. Однако было показано, что он ингибирует протеасомы, а также свободные протеазы; а именно, ритонавир ингибирует химотрипсин -подобную активность протеасомы, тогда как трипсин -подобная активность несколько усиливается. [113] Исследования на животных моделях показывают, что ритонавир может оказывать ингибирующее действие на рост клеток глиомы . [114]
Ингибиторы протеасом также показали многообещающую эффективность в лечении аутоиммунных заболеваний на животных моделях. Например, исследования на мышах с трансплантатами человеческой кожи обнаружили уменьшение размера поражений псориаза после лечения ингибитором протеасом. [115] Ингибиторы также показывают положительные эффекты на моделях астмы на грызунах . [116]
Мечение и ингибирование протеасом также представляют интерес в лабораторных условиях для изучения протеасомной активности в клетках как in vitro , так и in vivo . Наиболее часто используемыми лабораторными ингибиторами являются лактацистин и пептидный альдегид MG132, первоначально разработанный лабораторией Голдберга. Также были разработаны флуоресцентные ингибиторы для специфической маркировки активных участков собранной протеасомы. [117]
Протеасома и ее субъединицы имеют клиническое значение по крайней мере по двум причинам: (1) нарушенная комплексная сборка или дисфункциональная протеасома могут быть связаны с основной патофизиологией конкретных заболеваний и (2) они могут использоваться в качестве мишеней для лекарственных средств для терапевтических целей. вмешательства. Совсем недавно были предприняты дополнительные усилия по рассмотрению протеасом для разработки новых диагностических маркеров и стратегий. Улучшенное и всестороннее понимание патофизиологии протеасом должно привести к их клиническому применению в будущем.
Протеасомы образуют ключевой компонент системы убиквитин-протеасома (UPS) [118] и соответствующего контроля качества клеточного белка (PQC). Убиквитинирование белка и последующий протеолиз и деградация протеасомой являются важными механизмами регуляции клеточного цикла , роста и дифференцировки клеток , транскрипции генов, передачи сигнала и апоптоза . [119] Дефекты протеасом приводят к снижению протеолитической активности и накоплению поврежденных или неправильно свернутых белков, что может способствовать нейродегенеративным заболеваниям, [120] [121] сердечно-сосудистым заболеваниям, [122] [123] [124] воспалительным реакциям и аутоиммунным заболеваниям, [125] и системные реакции на повреждение ДНК, приводящие к злокачественным новообразованиям . [126]
Исследования показали участие дефектов ИБС в патогенезе нейродегенеративных и миодегенеративных заболеваний, включая болезнь Альцгеймера , [127] болезнь Паркинсона [128] и болезнь Пика , [129] боковой амиотрофический склероз (БАС), [129] болезнь Хантингтона , [128] Крейцфельдта – болезнь Якоба , [130] и болезни двигательных нейронов, полиглутаминовые (PolyQ) болезни, мышечные дистрофии [131] и несколько редких форм нейродегенеративных заболеваний, связанных с деменцией . [132] Как часть убиквитин-протеасомной системы (UPS), протеасома поддерживает гомеостаз сердечных белков и, таким образом, играет значительную роль в ишемическом повреждении сердца , [133] гипертрофии желудочков [134] и сердечной недостаточности . [135] Кроме того, накапливаются данные о том, что УПС играет важную роль в злокачественной трансформации. Протеолиз UPS играет важную роль в ответах раковых клеток на стимулирующие сигналы, которые имеют решающее значение для развития рака. Соответственно, экспрессия генов путем деградации факторов транскрипции , таких как p53 , c-jun , c-Fos , NF-κB , c-Myc , HIF-1α, MATα2, STAT3 , белки, связывающие элементы, регулируемые стеролом, и рецепторы андрогенов являются контролируется UPS и, таким образом, участвует в развитии различных злокачественных новообразований. [136] Более того, UPS регулирует деградацию продуктов генов-супрессоров опухоли, таких как аденоматозный полипоз кишечной палочки (APC) при колоректальном раке и ретинобластоме (Rb). и супрессор опухоли фон Хиппель-Линдау (VHL), а также ряд протоонкогенов ( Raf , Myc , Myb , Rel , Src , Mos , ABL ). ИБП также участвует в регуляции воспалительных реакций. Эту активность обычно связывают с ролью протеасом в активации NF-κB, который дополнительно регулирует экспрессию провоспалительных цитокинов , таких как TNF-α , IL-β, IL-8 , молекулы адгезии ( ICAM-1 , VCAM-1). , P-селектин ) ипростагландины и оксид азота (NO). [125] Кроме того, UPS также играет роль в воспалительных реакциях в качестве регуляторов пролиферации лейкоцитов, главным образом посредством протеолиза циклинов и деградации ингибиторов CDK . [137] Наконец, у пациентов с аутоиммунными заболеваниями , такими как СКВ , синдром Шегрена и ревматоидный артрит (РА), преимущественно наблюдаются циркулирующие протеасомы, которые можно применять в качестве клинических биомаркеров. [138]