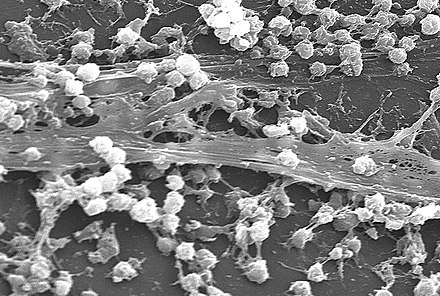

Совокупность микроорганизмов, в которой клетки, часто встроенные в самопроизвольно созданную матрицу внеклеточных полимерных веществ (ЭПС), прилипают друг к другу и/или к поверхности.
- Биопленка — это система, способная адаптироваться к внутренним условиям окружающей среды ее обитателями.
- Самопроизведенная матрица внеклеточных полимерных веществ , также называемая слизью, представляет собой полимерный конгломерат, обычно состоящий из внеклеточных биополимеров в различных структурных формах. [1]
Биопленка — это синтрофное сообщество микроорганизмов , в котором клетки прилипают друг к другу и часто также к поверхности. [2] [3] Эти адгезивные клетки внедряются в слизистый внеклеточный матрикс , состоящий из внеклеточных полимерных веществ (ЭПС). [2] [3] Клетки внутри биопленки вырабатывают компоненты ЭПС, которые обычно представляют собой полимерную комбинацию внеклеточных полисахаридов , белков , липидов и ДНК . [2] [3] [4] Поскольку они имеют трехмерную структуру и представляют собой образ жизни сообщества микроорганизмов, их метафорически называют «городами для микробов». [5] [6]
Биопленки могут образовываться на живых (биотических) или неживых (абиотических) поверхностях и могут быть обычным явлением в природных, промышленных и больничных условиях. [3] [7] Они могут составлять микробиом или быть его частью. Микробные клетки, растущие в биопленке, физиологически отличаются от планктонных клеток того же организма, которые, напротив, являются отдельными клетками, которые могут плавать или плавать в жидкой среде. [8] Биопленки могут образовываться на зубах большинства животных в виде зубного налета , где они могут вызывать кариес и заболевания десен .
Микробы образуют биопленку в ответ на ряд различных факторов, [9] которые могут включать в себя клеточное распознавание специфических или неспецифических участков прикрепления на поверхности, пищевые сигналы или, в некоторых случаях, воздействие на планктонные клетки субингибиторных концентраций антибиотиков . [ 10] [11] Клетка, которая переключается на биопленочный режим роста, претерпевает фенотипический сдвиг в поведении, при котором большие наборы генов регулируются по-разному . [12]
Биопленку также можно считать гидрогелем , который представляет собой сложный полимер, содержащий во много раз больше своего сухого веса в воде. Биопленки — это не просто бактериальные слои слизи, а биологические системы; бактерии организуются в скоординированное функциональное сообщество. Биопленки могут прикрепляться к поверхности, такой как зуб или камень, и могут включать один вид или разнообразную группу микроорганизмов. Субпопуляции клеток внутри биопленки дифференцируются для выполнения различных действий для подвижности, производства матрицы и споруляции, поддерживая общий успех биопленки. [13] Бактерии биопленки могут делиться питательными веществами и защищены от вредных факторов окружающей среды, таких как высыхание, антибиотики и иммунная система организма-хозяина. Биопленка обычно начинает формироваться, когда свободно плавающая планктонная бактерия прикрепляется к поверхности. [14] [ нужна страница ]
Биопленки, как полагают, возникли во времена примитивной Земли как защитный механизм для прокариот, поскольку условия в то время были слишком суровыми для их выживания. Их можно найти очень рано в ископаемых записях Земли (около 3,25 млрд лет назад) как археи и бактерии, и они обычно защищают прокариотические клетки, обеспечивая им гомеостаз, способствуя развитию сложных взаимодействий между клетками в биопленке. [3]
Формирование биопленки начинается с прикрепления свободно плавающих микроорганизмов к поверхности. [8] [5] Первые бактерии-колонисты биопленки могут изначально прилипать к поверхности за счет слабых сил Ван-дер-Ваальса и гидрофобных эффектов. [15] [16] Если колонисты не сразу отделяются от поверхности, они могут закрепиться более прочно, используя клеточные адгезионные структуры, такие как пили . Уникальная группа архей, обитающих в бескислородных грунтовых водах, имеет похожие структуры, называемые хами . Каждый хамус представляет собой длинную трубку с тремя крючкообразными прикреплениями, которые используются для прикрепления друг к другу или к поверхности, что позволяет сообществу развиваться. [17] [18] Гипертермофильная архея Pyrobaculum calidifontis продуцирует связывающие пили, которые гомологичны бактериальным нитям TasA, основному компоненту внеклеточного матрикса в бактериальных биопленках, которые способствуют стабильности биопленки. [19] Гомологи TasA кодируются многими другими археями, что предполагает механистическое сходство и эволюционную связь между бактериальными и архейными биопленками. [19]

Гидрофобность также может влиять на способность бактерий образовывать биопленки. Бактерии с повышенной гидрофобностью имеют сниженное отталкивание между субстратом и бактерией. [21] Некоторые виды бактерий не способны самостоятельно успешно прикрепляться к поверхности из-за своей ограниченной подвижности, но вместо этого способны прикрепляться к матрице или напрямую к другим, более ранним бактериям-колонистам. Неподвижные бактерии не могут распознавать поверхности или объединяться вместе так же легко, как подвижные бактерии. [21]
Во время колонизации поверхности клетки бактерий способны общаться с помощью продуктов кворум-сенсинга (QS), таких как N-ацилгомосеринлактон (AHL). После начала колонизации биопленка растет за счет комбинации деления клеток и рекрутинга. Полисахаридные матрицы обычно заключают в себе бактериальные биопленки. Экзополисахариды матрицы могут захватывать аутоиндукторы QS внутри биопленки, чтобы предотвратить обнаружение хищниками и обеспечить выживание бактерий. [22] Помимо полисахаридов, эти матрицы также могут содержать материал из окружающей среды, включая, помимо прочего, минералы, частицы почвы и компоненты крови, такие как эритроциты и фибрин. [21] Заключительная стадия формирования биопленки известна как развитие и является стадией, на которой биопленка устанавливается и может изменять только форму и размер. [ необходима цитата ]
Развитие биопленки может позволить совокупной клеточной колонии (или колониям) стать более толерантной [23] или устойчивой к антибиотикам . Было показано, что межклеточная коммуникация или кворумное восприятие участвуют в формировании биопленки у нескольких видов бактерий. [24]

Биопленки являются продуктом процесса развития микробов . [27] Процесс можно обобщить пятью основными стадиями развития биопленки, как показано на схеме ниже: [28]

Рассеивание клеток из колонии биопленки является неотъемлемой стадией жизненного цикла биопленки. Рассеивание позволяет биопленкам распространяться и колонизировать новые поверхности. Ферменты, которые разрушают внеклеточный матрикс биопленки, такие как дисперсин B и дезоксирибонуклеаза , могут способствовать рассеиванию биопленки. [29] [30] Ферменты, которые разрушают матрикс биопленки, могут быть полезны в качестве антибиопленочных агентов. [31] [32] Имеются данные, что жирнокислотный мессенджер, цис -2-деценовая кислота , способен вызывать дисперсию и ингибировать рост колоний биопленки. Выделяемое Pseudomonas aeruginosa , это соединение индуцирует циклогетероморфные клетки у нескольких видов бактерий и дрожжей Candida albicans . [33] Было также показано, что оксид азота запускает рассеивание биопленок нескольких видов бактерий [34] [35] при субтоксичных концентрациях. Оксид азота имеет потенциал в качестве лечения для пациентов с хроническими инфекциями, вызванными биопленками. [36]
Обычно предполагалось, что клетки, диспергированные из биопленок, немедленно переходят в фазу планктонного роста. Однако исследования показали, что физиология диспергированных клеток из биопленок Pseudomonas aeruginosa сильно отличается от физиологии планктонных и биопленочных клеток. [37] [38] Таким образом, процесс диспергирования является уникальной стадией при переходе от биопленочного к планктонному образу жизни у бактерий. Установлено, что диспергированные клетки очень вирулентны против макрофагов и Caenorhabditis elegans , но очень чувствительны к стрессу от железа по сравнению с планктонными клетками. [37]
Кроме того, биопленки Pseudomonas aeruginosa претерпевают отчетливую пространственно-временную динамику во время рассеивания или разборки биопленки, с контрастными последствиями при реколонизации и распространении заболеваний. [39] Рассеивание биопленки побудило бактерии активировать гены рассеивания для активного выхода из биопленки в виде отдельных клеток с постоянной скоростью, но не смогло повторно заселить свежие поверхности. Напротив, разборка биопленки путем деградации экзополисахарида биопленки высвобождала неподвижные агрегаты с высокой начальной скоростью, что позволяло бактериям повторно заселять свежие поверхности и эффективно вызывать инфекции у хозяев. Следовательно, рассеивание биопленки является более сложным, чем считалось ранее, где бактериальные популяции, принимающие определенное поведение после ухода из биопленки, могут быть ключом к выживанию бактериальных видов и распространению заболеваний.

Биопленки обычно находятся на твердых субстратах, погруженных в водный раствор или подвергающихся его воздействию , хотя они могут образовываться в виде плавающих матов на жидких поверхностях, а также на поверхности листьев, особенно в климате с высокой влажностью. При наличии достаточных ресурсов для роста биопленка быстро вырастет и станет макроскопической (видимой невооруженным глазом). Биопленки могут содержать множество различных типов микроорганизмов, например, бактерии, археи , простейшие , грибы и водоросли ; каждая группа выполняет специализированные метаболические функции. Однако некоторые организмы при определенных условиях будут образовывать одновидовые пленки. Социальная структура (сотрудничество/конкуренция) внутри биопленки в значительной степени зависит от различных присутствующих видов. [40]

Матрица EPS состоит из экзополисахаридов , белков и нуклеиновых кислот. [41] [42] [43] Большая часть EPS более или менее сильно гидратирована, однако встречаются и гидрофобные EPS; одним из примеров является целлюлоза [44] , которая вырабатывается рядом микроорганизмов. Эта матрица охватывает клетки внутри себя и облегчает связь между ними посредством биохимических сигналов, а также обмена генами. Матрица EPS также улавливает внеклеточные ферменты и удерживает их в непосредственной близости от клеток. Таким образом, матрица представляет собой внешнюю систему пищеварения и допускает стабильные синергические микроконсорциумы различных видов. [45] Было обнаружено, что некоторые биопленки содержат водные каналы, которые помогают распределять питательные вещества и сигнальные молекулы. [46] Эта матрица достаточно прочна, чтобы при определенных условиях биопленки могли стать окаменевшими ( строматолитами ).
Бактерии, живущие в биопленке, обычно имеют существенно отличающиеся свойства от свободно плавающих бактерий того же вида, поскольку плотная и защищенная среда пленки позволяет им сотрудничать и взаимодействовать различными способами. [47] Одним из преимуществ этой среды является повышенная устойчивость к детергентам и антибиотикам , поскольку плотный внеклеточный матрикс и внешний слой клеток защищают внутреннюю часть сообщества. [48] [49] В некоторых случаях устойчивость к антибиотикам может быть увеличена до 5000 раз. [50] Латеральный перенос генов часто облегчается внутри бактериальных и архейных биопленок [51] и может привести к более стабильной структуре биопленки. [52] Внеклеточная ДНК является основным структурным компонентом многих различных микробных биопленок. [53] Ферментативная деградация внеклеточной ДНК может ослабить структуру биопленки и высвободить микробные клетки с поверхности.
Однако биопленки не всегда менее восприимчивы к антибиотикам. Например, биопленочная форма Pseudomonas aeruginosa не имеет большей устойчивости к противомикробным препаратам, чем планктонные клетки стационарной фазы, хотя при сравнении биопленки с планктонными клетками логарифмической фазы биопленка действительно имеет большую устойчивость к противомикробным препаратам. Эта устойчивость к антибиотикам как в клетках стационарной фазы, так и в биопленках может быть обусловлена наличием персистирующих клеток . [54]


Биопленки повсеместно распространены в органической жизни. Почти у каждого вида микроорганизмов есть механизмы, с помощью которых они могут прилипать к поверхностям и друг к другу. Биопленки будут образовываться практически на каждой нелиняющей поверхности в нестерильных водных или влажных средах. Биопленки могут расти в самых экстремальных условиях: например, от чрезвычайно горячих, соленых вод горячих источников, варьирующихся от очень кислых до очень щелочных, до замерзших ледников .
Биопленки можно найти на камнях и гальке на дне большинства ручьев или рек, и они часто образуются на поверхности стоячих водоемов. Биопленки являются важными компонентами пищевых цепей в реках и ручьях и поедаются водными беспозвоночными , которыми питаются многие рыбы. Биопленки находятся на поверхности и внутри растений. Они могут либо способствовать заболеванию сельскохозяйственных культур, либо, как в случае азотфиксирующих ризобий на корневых клубеньках , существовать в симбиозе с растением . [55] Примерами заболеваний сельскохозяйственных культур, связанных с биопленками, являются рак цитрусовых, болезнь Пирса винограда и бактериальная пятнистость растений, таких как перец и томаты. [56]
Фильтрующие фильтры в очистных сооружениях являются высокоэффективными устройствами для удаления загрязняющих веществ из отстоявшейся сточной воды. Они работают, пропуская жидкость через слой твердого материала, который разработан так, чтобы иметь очень большую площадь поверхности. На поверхности среды образуется сложная биопленка, которая поглощает, адсорбирует и метаболизирует загрязняющие вещества. Биопленка быстро растет, и когда она становится слишком толстой, чтобы удерживать ее на среде, она смывается и заменяется новой выращенной пленкой. Смытая («отшелушенная») пленка осаждается из потока жидкости, оставляя высокоочищенные сточные воды. [57]
Медленные песчаные фильтры используются для очистки воды для обработки сырой воды с целью получения питьевого продукта. Они работают посредством образования биопленки, называемой подземным слоем или Schmutzdecke, в верхних нескольких миллиметрах слоя мелкого песка. Schmutzdecke образуется в первые 10–20 дней работы [58] и состоит из бактерий , грибков, простейших , коловраток и ряда личинок водных насекомых. По мере старения эпигейной биопленки, как правило, развивается больше водорослей, и могут присутствовать более крупные водные организмы, включая некоторые мшанки , улиток и кольчатых червей. Поверхностная биопленка является слоем, который обеспечивает эффективную очистку при очистке питьевой воды, а лежащий под ней песок обеспечивает опорную среду для этого слоя биологической очистки. Когда вода проходит через подземный слой, частицы посторонних веществ задерживаются в слизистой матрице, а растворимый органический материал адсорбируется . Загрязнители метаболизируются бактериями, грибками и простейшими. Вода, полученная из образцового медленного песчаного фильтра, имеет превосходное качество с 90–99% сокращением количества бактериальных клеток. [59]
Микробы, полезные для растений, можно отнести к категории ризобактерий, способствующих росту растений . [60] Эти стимуляторы роста растений колонизируют корни растений и обеспечивают широкий спектр полезных функций для своего хозяина, включая фиксацию азота, подавление патогенов, противогрибковые свойства и расщепление органических материалов. [61] Одной из этих функций является защита от патогенных почвенных бактерий и грибков посредством индуцированной системной резистентности (ИСР) [62] или индуцированных системных ответов, вызванных патогенными микробами (индуцированная патогеном системная приобретенная резистентность). [63] Растительные экссудаты действуют как химические сигналы для специфичных для хозяина бактерий к колонизации. [64] Этапы колонизации ризобактерий включают привлечение, распознавание, прилипание, колонизацию и рост. [ 61] Бактерии, которые, как было показано, являются полезными и образуют биопленки, включают Bacillus , Pseudomonas и Azospirillum . [65] [66] Биопленки в ризосфере часто приводят к системной устойчивости, вызванной патогенами или растениями. Молекулярные свойства на поверхности бактерии вызывают иммунный ответ у растения-хозяина. [64] Эти связанные с микробами молекулы взаимодействуют с рецепторами на поверхности растительных клеток и активируют биохимический ответ, который, как полагают, включает несколько различных генов в ряде локусов. [64] Несколько других сигнальных молекул были связаны как с индуцированными системными ответами, так и с системными ответами, индуцированными патогенами, такими как жасмоновая кислота и этилен. [61] Компоненты клеточной оболочки, такие как бактериальные жгутики и липополисахариды, которые распознаются растительными клетками как компоненты патогенов. [67] Было также показано, что некоторые метаболиты железа, вырабатываемые Pseudomonas , создают индуцированный системный ответ. [64] Эта функция биопленки помогает растениям вырабатывать более сильную устойчивость к патогенам.
Растения, которые были колонизированы PGPR, образующими биопленку, приобрели системную устойчивость и готовы к защите от патогенов. Это означает, что гены, необходимые для производства белков, которые работают над защитой растения от патогенов, были выражены, и у растения есть «запас» соединений, которые можно высвободить для борьбы с патогенами. [64] Готовая система защиты гораздо быстрее реагирует на инфекцию, вызванную патогеном, и может быть способна отклонить патогены до того, как они успеют закрепиться. [68] Растения увеличивают выработку лигнина, укрепляя клеточные стенки и затрудняя проникновение патогенов в клетку, а также отсекая питательные вещества для уже инфицированных клеток, эффективно останавливая вторжение. [61] Они вырабатывают антимикробные соединения, такие как фитоалексины, хитиназы и ингибиторы протеиназ, которые предотвращают рост патогенов. [63] Эти функции подавления болезней и устойчивости к патогенам в конечном итоге приводят к увеличению сельскохозяйственного производства и снижению использования химических пестицидов, гербицидов и фунгицидов, поскольку снижается количество потерь урожая из-за болезней. [69] Индуцированная системная устойчивость и вызванная патогенами приобретенная системная устойчивость являются потенциальными функциями биопленок в ризосфере и должны учитываться при применении к новым сельскохозяйственным методам из-за их влияния на подавление болезней без использования опасных химикатов.
Исследования 2003 года показали, что иммунная система поддерживает развитие биопленки в толстом кишечнике. Это было подкреплено главным образом тем фактом, что две наиболее обильно продуцируемые иммунной системой молекулы также поддерживают производство биопленки и связаны с биопленками, развивающимися в кишечнике. Это особенно важно, поскольку аппендикс содержит огромное количество этих бактериальных биопленок. [70] Это открытие помогает различить возможную функцию аппендикса и идею о том, что аппендикс может помочь повторно заселить кишечник хорошей кишечной флорой. Однако измененные или нарушенные состояния биопленок в кишечнике были связаны с такими заболеваниями, как воспалительное заболевание кишечника и колоректальный рак . [71]
В среде обитания человека биопленки могут очень легко расти в душевых, поскольку они обеспечивают влажную и теплую среду для их процветания. Они могут образовываться внутри водопроводных и канализационных труб и вызывать засорение и коррозию . На полах и прилавках они могут затруднять санитарию в зонах приготовления пищи. В почве они могут вызывать биологическое засорение . Известно, что в системах охлаждения или нагрева воды они снижают теплопередачу. [72] Биопленки в морских инженерных системах, таких как трубопроводы морской нефтегазовой промышленности, [73] могут приводить к существенным проблемам с коррозией. Коррозия в основном вызвана абиотическими факторами; однако, по крайней мере, 20% коррозии вызвано микроорганизмами, которые прикреплены к металлической подповерхности (т. е. коррозия под воздействием микробов ).
Бактериальная адгезия к корпусам лодок служит основой для биообрастания морских судов. После того, как образуется пленка бактерий, другим морским организмам, таким как ракушки, легче прикрепиться. Такое обрастание может снизить максимальную скорость судна до 20%, удлиняя плавание и расходуя топливо. Время в сухом доке для переоборудования и перекраски снижает производительность судоходных активов, а срок службы судов также сокращается из-за коррозии и механического удаления (соскабливания) морских организмов с корпусов судов.
Строматолиты — это слоистые аккреционные структуры, образованные на мелководье путем захвата, связывания и цементации осадочных зерен микробными биопленками, особенно цианобактериями . Строматолиты включают в себя некоторые из древнейших следов жизни на Земле и продолжают формироваться сегодня.
В организме человека биопленки присутствуют на зубах в виде зубного налета , где они могут вызывать кариес и заболевания десен . Эти биопленки могут быть либо в некальцинированном состоянии, которое можно удалить стоматологическими инструментами, либо в кальцинированном состоянии, которое удалить сложнее. Методы удаления могут также включать противомикробные препараты . [74]
Зубной налет — это оральная биопленка, которая прилипает к зубам и состоит из многих видов бактерий и грибков (таких как Streptococcus mutans и Candida albicans ), встроенных в полимеры слюны и микробные внеклеточные продукты. Накопление микроорганизмов подвергает зубы и десневые ткани воздействию высоких концентраций бактериальных метаболитов , что приводит к стоматологическим заболеваниям. [75] Биопленка на поверхности зубов часто подвергается окислительному стрессу [76] и кислотному стрессу. [77] Пищевые углеводы могут вызывать резкое снижение pH в оральных биопленках до значений 4 и ниже (кислотный стресс). [77] pH 4 при температуре тела 37 °C вызывает депуринизацию ДНК, оставляя апуриновые (AP) участки в ДНК, [78] особенно потерю гуанина. [79]
Биопленка зубного налета может привести к кариесу, если позволить ей развиваться с течением времени. Экологический сдвиг от сбалансированных популяций в зубной биопленке обусловлен определенными (кариесогенными) микробиологическими популяциями, которые начинают доминировать, когда окружающая среда благоприятствует им. Сдвиг к ацидогенной , ацидурической и кариесогенной микробиологической популяции развивается и поддерживается частым потреблением ферментируемых пищевых углеводов . Результирующий сдвиг активности в биопленке (и результирующее образование кислоты в биопленке на поверхности зуба) связано с дисбалансом деминерализации над реминерализацией, что приводит к чистой потере минералов в твердых тканях зуба ( эмали , а затем дентине ), симптомом чего является кариозное поражение или полость. Предотвращая созревание биопленки зубного налета или возвращая ее обратно в некариесогенное состояние, можно предотвратить и остановить кариес. [80] [81] Этого можно достичь посредством поведенческого шага по сокращению поступления ферментируемых углеводов (т. е. потребления сахара) и частого удаления биопленки (т. е. чистки зубов ). [80]
Пептидная феромонная сигнальная система кворум-сенсора в S. mutans включает пептид, стимулирующий компетентность (CSP), который контролирует генетическую компетентность. [82] [83] Генетическая компетентность — это способность клетки принимать ДНК, высвобождаемую другой клеткой. Компетенция может привести к генетической трансформации, форме полового взаимодействия, благоприятствуемой в условиях высокой плотности клеток и/или стресса, когда существует максимальная возможность для взаимодействия между компетентной клеткой и ДНК, высвобождаемой из соседних донорских клеток. Эта система оптимально выражена, когда клетки S. mutans находятся в активно растущей биопленке. Выращенные в биопленке клетки S. mutans генетически трансформируются со скоростью в 10–600 раз выше, чем S. mutans, растущие как свободно плавающие планктонные клетки, взвешенные в жидкости. [82]
Когда биопленка, содержащая S. mutans и родственные оральные стрептококки, подвергается кислотному стрессу, индуцируется регулон компетентности, что приводит к устойчивости к уничтожению кислотой. [77] Как указали Мишод и др., трансформация в бактериальных патогенах, вероятно, обеспечивает эффективную и действенную рекомбинационную репарацию повреждений ДНК. [84] Похоже, что S. mutans может выдерживать частый кислотный стресс в оральных биопленках, отчасти, благодаря рекомбинационной репарации, обеспечиваемой компетентностью и трансформацией.
Взаимодействие хищника и жертвы
Взаимодействие хищника и жертвы между биопленками и бактериофагами, такими как почвенная нематода Caenorhabditis elegans , было тщательно изучено. Благодаря образованию липкой матрицы и образованию агрегатов биопленки Yersinia pestis могут препятствовать питанию, закупоривая рот C. elegans . [85] Более того, биопленки Pseudomonas aeruginosa могут препятствовать скользящей подвижности C. elegans , называемой «фенотипом болота», что приводит к захвату C. elegans внутри биопленок и препятствует исследованию нематодами восприимчивых биопленок. [86] Это значительно снижает способность хищника питаться и размножаться, тем самым способствуя выживанию биопленок. Биопленки Pseudomonas aeruginosa также могут маскировать свои химические сигнатуры, снижая диффузию молекул, чувствительных к кворуму, в окружающую среду и препятствуя обнаружению C. elegans . [87]
Биопленки образуют многие различные бактерии, включая грамположительные (например, Bacillus spp, Listeria monocytogenes , Staphylococcus spp и молочнокислые бактерии , включая Lactobacillus plantarum и Lactococcus lactis ), а также грамотрицательные виды (например, Escherichia coli или Pseudomonas aeruginosa ). [88] Цианобактерии также образуют биопленки в водной среде. [89]
Биопленки образуются бактериями, которые колонизируют растения, например, Pseudomonas putida , Pseudomonas fluorescens и родственные псевдомонады, которые являются обычными бактериями, ассоциированными с растениями, которые обнаруживаются на листьях, корнях и в почве, и большинство их природных изолятов образуют биопленки. [90] Несколько азотфиксирующих симбионтов бобовых, таких как Rhizobium leguminosarum и Sinorhizobium meliloti, образуют биопленки на корнях бобовых и других инертных поверхностях. [90]
Наряду с бактериями биопленки также генерируются археями [51] и рядом эукариотических организмов, включая грибы, например Cryptococcus laurentii [91] и микроводоросли . Среди микроводорослей одними из основных предшественников биопленок являются диатомовые водоросли , которые колонизируют как пресные, так и морские среды по всему миру. [92] [93]
Информацию о других видах в биопленках, связанных с заболеваниями, и биопленках, возникающих из эукариот , см. ниже.
Было обнаружено, что биопленки участвуют в широком спектре микробных инфекций в организме, по одной из оценок, в 80% всех инфекций. [94] Инфекционные процессы, в которых участвуют биопленки, включают такие распространенные проблемы, как бактериальный вагиноз , инфекции мочевыводящих путей , инфекции катетера , инфекции среднего уха , образование зубного налета , [95] гингивит , покрытие контактных линз , [96] и менее распространенные, но более летальные процессы, такие как эндокардит , инфекции при муковисцидозе и инфекции постоянных постоянных устройств, таких как протезы суставов , сердечные клапаны и межпозвоночные диски. [97] [98] [99] Первое визуальное доказательство наличия биопленки было зафиксировано после операции на позвоночнике. [100] Было обнаружено, что при отсутствии клинических проявлений инфекции пропитанные бактерии могут образовывать биопленку вокруг имплантата, и эта биопленка может оставаться незамеченной с помощью современных диагностических методов, включая взятие мазка. Биопленка имплантата часто присутствует в случаях «асептического» псевдоартроза. [100] [101] [102] Кроме того, было отмечено, что бактериальные биопленки могут ухудшать заживление кожных ран и снижать местную антибактериальную эффективность при заживлении или лечении инфицированных кожных ран. [103] Считается, что разнообразие клеток P. aeruginosa в биопленке затрудняет лечение инфицированных легких у людей с муковисцидозом. [13] Раннее обнаружение биопленок в ранах имеет решающее значение для успешного лечения хронических ран. Хотя было разработано много методов для выявления планктонных бактерий в жизнеспособных ранах, немногие смогли быстро и точно идентифицировать бактериальные биопленки. Необходимы дальнейшие исследования для поиска средств выявления и мониторинга колонизации биопленки у постели больного, чтобы обеспечить своевременное начало лечения. [104]
Было показано, что биопленки присутствуют на удаленной ткани 80% пациентов, перенесших операцию по поводу хронического синусита . Было показано, что у пациентов с биопленками отсутствуют реснички и бокаловидные клетки , в отличие от контрольной группы без биопленок, у которой была нормальная морфология ресничек и бокаловидных клеток. [105] Биопленки также были обнаружены в образцах от двух из 10 упомянутых здоровых контрольных лиц. Виды бактерий из интраоперационных культур не соответствовали видам бактерий в биопленке на ткани соответствующего пациента. Другими словами, культуры были отрицательными, хотя бактерии присутствовали. [106] Разрабатываются новые методы окрашивания для дифференциации бактериальных клеток, растущих у живых животных, например, из тканей с аллергическими воспалениями. [107]
Исследования показали, что субтерапевтические уровни β-лактамных антибиотиков вызывают образование биопленки у Staphylococcus aureus . Этот субтерапевтический уровень антибиотика может быть результатом использования антибиотиков в качестве стимуляторов роста в сельском хозяйстве или во время обычного курса антибиотикотерапии. Образование биопленки, вызванное низким уровнем метициллина, было ингибировано ДНКазой, что позволяет предположить, что субтерапевтические уровни антибиотика также вызывают высвобождение внеклеточной ДНК. [108] Более того, с эволюционной точки зрения, создание трагедии общего достояния у патогенных микробов может обеспечить передовые терапевтические пути для хронических инфекций, вызванных биопленками, через генетически модифицированных инвазивных обманщиков, которые могут вторгаться в дикие типы «кооператоров» патогенных бактерий до тех пор, пока популяции кооператоров не вымрут или общая популяция «кооператоров и обманщиков» не вымрет. [109]
P. aeruginosa представляет собой часто используемый модельный организм биопленки, поскольку он участвует в различных типах хронических инфекций, связанных с биопленкой. [41] Примерами таких инфекций являются хронические раны, хронический средний отит, хронический простатит и хронические инфекции легких у пациентов с муковисцидозом (МВ). Около 80% пациентов с МВ имеют хроническую инфекцию легких, вызванную в основном P. aeruginosa, растущей в неповерхностных прикрепленных биопленках, окруженных ПМН . [110] Инфекция сохраняется, несмотря на агрессивную терапию антибиотиками, и является частой причиной смерти у пациентов с МВ из-за постоянного воспалительного повреждения легких. [41] У пациентов с МВ одним из методов лечения раннего развития биопленки является использование ДНКазы для структурного ослабления биопленки. [4] [111]
Образование биопленки P. aeruginosa , наряду с другими бактериями, обнаруживается в 90% хронических раневых инфекций, что приводит к плохому заживлению и высокой стоимости лечения, которая оценивается более чем в 25 миллиардов долларов США в год в Соединенных Штатах . [112] Чтобы минимизировать инфекцию P. aeruginosa , эпителиальные клетки хозяина секретируют антимикробные пептиды , такие как лактоферрин , для предотвращения образования биопленки. [113]
Streptococcus pneumoniae является основной причиной внебольничной пневмонии и менингита у детей и пожилых людей, а также сепсиса у ВИЧ-инфицированных лиц. Когда S. pneumoniae растет в биопленках, специфически экспрессируются гены, которые реагируют на окислительный стресс и индуцируют компетентность. [114] Образование биопленки зависит от пептида, стимулирующего компетентность (CSP). CSP также функционирует как пептид, чувствительный к кворуму. Он не только индуцирует образование биопленки, но и повышает вирулентность при пневмонии и менингите.
Было высказано предположение, что развитие компетентности и образование биопленки является адаптацией S. pneumoniae для выживания в условиях защиты хозяина. [84] В частности, полиморфноядерные лейкоциты хозяина производят окислительный взрыв для защиты от вторгающихся бактерий, и этот ответ может убивать бактерии, повреждая их ДНК. Компетентные S. pneumoniae в биопленке имеют преимущество в выживании, поскольку они могут легче захватывать трансформирующую ДНК из соседних клеток в биопленке, чтобы использовать ее для рекомбинационного восстановления окислительных повреждений в своей ДНК. Компетентные S. pneumoniae также могут секретировать фермент (муреингидролазу), который разрушает некомпетентные клетки (братоцид), вызывая высвобождение ДНК в окружающую среду для потенциального использования компетентными клетками. [115]
Антимикробный пептид насекомых цекропин А может разрушать планктонные и сидячие биопленкообразующие уропатогенные клетки E. coli , как в отдельности, так и в сочетании с антибиотиком налидиксовой кислотой , синергически устраняя инфекцию in vivo (у насекомого-хозяина Galleria mellonella ) без нецелевой цитотоксичности. Многоцелевой механизм действия включает в себя проницаемость внешней мембраны с последующим разрушением биопленки, вызванным ингибированием активности эффлюксного насоса и взаимодействием с внеклеточными и внутриклеточными нуклеиновыми кислотами. [116]
Биопленки Escherichia coli ответственны за многие кишечные инфекционные заболевания. [117] Внекишечная группа E. coli (ExPEC) является доминирующей бактериальной группой, которая поражает мочевыделительную систему , что приводит к инфекциям мочевыводящих путей . [118] Образование биопленки этих патогенных E. coli трудно искоренить из-за сложности их агрегационной структуры, и оно вносит значительный вклад в развитие агрессивных медицинских осложнений, увеличение частоты госпитализаций и стоимости лечения. [119] [120] Развитие биопленки E. coli является распространенной ведущей причиной инфекций мочевыводящих путей (ИМП) в больницах из-за ее вклада в развитие инфекций, связанных с медицинскими устройствами . Инфекции мочевыводящих путей, связанные с катетером (CAUTI), представляют собой наиболее распространенную внутрибольничную инфекцию из-за образования патогенной биопленки E. coli внутри катетеров. [121]
Возбудитель золотистого стафилококка может поражать кожу и легкие, что приводит к кожной инфекции и пневмонии . [122] [123] Более того, сеть биопленочных инфекций S. aureus играет решающую роль в предотвращенииуничтожения и разрушения бактериальных клеток иммунными клетками, такими как макрофаги . [124] Кроме того, образование биопленки бактериями, такими как S. aureus , не только развивает устойчивость к антибиотикам , но и развивает внутреннюю устойчивость к антимикробным пептидам (AMP) , что приводит к предотвращению ингибирования патогена и поддержанию его выживания. [125]
Serratia marcescens — довольно распространенный условно-патогенный микроорганизм, способный образовывать биопленки на различных поверхностях, включая медицинские устройства, такие как катетеры и имплантаты, а также в таких природных средах, как почва и вода. Образование биопленок S. marcescens вызывает серьезную озабоченность из-за его способности прилипать к поверхностям и колонизировать их, защищая себя от иммунных реакций хозяина и противомикробных агентов. Эта сила делает инфекции, вызванные S. marcescens, сложными для лечения, особенно в больницах, где эта бактерия может вызывать тяжелые и специфические инфекции.
Исследования показывают, что образование биопленки S. marcescens — это процесс, контролируемый как сигналами питательных веществ, так и системой кворум-сенсорики. [126] Кворум-сенсорика влияет на способность бактерии прикрепляться к поверхностям и образовывать зрелые биопленки, тогда как доступность определенных питательных веществ может усиливать или подавлять развитие биопленки.
S. marcescens создает биопленки, которые в конечном итоге развиваются в высокопористую, нитевидную структуру, состоящую из цепочек клеток, нитей и клеточных кластеров. Исследования показали, что биопленки S. marcescens демонстрируют сложную структурную организацию, включая образование микроколоний и каналов, которые облегчают обмен питательными веществами и отходами. Производство внеклеточных полимерных веществ (EPS) является ключевым фактором в развитии биопленки, способствуя адгезии бактерий и устойчивости к антимикробным агентам. Помимо своей роли в инфекциях, связанных с оказанием медицинской помощи, биопленки S. marcescens были вовлечены в ухудшение промышленного оборудования и процессов. Например, рост биопленки в градирнях может привести к биообрастанию и снижению эффективности.
Усилия по контролю и предотвращению образования биопленки S. marcescens включают использование антимикробных покрытий на медицинских устройствах, разработку целевых разрушителей биопленки и улучшенных протоколов стерилизации. Дальнейшие исследования молекулярных механизмов, управляющих образованием и устойчивостью биопленки S. marcescens, имеют решающее значение для разработки эффективных стратегий борьбы с сопутствующими рисками. Было изучено использование индольных соединений для защиты от образования биопленки. [127]
Предполагается, что около двух третей бактериальных инфекций у людей связаны с биопленками. [50] [128] Инфекции, связанные с ростом биопленки, обычно трудно искоренить. [129] Это в основном связано с тем, что зрелые биопленки демонстрируют антимикробную толерантность и уклоняются от иммунного ответа. [130] [41] Биопленки часто образуются на инертных поверхностях имплантированных устройств, таких как катетеры, протезы сердечных клапанов и внутриматочные устройства. [131] Некоторые из самых сложных для лечения инфекций связаны с использованием медицинских устройств. [50] [101]
Быстрорастущая мировая индустрия биомедицинских устройств и продуктов, связанных с тканевой инженерией, уже достигает 180 миллиардов долларов в год, однако эта индустрия продолжает страдать от микробной колонизации. Независимо от сложности, микробные инфекции могут развиваться на всех медицинских устройствах и конструкциях тканевой инженерии. [130] 60-70% внутрибольничных инфекций связаны с имплантацией биомедицинского устройства. [130] Это приводит к 2 миллионам случаев в год в США, что обходится системе здравоохранения более чем в 5 миллиардов долларов дополнительных расходов на здравоохранение. [130]
Уровень устойчивости к антибиотикам в биопленке намного выше, чем у небиопленочных бактерий, и может быть в 5000 раз выше. [50] Внеклеточный матрикс биопленки считается одним из ведущих факторов, который может снизить проникновение антибиотиков в структуру биопленки и способствует устойчивости к антибиотикам. [132] Кроме того, было показано, что на эволюцию устойчивости к антибиотикам может влиять образ жизни биопленки. [133] Терапия бактериофагами может рассеивать биопленку, созданную бактериями, устойчивыми к антибиотикам. [134]
Было показано, что введение небольшого тока электричества в жидкость, окружающую биопленку, вместе с небольшим количеством антибиотика может снизить уровень устойчивости к антибиотикам до уровня бактерий, не входящих в биопленку. Это называется биоэлектрическим эффектом . [50] [135] Применение небольшого постоянного тока само по себе может вызвать отсоединение биопленки от ее поверхности. [50] Исследование показало, что тип используемого тока не влияет на биоэлектрический эффект. [135]
Биопленки также могут быть использованы в конструктивных целях. Например, многие очистные сооружения включают вторичную стадию очистки , на которой сточные воды проходят через биопленки, выращенные на фильтрах, которые извлекают и переваривают органические соединения. В таких биопленках бактерии в основном отвечают за удаление органических веществ ( БПК ), в то время как простейшие и коловратки в основном отвечают за удаление взвешенных твердых частиц (ВЧ), включая патогены и другие микроорганизмы. Медленные песчаные фильтры полагаются на развитие биопленки таким же образом, чтобы фильтровать поверхностную воду из озер, родников или речных источников для питья. То, что считается чистой водой, фактически является отходами для этих микроклеточных организмов. Биопленки могут помочь устранить нефтяную нефть из загрязненных океанов или морских систем. Нефть устраняется в результате деятельности по разложению углеводородов сообществ углеводородокластических бактерий (ГКБ). [136] Биопленки используются в микробных топливных элементах (МТЭ) для выработки электроэнергии из различных исходных материалов, включая сложные органические отходы и возобновляемую биомассу. [7] [137] [138] Биопленки также важны для улучшения растворения металлов в биовыщелачивающей промышленности, [139] и агрегации микропластиковых загрязняющих веществ для удобного удаления из окружающей среды. [140] [141]
Биопленки стали проблемой в нескольких отраслях пищевой промышленности из-за способности образовываться на растениях и во время промышленных процессов. [142] Бактерии могут выживать в течение длительного времени в воде, навозе и почве, вызывая образование биопленки на растениях или в технологическом оборудовании. [143] Накопление биопленок может повлиять на тепловой поток через поверхность и увеличить поверхностную коррозию и сопротивление трения жидкостей. [144] Это может привести к потере энергии в системе и общей потере продуктов. [144] Наряду с экономическими проблемами, образование биопленки на продуктах питания представляет риск для здоровья потребителей из-за способности делать продукты питания более устойчивыми к дезинфицирующим средствам. [142] В результате, с 1996 по 2010 год Центры по контролю и профилактике заболеваний оценили 48 миллионов пищевых заболеваний в год. [142] Биопленки были связаны примерно с 80% бактериальных инфекций в Соединенных Штатах. [142]
В продуктах микроорганизмы прикрепляются к поверхностям, и внутри образуются биопленки. [142] Во время процесса мытья биопленки сопротивляются дезинфекции и позволяют бактериям распространяться по продукту, [142] особенно через кухонные принадлежности. [145] Эта проблема также встречается в готовых к употреблению продуктах, поскольку продукты проходят ограниченные процедуры очистки перед употреблением. [142] Из-за скоропортящихся молочных продуктов и ограничений в процедурах очистки, приводящих к накоплению бактерий, молочные продукты подвержены образованию биопленки и загрязнению. [142] [144] Бактерии могут быстрее портить продукты, а загрязненные продукты представляют риск для здоровья потребителей. Одним из видов бактерий, который можно найти в различных отраслях промышленности и который является основной причиной заболеваний пищевого происхождения, является сальмонелла . [146] Большое количество заражения сальмонеллой можно обнаружить в птицеперерабатывающей промышленности, поскольку около 50% штаммов сальмонеллы могут образовывать биопленки на птицефермах. [142] Сальмонелла увеличивает риск пищевых заболеваний, когда продукты из птицы не очищаются и не готовятся должным образом. Сальмонелла также встречается в индустрии морепродуктов, где биопленки образуются из патогенов, переносимых морепродуктами, на самих морепродуктах, а также в воде. [146] Продукты из креветок обычно поражаются сальмонеллой из-за негигиеничных методов обработки и обращения. [146] Методы приготовления креветок и других морепродуктов могут привести к накоплению бактерий на продуктах. [146]
Новые формы процедур очистки тестируются для снижения образования биопленки в этих процессах, что приведет к более безопасной и производительной пищевой промышленности. Эти новые формы процедур очистки также оказывают глубокое воздействие на окружающую среду, часто выделяя токсичные газы в грунтовые водохранилища. [144] В ответ на агрессивные методы, используемые для контроля образования биопленки, исследуется ряд новых технологий и химикатов, которые могут предотвратить либо пролиферацию, либо адгезию микробов, секретирующих биопленку. Последние предложенные биомолекулы, представляющие выраженную антибиопленочную активность, включают ряд метаболитов, таких как бактериальные рамнолипиды [147] и даже алкалоиды растительного [148] и животного происхождения . [149]

В аквакультуре моллюсков и водорослей биообрастающие виды микроорганизмов имеют тенденцию блокировать сети и клетки и в конечном итоге вытеснять выращиваемые виды за пространство и пищу. [150] Бактериальные биопленки начинают процесс колонизации, создавая микросреду , более благоприятную для биообрастающих видов. В морской среде биопленки могут снижать гидродинамическую эффективность судов и винтов, приводить к закупорке трубопроводов и сбоям в работе датчиков, а также увеличивать вес приборов, используемых в морской воде. [151] Многочисленные исследования показали, что биопленка может быть резервуаром для потенциально патогенных бактерий в пресноводной аквакультуре. [152] [153] [154] [155] Более того, биопленки играют важную роль в установлении инфекций у рыб. [156] Как упоминалось ранее, биопленки может быть трудно устранить даже при использовании антибиотиков или химикатов в высоких дозах. [157] [158] Роль биопленки как резервуара бактериальных патогенов рыб не была подробно изучена, но она, безусловно, заслуживает изучения.
Наряду с бактериями биопленки часто инициируются и производятся эукариотическими микробами. Биопленки, производимые эукариотами, обычно занимают бактерии и другие эукариоты, однако поверхность культивируется и ЭПС изначально секретируется эукариотами. [91] [92] [159] Известно, что и грибы , и микроводоросли образуют биопленки таким образом. Биопленки грибкового происхождения являются важными аспектами человеческой инфекции и патогенности грибков, поскольку грибковая инфекция более устойчива к противогрибковым препаратам. [160] [161]
В окружающей среде грибковые биопленки являются областью продолжающихся исследований. Одной из ключевых областей исследований являются грибковые биопленки на растениях. Например, в почве было показано, что связанные с растениями грибы, включая микоризу , разлагают органические вещества и защищают растения от бактериальных патогенов. [162]
Биопленки в водной среде часто основаны диатомовыми водорослями . Точное назначение этих биопленок неизвестно, однако есть доказательства того, что EPS, продуцируемый диатомовыми водорослями, облегчает как холодовой, так и соленый стресс. [93] [163] Эти эукариоты взаимодействуют с разнообразным спектром других организмов в пределах области, известной как фикосфера , но важными являются бактерии, связанные с диатомовыми водорослями, поскольку было показано, что хотя диатомовые водоросли выделяют EPS, они делают это только при взаимодействии с определенными видами бактерий. [164] [165]
Горизонтальный перенос генов — это боковой перенос генетического материала между клеточными организмами. Он часто происходит у прокариот и реже у эукариот. У бактерий горизонтальный перенос генов может происходить посредством трансформации (поглощения свободно плавающей ДНК в окружающей среде), трансдукции (поглощения ДНК, опосредованного вирусом) или конъюгации (переноса ДНК между пили-структурами двух соседних бактерий). [166] Недавние исследования также выявили другие механизмы, такие как передача мембранных везикул или агенты переноса генов. [167] Биопленки способствуют горизонтальному переносу генов различными способами.

Было показано, что бактериальная конъюгация ускоряет образование биопленки в сложных условиях из-за прочных связей, устанавливаемых конъюгативными пилями . [168] Эти связи часто могут способствовать межвидовым переносам из-за разнообразной гетерогенности многих биопленок. Кроме того, биопленки структурно ограничены полисахаридной матрицей, что обеспечивает близкие пространственные требования для конъюгации. Трансформация также часто наблюдается в биопленках. Бактериальный автолиз является ключевым механизмом в структурной регуляции биопленки, обеспечивая обильный источник компетентной ДНК, подготовленной к преобразующему поглощению. [169] [167] В некоторых случаях межбиопленочное кворумное восприятие может повысить компетентность свободно плавающей eDNA, дополнительно способствуя трансформации. [167] Перенос гена Stx через носителей бактериофагов был засвидетельствован внутри биопленок, что позволяет предположить, что биопленки также являются подходящей средой для трансдукции. [167] Мембранные везикулы HGT происходят, когда высвобожденные мембранные везикулы (содержащие генетическую информацию) сливаются с бактерией-реципиентом и высвобождают генетический материал в цитоплазму бактерии. [167] Недавние исследования показали, что мембранные везикулы HGT могут способствовать образованию одноштаммовой биопленки, однако роль, которую мембранные везикулы HGT играют в образовании многоштаммовых биопленок, до сих пор неизвестна. [167] GTA, или агенты переноса генов, представляют собой фагоподобные частицы, продуцируемые бактериями-хозяевами, и содержат случайные фрагменты ДНК из генома бактерий-хозяев. [167] Горизонтальный перенос генов внутри биопленок может приводить к устойчивости к антибиотикам или повышению патогенности в популяции биопленок, способствуя гомеостазу биопленки. [167]
Конъюгативные плазмиды могут кодировать белки, связанные с биопленкой, такие как PtgA, PrgB или PrgC, которые способствуют адгезии клеток (необходимой для раннего формирования биопленки). [170] Гены, кодирующие фимбрии типа III, обнаружены в pOLA52 ( плазмида Klebsiella pneumoniae ), которые способствуют образованию биопленки, зависящей от конъюгативных пилей. [170]
Трансформация обычно происходит внутри биопленок. Явление, называемое братоцидом, можно наблюдать среди видов стрептококков, в которых высвобождаются ферменты, разрушающие клеточную стенку, лизирующие соседние бактерии и высвобождающие их ДНК. Затем эта ДНК может быть захвачена выжившими бактериями (трансформация). [170] Пептиды, стимулирующие компетентность, могут играть важную роль в формировании биопленки среди S. pneumoniae и S. mutans . [170] Среди V. cholerae сама компетентность пилей способствует агрегации клеток посредством взаимодействия пилей-пилей в начале формирования биопленки. [170]
Вторжение фага может играть роль в жизненных циклах биопленки, лизируя бактерии и высвобождая их eDNA, которая укрепляет структуры биопленки и может быть захвачена соседними бактериями при трансформации. [170] Разрушение биопленки, вызванное фагом E. coli Rac и профагом P. aeruginosa Pf4, вызывает отсоединение клеток от биопленки. [170] Отсоединение — это явление биопленки, которое требует дальнейшего изучения, но, как предполагается, способствует размножению видов бактерий, составляющих биопленку.
Мембранный везикулярный горизонтальный перенос генов был замечен в морской среде, среди Neisseria gonorrhoeae , Pseudomonas aeruginosa , Helicobacter pylori и многих других видов бактерий. [170] Несмотря на то, что мембранный везикулярный горизонтальный перенос генов был показан как фактор, способствующий образованию биопленки, все еще необходимы исследования, чтобы доказать, что мембранный везикулярный горизонтальный перенос генов происходит внутри биопленок. [167] [170] Также было показано, что мембранный везикулярный горизонтальный перенос генов модулирует взаимодействие фагов и бактерий в клетках Bacillus subtilis SPP1, устойчивых к фагу (отсутствующих рецепторный белок SPP1). При воздействии везикул, содержащих рецепторы, происходит трансдукция pBT163 (плазмиды, кодирующей cat), что приводит к экспрессии рецепторного белка SPP1, открывая восприимчивые бактерии для будущей фаговой инфекции. [170]
Недавние исследования показали, что архейный вид H. volcanii имеет некоторые фенотипы биопленки, похожие на бактериальные биопленки, такие как дифференциация и горизонтальный перенос генов (HGT), которые требуют контакта клеток с клетками и включают образование цитозольных мостиков и слияние клеток. [171]
Существует широкий спектр устройств для культивирования биопленки, имитирующих естественную или промышленную среду. Хотя важно учитывать, что конкретная экспериментальная платформа для исследования биопленки определяет, какой вид биопленки культивируется и какие данные могут быть извлечены. Эти устройства можно сгруппировать следующим образом: [172]