
Азотный цикл — это биогеохимический цикл , в ходе которого азот преобразуется во множество химических форм по мере его циркуляции в атмосфере , наземных и морских экосистемах . Преобразование азота может осуществляться как биологическими, так и физическими процессами. Важные процессы круговорота азота включают фиксацию , аммонификацию , нитрификацию и денитрификацию . Большую часть атмосферы Земли (78%) составляет атмосферный азот , [16] что делает ее крупнейшим источником азота. Однако доступность атмосферного азота для биологического использования ограничена, что приводит к нехватке пригодного для использования азота во многих типах экосистем .
Азотный цикл представляет особый интерес для экологов , поскольку доступность азота может влиять на скорость ключевых экосистемных процессов, включая первичное производство и разложение . Деятельность человека, такая как сжигание ископаемого топлива, использование искусственных азотных удобрений и выбросы азота в сточные воды, резко изменила глобальный цикл азота . [17] [18] [19] Изменение человеком глобального цикла азота может негативно повлиять на природную среду, а также на здоровье человека. [20] [21]
Азот присутствует в окружающей среде в самых разных химических формах, включая органический азот, аммоний ( NH+4), нитрит ( NO−2), нитрат ( NO−3), закись азота ( N 2 O ), оксид азота (NO) или неорганический газообразный азот ( N 2 ). Органический азот может находиться в виде живого организма, гумуса или в виде промежуточных продуктов разложения органического вещества. Процессы круговорота азота заключаются в преобразовании азота из одной формы в другую. Многие из этих процессов осуществляются микробами либо в попытке собрать энергию, либо накопить азот в форме, необходимой для их роста. Например, азотистые отходы в моче животных расщепляются нитрифицирующими бактериями в почве, которые используются растениями. На диаграмме рядом показано, как эти процессы объединяются, образуя азотный цикл.
Превращение газообразного азота ( N 2 ) в нитраты и нитриты посредством атмосферных, промышленных и биологических процессов называется азотфиксацией. Атмосферный азот должен быть переработан или « фиксирован » в пригодную для использования в растениях форму. От 5 до 10 миллиардов кг в год фиксируется ударами молний , но большая часть фиксации осуществляется свободноживущими или симбиотическими бактериями , известными как диазотрофы . Эти бактерии обладают ферментом нитрогеназой , который соединяет газообразный азот с водородом с образованием аммиака , который бактерии преобразуют в другие органические соединения . Большая часть биологической фиксации азота происходит за счет активности молибден (Мо)-нитрогеназы, обнаруженной у самых разных бактерий и некоторых архей . Мо-нитрогеназа представляет собой сложный двухкомпонентный фермент , имеющий несколько металлсодержащих простетических групп. [22] Примером свободноживущих бактерий является Azotobacter . Симбиотические азотфиксирующие бактерии, такие как Rhizobium, обычно живут в корневых клубеньках бобовых (например, гороха, люцерны и акации). Здесь они образуют мутуалистические отношения с растением, производя аммиак в обмен на углеводы . Из-за этой взаимосвязи бобовые часто увеличивают содержание азота в бедных азотом почвах. Некоторые виды, не относящиеся к бобовым, также могут образовывать такие симбиозы . Сегодня около 30% общего фиксированного азота производится промышленным путем с использованием процесса Хабера-Боша , [23] который использует высокие температуры и давления для преобразования газообразного азота и источника водорода (природного газа или нефти) в аммиак. [24]
Растения могут поглощать нитраты или аммоний из почвы своими корневыми волосками. Если нитрат абсорбируется, он сначала восстанавливается до ионов нитрита, а затем ионов аммония для включения в аминокислоты, нуклеиновые кислоты и хлорофилл. У растений, находящихся в симбиотических отношениях с ризобиями, часть азота усваивается в виде ионов аммония непосредственно из клубеньков. Сейчас известно, что между бактероидами ризобий и растениями существует более сложный круговорот аминокислот . Растение снабжает бактероиды аминокислотами, поэтому ассимиляция аммиака не требуется, и бактероиды передают аминокислоты (с новым фиксированным азотом) обратно растению, образуя таким образом взаимозависимые отношения. [25] В то время как многие животные, грибы и другие гетеротрофные организмы получают азот, потребляя аминокислоты , нуклеотиды и другие небольшие органические молекулы, другие гетеротрофы (включая многие бактерии ) способны использовать неорганические соединения, такие как аммоний, в качестве единственного источника азота. . Использование различных источников азота тщательно регулируется у всех организмов.
Когда растение или животное умирает или животное выделяет отходы, первоначальная форма азота является органической . Бактерии или грибы превращают органический азот в останках обратно в аммоний ( NH+4), процесс, называемый аммонификацией или минерализацией . Участвующие ферменты:

Превращение аммония в нитраты осуществляют преимущественно почвенные бактерии и другие нитрифицирующие бактерии. На первичной стадии нитрификации происходит окисление аммония ( NH+4) осуществляется бактериями, такими как виды Nitrosomonas , которые превращают аммиак в нитриты ( NO−2). Другие виды бактерий, такие как Nitrobacter , ответственны за окисление нитритов ( NO−2) в нитраты ( NO−3). Важно, чтобы аммиак ( NH 3 ) превращался в нитраты или нитриты, поскольку газообразный аммиак токсичен для растений.
Из-за очень высокой растворимости и неспособности почв удерживать анионы нитраты могут попадать в грунтовые воды . Повышенное содержание нитратов в грунтовых водах является проблемой при использовании питьевой воды, поскольку нитраты могут влиять на уровень кислорода в крови у младенцев и вызывать метгемоглобинемию или синдром голубого ребенка. [28] Там, где подземные воды пополняют речной поток, обогащенные нитратами подземные воды могут способствовать эвтрофикации - процессу, который приводит к высокой популяции и росту водорослей, особенно популяций сине-зеленых водорослей. Хотя нитраты не токсичны напрямую для рыб, как аммиак, они могут оказывать косвенное воздействие на рыбу, если способствуют эвтрофикации. Азот способствовал возникновению серьезных проблем эвтрофикации в некоторых водоемах. С 2006 года применение азотных удобрений все больше контролируется в Великобритании и США. Это происходит по той же схеме, что и контроль над фосфорными удобрениями, ограничение которых обычно считается необходимым для восстановления эвтрофированных водоемов.
Денитрификация — это восстановление нитратов обратно в газообразный азот ( N
2), завершая азотный цикл. Этот процесс осуществляется бактериальными видами, такими как Pseudomonas и Paracoccus , в анаэробных условиях. Они используют нитрат в качестве акцептора электронов вместо кислорода во время дыхания. Эти факультативно (то есть факультативно) анаэробные бактерии могут жить и в аэробных условиях. Денитрификация происходит в анаэробных условиях, например, в заболоченных почвах. Денитрифицирующие бактерии используют нитраты в почве для дыхания и, следовательно, производят газообразный азот, который инертен и недоступен для растений. Денитрификация происходит как у свободноживущих микроорганизмов, так и у облигатных симбионтов анаэробных инфузорий. [29]
Диссимиляционное восстановление нитратов до аммония (ДНРА), или аммонификация нитратов/нитритов, представляет собой анаэробный процесс дыхания . Микробы, которые осуществляют ДНКРА, окисляют органическое вещество и используют нитрат в качестве акцептора электронов, восстанавливая его до нитрита , а затем до аммония ( NO−3 → НЕТ−2 → Нью-Хэмпшир+4). [30] И денитрифицирующие, и нитрат-аммонифицирующие бактерии будут конкурировать за нитраты в окружающей среде, хотя DNRA действует для сохранения биодоступного азота в виде растворимого аммония, а не для производства газообразного динитрога. [31]
В этом биологическом процессе нитрит и аммиак преобразуются непосредственно в молекулярный азот ( N
2) газ. Этот процесс составляет основную часть преобразования азота в океанах. Сбалансированная формула этой химической реакции « анаммокс »: NH.+4+ НЕТ−2 → N 2 + 2 H 2 O (Δ G ° =−357 кДж⋅моль −1 ). [32]
Хотя фиксация азота является основным источником доступного для растений азота в большинстве экосистем , в районах с богатой азотом коренной породой разрушение этой породы также служит источником азота. [33] [34] [35] Восстановление нитратов также является частью цикла железа : в бескислородных условиях Fe(II) может отдавать электрон NO.−3и окисляется до Fe(III), а NO−3сводится к НЕТ−2, N 2 O, N 2 и NH+4в зависимости от условий и видов микроорганизмов. [36] Фекальные шлейфы китообразных также действуют как связующее звено в морском азотном цикле, концентрируя азот в эпипелагических зонах океанской среды перед его рассеиванием через различные морские слои, что в конечном итоге повышает первичную продуктивность океана. [37]
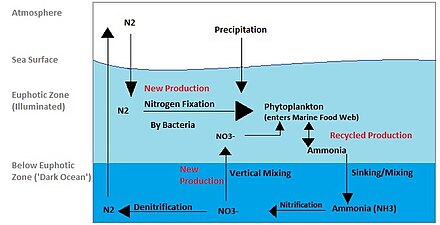


Круговорот азота также является важным процессом в океане. Хотя общий цикл аналогичен, существуют разные игроки [40] и способы переноса азота в океане. Азот попадает в воду с осадками, стоками или в виде N.
2из атмосферы. Азот не может быть использован фитопланктоном в виде N
2поэтому он должен подвергаться фиксации азота, которая осуществляется преимущественно цианобактериями . [41] Без поставок фиксированного азота в морской цикл, фиксированный азот будет израсходован примерно за 2000 лет. [42] Фитопланктону необходим азот в биологически доступных формах для первоначального синтеза органического вещества. Аммиак и мочевина попадают в воду при выделении планктона. Источники азота удаляются из эвфотической зоны за счет движения органического вещества вниз. Это может произойти в результате затопления фитопланктона, вертикального перемешивания или затопления отходов вертикальных мигрантов. В результате погружения аммиак попадает на меньшие глубины ниже эвфотической зоны. Бактерии способны превращать аммиак в нитрит и нитрат, но они ингибируются светом, поэтому это должно происходить ниже эвфотической зоны. [43] Аммонификация или минерализация осуществляется бактериями для преобразования органического азота в аммиак. Затем может произойти нитрификация с преобразованием аммония в нитрит и нитрат. [44] Нитраты могут быть возвращены в эвфотическую зону путем вертикального перемешивания и подъема вверх, где они могут быть поглощены фитопланктоном для продолжения цикла. Н
2могут быть возвращены в атмосферу путем денитрификации .
Считается, что аммоний является предпочтительным источником фиксированного азота для фитопланктона, поскольку его ассимиляция не включает окислительно-восстановительную реакцию и, следовательно, требует мало энергии. Для ассимиляции нитрата требуется окислительно-восстановительная реакция, но он более распространен, поэтому большая часть фитопланктона адаптировалась к ферментам, необходимым для такого восстановления ( нитратредуктаза ). Есть несколько примечательных и хорошо известных исключений, к которым относятся большинство прохлорококков и некоторые синехококки , которые могут поглощать азот только в виде аммония. [42]
Питательные вещества в океане распределены неравномерно. Области апвеллинга обеспечивают поступление азота из-под эвфотической зоны. Прибрежные зоны обеспечивают азот из стока, и вдоль побережья легко происходит апвеллинг. Однако скорость поглощения азота фитопланктоном снижается в олиготрофных водах круглый год и в водах умеренного пояса летом, что приводит к снижению первичной продукции. [45] Распределение различных форм азота также варьируется в океанах.
Нитраты обеднены в приповерхностных водах, за исключением районов апвеллинга. Прибрежные регионы апвеллинга обычно имеют высокие уровни нитратов и хлорофиллов в результате увеличения производства. Однако существуют области с высоким содержанием нитратов на поверхности, но низким содержанием хлорофилла, которые называются областями HNLC (высокий азот, низкий хлорофилл). Лучшее объяснение регионов HNLC связано с нехваткой железа в океане, которое может играть важную роль в динамике океана и круговороте питательных веществ. Поступление железа варьируется в зависимости от региона и попадает в океан с пылью (пылевыми бурями) и вымывается из горных пород. Железо рассматривается как настоящий элемент, ограничивающий продуктивность экосистемы океана.
Максимальные концентрации аммония и нитрита наблюдаются на глубине 50–80 м (нижний конец эвфотической зоны) с уменьшением концентрации ниже этой глубины. Такое распределение можно объяснить тем, что нитрит и аммоний являются промежуточными соединениями. Они быстро производятся и потребляются через толщу воды. [42] Количество аммония в океане примерно на 3 порядка меньше, чем нитратов. [42] Среди аммония, нитрита и нитрата нитрит имеет самую высокую скорость оборота. Он может образовываться при ассимиляции нитратов, нитрификации и денитрификации; однако он немедленно снова потребляется.
Азот, поступающий в эвфотическую зону, называется новым азотом, поскольку он вновь поступает из-за пределов продуктивного слоя. [41] Новый азот может поступать из-под эвфотической зоны или из внешних источников. Внешние источники — это апвеллинг из глубокой воды и фиксация азота. Если органическое вещество съедается, выдыхается, попадает в воду в виде аммиака и повторно включается в органическое вещество фитопланктоном, это считается переработанным/регенерированным производством.
Новая продукция является важным компонентом морской среды. Одна из причин заключается в том, что только постоянный приток нового азота может определить общую способность океана производить устойчивый улов рыбы. [45] Вылов рыбы на участках с регенерированным азотом приведет к снижению содержания азота и, следовательно, к снижению первичной продукции. Это окажет негативное влияние на систему. Однако, если рыбу вылавливать в районах с новым азотом, азот будет пополняться.
Как показано на диаграмме справа, дополнительный углекислый газ поглощается океаном и реагирует с водой, образуется угольная кислота, которая расщепляется как на бикарбонат ( H
2СО
3) и водород ( H+
) ионы (серая стрелка), которые уменьшают биодоступность карбонатов и снижают pH океана (черная стрелка). Это, вероятно, усилит фиксацию азота диазотрофами (серая стрелка), которые используют H+
ионы для преобразования азота в биодоступные формы, такие как аммиак ( NH
3) и ионы аммония ( NH+4). Однако по мере снижения pH и большего количества аммиака в ионы аммония (серая стрелка) происходит меньше окисления аммиака в нитрит (NO–
2), что приводит к общему снижению нитрификации и денитрификации (черные стрелки). Это, в свою очередь, приведет к дальнейшему накоплению фиксированного азота в океане, что может привести к эвтрофикации . Серые стрелки обозначают увеличение, а черные стрелки — уменьшение соответствующего процесса. [39]
.jpg/440px-Global_-_Global_Fertilizer_and_Manure,_Version_1_Nitrogen_Fertilizer_Application_(6074011960).jpg)
.jpg/440px-Global_Global_Fertilizer_and_Manure,_Version_1_Nitrogen_in_Manure_Production_(6173194512).jpg)
В результате широкого выращивания бобовых культур (особенно сои , люцерны и клевера ), растущего использования процесса Габера-Боша при создании химических удобрений, а также загрязнения окружающей среды, выбрасываемого транспортными средствами и промышленными предприятиями, человечество более чем вдвое увеличило ежегодный объем выбросов. перевод азота в биологически доступные формы. [28] Кроме того, люди внесли значительный вклад в перенос следов азота с Земли в атмосферу и с суши в водные системы. Антропогенные изменения глобального азотного цикла наиболее интенсивны в развитых странах и в Азии, где выбросы транспортных средств и промышленное сельское хозяйство являются самыми высокими. [46]
Производство Nr, реактивного азота , за последнее столетие увеличилось более чем в 10 раз из-за глобальной индустриализации . [2] [47] Эта форма азота каскадно проходит через биосферу с помощью различных механизмов и накапливается, поскольку скорость его образования превышает скорость денитрификации . [48]
Закись азота ( N
2O ) поднялся в атмосферу в результате сельскохозяйственных удобрений, сжигания биомассы, скота и откормочных площадок, а также промышленных источников. [49] Н
2O оказывает вредное воздействие на стратосферу , где он распадается и действует как катализатор разрушения атмосферного озона . Закись азота также является парниковым газом и в настоящее время является третьим по величине фактором глобального потепления после углекислого газа и метана . Хотя он не так распространен в атмосфере, как углекислый газ, при эквивалентной массе он почти в 300 раз более эффективен по своей способности согревать планету. [50]
Аммиак ( NH
3) в атмосфере утроилось в результате деятельности человека. Это реагент в атмосфере, где он действует как аэрозоль , ухудшая качество воздуха и прилипая к каплям воды, что в конечном итоге приводит к образованию азотной кислоты ( H NO 3 ), вызывающей кислотные дожди . Атмосферный аммиак и азотная кислота также повреждают дыхательные системы.
Очень высокая температура молнии естественным образом производит небольшое количество NO.
Икс, Нью-Хэмпшир
3и ХНО
3, но высокотемпературное горение способствовало увеличению потока NO в 6 или 7 раз.
Иксв атмосферу. Его производство зависит от температуры сгорания: чем выше температура, тем больше NO.
Икспроизводится. Сжигание ископаемого топлива вносит основной вклад, но также и биотопливо, и даже сжигание водорода. Однако скорость, с которой водород впрыскивается непосредственно в камеры сгорания двигателей внутреннего сгорания, можно контролировать, чтобы предотвратить более высокие температуры сгорания, приводящие к образованию NO.
Икс.
Аммиак и оксиды азота активно изменяют химический состав атмосферы . Они являются предшественниками образования тропосферного (нижних слоев атмосферы) озона, который способствует образованию смога и кислотных дождей , наносит ущерб растениям и увеличивает поступление азота в экосистемы. Экосистемные процессы могут усиливаться при внесении азотных удобрений , но антропогенное воздействие также может привести к насыщению азотом, что снижает продуктивность и может нанести ущерб здоровью растений, животных, рыб и людей. [28]
Сокращение биоразнообразия может также произойти, если более высокая доступность азота приведет к увеличению количества трав, требовательных к азоту, что приведет к деградации бедных азотом пустошей с большим видовым разнообразием . [51]

Показано , что повышение уровня отложений азота оказывает ряд негативных последствий как на наземные, так и на водные экосистемы. [52] [53] Азотные газы и аэрозоли могут быть непосредственно токсичными для некоторых видов растений, влияя на надземную физиологию и рост растений вблизи крупных точечных источников азотного загрязнения. Могут также произойти изменения в видах растений, поскольку накопление соединений азота увеличивает его доступность в данной экосистеме, что в конечном итоге приводит к изменению видового состава, разнообразия растений и круговорота азота. Аммиак и аммоний — две восстановленные формы азота — могут со временем оказаться вредными из-за повышенной токсичности для чувствительных видов растений, [54] особенно тех, которые привыкли использовать нитраты в качестве источника азота, вызывая плохое развитие их корней и стреляет. Повышенное отложение азота также приводит к подкислению почвы, что увеличивает выщелачивание основных катионов в почве и количество алюминия и других потенциально токсичных металлов, а также уменьшает количество происходящей нитрификации и увеличивает количество растительного мусора. Из-за продолжающихся изменений, вызванных высокими отложениями азота, восприимчивость окружающей среды к экологическому стрессу и нарушениям, таким как вредители и патогены , может увеличиться, что делает ее менее устойчивой к ситуациям, которые в противном случае мало повлияли бы на ее долгосрочную жизнеспособность.
Дополнительные риски, связанные с увеличением доступности неорганического азота в водных экосистемах, включают закисление воды; эвтрофикация систем пресной и соленой воды; и проблемы токсичности для животных, включая человека. [55] Эвтрофикация часто приводит к снижению уровня растворенного кислорода в толще воды, включая гипоксические и бескислородные условия, что может привести к гибели водной фауны. Относительно сидячие бентосы, или обитающие на дне существа, особенно уязвимы из-за отсутствия подвижности, хотя гибель крупных рыб не является редкостью. Океанические мертвые зоны возле устья Миссисипи в Мексиканском заливе являются хорошо известным примером гипоксии , вызванной цветением водорослей . [56] [57] Нью-йоркские озера Адирондак, Катскиллс , Гудзонское нагорье, плато Ренсселер и некоторые части Лонг-Айленда демонстрируют воздействие осадков азотной кислоты, что приводит к гибели рыбы и многих других водных видов. [58]
Аммиак ( NH
3) очень токсичен для рыб, поэтому необходимо тщательно контролировать уровень аммиака, выбрасываемого из очистных сооружений. Чтобы предотвратить гибель рыбы, часто желательно проводить нитрификацию посредством аэрации перед сбросом. Внесение земли может быть привлекательной альтернативой аэрации.
Утечка Nr (реактивного азота) в результате деятельности человека может вызвать накопление нитратов в природной водной среде, что может оказать вредное воздействие на здоровье человека. Чрезмерное использование азотных удобрений в сельском хозяйстве было одним из основных источников загрязнения нитратами грунтовых и поверхностных вод. [59] [60] Из-за своей высокой растворимости и низкой задержки в почве нитраты могут легко выходить из подпочвенного слоя в грунтовые воды, вызывая загрязнение нитратами. Некоторые другие рассредоточенные источники загрязнения нитратами подземных вод связаны с кормлением скота, загрязнением животных и людей, а также бытовыми и промышленными отходами. Поскольку подземные воды часто служат основным источником бытовой воды, загрязнение нитратами может распространяться из подземных вод в поверхностные и питьевые воды в процессе производства питьевой воды , особенно для небольших общинных систем водоснабжения, где используются плохо регулируемые и антисанитарные воды. [61]
Стандарт ВОЗ для питьевой воды составляет 50 мг NO.−3L -1 для кратковременного воздействия и для 3 мг NO.−3L -1 хронические эффекты. [62] Попадая в организм человека, нитрат может вступать в реакцию с органическими соединениями посредством реакций нитрозирования в желудке с образованием нитрозаминов и нитрозамидов , которые участвуют в некоторых типах рака (например, раке полости рта и раке желудка ). [63]
Деятельность человека также радикально изменила глобальный цикл азота за счет производства азотистых газов, что связано с глобальным загрязнением атмосферы азотом. Существует множество источников атмосферных потоков реактивного азота (Nr). Сельскохозяйственные источники реактивного азота могут производить выбросы в атмосферу аммиака ( NH 3 ), оксидов азота ( NO
Икс) и закись азота ( N
2О ). Процессы горения в производстве энергии, на транспорте и в промышленности также могут приводить к образованию нового химически активного азота за счет выбросов NO .
Икс, непреднамеренный ненужный продукт. Когда эти химически активные азоты выбрасываются в нижние слои атмосферы, они могут вызвать образование смога, твердых частиц и аэрозолей, которые вносят основной вклад в неблагоприятное воздействие загрязнения воздуха на здоровье человека. [64] В атмосфере НЕТ.
2можно окислить до азотной кислоты ( HNO
3), и он может далее реагировать с NH
3с образованием нитрата аммония, что способствует образованию той или иной нитрата. Более того, НХ
3может реагировать с другими кислыми газами ( серной и соляной кислотами ) с образованием аммонийсодержащих частиц, которые являются предшественниками вторичных органических аэрозольных частиц в фотохимическом смоге . [65]
{{cite web}}: CS1 maint: несколько имен: список авторов ( ссылка ){{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка )