Позитронно-эмиссионная томография ( ПЭТ ) [1] представляет собой метод функциональной визуализации , в котором используются радиоактивные вещества, известные как радиофармпрепараты , для визуализации и измерения изменений в метаболических процессах и других физиологических процессах, включая кровоток , региональный химический состав и абсорбцию. Различные индикаторы используются для различных целей визуализации, в зависимости от целевого процесса в организме.
Например:
ПЭТ – распространенный метод визуализации , метод медицинской сцинтилографии , используемый в ядерной медицине . Радиофармацевтический препарат – радиоизотоп, присоединенный к лекарственному средству – вводится в организм в качестве индикатора . Когда радиофармпрепарат подвергается бета-распаду , испускается позитрон , а когда позитрон взаимодействует с обычным электроном, две частицы аннигилируют и два гамма-луча испускаются в противоположных направлениях. [2] Эти гамма-лучи улавливаются двумя гамма-камерами и формируют трехмерное изображение.
ПЭТ-сканеры могут включать в себя сканер компьютерной томографии (КТ) и известны как сканеры ПЭТ-КТ . Изображения ПЭТ-сканирования можно реконструировать с помощью компьютерной томографии, выполняемой с использованием одного сканера в течение одного сеанса.
Одним из недостатков ПЭТ-сканера является его высокая первоначальная стоимость и текущие эксплуатационные расходы. [3]
ПЭТ — это одновременно медицинский и исследовательский инструмент, используемый в доклинических и клинических условиях. Он широко используется при визуализации опухолей и поиске метастазов в области клинической онкологии , а также для клинической диагностики некоторых диффузных заболеваний головного мозга, например, вызывающих различные виды деменции . ПЭТ — ценный исследовательский инструмент, позволяющий изучить и расширить наши знания о нормальном человеческом мозге, функции сердца, а также поддержать разработку лекарств. ПЭТ также используется в доклинических исследованиях на животных. Это позволяет проводить повторные исследования одних и тех же субъектов с течением времени, где субъекты могут выступать в качестве собственного контроля, и существенно сокращает количество животных, необходимых для данного исследования. Такой подход позволяет исследовательским исследованиям сократить необходимый размер выборки, одновременно повышая статистическое качество ее результатов. [ нужна цитата ]
Физиологические процессы приводят к анатомическим изменениям в организме. Поскольку ПЭТ способен обнаруживать биохимические процессы, а также экспрессию некоторых белков, ПЭТ может предоставить информацию на молекулярном уровне задолго до того, как станут видны какие-либо анатомические изменения. ПЭТ-сканирование делает это с помощью меченных радиоактивным изотопом молекулярных зондов, которые имеют разную скорость поглощения в зависимости от типа и функции вовлеченной ткани. Региональное поглощение индикатора в различных анатомических структурах можно визуализировать и относительно количественно оценить с точки зрения введенного излучателя позитронов при ПЭТ-сканировании. [ нужна цитата ]
ПЭТ-визуализацию лучше всего выполнять с помощью специального ПЭТ-сканера. Также возможно получить изображения ПЭТ с помощью обычной двойной гамма-камеры, оснащенной детектором совпадений. Качество изображений ПЭТ, полученных с помощью гамма-камеры, ниже, а получение сканов занимает больше времени. Однако этот метод позволяет получить недорогое решение на месте для учреждений с низким спросом на ПЭТ-сканирование. Альтернативой может быть направление этих пациентов в другой центр или посещение с помощью мобильного сканера.
Альтернативные методы медицинской визуализации включают однофотонную эмиссионную компьютерную томографию (ОФЭКТ), компьютерную томографию (КТ), магнитно-резонансную томографию (МРТ), функциональную магнитно-резонансную томографию (фМРТ) и ультразвук . ОФЭКТ — это метод визуализации, аналогичный ПЭТ, который использует радиолиганды для обнаружения молекул в организме. ОФЭКТ дешевле и обеспечивает более низкое качество изображения, чем ПЭТ.

ПЭТ-сканирование с радиофармпрепаратом [ 18 F]фтордезоксиглюкозой (ФДГ) широко применяется в клинической онкологии. ФДГ представляет собой аналог глюкозы , который поглощается клетками, использующими глюкозу, и фосфорилируется гексокиназой ( митохондриальная форма которой значительно повышена в быстро растущих злокачественных опухолях). [4] Метаболическое улавливание радиоактивной молекулы глюкозы позволяет использовать ПЭТ-сканирование. Концентрации отображаемого индикатора ФДГ указывают на метаболическую активность тканей, поскольку они соответствуют региональному поглощению глюкозы. ФДГ используется для изучения возможности распространения рака на другие участки тела ( метастазирования рака ). Эти ПЭТ-сканирования с ФДГ для выявления метастазов рака наиболее распространены в стандартной медицинской помощи (составляют 90% текущих сканирований). Тот же индикатор можно также использовать для диагностики типов деменции . Реже другие радиоактивные индикаторы , обычно, но не всегда, меченные фтором-18 ( 18 F), используются для визуализации концентрации в тканях различных типов представляющих интерес молекул внутри организма. [ нужна цитата ]
Типичная доза ФДГ, используемая при онкологическом сканировании, имеет эффективную дозу облучения 7,6 мЗв . [5] Поскольку гидроксигруппа, которая заменяется фтором-18 для образования ФДГ, необходима для следующего этапа метаболизма глюкозы во всех клетках, никаких дальнейших реакций в ФДГ не происходит. Более того, большинство тканей (за исключением печени и почек) не могут удалять фосфат, добавляемый гексокиназой. Это означает, что ФДГ задерживается в любой клетке, которая его поглощает, до тех пор, пока она не распадется, поскольку фосфорилированные сахара из-за своего ионного заряда не могут выйти из клетки. Это приводит к интенсивному радиоактивному мечению тканей с высоким поглощением глюкозы, таких как нормальный мозг, печень, почки и большинство раковых опухолей, которые имеют более высокое поглощение глюкозы, чем большинство нормальных тканей, из-за эффекта Варбурга . В результате ФДГ-ПЭТ может использоваться для диагностики, определения стадии и мониторинга лечения рака, особенно лимфомы Ходжкина , [6] неходжкинской лимфомы , [7] и рака легких . [8] [9] [10]
Обзор исследований по использованию ПЭТ при лимфоме Ходжкина в 2020 году обнаружил доказательства того, что отрицательные результаты промежуточных ПЭТ-сканирований связаны с более высокой общей выживаемостью и выживаемостью без прогрессирования ; однако достоверность имеющихся данных была умеренной в отношении выживаемости и очень низкой в отношении выживаемости без прогрессирования. [11]
Несколько других изотопов и радиофармпрепаратов постепенно внедряются в онкологию для конкретных целей. Например,Метомидат, меченный 11 C (11 C-метомидат), использовался для обнаружения опухолей надпочечникового происхождения. [12] [13] Кроме того, ПЭТ/КТ с фтородопой ( FDOPA ) (также называемая ПЭТ/КТ F-18-DOPA) оказалась более чувствительной альтернативой обнаружению и локализации феохромоцитомы , чем сканирование с иобенгуаном (MIBG) . [14] [15] [16]

ПЭТ-визуализация с кислородом-15 косвенно измеряет приток крови к мозгу. В этом методе повышенный сигнал радиоактивности указывает на усиление кровотока, что, как предполагается, коррелирует с повышенной активностью мозга. Из-за периода полураспада кислорода-15, составляющего 2 минуты , для такого использования кислород-15 необходимо подавать непосредственно из медицинского циклотрона , что затруднительно. [17]
ПЭТ-визуализация с ФДГ использует тот факт, что мозг обычно быстро потребляет глюкозу. Стандартная ФДГ-ПЭТ головного мозга измеряет региональное использование глюкозы и может использоваться в диагностике нейропатологий.
Патологии головного мозга, такие как болезнь Альцгеймера (БА), значительно снижают мозговой метаболизм глюкозы и кислорода одновременно. Поэтому ФДГ-ПЭТ головного мозга также может быть использована для успешной дифференциации болезни Альцгеймера от других процессов деменции, а также для ранней диагностики болезни Альцгеймера. Преимуществом FDG PET для этих целей является его гораздо более широкая доступность. Некоторые радиоактивные индикаторы на основе фтора-18, используемые при болезни Альцгеймера, включают флорбетапир , флютеметамол , питтсбургское соединение B (PiB) и флорбетабен , которые используются для обнаружения бета-амилоидных бляшек, потенциального биомаркера болезни Альцгеймера в мозге. [18]
ПЭТ-визуализация с ФДГ также может использоваться для локализации «очага припадка». Во время межприступного сканирования очаг приступа будет выглядеть как гипометаболический. [19] Для ПЭТ было разработано несколько радиотрейсеров (т.е. радиолигандов), которые являются лигандами для конкретных подтипов нейрорецепторов , таких как [ 11 C] раклоприд , [ 18 F] фаллиприд и [ 18 F] десметоксифаллиприд для дофаминовых рецепторов D 2 / D 3 ; [ 11 C] McN5652 и [ 11 C] DASB для переносчиков серотонина ; [ 18 F] mefway для серотониновых 5НТ 1А рецепторов ; и [ 18 F] Нифен для никотиновых рецепторов ацетилхолина или субстратов ферментов (например, 6- FDOPA для фермента AADC ). Эти агенты позволяют визуализировать пулы нейрорецепторов в контексте множества нервно-психических и неврологических заболеваний.
ПЭТ также может использоваться для диагностики склероза гиппокампа , вызывающего эпилепсию. С этой целью были исследованы ФДГ и менее распространенные индикаторы флумазенил и MPPF . [20] [21] Если склероз односторонний (правый или левый гиппокамп), поглощение ФДГ можно сравнить со здоровой стороной. Даже если диагноз с помощью МРТ затруднен, его можно поставить с помощью ПЭТ. [22] [23]
Разработка ряда новых зондов для неинвазивной ПЭТ - визуализации нейроагрегатов в головном мозге человека приблизила визуализацию амилоида к клиническому использованию. Самые ранние зонды для визуализации амилоида включали [ 18 F]FDNP [24], разработанный в Калифорнийском университете в Лос-Анджелесе, и питтсбургское соединение B (PiB) [25], разработанное в Питтсбургском университете . Эти зонды позволяют визуализировать амилоидные бляшки в мозге пациентов с болезнью Альцгеймера и могут помочь клиницистам в постановке положительного клинического диагноза БА прижизненно, а также в разработке новых антиамилоидных методов лечения. [ 11 C] полиметилпентен (ПМП) представляет собой новый радиофармацевтический препарат, используемый в ПЭТ-визуализации для определения активности ацетилхолинергической нейротрансмиттерной системы, действуя в качестве субстрата для ацетилхолинэстеразы . Посмертное обследование пациентов с АД показало снижение уровня ацетилхолинэстеразы. [ 11 C]PMP используется для картирования активности ацетилхолинэстеразы в головном мозге, что может позволить проводить присмертную диагностику БА и контролировать лечение БА. [26] Компания Avid Radiopharmaceuticals разработала и коммерциализирует соединение под названием флорбетапир, которое использует радионуклид более длительного действия фтор-18 для обнаружения амилоидных бляшек с помощью ПЭТ-сканирования. [27]
Изучить связи между конкретными психологическими процессами или расстройствами и активностью мозга.
Многочисленные соединения, избирательно связывающиеся с нейрорецепторами, представляющими интерес для биологической психиатрии, были помечены радиоактивным изотопом C-11 или F-18. Радиолиганды, которые связываются с рецепторами дофамина ( D 1 , [28] D 2 , [29] [30] транспортер обратного захвата), рецепторами серотонина ( 5HT 1A , 5HT 2A , транспортер обратного захвата), опиоидными рецепторами ( мю и каппа ), холинергическими рецепторами ( никотиновый и мускариновый ) и другие сайты успешно использовались в исследованиях на людях. Были проведены исследования по изучению состояния этих рецепторов у пациентов по сравнению со здоровыми людьми при шизофрении , злоупотреблении психоактивными веществами , расстройствах настроения и других психических состояниях. [ нужна цитата ]
ПЭТ также может использоваться в хирургии под визуальным контролем для лечения внутричерепных опухолей, артериовенозных мальформаций и других состояний, поддающихся хирургическому лечению. [31]
Кардиология , исследование атеросклероза и сосудистых заболеваний: ПЭТ с ФДГ может помочь в выявлении гибернирующего миокарда . Однако экономическая эффективность ПЭТ для этой роли по сравнению с ОФЭКТ неясна. Также возможна ФДГ-ПЭТ-визуализация атеросклероза для выявления пациентов с риском инсульта . Кроме того, это может помочь проверить эффективность новых методов лечения атеросклероза. [32]
Визуализация инфекций с помощью технологий молекулярной визуализации может улучшить диагностику и последующее лечение. В клинической практике ПЭТ широко используется для визуализации бактериальных инфекций с использованием ФДГ для выявления воспалительной реакции, связанной с инфекцией. Для визуализации бактериальных инфекций in vivo были разработаны три различных контрастных вещества для ПЭТ: [ 18 F] мальтоза , [33] [ 18 F]мальтогексаоза и [ 18 F]2-фтордезоксисорбит ( FDS). [34] FDS имеет дополнительное преимущество, поскольку может воздействовать только на Enterobacteriaceae .
В ходе доклинических испытаний новый препарат можно пометить радиоактивным изотопом и ввести животным. Такие сканирования называются исследованиями биораспределения. Информацию о поглощении, удержании и выведении лекарств с течением времени можно получить быстро и с меньшими затратами по сравнению со старыми методами умерщвления и вскрытия животных. Обычно о присутствии лекарственного средства в предполагаемом месте действия можно косвенно судить по результатам исследований конкуренции между немеченым лекарственным средством и радиоактивно мечеными соединениями за специфичность связывания с этим участком. Таким образом, один радиолиганд можно использовать для тестирования множества потенциальных кандидатов на лекарство для одной и той же цели. Сопутствующий метод включает сканирование с помощью радиолигандов, которые конкурируют с эндогенным (естественным) веществом на данном рецепторе, чтобы продемонстрировать, что лекарство вызывает высвобождение природного вещества. [35]
Был создан миниатюрный ПЭТ для животных, который достаточно мал для сканирования полностью находящейся в сознании крысы . [36] Этот RatCAP (ПЭТ-ПЭТ для крыс в сознании) позволяет сканировать животных без мешающего воздействия анестезии . ПЭТ-сканеры, разработанные специально для визуализации грызунов , часто называемые микроПЭТ, а также сканеры для мелких приматов , продаются для академических и фармацевтических исследований. Сканеры основаны на микроминиатюрных сцинтилляторах и усиливающих лавинных фотодиодах (ЛФД) через систему, в которой используются однокристальные кремниевые фотоумножители . [1]
В 2018 году Школа ветеринарной медицины Калифорнийского университета в Дэвисе стала первым ветеринарным центром, который использовал небольшой клинический ПЭТ-сканер в качестве сканера для клинической (а не исследовательской) диагностики животных. Ожидается, что из-за стоимости, а также предельной полезности обнаружения метастазов рака у домашних животных (основное использование этого метода) ветеринарное ПЭТ-сканирование в ближайшем будущем будет редко доступно. [ нужна цитата ]
ПЭТ-визуализация использовалась для визуализации мышц и костей. ФДГ является наиболее часто используемым индикатором для визуализации мышц, а NaF-F18 — наиболее широко используемым индикатором для визуализации костей.
ПЭТ — это возможный метод исследования скелетных мышц во время физических упражнений. [37] Кроме того, ПЭТ может предоставить данные об активации глубоко расположенных мышц (таких как промежуточная широкая мышца и малая ягодичная мышца ) по сравнению с такими методами, как электромиография , которые можно использовать только на поверхностных мышцах непосредственно под кожей. Однако недостатком является то, что ПЭТ не дает информации о времени активации мышц, поскольку ее необходимо измерять после завершения упражнения. Это связано со временем, которое требуется ФДГ для накопления в активированных мышцах. [ нужна цитата ]
Вместе с [ 18 F] фторидом натрия ПЭТ для визуализации костей используется уже 60 лет для измерения регионального костного метаболизма и кровотока с использованием статического и динамического сканирования. Недавно исследователи также начали использовать [ 18 F] фторид натрия для изучения костных метастазов. [38]
ПЭТ-сканирование неинвазивно, но предполагает воздействие ионизирующего излучения . [3] ФДГ, который в настоящее время является стандартным радиофармпрепаратом, используемым для ПЭТ-нейровизуализации и лечения онкологических больных, [39] имеет эффективную дозу облучения 14 мЗв . [5]
Количество радиации в ФДГ аналогично эффективной дозе пребывания за один год в американском городе Денвер, штат Колорадо (12,4 мЗв/год). [40] Для сравнения, дозировка радиации при других медицинских процедурах колеблется от 0,02 мЗв для рентгенографии грудной клетки до 6,5–8 мЗв для компьютерной томографии грудной клетки. [41] [42] В среднем гражданские летные экипажи подвергаются дозе 3 мЗв/год, [43] а предел профессиональной дозы для всего тела для работников атомной энергетики в США составляет 50 мЗв/год. [44] О масштабе см. Порядки величины (излучение) .
При ПЭТ-КТ-сканировании радиационное воздействие может быть значительным — около 23–26 мЗв (для человека массой 70 кг доза, вероятно, будет выше при большей массе тела). [45] [46]

Радионуклиды включаются либо в соединения, обычно используемые организмом, такие как глюкоза (или аналоги глюкозы), вода или аммиак , либо в молекулы, которые связываются с рецепторами или другими местами действия лекарств. Такие меченые соединения известны как радиоиндикаторы . Технология ПЭТ может использоваться для отслеживания биологического пути любого соединения у живых людей (а также у многих других видов) при условии, что оно может быть помечено радиоактивным изотопом ПЭТ. Таким образом, конкретные процессы, которые можно исследовать с помощью ПЭТ, практически безграничны, а радиоиндикаторы для новых целевых молекул и процессов продолжают синтезироваться. На момент написания этой статьи десятки из них уже используются в клинической практике и сотни применяются в исследованиях. В 2020 году наиболее часто используемым радиофармпрепаратом при клиническом ПЭТ-сканировании является производное углеводов ФДГ. Этот радиофармпрепарат используется практически во всех онкологических исследованиях и большинстве сканирований в неврологии, таким образом, он составляет большую часть радиофармпрепаратов (>95%), используемых при ПЭТ и ПЭТ-КТ.
Из-за короткого периода полураспада большинства радиоизотопов, излучающих позитроны, радиоиндикаторы традиционно производятся с использованием циклотрона в непосредственной близости от установки для получения изображений ПЭТ. Период полураспада фтора-18 достаточно велик, чтобы радиоизотопные индикаторы, меченные фтором-18, можно было производить на коммерческой основе за пределами предприятия и отправлять в центры визуализации. Недавно генераторы рубидия-82 стали коммерчески доступны. [48] Они содержат стронций-82, который распадается в результате захвата электронов с образованием рубидия-82, испускающего позитроны.
Был рассмотрен обзор использования позитронно-эмиссионных изотопов металлов при ПЭТ-сканировании, включая элементы, не перечисленные выше, такие как лантаноиды. [49]
Изотоп 89 Zr применялся для отслеживания и количественного определения молекулярных антител с помощью ПЭТ-камер (метод, называемый «иммуно-ПЭТ»). [50] [51] [52]
Биологический период полураспада антител обычно составляет несколько дней, см., например, даклизумаб и эренумаб . Для визуализации и количественной оценки распределения таких антител в организме хорошо подходит ПЭТ-изотоп 89 Zr, поскольку его физический период полураспада соответствует типичному биологическому периоду полураспада антител, см. таблицу выше.

Для проведения сканирования живому субъекту (обычно в кровообращение) вводится короткоживущий радиоактивный изотоп-индикатор . Каждый атом-индикатор химически включен в биологически активную молекулу. Существует период ожидания, пока активная молекула концентрируется в интересующих тканях. Затем объект помещается в сканер изображений. Молекулой, наиболее часто используемой для этой цели, является ФДГ, сахар, период ожидания которого обычно составляет час. Во время сканирования производится запись концентрации в ткани по мере распада индикатора.
Когда радиоизотоп подвергается эмиссионному позитронному распаду (также известному как положительный бета-распад ), он испускает позитрон, античастицу электрона с противоположным зарядом. Испущенный позитрон перемещается в ткани на небольшое расстояние (обычно менее 1 мм, но в зависимости от изотопа [53] ), в течение которого он теряет кинетическую энергию, пока не замедляется до точки, где он может взаимодействовать с электроном. [54] Столкновение аннигилирует как электрон, так и позитрон, создавая пару аннигиляционных ( гамма ) фотонов , движущихся примерно в противоположных направлениях. Они обнаруживаются, когда достигают сцинтиллятора в сканирующем устройстве, создавая вспышку света, которая обнаруживается фотоумножителями или кремниевыми лавинными фотодиодами (Si APD). Методика зависит от одновременного или одновременного обнаружения пары фотонов, движущихся примерно в противоположных направлениях (они были бы точно противоположны в их центре масс , но сканер не имеет возможности узнать это, и поэтому имеет встроенное небольшое направление). - толерантность к ошибкам). Фотоны, которые не прибывают во времени «парами» (т.е. в пределах временного окна в несколько наносекунд), игнорируются.
Наиболее значительная часть электрон-позитронной аннигиляции приводит к излучению двух гамма-фотонов с энергией 511 кэВ под углом почти 180 градусов друг к другу. Следовательно, можно локализовать их источник вдоль прямой линии совпадения (также называемой линией отклика , или ЛОР ). На практике LOR имеет ненулевую ширину, поскольку испускаемые фотоны не расположены точно на 180 градусов друг от друга. Если разрешающее время детекторов составляет менее 500 пикосекунд , а не около 10 наносекунд , можно локализовать событие на сегменте хорды , длина которого определяется временным разрешением детектора. По мере улучшения временного разрешения отношение сигнал/шум (SNR) изображения будет улучшаться, поэтому для достижения того же качества изображения потребуется меньше событий. Эта технология пока не распространена, но она доступна в некоторых новых системах. [55]
Необработанные данные, собранные ПЭТ-сканером, представляют собой список «событий совпадений», представляющих почти одновременное обнаружение (обычно в пределах окна от 6 до 12 наносекунд друг от друга) аннигиляционных фотонов парой детекторов. Каждое событие совпадения представляет собой линию в пространстве, соединяющую два детектора, вдоль которой произошла эмиссия позитрона (т. е. линию отклика (ЛОР)).
Обычно используются аналитические методы, во многом подобные реконструкции данных компьютерной томографии (КТ) и однофотонной эмиссионной компьютерной томографии (ОФЭКТ), хотя набор данных , собранный с помощью ПЭТ, намного беднее, чем с помощью КТ, поэтому методы реконструкции более сложны. Совпадающие события можно сгруппировать в проекционные изображения, называемые синограммами . Синограммы сортируются по углу обзора и наклону (для 3D-изображений). Изображения синограмм аналогичны проекциям, снятым компьютерными томографами, и могут быть реконструированы аналогичным образом. Статистика полученных таким образом данных значительно хуже, чем статистика, полученная с помощью трансмиссионной томографии. Обычный набор данных ПЭТ содержит миллионы отсчетов для всего сбора данных, тогда как КТ может достигать нескольких миллиардов отсчетов. Это приводит к тому, что ПЭТ-изображения кажутся «более шумными», чем КТ. Двумя основными источниками шума в ПЭТ являются рассеяние (обнаруженная пара фотонов, по крайней мере один из которых был отклонен от исходного пути в результате взаимодействия с веществом в поле зрения, что привело к тому, что паре был присвоен неправильный LOR) и случайный события (фотоны, возникшие в результате двух разных событий аннигиляции, но неправильно записанные как пара совпадений, поскольку их прибытие в соответствующие детекторы произошло в пределах временного окна совпадения).
На практике требуется значительная предварительная обработка данных – поправка на случайные совпадения, оценка и вычитание рассеянных фотонов, коррекция мертвого времени детектора (после регистрации фотона детектор должен снова «остыть») и детектор- коррекция чувствительности (как для собственной чувствительности детектора, так и для изменения чувствительности из-за угла падения).
Обратная проекция с фильтром (FBP) часто используется для восстановления изображений по проекциям. Преимущество этого алгоритма заключается в его простоте и малой потребности в вычислительных ресурсах. Недостатком является то, что дробовой шум в необработанных данных заметен на реконструированных изображениях, а области с высоким поглощением трассера имеют тенденцию образовывать полосы поперек изображения. Кроме того, FBP обрабатывает данные детерминированно – он не учитывает присущую им случайность, связанную с данными ПЭТ, поэтому требует всех корректировок перед реконструкцией, описанных выше.
Статистические подходы, основанные на правдоподобии . Статистические, основанные на правдоподобии [56] [57] итеративные алгоритмы максимизации ожидания, такие как алгоритм Шеппа-Варди [58], в настоящее время являются предпочтительным методом реконструкции. Эти алгоритмы вычисляют оценку вероятного распределения событий аннигиляции, которые привели к получению измеренных данных, на основе статистических принципов. Преимущество — лучший профиль шума и устойчивость к полосовым артефактам, характерным для FBP, но недостатком — более высокие требования к компьютерным ресурсам. Еще одним преимуществом методов статистической реконструкции изображений является то, что в вероятность можно включить физические эффекты, которые необходимо предварительно скорректировать при использовании алгоритма аналитической реконструкции, такие как рассеянные фотоны, случайные совпадения, затухание и мертвое время детектора. модель, используемая при реконструкции, позволяющая дополнительно снизить шум. Также было показано, что итеративная реконструкция приводит к улучшению разрешения реконструированных изображений, поскольку в правдоподобную модель можно включить более сложные модели физики сканера, чем те, которые используются методами аналитической реконструкции, что позволяет улучшить количественную оценку распределения радиоактивности. [59]
Исследования показали, что байесовские методы, включающие функцию правдоподобия Пуассона и соответствующую априорную вероятность (например, предварительное сглаживание, ведущее к полной регуляризации вариаций , или распределение Лапласа , ведущее к регуляризации на основе - вейвлета или другой области), например, с помощью Ульфа Гренандера Оценка сита [ 60] [61] или с помощью методов штрафа Байеса [62] [63] или с помощью метода шероховатости И. Дж. Гуда [64] [65] может обеспечить более высокую производительность по сравнению с методами, основанными на максимизации ожидания, которые включают в себя метод Пуассона. функция правдоподобия, но не используйте такой априор. [66] [67] [68]
Коррекция затухания : Количественная ПЭТ-визуализация требует коррекции затухания. [69] В этих системах коррекция затухания основана на сканировании пропускания с использованием вращающегося стержневого источника на 68 Ge. [70]
Сканирование передачи напрямую измеряет значения затухания при 511 кэВ. [71] Ослабление происходит, когда фотоны, испускаемые радиофармпрепаратом внутри тела, поглощаются тканями, находящимися между детектором и испускаемым фотоном. Поскольку разные LOR должны проходить через ткань разной толщины, фотоны ослабляются по-разному. В результате структуры глубоко в организме реконструируются как имеющие ложно низкое поглощение индикатора. Современные сканеры могут оценивать затухание с помощью встроенного рентгеновского КТ-оборудования вместо более раннего оборудования, которое предлагало грубую форму КТ с использованием источника гамма-лучей ( излучающих позитроны ) и ПЭТ-детекторов.
Хотя изображения с коррекцией затухания, как правило, являются более точным представлением, процесс коррекции сам по себе подвержен значительным артефактам. В результате как исправленные, так и нескорректированные изображения всегда реконструируются и читаются вместе.
2D/3D реконструкция . Ранние ПЭТ-сканеры имели только одно кольцо детекторов, поэтому сбор данных и последующая реконструкция были ограничены одной поперечной плоскостью. Более современные сканеры теперь включают в себя несколько колец, по сути образующих цилиндр детекторов.
Существует два подхода к восстановлению данных с такого сканера:
3D-методы обладают большей чувствительностью (поскольку обнаруживается и используется больше совпадений), следовательно, меньше шума, но более чувствительны к эффектам разброса и случайных совпадений, а также требуют больше компьютерных ресурсов. Появление детекторов с временным разрешением менее наносекунды обеспечивает лучшее отклонение случайных совпадений, что способствует реконструкции трехмерного изображения.
Времяпролетное (TOF) ПЭТ : в современных системах с более высоким временным разрешением (примерно 3 наносекунды) для улучшения общей производительности используется метод, называемый «времяпролетным». Времяпролетный ПЭТ использует очень быстрые детекторы гамма-излучения и систему обработки данных, которые могут более точно определить разницу во времени между обнаружением двух фотонов. Точно локализовать точку возникновения аннигиляционного события невозможно (в настоящее время в пределах 10 см). Поэтому реконструкция изображения все еще необходима. Метод TOF дает значительное улучшение качества изображения, особенно соотношения сигнал/шум.
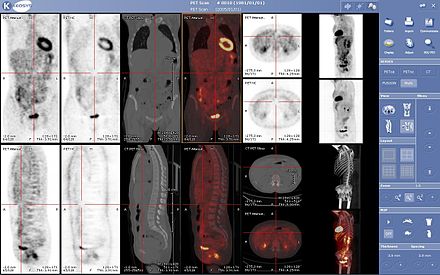

ПЭТ-сканы все чаще считываются вместе с КТ или МРТ, причем их комбинация ( совместная регистрация ) дает как анатомическую, так и метаболическую информацию (т. е., какова структура и что она делает биохимически). Поскольку ПЭТ-визуализация наиболее полезна в сочетании с анатомической визуализацией, такой как КТ, современные ПЭТ-сканеры теперь доступны со встроенными высокопроизводительными КТ-сканерами с несколькими рядами детекторов (ПЭТ-КТ). Поскольку два сканирования могут выполняться в непосредственной последовательности во время одного и того же сеанса, при этом пациент не меняет положение между двумя типами сканирований, два набора изображений регистрируются более точно , так что области отклонений на ПЭТ-изображениях могут быть более точными. прекрасно коррелирует с анатомией на КТ-изображениях. Это очень полезно для демонстрации подробных изображений движущихся органов или структур с более высокими анатомическими вариациями, которые чаще встречаются за пределами мозга.
В Институте нейронаук и биофизики Юлиха в апреле 2009 года начал работу самый большой в мире аппарат ПЭТ-МРТ. Магнитно-резонансный томограф (МРТ) с силой тока 9,4 Тесла в сочетании с ПЭТ. В настоящее время при такой высокой напряженности магнитного поля можно получить изображения только головы и мозга. [72]
Для визуализации головного мозга регистрация КТ, МРТ и ПЭТ-сканирований может быть выполнена без необходимости использования встроенного сканера ПЭТ-КТ или ПЭТ-МРТ с использованием устройства, известного как N-локализатор . [31] [73] [74] [75]
Минимизация дозы облучения субъекта является привлекательной особенностью использования короткоживущих радионуклидов. Помимо своей устоявшейся роли в качестве диагностического метода, ПЭТ играет расширяющуюся роль как метод оценки ответа на терапию, в частности на терапию рака [76] , где риск для пациента из-за отсутствия знаний о ходе заболевания намного выше, чем риск риск от испытательного излучения. Поскольку трассеры радиоактивны, пожилые [ сомнительно ] и беременные не могут их использовать из-за рисков, связанных с радиацией.
Ограничения на широкое использование ПЭТ возникают из-за высокой стоимости циклотронов, необходимых для производства короткоживущих радионуклидов для ПЭТ-сканирования, и необходимости специально адаптированного оборудования для химического синтеза на месте для производства радиофармацевтических препаратов после получения радиоизотопов. Молекулы органических радиоизотопов, которые будут содержать радиоизотоп, излучающий позитроны, не могут быть сначала синтезированы, а затем приготовлены в них радиоизотопы, поскольку бомбардировка циклотроном для получения радиоизотопа разрушает любой органический носитель для него. Вместо этого сначала необходимо приготовить изотоп, а затем очень быстро, за короткое время до распада изотопа, выполнить химические процессы по приготовлению любого органического радиоизотопа (например, ФДГ). Лишь немногие больницы и университеты способны поддерживать такие системы, а большая часть клинической ПЭТ поддерживается сторонними поставщиками радиофармпрепаратов, которые могут снабжать множество учреждений одновременно. Это ограничение ограничивает клиническую ПЭТ прежде всего использованием индикаторов, меченных фтором-18, период полураспада которого составляет 110 минут и которые можно транспортировать на разумное расстояние перед использованием, или рубидием-82 (используемым в виде хлорида рубидия-82 ) с период полураспада 1,27 минуты, который создается в портативном генераторе и используется для исследований перфузии миокарда . В последние годы несколько локальных циклотронов со встроенной защитой и «горячих лабораторий» (автоматизированных химических лабораторий, способных работать с радиоизотопами) начали сопровождать установки ПЭТ в отдаленные больницы. Наличие небольшого локального циклотрона обещает расшириться в будущем, поскольку циклотроны уменьшаются в ответ на высокую стоимость транспортировки изотопов к удаленным машинам ПЭТ. [77] В последние годы нехватка ПЭТ-сканирований в США уменьшилась, поскольку количество радиоаптек, поставляющих радиоизотопы, выросло на 30% в год. [78]
Поскольку период полураспада фтора-18 составляет около двух часов, приготовленная доза радиофармпрепарата, содержащего этот радионуклид, в течение рабочего дня претерпит несколько периодов полураспада. Это требует частой повторной калибровки оставшейся дозы (определение активности на единицу объема) и тщательного планирования графика приема пациентов.

Концепция эмиссионной и трансмиссионной томографии была представлена Дэвидом Э. Кулем , Люком Чепменом и Роем Эдвардсом в конце 1950-х годов. Их работа позже привела к проектированию и созданию нескольких томографических инструментов в Пенсильванском университете . В 1975 году методы томографической визуализации получили дальнейшее развитие Мишель Тер-Погосян , Майкл Э. Фелпс , Эдвард Дж. Хоффман и другие в Медицинской школе Вашингтонского университета . [79] [80]
Работа Гордона Браунелла, Чарльза Бернема и их коллег в Массачусетской больнице общего профиля , начавшаяся в 1950-х годах, внесла значительный вклад в развитие технологии ПЭТ и включала первую демонстрацию аннигиляционного излучения для медицинской визуализации. [81] Их инновации, в том числе использование световодов и объемного анализа, сыграли важную роль в развертывании ПЭТ-визуализации. В 1961 году Джеймс Робертсон и его коллеги из Брукхейвенской национальной лаборатории создали первый одноплоскостной ПЭТ-сканер, получивший прозвище «сжиматель головы». [82]
Одним из факторов, наиболее ответственных за признание позитронной визуализации, была разработка радиофармацевтических препаратов. В частности, была разработана группой из Брукхейвена под руководством Эла Вольфа и Джоанны Фаулер меченая 2-фтордезокси-D-глюкоза (ФДГ-впервые синтезирована и описана двумя чешскими учеными из Карлова университета в Праге в 1968 году) [83]. основной фактор в расширении возможностей ПЭТ-визуализации. [84] Соединение впервые было введено Абасом Алави двум нормальным людям-добровольцам в августе 1976 года в Пенсильванском университете. Изображения мозга, полученные с помощью обычного ядерного сканера (не ПЭТ), продемонстрировали концентрацию ФДГ в этом органе. Позже это вещество использовалось в специальных позитронных томографах, чтобы создать современную процедуру.
Логическим продолжением позитронной аппаратуры стала конструкция с использованием двух двумерных матриц. PC-I был первым прибором, использующим эту концепцию, он был разработан в 1968 году, завершен в 1969 году и о нем сообщалось в 1972 году. О первых применениях PC-I в томографическом режиме, отличном от режима компьютерной томографии, сообщалось в 1970 году. [85 ] вскоре многим из тех, кто участвовал в разработке ПЭТ, стало ясно, что круглая или цилиндрическая решетка детекторов является логическим следующим шагом в создании приборов для ПЭТ. Хотя многие исследователи придерживались этого подхода, Джеймс Робертсон [86] и Занг-Хи Чо [87] были первыми, кто предложил кольцевую систему, которая стала прототипом современной формы ПЭТ.
Сканер ПЭТ-КТ, авторство которого принадлежит Дэвиду Таунсенду и Рональду Натту, был назван журналом Time в 2000 году медицинским изобретением года. [88]
По состоянию на август 2008 года Cancer Care Ontario сообщает, что текущие средние дополнительные затраты на выполнение ПЭТ-сканирования в провинции составляют 1000–1200 канадских долларов за сканирование. Сюда входит стоимость радиофармпрепарата и стипендия врачу, проводящему сканирование. [89]
В Соединенных Штатах стоимость ПЭТ-сканирования оценивается в 1500–5000 долларов США.
В Англии справочная стоимость амбулаторной ПЭТ-сканирования для взрослых, установленная Национальной службой здравоохранения (2015–2016 гг.), составляет 798 фунтов стерлингов. [90]
В Австралии по состоянию на июль 2018 года плата за план льгот Medicare за ПЭТ с ФДГ всего тела варьируется от 953 до 999 австралийских долларов, в зависимости от показаний к сканированию. [91]
Общую производительность ПЭТ-систем можно оценить с помощью инструментов контроля качества, таких как фантом Ящака . [92]
{{cite journal}}: Требуется цитировать журнал |journal=( помощь )