Ангиопластика , также известная как баллонная ангиопластика и чрескожная транслюминальная ангиопластика ( ЧТА ), представляет собой минимально инвазивную эндоваскулярную процедуру , используемую для расширения суженных или закупоренных артерий или вен, обычно для лечения артериального атеросклероза . [1]
Сдутый баллон, прикрепленный к катетеру ( баллонный катетер ), проводят по проводнику в суженный сосуд , а затем надувают до фиксированного размера. [1] Баллон расширяет кровеносный сосуд и окружающую мышечную стенку, обеспечивая улучшение кровотока. [1] Стент может быть установлен во время надувания баллона , чтобы гарантировать, что сосуд остается открытым, а затем баллон сдувается и извлекается. [2] Ангиопластика стала включать в себя все виды сосудистых вмешательств, которые обычно выполняются чрескожно .
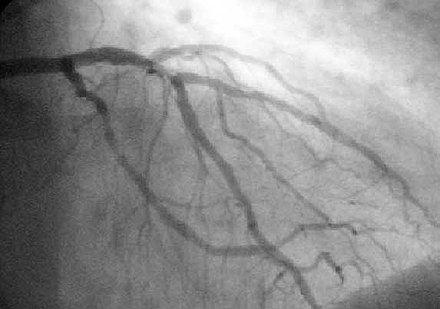
Коронарная ангиопластика — это терапевтическая процедура для лечения стенозированных (суженных) коронарных артерий сердца , возникающих при ишемической болезни сердца . [1] Эти стенотические сегменты коронарных артерий возникают из-за накопления холестериновых бляшек , которые образуются при состоянии, известном как атеросклероз . [3] Чрескожное коронарное вмешательство ( ЧКВ) или коронарная ангиопластика со стентированием — это нехирургическая процедура, используемая для улучшения притока крови к сердцу. [1]
Коронарная ангиопластика показана при заболеваниях коронарных артерий, таких как нестабильная стенокардия , ИМбпST , ИМпST и спонтанная перфорация коронарной артерии. [1] Было показано, что ЧКВ при стабильной ишемической болезни сердца значительно облегчает такие симптомы, как стенокардия или боль в груди, тем самым улучшая функциональные ограничения и качество жизни. [4]
Периферическая ангиопластика подразумевает использование баллона для открытия кровеносного сосуда за пределами коронарных артерий. Чаще всего это делается для лечения атеросклеротических сужений брюшной полости, ног и почечных артерий, вызванных заболеванием периферических артерий . Часто периферическую ангиопластику используют в сочетании с проволочным направителем, периферическим стентированием и атерэктомией . [5]
Ангиопластику можно использовать для лечения запущенного заболевания периферических артерий , чтобы облегчить хромоту или боль в ногах, которая классически связана с этим заболеванием. [6]
В исследовании BASIL в сравнении с шунтированием и ангиопластикой при тяжелой ишемии ног (BASIL) сначала изучали инфраингвинальное шунтирование по сравнению с ангиопластикой у отдельных пациентов с тяжелой ишемией нижних конечностей, которые были кандидатами на любую процедуру. Исследование BASIL показало, что ангиопластика связана с меньшей краткосрочной заболеваемостью по сравнению с операцией шунтирования, однако долгосрочные результаты говорят в пользу шунтирования. [7]
На основании исследования BASIL рекомендации ACCF/AHA рекомендуют баллонную ангиопластику только пациентам с ожидаемой продолжительностью жизни 2 года или менее или тем, у кого нет аутогенной вены . Пациентам с ожидаемой продолжительностью жизни более 2 лет или пациентам с аутогенной веной в первую очередь может быть проведено шунтирование. [8]
Стеноз почечной артерии связан с гипертензией и потерей функции почек . [9] Атеросклеротическую обструкцию почечной артерии можно лечить с помощью ангиопластики со стентированием почечной артерии или без него. [10] Существует слабая рекомендация по ангиопластике почечных артерий у пациентов со стенозом почечной артерии, резкими отеками или застойной сердечной недостаточностью. [10]
Стеноз сонной артерии можно лечить с помощью ангиопластики и стентирования сонных артерий у пациентов с высоким риском каротидной эндартерэктомии (КЭА). [11] Хотя каротидная эндартерэктомия обычно предпочтительнее стентирования сонной артерии, стентирование показано некоторым пациентам с радиационно-индуцированным стенозом или поражением сонной артерии, не подходящим для хирургического вмешательства. [12]
Ангиопластика используется для лечения венозного стеноза, влияющего на доступ к диализу , при этом баллонная ангиопластика с лекарственным покрытием обеспечивает лучшую проходимость через 6 и 12 месяцев, чем традиционная баллонная ангиопластика. [13] Ангиопластика иногда используется для лечения остаточного стеноза подключичной вены после декомпрессионной операции по поводу синдрома грудного апертуры . [14] Существует слабая рекомендация по стентированию глубоких вен для лечения обструктивного хронического заболевания вен. [15]
Ангиопластика требует сосуда доступа, обычно бедренной или лучевой артерии или бедренной вены , чтобы обеспечить доступ к сосудистой системе для используемых проводов и катетеров . Если нет доступного сосуда достаточного размера и качества, ангиопластика противопоказана. Небольшой диаметр сосуда, наличие задней кальцификации, окклюзии, гематомы или ранее установленное шунтирующее устройство могут слишком затруднить доступ к сосудистой системе. [ нужна цитата ]
Чрескожная транслюминальная коронарная ангиопластика (ЧТКА) противопоказана пациентам с заболеванием левой главной коронарной артерии из-за риска спазма левой коронарной артерии во время процедуры. [16] Кроме того, ЧТКА не рекомендуется при стенозе коронарных артерий менее 70%, поскольку стеноз ниже этого уровня не считается гемодинамически значимым. [16]



Доступ к сосудистой системе обычно осуществляется чрескожно (через кожу, без большого хирургического разреза). Интродьюсер вводится в кровеносный сосуд по методу Сельдингера . [17] Рентгеноскопический контроль использует магнитно-резонансную или рентгеновскую флюороскопию и рентгеноконтрастный краситель для направления изогнутых проводов и катетеров к области тела, подлежащей лечению, в режиме реального времени. [18] Конический проводник выбирается при небольшой окклюзии, за ним следуют проводники промежуточного типа при извилистых артериях и трудностях прохождения через чрезвычайно узкие каналы, а также жесткие проводники при жесткой, плотной и тупой окклюзии. [19]
Для лечения сужения кровеносного сосуда проволоку пропускают через стеноз сосуда, а баллон на катетере проводят по проволоке в желаемое положение. [20] Положение проверяется с помощью рентгеноскопии, и баллон надувается водой, смешанной с контрастным красителем, до давления, в 75–500 раз превышающего нормальное кровяное давление (от 6 до 20 атмосфер), при этом для большинства коронарных ангиопластик требуется менее 10 атмосфер. [21] Стент также может быть установлен или не установлен.
По завершении процедуры баллоны, провода и катетеры удаляются, а место прокола сосуда обрабатывается либо прямым давлением, либо устройством для закрытия сосудов . [22]
Трансрадиальный доступ к артерии (TRA) и доступ к трансбедренной артерии (TFA) представляют собой два метода чрескожного коронарного вмешательства. [23] TRA является методом выбора для лечения острого коронарного синдрома (ОКС), поскольку он имеет значительно меньшую частоту кровотечений и сосудистых осложнений по сравнению с подходом TFA. [23] TRA также имеет преимущество в смертности у пациентов с высоким риском ОКС и пациентов с высоким риском кровотечения. [23] Также было обнаружено, что TRA улучшает качество жизни, а также снижает затраты и ресурсы на здравоохранение. [23]
По сравнению с хирургическим вмешательством ангиопластика является вариантом лечения состояний с меньшим риском, но существуют уникальные и потенциально опасные риски и осложнения, связанные с ангиопластикой:
Ангиопластика также может обеспечить менее длительный метод лечения атеросклероза и быть более склонной к рестенозу по сравнению с сосудистым шунтированием или аортокоронарным шунтированием . [28] Баллонная ангиопластика с лекарственным покрытием имеет значительно меньший рестеноз, позднюю потерю просвета и реваскуляризацию целевого поражения как при краткосрочном, так и в среднесрочном периоде наблюдения по сравнению с баллонной ангиопластикой без покрытия при окклюзионном заболевании бедренно-подколенной артерии. [29] Хотя ангиопластика бедренно-подколенной артерии с помощью стентов и баллонов, покрытых паклитакселом, значительно снижает частоту рестеноза сосудов и реваскуляризации целевого поражения, было также обнаружено, что она увеличивает риск смерти. [30]
После ангиопластики большинство пациентов находятся под наблюдением в больнице в течение ночи, но при отсутствии осложнений на следующий день пациентов отправляют домой. [26]
Место катетера проверяют на предмет кровотечения и отека, а также контролируют частоту сердечных сокращений и артериальное давление для выявления позднего разрыва и кровотечения. [26] Протокол после процедуры также включает мониторинг диуреза, сердечных симптомов, боли и других признаков системных проблем. [26] Обычно пациенты получают лекарства, которые расслабляют их и защищают артерии от спазмов . Пациенты обычно могут ходить в течение двух-шести часов после процедуры и возвращаются к своему обычному образу жизни на следующей неделе. [31]
Восстановление после ангиопластики заключается в отказе от физической активности в течение нескольких дней после процедуры. Пациентам рекомендуется избегать поднятия тяжестей и напряженной деятельности в течение недели. [32] [33] Пациентам необходимо избегать физического стресса или длительных занятий спортом в течение максимум двух недель после деликатной баллонной ангиопластики. [34]
После начальной двухнедельной фазы восстановления большинство пациентов, перенесших ангиопластику, могут безопасно вернуться к упражнениям низкого уровня. Рекомендуется поэтапная программа упражнений, при которой пациенты сначала выполняют несколько коротких упражнений каждый день, постепенно увеличивая их до одного или двух более длительных подходов. [35] В качестве меры предосторожности все структурированные упражнения перед началом должны быть одобрены кардиологом. Реабилитация на основе физических упражнений после чрескожного коронарного вмешательства показала улучшение показателей рецидивирующей стенокардии, общего времени выполнения упражнений, снижения сегмента ST и максимальной толерантности к физической нагрузке. [36]
Пациенты, которые испытывают отек, кровотечение или боль в месте введения, повышают температуру , чувствуют слабость или слабость, замечают изменение температуры или цвета в использованной руке или ноге, одышку или боль в груди, должны немедленно обратиться за медицинской помощью.
Пациентам со стентами обычно назначают двойную антиагрегантную терапию (ДАТТ), состоящую из ингибитора P2Y12 , такого как клопидогрел , который принимают одновременно с ацетилсалициловой кислотой (аспирином). [37] Двойная антиагрегантная терапия (ДАТТ) рекомендуется в течение 1 месяца после установки голого металлического стента, в течение 3 месяцев после установки стента с лекарственным покрытием второго поколения и в течение 6–12 месяцев после установки стента с лекарственным покрытием первого поколения . [1] Антиагрегантные свойства ДАТТ направлены на предотвращение образования тромбов, однако они также увеличивают риск кровотечения, поэтому при определении продолжительности лечения ДАТТ важно учитывать предпочтения каждого пациента, состояние сердца и риск кровотечения. [37] Еще одним важным фактором является то, что одновременное применение клопидогрела и ингибиторов протонной помпы после коронарной ангиографии связано со значительно более частыми неблагоприятными сердечно-сосудистыми осложнениями, такими как серьезные неблагоприятные сердечно-сосудистые события (MACE), тромбоз стента и инфаркт миокарда. [38]
Ангиопластика была впервые описана американским интервенционным радиологом Чарльзом Доттером в 1964 году. [39] Доттер стал пионером современной медицины, изобретя ангиопластику и катетерный стент, которые впервые были использованы для лечения заболеваний периферических артерий. 16 января 1964 года Доттер чрескожно расширил плотный локализованный стеноз субсарториальной артерии у 82-летней женщины с болезненной ишемией ног и гангреной, которая отказалась от ампутации ноги. После успешного расширения стеноза с помощью проводника и коаксиальных тефлоновых катетеров кровообращение в ноге восстановилось. Расширенная артерия оставалась открытой до ее смерти от пневмонии два с половиной года спустя. [40] Чарльз Доттер широко известен как «отец интервенционной радиологии » и был номинирован на Нобелевскую премию по медицине в 1978 году.
Первая чрескожная коронарная ангиопластика бодрствующему пациенту была выполнена в Цюрихе немецким кардиологом Андреасом Грюнцигом 16 сентября 1977 года. [41]
Первые чрескожные коронарные ангиопластики в США были выполнены в один и тот же день (1 марта 1978 г.) Саймоном Х. Стертцером в больнице Ленокс Хилл в Нью-Йорке и Ричардом К. Майлером в больнице Святой Марии в Сан-Франциско. В течение предыдущего года, также в больнице Св. Марии в Сан-Франциско, Майлер и Грюнциг выполнили дилатацию в условиях шунтирующей операции, чтобы проверить концепцию катетера, прежде чем Грюнциг выполнил первую ЧТКА в своей лаборатории катетеризации в Цюрихе.
Первоначальной формой ангиопластики была «простая баллонная ангиопластика» (POBA) без стентирования, пока в середине 1980-х годов не были изобретены голые металлические стенты для предотвращения резкого закрытия, иногда наблюдаемого при POBA. [1]
Было обнаружено, что голые металлические стенты вызывают рестеноз внутри стента в результате гиперплазии неоинтимы и тромбоза стента, что привело к изобретению стентов с лекарственным покрытием и антипролиферативными препаратами для борьбы с рестенозом внутри стента. [1]
Первая коронарная ангиопластика с использованием стент-системы для доставки лекарств была выполнена Штертцером и Луисом де ла Фуэнте в Аргентинском институте диагностики и лечения (англ. Аргентинский институт диагностики и лечения [42] ) в Буэнос-Айресе в 1999 году.
Ингемар Генри Лундквист изобрел баллонный катетер, который сейчас используется в большинстве процедур ангиопластики в мире. [43]
Подвид ангиопластики, известный как эксимерлазерная коронарная ангиопластика (ELCA), использует эксимерные лазеры для удаления небольших количеств ткани, в том числе нерасширяющихся и непроходимых поражений, в артерии, чтобы позволить баллону более эффективно сжимать бляшки в стенках артерии. [44] Такая работа была впервые разработана в 1984 году после более ранней работы в 1980–1983 годах, когда Рангасвами Шринивасан , Сэмюэл Блюм и Джеймс Дж. Винн из Исследовательского центра Ти Дж. Уотсона IBM наблюдали влияние ультрафиолетового эксимерного лазера на биологические материалы. Заинтригованные, они продолжили исследование и обнаружили, что лазер делает чистые и точные разрезы, которые идеально подходят для деликатных операций. В результате был получен фундаментальный патент [45] , и Шринивасан, Блюм и Винн были избраны в Национальный зал славы изобретателей в 2002 году. В 2012 году члены команды были награждены Национальной медалью технологий и инноваций президентом Бараком Обамой за свою работу . Относящийся к эксимерному лазеру. [46] Роберт Гинзбург впервые применил ELCA в 1984 году у пациента с тяжелым стенозом глубокой бедренной артерии и угрозой конечности. [47]