β-лактамные антибиотики ( бета-лактамные антибиотики ) — антибиотики , содержащие в своей химической структуре бета-лактамное кольцо. Сюда входят производные пенициллина ( пенамы ), цефалоспорины и цефамицины ( цефемы ), монобактамы , карбапенемы [1] и карбацефемы . [2] Большинство β-лактамных антибиотиков действуют путем ингибирования биосинтеза клеточной стенки бактериального организма и являются наиболее широко используемой группой антибиотиков. До 2003 года, если судить по объёму продаж, более половины всех коммерчески доступных антибиотиков представляли собой соединения β-лактамов. [3] Первый обнаруженный β-лактамный антибиотик, пенициллин , был выделен из штамма Penicillium Rubens ( в то время называвшегося Penicillium notatum ). [4] [5]
Бактерии часто развивают устойчивость к β-лактамным антибиотикам путем синтеза β-лактамазы — фермента, атакующего β-лактамное кольцо. Чтобы преодолеть эту резистентность, можно назначать β-лактамные антибиотики вместе с ингибиторами β-лактамаз, такими как клавулановая кислота . [6]
β-лактамные антибиотики показаны для профилактики и лечения бактериальных инфекций, вызванных чувствительными микроорганизмами. Первоначально β-лактамные антибиотики были активны в основном только против грамположительных бактерий, однако недавняя разработка β-лактамных антибиотиков широкого спектра действия, активных против различных грамотрицательных микроорганизмов, увеличила их полезность. [ нужна цитата ]
В невоспаленных (нормальных) мозговых оболочках проникновение бета-лактамных антибиотиков низкое и составляет 0,15 от соотношения AUC CSF /AUC S (отношение площади под кривой цереброспинальной жидкости к площади под кривой сыворотки). [7]
Общие побочные реакции на β-лактамные антибиотики включают диарею, тошноту, сыпь, крапивницу , суперинфекцию (включая кандидоз ). [8]
Нечастые побочные эффекты включают лихорадку, рвоту, эритему , дерматит, ангионевротический отек , псевдомембранозный колит . [8]
Боль и воспаление в месте инъекции также характерны для парентерально вводимых β-лактамных антибиотиков. [ нужна цитата ]
Иммунологически опосредованные побочные реакции на любой β-лактамный антибиотик могут возникнуть у 10% пациентов, получающих этот препарат (небольшая часть из них представляет собой действительно IgE -опосредованные аллергические реакции, см. сыпь от амоксициллина ). Анафилаксия возникает примерно у 0,01% пациентов. [8] [9] Перекрестная чувствительность между производными пенициллина, цефалоспоринами и карбапенемами составляет 5–10%; [ нужна ссылка ] , но эта цифра оспаривается различными исследователями. [ ВОЗ? ] [ нужна цитата ]
Тем не менее, риск перекрестной реактивности достаточен, чтобы оправдать противопоказание всех β-лактамных антибиотиков пациентам с тяжелыми аллергическими реакциями в анамнезе ( крапивница , анафилаксия, интерстициальный нефрит ) на любой β-лактамный антибиотик. В редких случаях аллергические реакции были вызваны поцелуями и сексуальным контактом с партнером, принимающим эти антибиотики. [10]
Реакция Яриша -Герксгеймера может возникнуть после первоначального лечения спирохетальной инфекции , такой как сифилис , β-лактамным антибиотиком.

β-лактамные антибиотики обладают бактерицидным действием и действуют путем ингибирования синтеза пептидогликанового слоя клеточных стенок бактерий . Слой пептидогликана важен для структурной целостности клеточной стенки [6] , особенно у грамположительных организмов, поскольку он является самым внешним и основным компонентом стенки. Заключительный этап транспептидации в синтезе пептидогликана осуществляется DD-транспептидазами , также известными как пенициллин-связывающие белки (PBP). PBP различаются по сродству к пенициллину и другим β-лактамным антибиотикам. Количество PBP варьируется в зависимости от вида бактерий. [11]
β-лактамные антибиотики являются аналогами d -аланил- d -аланина – концевых аминокислотных остатков субъединиц предшественника NAM/NAG-пептида образующегося слоя пептидогликана. Структурное сходство β-лактамных антибиотиков и d -аланил- d -аланина облегчает их связывание с активным центром PBP. β-лактамное ядро молекулы необратимо связывается ( ацилирует ) с остатком Ser 403 активного центра PBP. Это необратимое ингибирование PBP предотвращает окончательное сшивание (транспептидацию) формирующегося слоя пептидогликана, нарушая синтез клеточной стенки. [ 13] β -лактамные антибиотики блокируют не только деление бактерий, в том числе цианобактерий , но и деление цианелл, фотосинтетических органелл глаукофитов и деление хлоропластов мохообразных . Напротив, они не оказывают влияния на пластиды высокоразвитых сосудистых растений . Это подтверждает эндосимбиотическую теорию и указывает на эволюцию деления пластид у наземных растений . [14]
В нормальных условиях предшественники пептидогликана сигнализируют о реорганизации бактериальной клеточной стенки и, как следствие, запускают активацию аутолитических гидролаз клеточной стенки . Ингибирование поперечной сшивки β-лактамами вызывает накопление предшественников пептидогликана, что запускает расщепление существующего пептидогликана аутолитическими гидролазами без образования нового пептидогликана. В результате бактерицидное действие β-лактамных антибиотиков еще больше усиливается. [ нужна цитата ]
Другая возможность, которая, как было предложено, объясняет большую часть цитотоксичности бета-лактамов, связана с окислением гуанинового нуклеотида в пуле бактериальных нуклеотидов. [15] Включение окисленного гуанинового нуклеотида в ДНК может вызвать цитотоксичность. Бактериальная цитотоксичность может возникнуть в результате неполного восстановления близко расположенных 8-оксо-2'-дезоксигуанозиновых повреждений ДНК, что приводит к двухцепочечным разрывам. [15]
Две структурные особенности β-лактамных антибиотиков коррелируют с их антибиотической активностью. [16] Первый известен как «параметр Вудворда», h , и представляет собой высоту (в ангстремах ) пирамиды, образованной атомом азота β-лактама в качестве вершины и тремя соседними атомами углерода в качестве основания. [17] Второй называется «параметром Коэна», c , и представляет собой расстояние между атомом углерода карбоксилата и атомом кислорода карбонила β- лактама . [18] Считается, что это расстояние соответствует расстоянию между сайтом связывания карбоксилата и оксианионной дыркой фермента PBP. Лучшими антибиотиками являются те, у которых более высокие значения h (более активны к гидролизу) и более низкие значения c (лучшее связывание с PBP). [16]
По определению, все β-лактамные антибиотики имеют в своей структуре β-лактамное кольцо. Эффективность этих антибиотиков зависит от их способности достигать PBP в неизмененном виде и их способности связываться с PBP. Следовательно, существует два основных способа устойчивости бактерий к β-лактамам:
Если бактерия продуцирует фермент β-лактамазу или фермент пенициллиназу , фермент гидролизует β-лактамное кольцо антибиотика, делая антибиотик неэффективным. [19] (Примером такого фермента является металло-бета-лактамаза 1 из Нью-Дели , открытая в 2009 году.) Гены, кодирующие эти ферменты, могут изначально присутствовать на бактериальной хромосоме или могут быть приобретены посредством плазмидного переноса ( плазмидно-опосредованная устойчивость). ), а экспрессия гена β-лактамазы может быть индуцирована воздействием β-лактамов. [ нужна цитата ]


Производство β-лактамазы бактерией не обязательно исключает все варианты лечения β-лактамными антибиотиками. В некоторых случаях β-лактамные антибиотики можно назначать одновременно с ингибитором β-лактамаз . Например, Аугментин (ФГП) состоит из амоксициллина (β-лактамного антибиотика) и клавулановой кислоты (ингибитора β-лактамаз). Клавулановая кислота предназначена для подавления всех ферментов β-лактамаз и эффективно служит антагонистом, так что амоксициллин не подвергается воздействию ферментов β-лактамаз. Другой комбинацией ингибиторов β-лактамов и β-лактамаз является пиперациллин/тазобактам с широким спектром антибактериальной активности, включающим грамположительные и -отрицательные аэробные и анаэробные бактерии. Добавление тазобактама к пиперациллину повысило его стабильность против широкого спектра ферментов β-лактамаз, включая некоторые β-лактамазы расширенного спектра. [20]
Изучаются другие ингибиторы β-лактамаз , такие как бороновые кислоты, которые необратимо связываются с активным центром β-лактамаз. Это преимущество перед клавулановой кислотой и аналогичными бета-лактамными конкурентами, поскольку они не поддаются гидролизу и, следовательно, становятся бесполезными. В настоящее время проводятся обширные исследования по разработке адаптированных бороновых кислот для воздействия на различные изоферменты бета-лактамаз. [21]
Однако во всех случаях, когда есть подозрение на заражение бактериями, продуцирующими β-лактамазы, перед началом лечения следует тщательно обдумать выбор подходящего β-лактамного антибиотика. В частности, выбор подходящей терапии β-лактамными антибиотиками имеет первостепенное значение против организмов, которые обладают некоторым уровнем экспрессии β-лактамаз. В этом случае отказ от использования наиболее подходящей терапии β-лактамными антибиотиками в начале лечения может привести к отбору бактерий с более высоким уровнем экспрессии β-лактамаз, что затрудняет дальнейшие усилия по использованию других β-лактамных антибиотиков. [22]
В ответ на использование β-лактамов для борьбы с бактериальными инфекциями у некоторых бактерий появились пенициллинсвязывающие белки с новой структурой. β-лактамные антибиотики не могут так эффективно связываться с этими измененными PBP, и в результате β-лактамы менее эффективны в нарушении синтеза клеточной стенки. Яркими примерами этого типа устойчивости являются метициллин -резистентный Staphylococcus aureus ( MRSA ) [23] и пенициллин-резистентный Streptococcus pneumoniae . Изменение PBP не обязательно исключает все варианты лечения β-лактамными антибиотиками.

β-лактамы классифицируются в соответствии с их кольцевой структурой. [24]
Условно нумерацию бициклических β-лактамов начинают с позиции, занимаемой серой в пенамах и цефемах, независимо от того, к какому атому она относится в данном классе. То есть позиция 1 всегда соседствует с β-углеродом β-лактамного кольца. Нумерация продолжается по часовой стрелке от первой позиции до тех пор, пока не будет достигнут β-углерод β-лактама, после чего нумерация продолжается против часовой стрелки вокруг лактамного кольца, чтобы пронумеровать оставшиеся атомы углерода. Например, атом азота всех бициклических β-лактамов, слитых с пятичленными кольцами, обозначен в положении 4, как и в пенамах, а в цефемах азот находится в положении 5.
Нумерация монобактамов соответствует нумерации ИЮПАК ; атом азота находится в положении 1, карбонильный углерод — 2, α-углерод — 3 и β-углерод — 4.
На сегодняшний день открыты два различных метода биосинтеза β-лактамного ядра этого семейства антибиотиков. Первым обнаруженным путем были пенамы и цефемы. Этот путь начинается с нерибосомальной пептидсинтазы (NRPS), ACV-синтетазы (ACVS), которая генерирует линейный трипептид δ-( L -α-аминоадипил)-L - цистеин- D -валин (ACV). ACV подвергается окислительной циклизации (две циклизации одним ферментом) до бициклического промежуточного изопенициллина N синтетазой изопенициллина N (IPNS) с образованием основной структуры пенама. [25] Различные трансамиды приводят к образованию различных природных пенициллинов.
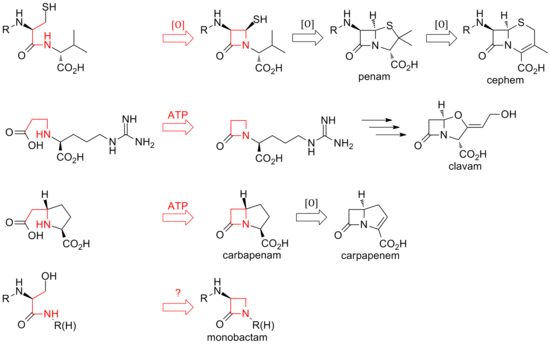
Биосинтез цефем ответвляется от изопенициллина N путем расширения окислительного кольца до ядра цефемы. Как и в случае с пенамами, разнообразие цефалоспоринов и цефамицинов происходит от различных трансамидирований, как и в случае с пенициллинами.
В то время как у пенамов и цефемов замыкание кольца происходит между положениями 1 и 4 β-лактама и является окислительным, у клавамов и карбапенемов кольца замыкаются посредством двухэлектронных процессов между положениями 1 и 2 кольца. За эти циклизации ответственны β-лактамсинтетазы, а карбоксилат субстратов с открытым кольцом активируется АТФ . [26] В клавамах β-лактам образуется до второго кольца; у карбапенемов β-лактамное кольцо замыкается вторым по порядку. [ нужна цитата ]
Биосинтез β-лактамного кольца табтоксина повторяет биосинтез клавамов и карбапенемов. Замыкание лактамного кольца у других монобактамов, таких как сульфазецин и нокардицины, может включать третий механизм, включающий инверсию конфигурации β-углерода. [27]