Гемицеллюлоза (также известная как полиоза ) — один из ряда гетерополимеров (матриксных полисахаридов), таких как арабиноксиланы , присутствующих наряду с целлюлозой почти во всех клеточных стенках наземных растений . [1] Целлюлоза кристаллическая, прочная и устойчивая к гидролизу . Гемицеллюлозы разветвлены, короче целлюлозы по длине, а также склонны к кристаллизации. [2] Они могут быть гидролизованы разбавленной кислотой или основанием , а также множеством ферментов гемицеллюлазы .
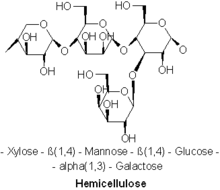
Известны различные виды гемицеллюлоз. Важные примеры включают ксилан , глюкуроноксилан , арабиноксилан , глюкоманнан и ксилоглюкан .
Гемицеллюлозы — это полисахариды, часто связанные с целлюлозой , но имеющие особый состав и структуру. В то время как целлюлоза получается исключительно из глюкозы , гемицеллюлозы состоят из различных сахаров и могут включать пятиуглеродные сахара ксилозу и арабинозу , шестиуглеродные сахара глюкозу, маннозу и галактозу , а также шестиуглеродный дезоксисахар рамнозу . Гемицеллюлозы содержат большую часть сахаров D- пентозы , а также иногда небольшое количество L-сахаров. Ксилоза в большинстве случаев представляет собой сахарный мономер, присутствующий в наибольшем количестве, хотя в хвойных породах наиболее распространенным сахаром может быть манноза. В гемицеллюлозе могут находиться не только обычные сахара, но и их подкисленные формы, например глюкуроновая кислота и галактуроновая кислота . [3] [4]
В отличие от целлюлозы гемицеллюлозы состоят из более коротких цепей – 500–3000 сахарных единиц. Напротив, каждый полимер целлюлозы содержит 7 000–15 000 молекул глюкозы. [5] Кроме того, гемицеллюлозы могут быть разветвленными полимерами , тогда как целлюлоза неразветвлена. Гемицеллюлозы встроены в клеточные стенки растений, иногда в виде цепочек, образующих « землю » — они связываются с пектином целлюлозы, образуя сеть поперечно-сшитых волокон. [ нужна цитата ]

На основании структурных различий, таких как связи основной цепи и боковые группы, а также других факторов, таких как распространенность и распределение в растениях, гемицеллюлозы можно разделить на следующие четыре группы: [4] 1) ксиланы, 2) маннаны ; 3) β-глюканы со смешанной связью ; 4) ксилоглюканы.
Ксиланы обычно состоят из основной цепи из β-(1→4)-связанных остатков ксилозы и могут быть далее разделены на гомоксиланы и гетероксиланы. Гомоксиланы имеют основу из остатков D-ксилопиранозы, связанных β(1→4) гликозидными связями. Гомоксиланы выполняют в основном структурные функции. Гетероксиланы, такие как глюкуроноксиланы, глюкуроноксиланы и сложные гетероксиланы, имеют основу из D-ксилопиранозы и короткие углеводные разветвления. Например, глюкуроноксилан имеет замену на α-(1→2)-связанные глюкуронозильные и 4-О-метилглюкуронозильные остатки. Арабиноксиланы и глюкуроноарабиноксиланы содержат остатки арабинозы, прикрепленные к основной цепи [6]
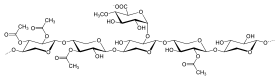
Гемицеллюлозу маннанового типа можно разделить на два типа в зависимости от различия их основных цепей: галактоманнаны и глюкоманнаны. Галактоманнаны содержат только β-(1→4) связанные остатки D-маннопиранозы в линейных цепях. Глюкоманнаны состоят как из β-(1→4)-связанных остатков D-маннопиранозы, так и из β-(1→4)-связанных остатков D-глюкопиранозы в основных цепях. Что касается боковых цепей, остатки D-галактопиранозы имеют тенденцию быть 6-связанными с обоими типами в виде одиночных боковых цепей с различным количеством. [1]
Конформация глюкановых цепей со смешанными связями обычно содержит блоки β-(1→4) D-глюкопиранозы, разделенные одиночной β-(1→3) D-глюкопиранозой. Население β-(1→4) и β-(1→3) составляет около 70% и 30%. Эти глюканы в основном состоят из целлотриозильных (C 18 H 32 O 16 ) и целлотраозильных (C 24 H 42 O 21 ) сегментов в случайном порядке. Некоторые исследования показывают молярное соотношение целлотриозил/целлотраозил для овса (2,1–2,4), ячменя (2,8–3,3) и пшеницы (4,2–4,5). [1] [5]

Ксилоглюканы имеют основную цепь, аналогичную целлюлозе, с остатками α-D-ксилопиранозы в положении 6. Чтобы лучше описать различные боковые цепи, для каждого типа боковой цепи используется однобуквенное обозначение. G -- неразветвленный остаток Glc; X -- α-d-Ксил-(1→6)-Glc. L -- β-Гал, S -- α-1-Араф, F-- α-1-Фук. Это наиболее распространенные боковые цепи. [5]
Два наиболее распространенных типа ксилоглюканов в клеточных стенках растений обозначаются как XXXG и XXGG. [1]
Гемицеллюлозы синтезируются из сахарных нуклеотидов в аппарате Гольджи клетки . [8] Их синтез объясняют две модели: 1) «2-компонентная модель», где модификация происходит в двух трансмембранных белках, и 2) «1-компонентная модель», где модификация происходит только в одном трансмембранном белке. После синтеза гемицеллюлозы транспортируются к плазматической мембране через пузырьки Гольджи.
Каждый вид гемицеллюлозы биосинтезируется специализированными ферментами. [8] [9]
Основы цепи маннана синтезируются с помощью семейства белков A, подобных целлюлозо-синтазе (CSLA), и, возможно, ферментов семейства D, подобных синтазы целлюлозы (CSLD). [8] [9] Маннансинтаза, особый фермент CSLA, отвечает за добавление маннозных единиц к основной цепи. [8] [9] Боковые цепи галактозы некоторых маннанов добавляются галактоманнангалактозилтрансферазой. [8] [9] Ацетилирование маннанов опосредуется маннан-О-ацетилтрансферазой, однако этот фермент окончательно не идентифицирован. [9]
Синтез основной цепи ксилоглюкана опосредован целлюлозо-синтазоподобными белками семейства C (CSLC), особенно глюкансинтазой , которая добавляет звенья глюкозы к цепи. [8] [9] Синтез остова ксилоглюкана также каким-то образом опосредован ксилозилтрансферазой , но этот механизм отделен от его трансферазной функции и остается неясным. [9] Ксилозилтрансфераза в своей трансферазной функции, однако, используется для добавления ксилозы к боковой цепи. [8] [9] Другие ферменты, используемые для синтеза боковой цепи ксилоглюкана, включают галактозилтрансферазу (которая отвечает за добавление [галактозы и используются две разные формы), фукозилтрансферазу (которая отвечает за добавление фукозы), и ацетилтрансфераза (отвечающая за ацетилирование). [8] [9]
Синтез основной цепи ксилана, в отличие от синтеза других гемицеллюлоз, не опосредован какими-либо белками, подобными целлюлозо-синтазе. [9] Вместо этого за синтез основной цепи отвечает ксилансинтаза, способствуя добавлению ксилозы. [9] Идентифицировано несколько генов ксилансинтаз. [9] Для добавления и модификации звеньев боковой цепи ксилана используются несколько других ферментов, в том числе глюкуронозилтрансфераза (которая добавляет звенья глюкуроновой кислоты), ксилозилтрансфераза (которая добавляет дополнительные звенья ксилозы), арабинозилтрансфераза (которая добавляет арабинозу), метилтрансфераза. (отвечает за метилирование ) и ацетилтрансфераза] (отвечает за ацетилирование). [9] Учитывая, что глюкан со смешанными связями представляет собой неразветвленный гомополимер глюкозы, синтез боковой цепи отсутствует, а только добавление глюкозы к основной цепи по двум связям: β1-3 и β1-4. [9] Синтез основной цепи опосредован ферментами семейств целлюлозо-синтазоподобных белков F и H (CSLF и CSLH), в частности глюкансинтазой. [8] [9] Было идентифицировано несколько форм глюкансинтазы из CSLF и CSLH. [8] [9] Все они ответственны за добавление глюкозы к основной цепи и все способны производить связи как β1-3, так и β1-4, однако неизвестно, насколько каждый конкретный фермент способствует распределению β1. -3 и β1-4 связи. [8] [9]
В процессе сульфитной целлюлозы гемицеллюлоза в значительной степени гидролизуется кислым раствором варки целлюлозы и попадает в коричневый щелок, где сбраживаемые гексозные сахара (около 2%) могут быть использованы для производства этанола . Этот процесс в первую очередь применялся к коричневым щелокам сульфита кальция. [10]
Арабиногалактаны могут использоваться в качестве эмульгаторов , стабилизаторов и связующих в соответствии с Федеральным законом о пищевых продуктах, лекарствах и косметике. Арабиногалактаны также можно использовать в качестве связующего вещества в подсластителях . [11]
Пленки на основе ксилана обладают низкой кислородопроницаемостью и поэтому представляют потенциальный интерес в качестве упаковки для чувствительных к кислороду продуктов. [12]
Агар используется при приготовлении желе и пудингов. Это также питательная среда с другими питательными веществами для микроорганизмов . [13]
Курдлан можно использовать в качестве заменителя жира для производства диетических продуктов, сохраняя при этом вкус и ощущение во рту настоящих жиросодержащих продуктов. [13]
b-глюканы играют важную роль в пищевых добавках, в то время как b-глюканы также перспективны в вопросах, связанных со здоровьем, особенно в иммунных реакциях и лечении рака. [14]
Ксантан вместе с другими полисахаридами может образовывать гели, обладающие высокой вязкостью раствора , которые можно использовать в нефтяной промышленности для загущения бурового раствора. В пищевой промышленности ксантан используется в таких продуктах, как заправки и соусы. [15]
Альгинат играет важную роль в разработке антимикробного текстиля благодаря своим характеристикам экологичности и высокому уровню индустриализации в качестве устойчивого биополимера . [16]

Будучи полисахаридным соединением в стенках растительных клеток, подобным целлюлозе, гемицеллюлоза помогает целлюлозе укреплять стенки растительных клеток. [6] Гемицеллюлоза взаимодействует с целлюлозой , обеспечивая сшивку микрофибрилл целлюлозы : гемицеллюлоза будет искать пустоты в клеточной стенке во время ее формирования и обеспечивать поддержку вокруг фибрилл целлюлозы , чтобы придать клеточной стенке максимально возможную прочность, которую она может обеспечить. . [6] Гемицеллюлоза доминирует в средней пластинке растительной клетки, в отличие от целлюлозы , которая в основном находится во вторичных слоях. Это позволяет гемицеллюлозе обеспечивать промежуточную поддержку целлюлозы на внешних слоях растительной клетки. В некоторых клеточных стенках гемицеллюлоза также взаимодействует с лигнином , обеспечивая структурную поддержку тканей большего количества сосудистых растений. [3] [17]
Существует много способов получения гемицеллюлозы; все они основаны на методах экстракции из деревьев лиственных или хвойных пород, измельченных на более мелкие образцы. В лиственных породах основным экстрактом гемицеллюлозы является глюкуронокслян (ацетилированные ксиланы), а в хвойных породах содержится галактоглюкоманнан. [18] [19] Перед экстракцией древесину обычно необходимо измельчить в щепу различного размера в зависимости от используемого реактора. После этого используется процесс экстракции горячей водой, также известный как автогидролиз или гидротермальная обработка, с добавлением кислот и оснований для изменения размера выхода и свойств. [18] [19] Основным преимуществом экстракции горячей водой является то, что она предлагает метод, при котором единственным необходимым химическим веществом является вода, что делает его экологически чистым и дешевым. [20]
Целью обработки горячей водой является удаление как можно большего количества гемицеллюлозы из древесины. Это делается посредством гидролиза гемицеллюлозы для получения более мелких олигомеров и ксилозы. Ксилоза при обезвоживании превращается в фурфурол. [21] Когда целью являются ксилоза и фурфурол [ проверьте правописание ] , добавляются кислотные катализаторы, такие как муравьиная кислота, для увеличения перехода полисахаридов в моносахариды. Также было показано, что этот катализатор также использует эффект растворителя для облегчения реакции. [21]
Один из методов предварительной обработки — пропитка древесины разбавленными кислотами (концентрацией около 4%). Это превращает гемицеллюлозу в моносахариды. Предварительная обработка основаниями (например, гидроксидом натрия или калия) разрушает структуру лигнина. [19] Это меняет структуру с кристаллической на аморфную. Еще одним методом является гидротермальная предварительная обработка. [ необходимо дальнейшее объяснение ] Это дает такие преимущества, как отсутствие необходимости в токсичных или коррозийных растворителях, специальных реакторах и дополнительных затратах на утилизацию опасных химикатов. [18]
Процесс экстракции горячей водой осуществляется в реакторах периодического действия, полунепрерывных реакторах или суспензионных реакторах непрерывного действия. Для реакторов периодического и полунепрерывного действия образцы древесины могут использоваться в таких условиях, как щепа или гранулы, тогда как шламовый реактор должен содержать частицы размером от 200 до 300 микрометров. [19] Хотя размер частиц уменьшается, производительность также снижается. [22] Это связано с увеличением содержания целлюлозы. [ нужна цитата ]
Процесс с использованием горячей воды осуществляется при температуре от 160 до 240 градусов Цельсия, чтобы поддерживать жидкую фазу. Это делается при температуре выше нормальной температуры кипения воды, чтобы увеличить солюбилизацию гемицеллюлозы и деполимеризацию полисахаридов. [21] Этот процесс может занять от нескольких минут до нескольких часов в зависимости от температуры и pH системы. [19] Более высокие температуры в сочетании с более длительным временем экстракции приводят к более высоким выходам. Максимальный выход достигается при pH 3,5. [18] Если ниже, выход экстракции экспоненциально снижается. Для контроля pH обычно добавляют бикарбонат натрия. [18] Бикарбонат натрия ингибирует автолиз ацетильных групп, а также ингибирует гликозильные связи. В зависимости от температуры и времени гемицеллюлоза может далее превращаться в олигомеры, мономеры и лигнин. [18]
{{cite web}}: CS1 maint: несколько имен: список авторов ( ссылка ){{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка )