Глюконеогенез ( ГНГ ) – это метаболический путь , который приводит к биосинтезу глюкозы из определенных неуглеводных углеродных субстратов. Это повсеместный процесс, присутствующий у растений, животных, грибов, бактерий и других микроорганизмов. [1] У позвоночных глюконеогенез происходит главным образом в печени и, в меньшей степени, в коре почек . Это один из двух основных механизмов (второй — деградация гликогена ( гликогенолиз ) ), используемый людьми и многими другими животными для поддержания уровня сахара в крови , избегая его низкого уровня ( гипогликемии ). [2] У жвачных животных , поскольку пищевые углеводы, как правило, метаболизируются организмами рубца , глюконеогенез происходит независимо от голодания, низкоуглеводной диеты, физических упражнений и т. д . [3] У многих других животных этот процесс происходит в периоды голодания , голодания , низкоуглеводные диеты или интенсивные физические упражнения .
У человека субстраты глюконеогенеза могут поступать из любых неуглеводных источников, которые могут превращаться в пируват или промежуточные продукты гликолиза (см. рисунок). Эти субстраты для расщепления белков включают глюкогенные аминокислоты (но не кетогенные аминокислоты ); от распада липидов (таких как триглицериды ) к ним относятся глицерин , жирные кислоты с нечетной цепью (хотя и не жирные кислоты с четной цепью, см. ниже); и из других частей метаболизма , включая лактат из цикла Кори . В условиях длительного голодания ацетон, полученный из кетоновых тел , также может служить субстратом, обеспечивающим путь от жирных кислот к глюкозе. [4] Хотя большая часть глюконеогенеза происходит в печени, относительный вклад глюконеогенеза в почках увеличивается при диабете и длительном голодании. [5]
Путь глюконеогенеза является высоко эндергоническим до тех пор, пока он не соединяется с гидролизом АТФ или ГТФ , что фактически делает процесс экзергоническим . Например, путь, ведущий от пирувата к глюкозо-6-фосфату, требует, чтобы 4 молекулы АТФ и 2 молекулы ГТФ протекали спонтанно. Эти АТФ поступают в результате катаболизма жирных кислот посредством бета-окисления . [6]

У человека основными глюконеогенными предшественниками являются лактат , глицерин (входит в состав молекулы триглицеридов ), аланин и глютамин . В общей сложности на их долю приходится более 90% общего глюконеогенеза. [8] Другие глюкогенные аминокислоты и все промежуточные продукты цикла лимонной кислоты (путем превращения в оксалоацетат ) также могут выступать в качестве субстратов для глюконеогенеза. [9] Как правило, потребление человеком глюконеогенных субстратов с пищей не приводит к усилению глюконеогенеза. [10]
У жвачных животных пропионат является основным глюконеогенным субстратом. [3] [11] У нежвачных животных, включая человека, пропионат возникает в результате β-окисления жирных кислот с нечетной и разветвленной цепью и является (относительно второстепенным) субстратом глюконеогенеза. [12] [13]
Лактат транспортируется обратно в печень, где он превращается в пируват в цикле Кори с помощью фермента лактатдегидрогеназы . Пируват, первый назначенный субстрат глюконеогенного пути, затем можно использовать для выработки глюкозы. [9] Трансаминирование или дезаминирование аминокислот облегчает включение их углеродного скелета в цикл непосредственно (в виде пирувата или оксалоацетата) или опосредованно через цикл лимонной кислоты. Вклад лактата цикла Кори в общее производство глюкозы увеличивается с увеличением продолжительности голодания . [14] В частности, после 12, 20 и 40 часов голодания у людей-добровольцев вклад лактата цикла Кори в глюконеогенез составил 41%, 71% и 92% соответственно. [14]
Вопрос о том, могут ли жирные кислоты с четной цепью превращаться в глюкозу у животных, является давним вопросом в биохимии. [15] Жирные кислоты с нечетной цепью могут окисляться с образованием ацетил-КоА и пропионил-КоА , последний служит предшественником сукцинил-КоА , который может превращаться в оксалоацетат и вступать в глюконеогенез. Напротив, жирные кислоты с четной цепью окисляются с образованием только ацетил-КоА, вступление которого в глюконеогенез требует наличия глиоксилатного цикла (также известного как глиоксилатный шунт) для производства предшественников четырехуглеродных дикарбоновых кислот. [9] Глиоксилатный шунт состоит из двух ферментов: малатсинтазы и изоцитратлиазы и присутствует в грибах, растениях и бактериях. Несмотря на некоторые сообщения о шунтирующей ферментативной активности глиоксилата, обнаруженной в тканях животных, гены, кодирующие обе ферментативные функции, были обнаружены только у нематод , у которых они существуют как один бифункциональный фермент. [16] [17] Гены, кодирующие только малатсинтазу (но не изоцитратлиазу), были идентифицированы у других животных , включая членистоногих , иглокожих и даже некоторых позвоночных . Млекопитающие, у которых обнаружен ген малатсинтазы, включают однопроходных ( утконос ) и сумчатых ( опоссум ), но не плацентарных млекопитающих . [17]
Существование глиоксилатного цикла у человека не установлено, и широко распространено мнение, что жирные кислоты не могут быть напрямую преобразованы в глюкозу у человека. Было показано, что углерод-14 попадает в глюкозу, когда он поступает в жирные кислоты, [18] , но этого можно ожидать из-за включения меченых атомов, полученных из ацетил-КоА, в промежуточные соединения цикла лимонной кислоты , которые взаимозаменяемы с атомами, полученными из другие физиологические источники, такие как глюкогенные аминокислоты. [15] В отсутствие других источников глюкогена 2-углеродный ацетил-КоА , полученный в результате окисления жирных кислот, не может производить чистый выход глюкозы в цикле лимонной кислоты , поскольку эквивалентные два атома углерода высвобождаются в виде диоксида углерода во время цикл. Однако во время кетоза ацетил-КоА из жирных кислот образует кетоновые тела , включая ацетон , и до ~60% ацетона может окисляться в печени до предшественников пирувата - ацетола и метилглиоксаля . [19] [4] Таким образом, кетоновые тела, полученные из жирных кислот, могут составлять до 11% глюконеогенеза во время голодания. Катаболизм жирных кислот также производит энергию в форме АТФ, необходимую для пути глюконеогенеза.
Считалось, что у млекопитающих глюконеогенез ограничен печенью, [20] почками, [20] кишечником [21] и мышцами [22] , но недавние данные указывают на то, что глюконеогенез происходит в астроцитах головного мозга. [23] Эти органы используют несколько разные глюконеогенные предшественники. Печень преимущественно использует лактат, глицерин и глюкогенные аминокислоты (особенно аланин ), тогда как почки преимущественно используют лактат, глютамин и глицерин. [24] [8] Лактат цикла Кори количественно является крупнейшим источником субстрата для глюконеогенеза, особенно для почек. [8] Печень использует как гликогенолиз , так и глюконеогенез для производства глюкозы, тогда как почки используют только глюконеогенез. [8] После еды печень переключается на синтез гликогена , тогда как почки усиливают глюконеогенез. [10] Кишечник использует в основном глютамин и глицерин. [21]
Пропионат является основным субстратом глюконеогенеза в печени жвачных животных, и печень жвачных животных может усиленно использовать глюконеогенные аминокислоты (например, аланин), когда потребность в глюкозе увеличивается. [25] Способность клеток печени использовать лактат для глюконеогенеза снижается от дожвачной стадии к жвачной стадии у телят и ягнят. [26] В тканях почек овец наблюдались очень высокие темпы глюконеогенеза из пропионата. [26]
У всех видов образование оксалоацетата из пирувата и промежуточных продуктов цикла ТСА ограничено митохондриями, а ферменты, превращающие фосфоенолпировиноградную кислоту (ФЭП) в глюкозо-6-фосфат, обнаруживаются в цитозоле. [27] Расположение фермента, который связывает эти две части глюконеогенеза путем преобразования оксалоацетата в PEP – PEP карбоксикиназа (PEPCK) – варьируется в зависимости от вида: он может быть полностью обнаружен в митохондриях , полностью в цитозоле или равномерно распределен между два, как и у людей. [27] Транспорт PEP через митохондриальную мембрану осуществляется специальными транспортными белками; однако для оксалоацетата таких белков не существует . [27] Следовательно, у видов, у которых отсутствует внутримитохондриальный PEPCK, оксалоацетат должен превращаться в малат или аспартат , экспортироваться из митохондрий и превращаться обратно в оксалоацетат , чтобы глюконеогенез мог продолжаться. [27]
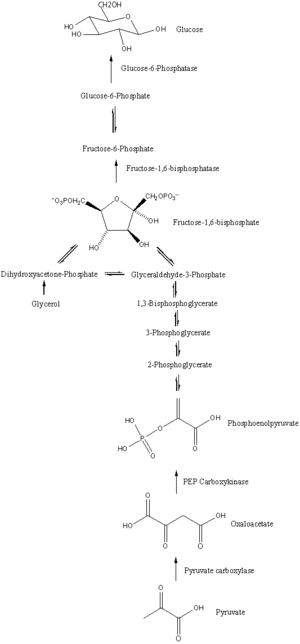
Глюконеогенез — это путь, состоящий из серии из одиннадцати реакций, катализируемых ферментами. Путь начнется либо в печени, либо в почках, в митохондриях или цитоплазме этих клеток, в зависимости от используемого субстрата. Многие реакции обратны стадиям гликолиза . [ нужна цитата ]
Хотя большинство стадий глюконеогенеза обратны тем, которые наблюдаются при гликолизе , три регулируемые и сильно эндергонические реакции заменяются более кинетически выгодными реакциями. Гексокиназа / глюкокиназа , фосфофруктокиназа и пируваткиназы - ферменты гликолиза заменяются глюкозо-6-фосфатазой , фруктозо-1,6-бисфосфатазой и ФЕП-карбоксикиназой /пируваткарбоксилазой. Эти ферменты обычно регулируются схожими молекулами, но с противоположными результатами. Например, ацетил-КоА и цитрат активируют ферменты глюконеогенеза (пируваткарбоксилазу и фруктозо-1,6-бисфосфатазу соответственно), одновременно ингибируя гликолитический фермент пируваткиназу . Эта система взаимного контроля позволяет гликолизу и глюконеогенезу ингибировать друг друга и предотвращает бесполезный цикл синтеза глюкозы, направленный только на ее расщепление. Пируваткиназу также можно обойти по 86 путям [28], не связанным с глюконеогенезом, с целью образования пирувата, а затем и лактата; в некоторых из этих путей используются атомы углерода, происходящие из глюкозы.
Большинство ферментов , ответственных за глюконеогенез, находятся в цитозоле ; исключениями являются митохондриальная пируваткарбоксилаза и у животных фосфоенолпируваткарбоксикиназа . Последний существует в виде изофермента, локализованного как в митохондриях , так и в цитозоле . [29] Скорость глюконеогенеза в конечном итоге контролируется действием ключевого фермента, фруктозо-1,6-бисфосфатазы , который также регулируется посредством передачи сигнала цАМФ и его фосфорилирования.
Глобальный контроль глюконеогенеза опосредован глюкагоном ( высвобождаемым при низком уровне глюкозы в крови ); он запускает фосфорилирование ферментов и регуляторных белков с помощью протеинкиназы А (циклической АМФ-регулируемой киназы), что приводит к ингибированию гликолиза и стимуляции глюконеогенеза. Инсулин противодействует глюкагону, ингибируя глюконеогенез. Диабет 2 типа характеризуется избытком глюкагона и резистентностью организма к инсулину. [30] Инсулин больше не может ингибировать экспрессию генов ферментов, таких как PEPCK, что приводит к повышению уровня гипергликемии в организме. [31] Противодиабетический препарат метформин снижает уровень глюкозы в крови в первую очередь за счет ингибирования глюконеогенеза, преодолевая неспособность инсулина ингибировать глюконеогенез из-за резистентности к инсулину. [32]
Исследования показали, что отсутствие продукции глюкозы печенью не оказывает существенного влияния на контроль концентрации глюкозы в плазме натощак. Компенсаторная индукция глюконеогенеза происходит в почках и кишечнике под действием глюкагона , глюкокортикоидов и ацидоза. [33]
В печени белок FOX FOXO6 обычно способствует глюконеогенезу натощак, но инсулин блокирует FOXO6 при приеме пищи. [34] В условиях резистентности к инсулину инсулин не может блокировать FOXO6, что приводит к продолжению глюконеогенеза даже при кормлении, что приводит к повышению уровня глюкозы в крови ( гипергликемии ). [34]
Инсулинорезистентность является общей чертой метаболического синдрома и диабета 2 типа . По этой причине глюконеогенез является целью терапии диабета 2 типа, например, противодиабетического препарата метформина , который ингибирует глюконеогенное образование глюкозы и стимулирует поглощение глюкозы клетками. [35]
Глюконеогенез считается одним из самых древних анаболических путей и, вероятно, был обнаружен у последнего универсального общего предка . [36] Рафаэль Ф. Сэй и Георг Фукс заявили в 2010 году, что «все группы архей, а также глубоко разветвленные бактериальные линии содержат бифункциональную фруктозо-1,6-бисфосфат (FBP) альдолазу / фосфатазу с активностью как альдолазы FBP, так и фосфатазы FBP. Этот фермент отсутствует у большинства других бактерий и у эукариот, и он термостабилен даже у мезофильных морских кренархеот». Предполагается, что фруктозо-1,6-бисфосфатальдолаза/фосфатаза была предковым глюконеогенным ферментом и предшествовала гликолизу. [37] Но химические механизмы глюконеогенеза и гликолиза, будь то анаболические или катаболические, схожи, что позволяет предположить, что они оба возникли в одно и то же время. Показано, что фруктозо-1,6-бисфосфат непрерывно синтезируется неферментативно в замораживающем растворе. Синтез ускоряется в присутствии аминокислот, таких как глицин и лизин, что означает, что первыми анаболическими ферментами были аминокислоты. Пребиотические реакции глюконеогенеза могут протекать и неферментативно в циклах дегидратации-высушивания. Такая химия могла произойти в гидротермальной среде, включая температурные градиенты и циклическое замерзание и оттаивание. Минеральные поверхности могли играть роль в фосфорилировании промежуточных продуктов метаболизма глюконеогенеза и, как было показано, производят тетрозу, гексозофосфаты и пентозу из формальдегида, глицеральдегида и гликоляльдегида. [38] [39] [40]