Имидазол (ImH) представляет собой органическое соединение формулы C 3 N 2 H 4 . Это белое или бесцветное твердое вещество, растворимое в воде с образованием слабощелочного раствора . В химии это ароматический гетероцикл , классифицируемый как диазол , имеющий несмежные атомы азота в метазамещении .
Многие натуральные продукты, особенно алкалоиды , содержат имидазольное кольцо. Эти имидазолы имеют общее кольцо 1,3-C 3 N 2 , но имеют различные заместители. Эта кольцевая система присутствует в важных биологических строительных блоках, таких как гистидин и родственный ему гормон гистамин . Многие лекарства содержат имидазольное кольцо, например, некоторые противогрибковые препараты , антибиотики нитроимидазолового ряда и седативный мидазолам . [5] [6] [7] [8] [9]
При слиянии с пиримидиновым кольцом он образует пурин , который является наиболее широко встречающимся в природе азотсодержащим гетероциклом . [10]
Название «имидазол» было придумано в 1887 году немецким химиком Артуром Рудольфом Ханчем (1857–1935). [11]
Имидазол представляет собой плоское 5-членное кольцо, существующее в двух эквивалентных таутомерных формах, поскольку водород может быть связан с тем или иным атомом азота . Имидазол является высокополярным соединением, о чем свидетельствует его электрический дипольный момент 3,67 Д [12] , и хорошо растворим в воде. Соединение отнесено к ароматическим из-за наличия плоского кольца, содержащего 6 π-электронов (пара электронов от протонированного атома азота и по одному от каждого из остальных четырех атомов кольца). Некоторые резонансные структуры имидазола показаны ниже:
Имидазол амфотерен , то есть может действовать как кислота, так и как основание. В качестве кислоты pKa имидазола составляет 14,5, что делает его менее кислым, чем карбоновые кислоты, фенолы и имиды, но немного более кислым, чем спирты . Кислотный протон – это тот, который связан с азотом. Депротонирование дает имидазолид-анион, который является симметричным. В качестве основания p K a сопряженной кислоты (обозначаемой как p K BH + , чтобы избежать путаницы между ними) составляет примерно 7, что делает имидазол примерно в шестьдесят раз более основным, чем пиридин . Основным сайтом является азот с неподеленной парой (не связанный с водородом). Протонирование дает катион имидазолия, который является симметричным.
Впервые об имидазоле сообщил в 1858 году немецкий химик Генрих Дебус , хотя различные производные имидазола были открыты еще в 1840-х годах. Было показано, что глиоксаль , формальдегид и аммиак конденсируются с образованием имидазола (глиоксалина, как он первоначально назывался). [13] Этот синтез, хотя и дает относительно низкие выходы, все еще используется для получения C -замещенных имидазолов.
В одной микроволновой модификации реагентами являются бензил , бензальдегид и аммиак в ледяной уксусной кислоте , образуя 2,4,5-трифенилимидазол («лофин»). [14]
Имидазол можно синтезировать множеством методов, помимо метода Дебуса . Многие из этих синтезов также можно применять к различным замещенным имидазолам и производным имидазола путем изменения функциональных групп в реагентах. Эти методы обычно классифицируются по тому, какие и сколько связей образуются для образования имидазольных колец. Например, метод Дебуса образует связи (1,2), (3,4) и (1,5) в имидазоле, используя каждый реагент как фрагмент кольца, и, таким образом, этот метод будет представлять собой метод с тремя связями. -образующий синтез. Ниже представлена небольшая выборка этих методов.
Связь (1,5) или (3,4) может быть образована реакцией имидата и α-аминоальдегида или α- аминоацеталя . Приведенный ниже пример применим к имидазолу, когда R 1 = R 2 = водород.
Связи (1,2) и (2,3) могут быть образованы обработкой 1,2-диаминоалкана при высоких температурах спиртом , альдегидом или карбоновой кислотой . Требуется катализатор дегидрирования, например платина на оксиде алюминия .
Связи (1,2) и (3,4) также могут образовываться из N -замещенных α-аминокетонов и формамида при нагревании. Продуктом будет 1,4-дизамещенный имидазол, но здесь, поскольку R 1 = R 2 = водород, продуктом является сам имидазол. Выход этой реакции умеренный, но это, по-видимому, наиболее эффективный метод замещения 1,4.
Это общий метод, который дает хорошие выходы замещенных имидазолов. По сути, это адаптация метода Дебуса, называемого синтезом имидазола Дебуса-Радзишевского . Исходными веществами являются замещенные глиоксаль, альдегид, амин и аммиак или соль аммония. [15]
Имидазол можно синтезировать фотолизом 1 - винилтетразола . Эта реакция даст существенные выходы только в том случае, если 1-винилтетразол эффективно получают из оловоорганического соединения , такого как 2-трибутилстаннилтетразол. Реакция, показанная ниже, дает имидазол, когда R 1 = R 2 = R 3 = водород.
Имидазол также может быть получен в парофазной реакции. Реакция происходит с формамидом , этилендиамином и водородом над платиной на оксиде алюминия , и она должна проходить при температуре от 340 до 480 ° C. При этом образуется очень чистый имидазольный продукт.
Реакцию Ван Лейзена также можно использовать для образования имидазолов, исходя из TosMIC и альдимина . Синтез имидазола Ван Лейзена позволяет получать имидазолы из альдиминов реакцией с тозилметилизоцианидом (TosMIC). Позже реакция была расширена до двухстадийного синтеза, в котором альдимин образуется на месте: трехкомпонентная реакция Ван Лейзена (vL-3CR).
Имидазол входит в состав многих важных биологических соединений. Наиболее распространенной является аминокислота гистидин , имеющая имидазольную боковую цепь . Гистидин присутствует во многих белках и ферментах , например, путем связывания кофакторов металлов, как это видно в гемоглобине .
Гистидиновые соединения на основе имидазола играют очень важную роль во внутриклеточной буферизации. [17] Гистидин может быть декарбоксилирован до гистамина . Гистамин может вызвать крапивницу (крапивницу), если он вырабатывается во время аллергической реакции.
Заместители имидазола встречаются во многих фармацевтических препаратах. Синтетические имидазолы присутствуют во многих фунгицидах , а также противогрибковых , противопротозойных и антигипертензивных препаратах. Имидазол является частью молекулы теофиллина , содержащейся в чайных листьях и кофейных зернах, которая стимулирует центральную нервную систему . Он присутствует в противораковом препарате меркаптопурине , который борется с лейкемией , вмешиваясь в активность ДНК .
Ряд замещенных имидазолов, включая клотримазол , являются селективными ингибиторами синтазы оксида азота , что делает их интересными лекарственными мишенями при воспалениях , нейродегенеративных заболеваниях и опухолях нервной системы. [18] [19] Другая биологическая активность фармакофора имидазола связана с подавлением внутриклеточных потоков Ca 2+ и K + и вмешательством в инициацию трансляции. [20]
Замещенные производные имидазола ценны при лечении многих системных грибковых инфекций . [21] Имидазолы относятся к классу азольных противогрибковых средств , в который входят кетоконазол , миконазол и клотримазол .
Для сравнения, другая группа азолов — это триазолы, в которую входят флуконазол , итраконазол и вориконазол . Разница между имидазолами и триазолами заключается в механизме ингибирования фермента цитохрома P450 . N3 имидазольного соединения связывается с атомом железа гема цитохрома P450 трехвалентного железа, тогда как N4 триазолов связывается с гемовой группой. Было показано, что триазолы обладают более высокой специфичностью к цитохрому P450, чем имидазолы, что делает их более эффективными, чем имидазолы. [22]
Некоторые производные имидазола оказывают воздействие на насекомых, например, нитрат сульконазола оказывает сильное противопитательное действие на переваривающих кератин личинок австралийского коврового жука Anthrenocerus australis , как и нитрат эконазола на обыкновенную платяную моль Tineola bisselliella . [23]
Сам имидазол имеет мало прямых применений. Вместо этого он является предшественником различных агрохимикатов, включая энилконазол , климбазол , клотримазол , прохлораз и бифоназол . [24]
Имидазол и его производные обладают высоким сродством к катионам металлов. Одним из применений имидазола является очистка белков , меченных His , с помощью аффинной хроматографии с иммобилизованными металлами (IMAC). Имидазол используется для элюирования меченых белков, связанных с ионами никеля , прикрепленными к поверхности шариков в хроматографической колонке. Через колонку пропускают избыток имидазола, который вытесняет His-метку из координации никеля, освобождая His-меченные белки.
Имидазол является подходящим буфером для pH от 6,2 до 7,8 [25] . Чистый имидазол практически не имеет поглощения на длинах волн, соответствующих белку (280 нм), [26] [27] , однако более низкие чистоты имидазола могут давать заметное поглощение при 280 нм. Имидазол может влиять на анализ белка Лоури . [28]
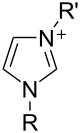
Соли имидазола, в которых имидазольное кольцо представляет собой катион , известны как соли имидазолия (например, хлорид или нитрат имидазолия ). [29] Эти соли образуются в результате протонирования или замещения азота имидазола. Эти соли использовались в качестве ионных жидкостей и предшественников стабильных карбенов . Также хорошо известны соли, в которых депротонированный имидазол является анионом ; эти соли известны как имидазолаты (например, имидазолат натрия, NaC 3 H 3 N 2 ).
Имидазол обладает низкой острой токсичностью, о чем свидетельствует LD 50 , равная 970 мг/кг (Крысы, перорально). [24]
{{cite encyclopedia}}: CS1 maint: несколько имен: список авторов ( ссылка )