
Ионы кальция (Ca 2+ ) вносят вклад в физиологию и биохимию клеток организмов . Они играют важную роль в путях передачи сигнала , [2] [3] , где они действуют как вторичные мессенджеры , в высвобождении нейротрансмиттеров из нейронов , в сокращении всех типов мышечных клеток и в оплодотворении . Многим ферментам требуются ионы кальция в качестве кофактора , включая несколько факторов коагуляции . Внеклеточный кальций также важен для поддержания разности потенциалов через возбудимые клеточные мембраны , а также для правильного формирования костей.
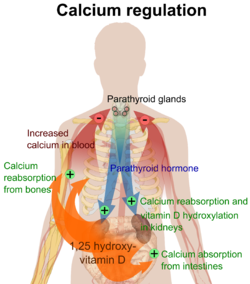
Уровень кальция в плазме у млекопитающих строго регулируется, [2] [3] при этом кость выступает в качестве основного места хранения минералов . Ионы кальция , Ca 2+ , высвобождаются из кости в кровоток в контролируемых условиях. Кальций транспортируется по кровотоку в виде растворенных ионов или связан с белками, такими как сывороточный альбумин . Паратиреоидный гормон , выделяемый паращитовидной железой, регулирует резорбцию Ca 2+ из кости, реабсорбцию в почках обратно в кровоток и увеличивает активацию витамина D 3 в кальцитриол . Кальцитриол, активная форма витамина D 3 , способствует абсорбции кальция из кишечника и костей. Кальцитонин, выделяемый парафолликулярными клетками щитовидной железы , также влияет на уровень кальция, противодействуя паратиреоидному гормону; однако его физиологическое значение для человека сомнительно.
Внутриклеточный кальций хранится в органеллах , которые периодически высвобождают и затем повторно накапливают ионы Ca 2+ в ответ на определенные клеточные события: места хранения включают митохондрии и эндоплазматический ретикулум . [4]
Характерные концентрации кальция в модельных организмах составляют: в E. coli 3 мМ (связанный), 100 нМ (свободный), в почкующихся дрожжах 2 мМ (связанный), в клетках млекопитающих 10–100 нМ (свободный) и в плазме крови 2 мМ. [5]
В 2021 году кальций был 243-м наиболее часто назначаемым лекарством в Соединенных Штатах, было выписано более 1 миллиона рецептов. [8] [9]
Институт медицины США (IOM) установил рекомендуемые нормы потребления кальция (RDA) в 1997 году и обновил эти значения в 2011 году. [6] См. таблицу. Европейское агентство по безопасности пищевых продуктов (EFSA) использует термин «рекомендуемая норма потребления для населения» (PRI) вместо RDA и устанавливает немного другие цифры: возраст 4–10 лет 800 мг, возраст 11–17 лет 1150 мг, возраст 18–24 года 1000 мг и >25 лет 950 мг. [10]
Из-за опасений долгосрочных неблагоприятных побочных эффектов, таких как кальцификация артерий и камни в почках, IOM и EFSA установили допустимые верхние уровни потребления (UL) для комбинации диетического и дополнительного кальция. Согласно IOM, люди в возрасте от 9 до 18 лет не должны превышать 3000 мг/день; для возраста от 19 до 50 лет не должны превышать 2500 мг/день; для возраста 51 года и старше не должны превышать 2000 мг/день. [11] EFSA установило UL на уровне 2500 мг/день для взрослых, но решило, что информации о детях и подростках недостаточно для определения UL. [12]
Для маркировки пищевых продуктов и диетических добавок в США количество в порции выражается в процентах от суточной нормы (%DV). Для маркировки кальция 100% суточной нормы составляли 1000 мг, но с 27 мая 2016 года эта цифра была пересмотрена до 1300 мг, чтобы соответствовать RDA. [13] [14] Таблица старых и новых суточных норм для взрослых приведена в Reference Daily Intake .
Хотя, как правило, маркировка и маркетинг пищевых добавок не разрешается делать заявления о профилактике или лечении заболеваний, FDA для некоторых продуктов питания и пищевых добавок рассмотрело науку, пришло к выводу, что существует значительное научное согласие, и опубликовало специально сформулированные разрешенные заявления о пользе для здоровья. Первоначальное постановление, разрешающее заявление о пользе для здоровья пищевых добавок с кальцием и остеопорозом, было позже изменено, чтобы включить добавки кальция и витамина D , вступившие в силу 1 января 2010 года. Примеры разрешенных формулировок приведены ниже. Чтобы соответствовать заявлению о пользе для здоровья кальция, пищевая добавка должна содержать не менее 20% от рекомендуемой суточной нормы потребления, что для кальция означает не менее 260 мг/порцию. [15]
В 2005 году FDA одобрило квалифицированное заявление о пользе для здоровья кальция и гипертонии с предложенной формулировкой «Некоторые научные данные свидетельствуют о том, что добавки кальция могут снижать риск гипертонии. Однако FDA определило, что эти данные противоречивы и не являются окончательными». Доказательства гипертонии и преэклампсии, вызванных беременностью, были признаны неокончательными. [16] В том же году FDA одобрило QHC для кальция и рака толстой кишки с предложенной формулировкой «Некоторые данные свидетельствуют о том, что добавки кальция могут снижать риск рака толстой/прямой кишки, однако FDA определило, что эти данные ограничены и не являются окончательными». Доказательства рака молочной железы и рака простаты были признаны неокончательными. [17] Предложения о QHC для кальция как средства защиты от камней в почках или от менструальных расстройств или боли были отклонены. [18] [19]
Европейское агентство по безопасности пищевых продуктов (EFSA) пришло к выводу, что «Кальций способствует нормальному развитию костей». [20] EFSA отвергло утверждение о том, что существует причинно-следственная связь между потреблением кальция и калия с пищей и поддержанием нормального кислотно-щелочного баланса. [21] EFSA также отвергло утверждения о влиянии кальция на ногти, волосы, липиды крови, предменструальный синдром и поддержание веса тела. [22]
На веб-сайте Министерства сельского хозяйства США (USDA) имеется очень полная таблица с возможностью поиска по содержанию кальция (в миллиграммах) в продуктах питания в общепринятых единицах измерения, например, на 100 граммов или на обычную порцию. [23] [24]
Количество кальция в крови (точнее, в плазме крови ) можно измерить как общий кальций , который включает как связанный с белком, так и свободный кальций. Напротив, ионизированный кальций является мерой свободного кальция. Аномально высокий уровень кальция в плазме называется гиперкальциемией , а аномально низкий уровень называется гипокальциемией , причем «аномальный» обычно относится к уровням, выходящим за пределы референтного диапазона .
Основными методами измерения уровня кальция в сыворотке являются: [32]
Общее количество Ca 2+, присутствующего в ткани, можно измерить с помощью атомно-абсорбционной спектроскопии , при которой ткань испаряется и сжигается. Для измерения концентрации Ca 2+ или его пространственного распределения в цитоплазме клеток in vivo или in vitro можно использовать ряд флуоресцентных репортеров. К ним относятся проницаемые для клеток, связывающие кальций флуоресцентные красители , такие как Fura-2 или генетически модифицированный вариант зеленого флуоресцентного белка (GFP), названный Cameleon .
Поскольку доступ к ионизированному кальцию не всегда возможен, вместо этого можно использовать скорректированный кальций. Чтобы рассчитать скорректированный кальций в ммоль/л, берется общий кальций в ммоль/л и добавляется к ((40 минус сывороточный альбумин в г/л), умноженному на 0,02). [33] Однако существуют разногласия относительно полезности скорректированного кальция, поскольку он может быть не лучше общего кальция. [34] Может быть полезнее скорректировать общий кальций как для альбумина, так и для анионной щели . [35] [36]
У позвоночных ионы кальция, как и многие другие ионы, имеют такое жизненно важное значение для многих физиологических процессов, что их концентрация поддерживается в определенных пределах для обеспечения адекватного гомеостаза. Об этом свидетельствует кальций в плазме человека , который является одной из наиболее строго регулируемых физиологических переменных в организме человека. Нормальные уровни в плазме колеблются от 1 до 2% в течение любого заданного времени. Примерно половина всего ионизированного кальция циркулирует в своей несвязанной форме, а другая половина находится в комплексе с белками плазмы, такими как альбумин , а также с анионами , включая бикарбонат , цитрат , фосфат и сульфат . [37]
Различные ткани содержат кальций в разных концентрациях. Например, Ca 2+ (в основном фосфат кальция и немного сульфата кальция ) является наиболее важным (и специфическим) элементом костей и кальцинированного хряща . У людей общее содержание кальция в организме присутствует в основном в форме костного минерала (примерно 99%). В этом состоянии он в значительной степени недоступен для обмена/биодоступности. Способ преодоления этого — процесс резорбции костей , при котором кальций высвобождается в кровоток под действием костных остеокластов . Остальной кальций присутствует во внеклеточной и внутриклеточной жидкостях.
Внутри типичной клетки внутриклеточная концентрация ионизированного кальция составляет примерно 100 нМ, но может увеличиваться в 10-100 раз во время различных клеточных функций. Уровень внутриклеточного кальция поддерживается относительно низким по отношению к внеклеточной жидкости, примерно в 12 000 раз. Этот градиент поддерживается посредством различных кальциевых насосов плазматической мембраны , которые используют АТФ для получения энергии, а также значительного хранилища во внутриклеточных отсеках. В электрически возбудимых клетках , таких как скелетные и сердечные мышцы и нейроны, деполяризация мембраны приводит к транзиенту Ca 2+ с концентрацией цитозольного Ca 2+ , достигающей около 1 мкМ. [39] Митохондрии способны секвестрировать и хранить часть этого Ca 2+ . Было подсчитано, что концентрация свободного кальция в митохондриальном матриксе возрастает до десятков микромолярных уровней in situ во время нейронной активности. [40]
Влияние кальция на клетки человека специфично, то есть разные типы клеток реагируют по-разному. Однако при определенных обстоятельствах его действие может быть более общим. Ионы Ca2 + являются одними из самых распространенных вторичных посредников, используемых в передаче сигнала . Они попадают в цитоплазму либо извне клетки через клеточную мембрану через кальциевые каналы (такие как кальций-связывающие белки или потенциалзависимые кальциевые каналы), либо из некоторых внутренних хранилищ кальция, таких как эндоплазматический ретикулум [4] и митохондрии . Уровни внутриклеточного кальция регулируются транспортными белками , которые удаляют его из клетки. Например, натрий-кальциевый обменник использует энергию из электрохимического градиента натрия, связывая приток натрия в клетку (и вниз по его градиенту концентрации) с транспортом кальция из клетки. Кроме того, плазматическая мембранная Ca2 + АТФаза (PMCA) получает энергию для выкачивания кальция из клетки путем гидролиза аденозинтрифосфата (АТФ). В нейронах потенциал-зависимые, селективные к кальцию ионные каналы важны для синаптической передачи посредством высвобождения нейротрансмиттеров в синаптическую щель путем слияния синаптических пузырьков .
Функция кальция в сокращении мышц была обнаружена еще в 1882 году Рингером. Последующие исследования выявили его роль как посредника примерно столетие спустя. Поскольку его действие взаимосвязано с цАМФ , их называют синархическими посредниками. Кальций может связываться с несколькими различными модулируемыми кальцием белками, такими как тропонин-С (первый из идентифицированных) и кальмодулин , белками, которые необходимы для содействия сокращению мышц.
В эндотелиальных клетках, выстилающих внутреннюю часть кровеносных сосудов, ионы Ca 2+ могут регулировать несколько сигнальных путей, которые вызывают расслабление гладких мышц, окружающих кровеносные сосуды. [ требуется ссылка ] Некоторые из этих путей, активируемых Ca 2+, включают стимуляцию eNOS для выработки оксида азота, а также стимуляцию каналов K ca для оттока K + и вызывают гиперполяризацию клеточной мембраны. Как оксид азота, так и гиперполяризация вызывают расслабление гладких мышц, чтобы регулировать тонус кровеносных сосудов. [41] Однако дисфункция в этих путях, активируемых Ca 2+, может привести к повышению тонуса, вызванному нерегулируемым сокращением гладких мышц. Этот тип дисфункции можно наблюдать при сердечно-сосудистых заболеваниях, гипертонии и диабете. [42]
Координация кальция играет важную роль в определении структуры и функции белков. Примером белка с координацией кальция является фактор Виллебранда (vWF), который играет важную роль в процессе образования сгустка крови. Было обнаружено с помощью измерения одиночной молекулы оптическим пинцетом , что связанный с кальцием vWF действует как датчик силы сдвига в крови. Сила сдвига приводит к развертыванию домена A2 vWF, скорость рефолдинга которого резко увеличивается в присутствии кальция. [43]
Поток ионов Ca 2+ регулирует несколько систем вторичных посредников в нейронной адаптации для зрительной, слуховой и обонятельной систем. Он часто может быть связан с кальмодулином , например, в обонятельной системе, чтобы либо усиливать, либо подавлять катионные каналы. [44] В других случаях изменение уровня кальция может фактически освободить гуанилатциклазу от ингибирования, как в системе фоторецепции. [45] Ион Ca 2+ также может определять скорость адаптации в нейронной системе в зависимости от рецепторов и белков, которые имеют различное сродство к обнаружению уровней кальция, чтобы открывать или закрывать каналы при высокой концентрации и низкой концентрации кальция в клетке в это время. [46]

Значительное снижение внеклеточной концентрации ионов Ca 2+ может привести к состоянию, известному как гипокальциемическая тетания , которая характеризуется спонтанным разрядом двигательных нейронов . Кроме того, тяжелая гипокальциемия начнет влиять на аспекты свертывания крови и передачи сигнала.
Ионы Ca2 + могут повредить клетки, если они поступают в избыточном количестве (например, в случае эксайтотоксичности или перевозбуждения нейронных цепей , что может возникнуть при нейродегенеративных заболеваниях или после инсультов, таких как черепно-мозговая травма или инсульт ). Избыточное поступление кальция в клетку может повредить ее или даже вызвать апоптоз или смерть от некроза . Кальций также действует как один из основных регуляторов осмотического стресса ( осмотический шок ). Хронически повышенный уровень кальция в плазме ( гиперкальциемия ) связан с сердечными аритмиями и снижением нервно-мышечной возбудимости. Одной из причин гиперкальциемии является состояние, известное как гиперпаратиреоз .
Некоторые беспозвоночные используют соединения кальция для построения своего экзоскелета ( панцирей и раковин ) или эндоскелета ( пластин иглокожих и известковых спикул пористых животных ).

Когда абсцизовая кислота подает сигнал замыкающим клеткам, свободные ионы Ca2 + поступают в цитозоль как извне клетки, так и из внутренних хранилищ, обращая градиент концентрации, так что ионы K+ начинают выходить из клетки. Потеря растворенных веществ делает клетку вялой и закрывает устьичные поры.
Кальций является необходимым ионом в формировании митотического веретена . Без митотического веретена клеточное деление не может происходить. Хотя молодые листья имеют более высокую потребность в кальции, старые листья содержат большее количество кальция, поскольку кальций относительно неподвижен в растении. Он не транспортируется через флоэму, поскольку может связываться с другими ионами питательных веществ и выпадать в осадок из жидких растворов.
Ионы Ca 2+ являются важным компонентом стенок и мембран растительных клеток и используются в качестве катионов для балансировки органических анионов в вакуоли растений . [49] Концентрация Ca 2+ в вакуоли может достигать миллимолярных уровней. Наиболее яркое использование ионов Ca 2+ в качестве структурного элемента в водорослях наблюдается у морских кокколитофорид , которые используют Ca 2+ для формирования пластин карбоната кальция , которыми они покрыты.
Кальций необходим для образования пектина в срединных пластинках вновь образованных клеток.
Кальций необходим для стабилизации проницаемости клеточных мембран. Без кальция клеточные стенки не способны стабилизироваться и удерживать свое содержимое. Это особенно важно для развития плодов. Без кальция клеточные стенки слабы и неспособны удерживать содержимое плода.
Некоторые растения накапливают Ca в своих тканях, делая их более прочными. Кальций хранится в виде кристаллов Ca- оксалата в пластидах .
Ионы Ca2 + обычно сохраняются на наномолярном уровне в цитозоле растительных клеток и действуют в ряде путей передачи сигналов как вторичные посредники .