Кальций — химический элемент ; он имеет символ Ca и атомный номер 20. Будучи щелочноземельным металлом , кальций является химически активным металлом, который при воздействии воздуха образует темный оксидно-нитридный слой. Его физические и химические свойства наиболее близки к его более тяжелым гомологам стронцию и барию . Это пятый по распространенности элемент в земной коре и третий по распространенности металл после железа и алюминия . Наиболее распространенным соединением кальция на Земле является карбонат кальция , обнаруженный в известняке и окаменелых остатках ранней морской жизни; гипс , ангидрит , флюорит и апатит также являются источниками кальция. Название происходит от латинского Calx « известь », полученного при нагревании известняка.
Некоторые соединения кальция были известны древним людям, хотя их химия была неизвестна до семнадцатого века. Чистый кальций был выделен в 1808 году электролизом его оксида Хамфри Дэви , который дал этому элементу название. Соединения кальция широко используются во многих отраслях промышленности: в пищевых продуктах и фармацевтических препаратах в качестве добавок кальция , в бумажной промышленности в качестве отбеливателей, в качестве компонентов цемента и электрических изоляторов, а также при производстве мыла. С другой стороны, металл в чистом виде имеет мало применений из-за его высокой реакционной способности; тем не менее, в небольших количествах его часто используют в качестве легирующего компонента при выплавке стали, а иногда, как кальциево-свинцовый сплав, при изготовлении автомобильных аккумуляторов.
Кальций — самый распространенный металл и пятый по распространенности элемент в организме человека . [8] Как электролиты , ионы кальция (Ca 2+ ) играют жизненно важную роль в физиологических и биохимических процессах организмов и клеток : в путях передачи сигналов , где они действуют как вторичные мессенджеры ; в высвобождении нейромедиаторов из нейронов ; в сокращении всех типов мышечных клеток ; как кофакторы во многих ферментах ; и в оплодотворении . [8] Ионы кальция вне клеток важны для поддержания разницы потенциалов на мембранах возбудимых клеток , синтеза белка и формирования костей. [8] [9]
Кальций — очень пластичный серебристый металл (иногда его называют бледно-желтым), свойства которого очень похожи на свойства более тяжелых элементов его группы — стронция , бария и радия . Атом кальция имеет двадцать электронов, расположенных в электронной конфигурации [Ar]4s 2 . Как и другие элементы, помещенные во 2-ю группу таблицы Менделеева, кальций имеет два валентных электрона на крайней s-орбитали, которые очень легко теряются в химических реакциях с образованием диположительного иона со стабильной электронной конфигурацией благородного газа . корпус аргон . [10]
Следовательно, кальций почти всегда двухвалентен в своих соединениях, которые обычно являются ионными . Гипотетические одновалентные соли кальция были бы стабильны по отношению к своим элементам, но не к диспропорционированию с двухвалентными солями и металлическим кальцием, поскольку энтальпия образования MX 2 значительно выше, чем у гипотетического MX. Это происходит из-за гораздо большей энергии решетки , которую обеспечивает более сильно заряженный катион Ca 2+ по сравнению с гипотетическим катионом Ca + . [10]
Кальций, стронций, барий и радий всегда считаются щелочноземельными металлами ; Также часто включают более легкие бериллий и магний , также входящие во 2-ю группу таблицы Менделеева. Тем не менее, бериллий и магний существенно отличаются от других членов группы по своему физическому и химическому поведению: они ведут себя больше как алюминий и цинк соответственно и имеют более слабый металлический характер, чем постпереходные металлы , поэтому традиционное определение термина «щелочноземельный металл» их исключает. [11]
Металлический кальций плавится при 842 °С и кипит при 1494 °С; эти значения выше, чем у магния и стронция, соседних металлов 2-й группы. Он кристаллизуется в гранецентрированной кубической форме, как стронций; выше 450 ° C он превращается в анизотропную гексагональную плотноупакованную структуру, как магний. Его плотность 1,55 г/см 3 является самой низкой в своей группе. [10]
Кальций тверже свинца , но его можно с усилием разрезать ножом. Хотя кальций является худшим проводником электричества, чем медь или алюминий по объему, он является лучшим проводником по массе, чем оба, из-за его очень низкой плотности. [12] Хотя кальций непригоден в качестве проводника для большинства наземных применений, поскольку он быстро реагирует с атмосферным кислородом, его использование как таковое в космосе рассматривалось. [12]

По химическому составу кальций аналогичен типичному тяжелому щелочноземельному металлу. Например, кальций самопроизвольно реагирует с водой быстрее, чем магний, и медленнее, чем стронций, с образованием гидроксида кальция и газообразного водорода. Он также реагирует с кислородом и азотом воздуха, образуя смесь оксида кальция и нитрида кальция . [13] При тонком измельчении он самопроизвольно сгорает на воздухе с образованием нитрида. В массе кальций менее реакционноспособен: он быстро образует гидратное покрытие во влажном воздухе, но при относительной влажности ниже 30% он может храниться неопределенно долго при комнатной температуре. [14]
Помимо простого оксида CaO, пероксид CaO 2 может быть получен прямым окислением металлического кальция под высоким давлением кислорода, и есть некоторые свидетельства существования желтого супероксида Ca(O 2 ) 2 . [15] Гидроксид кальция, Ca(OH) 2 , является сильным основанием, хотя и не таким сильным, как гидроксиды стронция, бария или щелочных металлов. [16] Известны все четыре дигалогенида кальция. [17] Карбонат кальция (CaCO 3 ) и сульфат кальция (CaSO 4 ) являются особенно распространенными минералами. [18] Подобно стронцию и барию, а также щелочным металлам и двухвалентным лантанидам европию и иттербию , металлический кальций растворяется непосредственно в жидком аммиаке , образуя темно-синий раствор. [10]
Из-за большого размера иона кальция (Ca 2+ ) часто встречаются высокие координационные числа, вплоть до 24 в некоторых интерметаллических соединениях , таких как CaZn 13 . [19] Кальций легко образует комплексы с кислородными хелатами , такими как ЭДТА и полифосфаты , которые полезны в аналитической химии и удалении ионов кальция из жесткой воды . В отсутствие стерических препятствий меньшие катионы группы 2 имеют тенденцию образовывать более прочные комплексы, но когда в процесс вовлечены большие полидентатные макроциклы , тенденция меняется на противоположную. [18]
Хотя кальций относится к той же группе, что и магний, и магнийорганические соединения очень часто используются в химии, кальцийорганические соединения не так широко распространены, поскольку их труднее получить и они более реакционноспособны, хотя недавно они были исследованы в качестве возможных катализаторов . [20] [21] [22] [23] [24] Кальцийорганические соединения имеют тенденцию быть более похожими на иттербиевые органические соединения из-за схожих ионных радиусов Yb 2+ (102 пм) и Ca 2+ (100 пм). [25]
Большинство этих соединений можно получить только при низких температурах; объемистые лиганды имеют тенденцию способствовать стабильности. Например, дициклопентадиенил кальция , Ca(C 5 H 5 ) 2 , должен быть получен путем прямой реакции металлического кальция с меркуоценом или самим циклопентадиеном ; замена лиганда C 5 H 5 более объемистым лигандом C 5 (CH 3 ) 5, с другой стороны, увеличивает растворимость, летучесть и кинетическую стабильность соединения. [25]
Природный кальций представляет собой смесь пяти стабильных изотопов ( 40 Ca, 42 Ca, 43 Ca, 44 Ca и 46 Ca) и одного изотопа с периодом полураспада настолько длинным, что его можно считать стабильным для всех практических целей ( 48 Ca , с периодом полураспада около 4,3×10 19 лет). Кальций — первый (самый легкий) элемент, имеющий шесть природных изотопов. [13]
На сегодняшний день наиболее распространенным изотопом кальция в природе является 40 Са, который составляет 96,941% всего природного кальция. Он образуется в процессе сжигания кремния в результате синтеза альфа-частиц и является самым тяжелым стабильным нуклидом с равным числом протонов и нейтронов; его появление также медленно дополняется распадом первичного 40 К. Добавление еще одной альфа-частицы приводит к нестабильному 44 Ti, который быстро распадается за счет двух последовательных захватов электронов до стабильного 44 Ca; это составляет 2,806% всего природного кальция и является вторым по распространенности изотопом. [26] [27]
Остальные четыре природных изотопа — 42 Ca, 43 Ca, 46 Ca и 48 Ca — встречаются значительно реже, каждый из них составляет менее 1% всего природного кальция. Четыре более легких изотопа в основном являются продуктами процессов сжигания кислорода и кремния, а два более тяжелых изотопа производятся в процессах захвата нейтронов . 46 Ca в основном производится в «горячем» s-процессе , поскольку для его образования требуется довольно высокий поток нейтронов, чтобы короткоживущий 45 Ca мог захватить нейтрон. 48 Ca образуется путем захвата электронов в r-процессе в сверхновых типа Ia , где высокий избыток нейтронов и достаточно низкая энтропия обеспечивают его выживание. [26] [27]
46 Ca и 48 Ca — первые «классически стабильные» нуклиды с шестинейтронным или восьминейтронным избытком соответственно. Хотя 48 Ca чрезвычайно богат нейтронами для такого легкого элемента, он очень стабилен, поскольку представляет собой вдвойне магическое ядро , имеющее 20 протонов и 28 нейтронов, расположенных в закрытых оболочках. Его бета-распад до 48 Sc очень затруднен из-за грубого несоответствия ядерного спина : 48 Ca имеет нулевой ядерный спин, будучи четным-четным , тогда как 48 Sc имеет спин 6+, поэтому распад запрещен из-за сохранения углового момента . Хотя два возбужденных состояния 48 Sc также доступны для распада, они также запрещены из-за их высоких спинов. В результате, когда 48 Ca действительно распадается, он делает это путем двойного бета-распада с образованием 48 Ti , который является самым легким нуклидом, который, как известно, подвергается двойному бета-распаду. [28] [29]
Тяжелый изотоп 46 Ca теоретически также может подвергаться двойному бета-распаду с образованием 46 Ti, но этого никогда не наблюдалось. Самый легкий и наиболее распространенный изотоп 40 Ca также является дважды магическим и может подвергаться двойному захвату электронов с помощью 40 Ar , но этого также никогда не наблюдалось. Кальций — единственный элемент, имеющий два первичных изотопа с двойной магией. Экспериментальные нижние пределы периодов полураспада 40 Ca и 46 Ca составляют 5,9 × 10 21 год и 2,8 × 10 15 лет соответственно. [28]
Помимо практически стабильного 48 Ca, самым долгоживущим радиоизотопом кальция является 41 Ca. Он распадается путем захвата электронов до стабильной температуры 41 К с периодом полураспада около ста тысяч лет. Его существование в ранней Солнечной системе в качестве вымершего радионуклида было предположено на основании избытка 41 К: следы 41 Са также существуют сегодня, поскольку это космогенный нуклид , непрерывно реформируемый посредством нейтронной активации природного 40 Са . [27]
Известно множество других радиоизотопов кальция в диапазоне от 35 Ca до 60 Ca. Все они гораздо короче, чем 41 Ca, наиболее стабильными среди них являются 45 Ca (период полураспада 163 дня) и 47 Ca (период полураспада 4,54 дня). Изотопы легче, чем 42 Ca, обычно подвергаются бета-плюс-распаду до изотопов калия, а изотопы тяжелее, чем 44 Ca, обычно подвергаются бета-минус-распаду до изотопов скандия , хотя вблизи ядерных капельных линий испускание протонов и нейтронное излучение становятся существенными модами распада. также. [28]
Как и в случае с другими элементами, относительное содержание изотопов кальция изменяется в результате различных процессов. [30] Наиболее изученным из этих процессов является массово-зависимое фракционирование изотопов кальция, которое сопровождает осаждение минералов кальция, таких как кальцит , арагонит и апатит, из раствора. Более легкие изотопы преимущественно включаются в эти минералы, в результате чего окружающий раствор обогащается более тяжелыми изотопами в количестве примерно 0,025% на единицу атомной массы (а.е.м.) при комнатной температуре. Зависимые от массы различия в изотопном составе кальция обычно выражаются соотношением двух изотопов (обычно 44 Ca/ 40 Ca) в образце по сравнению с таким же соотношением в стандартном эталонном материале. 44 Ca/ 40 Ca варьируется примерно на 1% среди обычных земных материалов. [31]

Соединения кальция были известны на протяжении тысячелетий, хотя их химический состав не был понят до 17 века. [32] Известь в качестве строительного материала [33] и гипса для статуй использовалась еще около 7000 г. до н.э. [34] Первая датированная печь для обжига извести датируется 2500 годом до нашей эры и была найдена в Хафадже , Месопотамия . [35] [36]
Примерно в то же время обезвоженный гипс (CaSO 4 ·2H 2 O) использовался в Великой пирамиде Гизы . Этот материал позже будет использован для штукатурки гробницы Тутанхамона . Вместо этого древние римляне использовали известковые растворы, приготовленные путем нагревания известняка (CaCO 3 ). Само название «кальций» происходит от латинского слова « calx » «известь». [32]
Витрувий отметил, что полученная известь была легче исходного известняка, объяснив это кипением воды. В 1755 году Джозеф Блэк доказал, что это произошло из-за потери углекислого газа , который древние римляне не признавали за газ. [37]
В 1789 году Антуан Лавуазье предположил, что известь может быть оксидом фундаментального химического элемента . В своей таблице элементов Лавуазье перечислил пять «поддающихся солеобразованию земель» (т.е. руд, которые можно заставить вступать в реакцию с кислотами с образованием солей ( salis = соль на латыни): chaux (оксид кальция), магнезия (магнезия, оксид магния). ), барит (сульфат бария), глинозем (оксид алюминия, оксид алюминия) и кремнезем (кремнезем, диоксид кремния)). Об этих «элементах» Лавуазье рассуждал:
Мы, вероятно, знакомы пока лишь с частью существующих в природе металлических веществ, так как все те, которые имеют более сильное сродство к кислороду, чем имеет углерод, не способны до сих пор приводиться в металлическое состояние и, следовательно, являются лишь представленные нашему наблюдению в виде оксидов, путают с землями. Весьма вероятно, что в таком положении находится барит, который мы только что расположили с землями; ибо во многих экспериментах он проявляет свойства, близкие к свойствам металлических тел. Возможно даже, что все вещества, которые мы называем землями, могут быть лишь оксидами металлов, невосстанавливаемыми ни одним из известных до сих пор процессов. [38]
Кальций вместе с родственными ему магнием, стронцием и барием был впервые выделен Хамфри Дэви в 1808 году. Следуя работам Йонса Якоба Берцелиуса и Магнуса Мартина аф Понтина по электролизу , Дэви выделил кальций и магний, поместив смесь соответствующих металлов оксиды с оксидом ртути(II) на платиновой пластине, которая использовалась в качестве анода, а катод представлял собой платиновую проволоку, частично погруженную в ртуть. Затем электролиз дал амальгамы кальция и ртути и магния и ртути, а отгонка ртути дала металл. [32] [39] Однако чистый кальций не может быть получен в больших количествах этим методом, и работоспособный коммерческий процесс его производства был найден только более века спустя. [37]

Кальций с содержанием 3% является пятым по распространенности элементом в земной коре и третьим по распространенности металлом после алюминия и железа . [32] Это также четвертый по распространенности элемент в лунном нагорье . [14] Осадочные отложения карбоната кальция пронизывают поверхность Земли как окаменелые останки прошлой морской жизни; они встречаются в двух формах: ромбоэдрический кальцит (более распространенный) и ромбический арагонит (образующийся в морях с более умеренным климатом). К минералам первого типа относятся известняк , доломит , мрамор , мел , исландский шпат ; Залежи арагонита слагают Багамские острова , Флорида-Кис и бассейны Красного моря . Кораллы , морские ракушки и жемчуг в основном состоят из карбоната кальция. К другим важным минералам кальция относятся гипс (CaSO 4 ·2H 2 O), ангидрит (CaSO 4 ), флюорит (CaF 2 ) и апатит ([Ca 5 (PO 4 ) 3 X], X = OH, Cl, или Ф). [32]
Основными производителями кальция являются Китай (около 10 000–12 000 тонн в год), Россия (около 6 000–8 000 тонн в год) и США (около 2 000–4 000 тонн в год). Канада и Франция также входят в число второстепенных производителей. В 2005 г. было произведено около 24 тыс. тонн кальция; около половины добываемого в мире кальция используется Соединенными Штатами, причем ежегодно используется около 80% произведенного кальция. [12]
В России и Китае до сих пор используется метод электролиза Дэви, но вместо него применяется расплавленный хлорид кальция . [12] Поскольку кальций менее реакционноспособен, чем стронций или барий, оксидно-нитридное покрытие, образующееся на воздухе, стабильно, а токарная обработка и другие стандартные металлургические методы подходят для кальция. [40] В США и Канаде кальций вместо этого производят путем восстановления извести алюминием при высоких температурах. [12]
Круговорот кальция обеспечивает связь между тектоникой , климатом и углеродным циклом . Проще говоря, поднятие гор подвергает содержащие кальций породы, такие как некоторые граниты , химическому выветриванию и высвобождает Ca 2+ в поверхностные воды. Эти ионы переносятся в океан, где они вступают в реакцию с растворенным CO 2 с образованием известняка ( CaCO
3), который, в свою очередь, оседает на морское дно, где включается в новые породы. Растворенный CO 2 вместе с ионами карбоната и бикарбоната называется « растворенным неорганическим углеродом » (DIC). [41]
Реальная реакция более сложна и включает в себя ион бикарбоната ( HCO−
3), который образуется при реакции CO 2 с водой при pH морской воды :
При pH морской воды большая часть CO 2 немедленно превращается обратно в HCO.−
3. Реакция приводит к чистому переносу одной молекулы CO 2 из океана/атмосферы в литосферу . [42] В результате каждый ион Ca 2+ , высвобождаемый в результате химического выветривания, в конечном итоге удаляет одну молекулу CO 2 из поверхностной системы (атмосферы, океана, почвы и живых организмов), сохраняя ее в карбонатных породах, где она, вероятно, останется на сотни лет. миллионов лет. Таким образом, выветривание кальция из горных пород удаляет CO 2 из океана и атмосферы, оказывая сильное долгосрочное воздействие на климат. [41] [43]
Металлический кальций наиболее широко используется в производстве стали из-за его сильного химического сродства к кислороду и сере . Его оксиды и сульфиды, однажды образовавшись, образуют в стали жидкие известково -алюминатные и сульфидные включения, которые всплывают наружу; при обработке эти включения рассеиваются по всей стали и становятся маленькими и сферическими, улучшая литейные качества, чистоту и общие механические свойства. Кальций также используется в необслуживаемых автомобильных аккумуляторах , в которых использование 0,1% кальций- свинцовых сплавов вместо обычных сурьмяно -свинцовых сплавов приводит к меньшим потерям воды и меньшему саморазряду. [44]
Из-за риска расширения и растрескивания в эти сплавы иногда также включают алюминий . Эти свинцово-кальциевые сплавы также используются в литье, заменяя свинцово-сурьмяные сплавы. [44] Кальций также используется для упрочнения алюминиевых сплавов, используемых для изготовления подшипников, для контроля содержания графитового углерода в чугуне и для удаления примесей висмута из свинца. [40] Металлический кальций содержится в некоторых средствах для очистки сточных вод, где он генерирует тепло и гидроксид кальция , который омыляет жиры и разжижает белки (например, белки в волосах), которые блокируют стоки. [45]
Помимо металлургии, реакционная способность кальция используется для удаления азота из газообразного аргона высокой чистоты, а также в качестве поглотителя кислорода и азота. Он также используется в качестве восстановителя при производстве хрома , циркония , тория , ванадия и урана . Его также можно использовать для хранения газообразного водорода, поскольку он вступает в реакцию с водородом с образованием твердого гидрида кальция , из которого водород можно легко повторно извлечь. [40]
Фракционирование изотопов кальция во время образования минералов привело к нескольким применениям изотопов кальция. В частности, открытие 1997 г. Скулана и ДеПаоло [46] о том, что минералы кальция изотопно легче растворов, из которых они выпадают, лежит в основе аналогичных приложений в медицине и палеоокеанографии. У животных с минерализованным кальцием скелетом изотопный состав кальция мягких тканей отражает относительную скорость образования и растворения скелетных минералов. [47]
Было показано, что у людей изменения изотопного состава кальция в моче связаны с изменениями минерального баланса костей. Когда скорость костеобразования превышает скорость резорбции кости, соотношение 44 Са/ 40 Са в мягких тканях повышается и наоборот. Из-за этой взаимосвязи измерения изотопов кальция в моче или крови могут быть полезны для раннего выявления метаболических заболеваний костей, таких как остеопороз . [47]
Аналогичная система существует и в морской воде, где соотношение 44 Ca/ 40 Ca имеет тенденцию возрастать, когда скорость удаления Ca 2+ минеральными осадками превышает поступление нового кальция в океан. В 1997 году Скулан и ДеПаоло представили первые доказательства изменения содержания 44 Ca/ 40 Ca в морской воде в течение геологического времени, а также теоретическое объяснение этих изменений. Более поздние работы подтвердили это наблюдение, показав, что концентрация Ca 2+ в морской воде не является постоянной и что океан никогда не находится в «стационарном состоянии» в отношении поступления и вывода кальция. Это имеет важные климатологические последствия, поскольку морской цикл кальция тесно связан с циклом углерода . [48] [49]
Многие соединения кальция используются, в частности, в пищевых продуктах, фармацевтических препаратах и медицине. Например, кальций и фосфор добавляются в пищу за счет добавления лактата кальция , дифосфата кальция и трикальцийфосфата . Последний также используется в качестве полирующего агента в зубной пасте и антацидах . Лактобионат кальция представляет собой белый порошок, который используется в качестве суспендирующего агента в фармацевтических препаратах. В выпечке фосфат кальция используется в качестве разрыхлителя . Сульфит кальция используется в качестве отбеливателя при производстве бумаги и в качестве дезинфицирующего средства, силикат кальция используется в качестве армирующего агента в резине, а ацетат кальция входит в состав известковой канифоли и используется для изготовления металлического мыла и синтетических смол. [44]
Кальций включен в Список основных лекарственных средств Всемирной организации здравоохранения . [50]
К продуктам, богатым кальцием, относятся молочные продукты , такие как йогурт и сыр , сардины , лосось , соевые продукты, капуста и обогащенные хлопья для завтрака . [9]
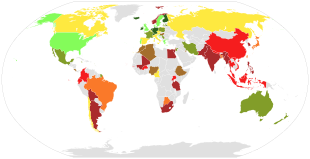
Из-за опасений по поводу долгосрочных побочных эффектов, включая кальцификацию артерий и камни в почках , Институт медицины США (IOM) и Европейское управление по безопасности пищевых продуктов (EFSA) установили допустимые верхние уровни потребления (UL) для комбинированных пищевых добавок и пищевых добавок. кальций. По данным МОМ, людям в возрасте 9–18 лет не следует превышать комбинированную дозу 3 г/день; для детей в возрасте 19–50 лет – не более 2,5 г/день; для детей в возрасте 51 года и старше не превышать 2 г/день. [51] EFSA установило UL для всех взрослых на уровне 2,5 г/день, но решило, что информации для детей и подростков недостаточно для определения UL. [52]
Кальций является важным элементом, необходимым в больших количествах. [8] [9] Ион Ca 2+ действует как электролит и жизненно важен для здоровья мышечной, кровеносной и пищеварительной систем; незаменим для построения костей; и поддерживает синтез и функцию клеток крови. Например, он регулирует сокращение мышц , нервную проводимость и свертывание крови. В результате уровень внутри- и внеклеточного кальция жестко регулируется организмом. Эту роль может играть кальций, поскольку ион Са 2+ образует устойчивые координационные комплексы со многими органическими соединениями, особенно с белками ; он также образует соединения с широким диапазоном растворимости, способствующие образованию скелета . [8] [55]
Ионы кальция могут образовывать комплексы с белками путем связывания карбоксильных групп остатков глутаминовой кислоты или аспарагиновой кислоты ; посредством взаимодействия с фосфорилированными остатками серина , тирозина или треонина ; или путем хелатирования γ-карбоксилированными аминокислотными остатками. Трипсин , пищеварительный фермент, использует первый метод; остеокальцин , белок костного матрикса, использует третий. [56]
Некоторые другие белки костного матрикса, такие как остеопонтин и костный сиалопротеин, используют как первый, так и второй. Прямая активация ферментов путем связывания кальция является обычным явлением; некоторые другие ферменты активируются путем нековалентной ассоциации с ферментами, непосредственно связывающими кальций. Кальций также связывается с фосфолипидным слоем клеточной мембраны , закрепляя белки, связанные с поверхностью клетки. [56]
В качестве примера широкого диапазона растворимости соединений кальция можно привести монокальцийфосфат , который хорошо растворим в воде, 85% внеклеточного кальция представляет собой дикальцийфосфат с растворимостью 2,00 мМ , а гидроксиапатит костей в органическом матриксе представляет собой трикальцийфосфат с растворимостью 2,00 мМ . растворимость 1000 мкМ. [56]
Кальций является распространенным компонентом поливитаминных пищевых добавок [8] , но состав комплексов кальция в добавках может влиять на его биодоступность , которая зависит от растворимости задействованной соли: цитрат кальция , малат и лактат обладают высокой биодоступностью, тогда как оксалат менее биодоступен. . Другие препараты кальция включают карбонат кальция , цитрат кальция малат и глюконат кальция . [8] Кишечник поглощает около одной трети потребляемого кальция в виде свободных ионов , а уровень кальция в плазме затем регулируется почками . [8]
Паратиреоидный гормон и витамин D способствуют формированию кости, позволяя и усиливая отложение там ионов кальция, обеспечивая быстрый обмен костной ткани, не влияя на костную массу или минеральный состав. [8] Когда уровень кальция в плазме падает, рецепторы клеточной поверхности активируются и происходит секреция паратиреоидного гормона; затем он начинает стимулировать поступление кальция в пул плазмы, забирая его из целевых клеток почек, кишечника и костей, при этом костеобразующему действию паратиреоидного гормона противодействует кальцитонин , секреция которого увеличивается с увеличением уровня кальция в плазме. [56]
Избыточное потребление кальция может вызвать гиперкальциемию . Однако, поскольку кальций довольно неэффективно всасывается в кишечнике, высокий уровень кальция в сыворотке крови, скорее всего, вызван чрезмерной секрецией паратгормона (ПТГ) или, возможно, чрезмерным потреблением витамина D, оба из которых способствуют абсорбции кальция. Все эти состояния приводят к избыточному отложению солей кальция в сердце, кровеносных сосудах или почках. Симптомы включают анорексию, тошноту, рвоту, потерю памяти, спутанность сознания, мышечную слабость, повышенное мочеиспускание, обезвоживание и метаболические заболевания костей. [56]
Хроническая гиперкальциемия обычно приводит к кальцификации мягких тканей и ее серьезным последствиям: например, кальцификация может вызвать потерю эластичности сосудистых стенок и нарушение ламинарного кровотока, а, следовательно, к разрыву бляшек и тромбозу . И наоборот, недостаточное потребление кальция или витамина D может привести к гипокальциемии , часто вызванной также недостаточной секрецией паратиреоидного гормона или дефектными рецепторами ПТГ в клетках. Симптомы включают нервно-мышечную возбудимость, которая потенциально может вызвать тетанию и нарушение проводимости сердечной ткани. [56]
Поскольку кальций необходим для развития костей, многие заболевания костей можно объяснить органическим матриксом или гидроксиапатитом в молекулярной структуре или организации кости. Остеопороз представляет собой снижение содержания минеральных веществ в кости на единицу объема, и его можно лечить добавлением кальция, витамина D и бисфосфонатов . [8] [9] Недостаточное количество кальция, витамина D или фосфатов может привести к размягчению костей, называемому остеомаляцией . [56]
Поскольку кальций экзотермически реагирует с водой и кислотами, контакт металлического кальция с влагой тела приводит к сильному коррозионному раздражению. [58] При проглатывании металлический кальций оказывает такое же воздействие на ротовую полость, пищевод и желудок и может привести к летальному исходу. [45] Однако не известно, что длительное воздействие имеет явные побочные эффекты. [58]